Acufeni
- Categoria: IPOACUSIA NEUROSENSORIALE DELL’ADULTO A RAPIDA INSORGENZA
- Pubblicato: Martedì, 02 Febbraio 2016 07:45
- Visite: 8310
in aggiornamento
in aggiornamento
Ipoacusia su Base Autoimmune dell'Orecchio Interno [Malattia Autoimmune Dell'orecchio Interno (AIED) AIEDs ]
Parole chiave : Sordità neurosensoriale, Malattia autoimmune, Autoimmunità, Malattia di sistema, Immunopatologia, Corticosteroidi, Orecchio interno
RIASSUNTO
La sordità autoimmune è un'entità clinica confermata da argomenti sperimentali e clinici che chiamano in causa un supporto immunologico nell'orecchio interno ed è osservata in tre tipi di situazioni: associata a una patologia nota per avere un sostegno immunologico quasi certo o associata a una malattia disimmunitaria o autoimmune e di cui l'orecchio non è che un bersaglio tra altri organi attraverso meccanismi non specifici dell'orecchio interno o totalmente isolata o associata a una malattia autoimmune specifica di organo, ma con evoluzione indipendente. La sordità è neurosensoriale, in genere rapidamente progressiva e invalidante, bilaterale nell'80% dei casi e spesso associata a disturbi vestibolari. In assenza di una prova formale della natura autoimmune della sordità, in particolare in assenza di test di laboratorio di certezza, la sua prevalenza è mal valutata e la diagnosi è di esclusione. Tuttavia, fra i test di immunità umorale, il Western blot sembra il più interessante, in quanto permette di sospettare il possibile ruolo della proteina di shock termico (HSP-70) nel meccanismo della reazione immunologica. Il trattamento, empirico e mal codificato, si basa sulla terapia corticosteroidea, che è un argomento diagnostico di conferma in caso di regressione dei sintomi. Il ruolo dei trattamenti immunosoppressivi, talvolta proposti in caso di corticoresistenza, resta molto discusso. La somministrazione farmacologica locale, come l'iniezione endotimpanica, suscita numerose speranze nel trattamento della sordità autoimmune, ma la sua efficacia resta da dimostrare. In caso di evoluzione verso una sordità profonda bilaterale, l'impianto cocleare permette di sperare in una riabilitazione uditiva paragonabile alle altre cause di sordità.
Malattia autoimmune dell'orecchio interno (AIED)
§ Che cosa è la malattia autoimmune dell'orecchio interno?
§ Quant’è comune la malattia autoimmune dell'orecchio interno?
§ Fisiopatologia dell'autoimmunità.
§ Quali sono le cause della malattia autoimmune dell'orecchio interno?
§ Come è la malattia autoimmune dell'orecchio interno diagnosticata?
§ Come è la malattia autoimmune dell'orecchio interno trattati?
§ Studi di ricerca sulle malattie autoimmuni dell'orecchio interno
Prospettiva storica:
Già nel 1958, Lehnhardt ha ipotizzato che i casi di sordità bilaterale recidivante erano dovuti a anticorpi anticocleari.
Nel 1979, McCabe ha riportato una serie di 18 pazienti che rappresentatavano casi di perdita dell'udito rapidamente progressiva bilaterale perdita dell'udito neurosensoriale (SNHL SensoriNeural Hearing Loss) autoimmune mediata. Il caso che ha descritto in dettaglio era quella di un uomo di 25 anni con perdita improvvisa in un orecchio e progressiva perdita nell'altro, così come una paralisi facciale unilaterale. Trattato con Decadron e Cytoxan (un soppressore di immunità cellulare), la perdita dell’ udito e la paralisi facciale sono migliorate. Dei 18 pazienti, 5 hanno avuto paralisi facciale e un certo numero aveva lesioni granulomatose vasculitiche distruttive. Il segno distintivo di questa condizione diagnosticata clinicamente è la presenza di una rapida progressione, spesso fluttuante, SNHL bilaterale per un periodo di settimane o mesi. La progressione di perdita dell'udito è troppo rapido per essere diagnostico per presbiacusia e troppo lenta per concludere una diagnosi di SNHL improvvisa. Possono essere presenti Sintomi Vestibolari, come vero Vertigini, Squilibrio generalizzato, e Atassia, E 'possibile che molti dei pazienti descritti da McCabe aveva PAN o di altre malattie autoimmuni e non solo organo AIED.
McCabe ha osservato che la perdita dell'udito autoimmune era tipicamente bilaterale. Tra le entità cliniche che elencati nella diagnosi differenziale di fluttuanti o perdita di udito rapidamente progressiva sono molti che ora sono considerati correlati ad autoimmunità in un numero significativo di pazienti, come la Meniere cocleare e la sordità improvvisa neurosensoriale.
'Idrope post-traumatici "- di come la sindrome di Meniere che si verifica qualche tempo dopo un trauma cranico - è ormai considerato da molti come una condizione autoimmune simile a oftalmia simpatica (bilaterale panuveite granulomatosa nell'occhio controlaterale dopo penetrante infortunio che coinvolge il uvea del altro occhio). Allo stesso modo, i pazienti che soffrono di perdita progressiva o fluttuanti in una o entrambe le orecchie dopo chirurgia dell'orecchio interno presumibilmente fanno a causa della sensibilizzazione immune dal trauma chirurgico o osso temporale
Che cosa è la malattia autoimmune dell'orecchio interno?
La sordità autoimmune [Malattie autoimmuni dell'orecchio interno (AIED)] è una sindrome caratterizzata da perdita progressiva dell'udito e / o vertigini che è causata da anticorpi o cellule immunitarie che attaccano l'orecchio interno. E’ un'entità clinica confermata da argomenti sperimentali e clinici che chiamano in causa un supporto immunologico nell'orecchio interno ed è osservata in tre tipi di situazioni: associata a una patologia nota per avere un sostegno immunologico quasi certo o associata a una malattia disimmunitaria o autoimmune e di cui l'orecchio non è che un bersaglio tra altri organi attraverso meccanismi non specifici dell'orecchio interno o totalmente isolata o associata a una malattia autoimmune specifica di organo, ma con evoluzione indipendente. Nella maggior parte dei casi, vi è la riduzione dell'udito accompagnata da tinnito (ronzio, sibilo, ruggente), che si verifica nel corso di pochi mesi. Le varianti sono attacchi bilaterali di perdita dell'udito e acufeni che somigliano malattia di Meniere , e gli attacchi di vertigini accompagnati da esami del sangue anomali per gli anticorpi. Circa il 50% dei pazienti con AIED hanno sintomi legati all’organo dell’equilibrio (vertigini o instabilità).
Il sistema immunitario è complesso e ci sono diversi modi che può danneggiare l'orecchio interno. Sia allergie e malattie tradizionali autoimmuni come la spondilite anchilosante, lupus eritematoso sistemico (LES), la sindrome di Sjogren (sindrome dell'occhio secco), la malattia di Cogan , colite ulcerosa, la granulomatosi di Wegener, artrite reumatoide, sclerodermia, artrite psoriasica (Srikumar et al 2004) può provocare o essere associato con l’AIED. Un'altra malattia multisistemica, Bechet di, ha spesso problemi audiovestibulari. Allergia è tradizionalmente sospettato di essere legati all'alimentazione, ma non vi è attualmente alcun accordo circa l'importanza di allergia alimentare.
L’AIED è rara, probabilmente rappresenta meno dell'1% di tutti i casi di ipoacusia o vertigini (Bovo et al 2009). L'esatta incidenza è controversa.
È importante riuscire a porre una diagnosi positiva, in quanto si tratta di una delle rare forme di sordità neurosensoriale potenzialmente reversibili dopo un trattamento medico a base di corticosteroidi.
Punto importante
Definizioni delle ipoacusie neurosensoriali
Sordità autoimmune
• Il più delle volte, sordità neurosensoriale rapidamente progressiva
• Sordità bilaterale e asimmetrica
• Segni vestibolari associati (frequenti, fino nel 50% dei casi)
• Leggera prevalenza della donna di età media
• Malattia autoimmune sistemica associata in meno del 30% dei casi
Sordità neurosensoriale rapidamente progressiva
• Perdita di più di 30 dB su tre frequenze adiacenti che compare in un periodo di alcune settimane o di qualche mese
Sordità improvvisa
• Perdita di più di 30 dB su tre frequenze adiacenti che compare in un periodo di meno di 3 giorni
• Causa per definizione ignota
Sordità brutale
• Causa per definizione conosciuta
Fisiopatologia
La malattia autoimmune dell'orecchio interno termine (AIED) implica un attacco diretto del sistema immunitario su un antigene endogena dell’orecchio interno. La maggior parte delle prove che collegano il sistema immunitario alla coclea sono indirette; Pertanto, la malattia dell'orecchio interno immuno-mediata può essere un termine preferito. AIED è una diagnosi clinica basata sul corso clinico della malattia, sui risultati dei test immunitari, e sulle risposte al trattamento. Il più importante risultato è il miglioramento diagnostico dell’ udito osservato con una prova di immunosoppressori.
I criteri specifici per sordità neurosensoriale idiopatica progressiva bilaterale (IPBSNHL) includono una SNHL bilaterale di almeno 30 dB a qualsiasi frequenza progressiva in almeno un orecchio, definita come un cambiamento di soglia che è maggiore di 15 dB a qualsiasi frequenza o 10 dB a 2 o più frequenze consecutivi o un cambiamento significativo nel punteggio di discriminazione vocale. Questa definizione esclude pazienti con SNHL improvvisa che si verificano in meno di 24 ore, che più probabilmente è dovuto a una eziologia virale microvascolare.
Un certo sottogruppo di pazienti con presunta malattia di Ménière (idrope endolinfatica idiopatica) in realtà potrebbe avere la sindrome di Ménière, in cui la fisiopatologia sottostante è immune mediata. In genere, la malattia di Ménière è inizialmente diagnosticata in questi pazienti; tuttavia, più tardi si sviluppa una perdita fluttuante uditiva nell'orecchio controlaterale. Questo cambiamento può richiedere un workup per AIED. Hughes et al trovato che circa la metà dei loro pazienti con AIED hanno manifestazioni della sindrome di Ménière autoimmune. [Hughes et al.,1983; Huang NC, Sataloff RT. 2011]
Quant’è comune la malattia autoimmune dell'orecchio interno?
L’AIED è rara, probabilmente rappresenta meno dell'1% di tutti i casi di ipoacusia o vertigini. L'esatta incidenza è controversa. Circa il 16% delle persone con bilaterale malattia di Meniere , e il 6% delle persone con malattia di Meniere di ogni varietà può essere dovuto a disfunzioni immunitarie.
Sesso
E’ stato suggerito che questa condizione può essere più comune nei pazienti di sesso femminile che possono o non possono avere malattia autoimmune sistemica concomitante rispetto ai pazienti di sesso maschile.
Eta’
Nella maggior parte dei pazienti, l'insorgenza dei sintomi si verifica iniziale all'età di 20-50 anni. Questi tipi di ipoacusia sono poco frequenti nei pazienti pediatrici . [Huang NC, Sataloff RT. 2011]
Quali sono le cause della malattia autoimmune dell'orecchio interno?
La causa di AIED Generalmente si ritiene essere correlato al anticorpi o cellule immunitarie che causano danni all'orecchio interno. Ci sono diverse teorie su come questi potrebbero sorgere, analogamente ad altre malattie autoimmuni:
La comparsa di malattie autoimmuni è dovuta a due tipi di fattori principali: fattori genetici e fattori ambientali.
Una predisposizione genetica è attestata dall'esistenza di casi familiari di malattia autoimmune, dall'associazione di aplotipi human leucocyte antigen (HLA) particolari che conferiscono una suscettibilità elevata alla malattia (gene di suscettibilità), di geni della frazione del complemento o di citochine e da una maggiore prevalenza delle malattie autoimmuni in gemelli monozigoti. aspetti controllati geneticamente del sistema immunitario possono aumentare o altrimenti essere associata ad una maggiore suscettibilità ai disturbi dell'udito comuni, come la malattia di Meniere. Una revisione sistematica della letteratura 1861-2011 ha concluso che fino a un terzo dei casi la malattia di Meniere può essere legato a cause immunologiche basate su dati clinici e risposta positiva agli steroidi. I fattori genetici possono anche avere un effetto positivo sulla dell'udito (Greco et al 2012). Gazquez e colleghi riferito che i pazienti con malattia di Meniere con la variante allelica MICA * 4, un complesso maggiore di istocompatibilità (MHC), ha avuto una progressione più lenta di perdita dell'udito rispetto a quelli con una diversa MHC. In casi confermati di improvvisa perdita dell'udito autoimmune legata, la più importante proteina dell'orecchio interno, Cochlin, in grado di produrre la risposta delle cellule T, ed è stato implicato come l'antigene responsabile per l'infiammazione e danni all'orecchio interno (Baek et al 2006). Questi dati suggeriscono che più della malattia di Meniere e altre sindromi progressisti può essere causata da disfunzione del sistema immunitario che è attualmente generalmente si pensa.
Cross-reazioni: Anticorpi o T-cellule canaglia causano danni accidentali dell'orecchio interno perché le quote orecchio antigeni comuni con una sostanza potenzialmente dannosa, virus o batteri che il corpo sta combattendo off. Questa è attualmente la teoria favorita di AIED. CTL2 è stato recentemente riportato che un antigene bersaglio in AIED (Kommareddi et al 2009).
Intolleranza: L'orecchio, come l'occhio, può essere solo un luogo privilegiato parzialmente immune.Ciò significa che il corpo non può conoscere tutti gli antigeni dell'orecchio interno, e quando vengono rilasciati (forse dopo un intervento chirurgico o un'infezione), il corpo può erroneamente un attacco su l'antigene "straniera". Nell'occhio, vi è una sindrome chiamata oftalmia simpatetica, in cui a seguito di una ferita penetrante di un occhio, l'altro occhio può andare ciechi. Questa teoria non è attualmente favorevole per l'orecchio.
Si tratta dei fattori esogeni come certi agenti infettivi, virali (p. es., Epstein-Barr virus [EBV] e lupus, CMV e sindrome di Guillain-Barré) e batterici (coxsackie B4 e diabete insulinodipendente), gli agenti tossici (p. es., sclerodermia e cloruro di vinile) e i farmaci (p. es., lupus indotto e procainamide). È stata osservata una relazione inversamente proporzionale tra la frequenza delle malattie autoimmuni e la prevalenza dei contagi infettivi. Questi agenti possono imitare degli antigeni self (mimetismo molecolare) o modificare la risposta immunitaria del soggetto. Sono anche ipotizzati dei fattori psicologici.
Presentazione clinica
I fattori endocrini, l'età e la risposta ai trattamenti immunosoppressivi formano un terreno evocatore. In effetti, davanti all'assenza di una prova formale della natura autoimmune della sordità, il medico si trova, il più delle volte, di fronte al dilemma dell'ipotesi diagnostica su un insieme di elementi, eventualmente rafforzato a posteriori dalla reversibilità della sordità dopo il trattamento con corticosteroidi (trattamento di prova). La prevalenza delle malattie autoimmuni è più importante nella donna in periodo di attività genitale. Gli androgeni hanno un ruolo protettivo e gli estrogeni un ruolo aggravante. Le malattie autoimmuni interessano preferenzialmente dei soggetti giovani, con la comparsa della malattia secondo la sindrome in causa nel secondo, nel terzo o nel quarto decennio.
• Perdita uditiva: Il segno distintivo della malattia dell'orecchio interno immuno-mediata è una sordità neurosensoriale (SNHL), che di solito è bilaterale e si verifica rapidamente nel corso di settimane o mesi.
• Fluttuazione: la perdita neurosensoriale può variare e stabilizzarsi a un certo livello, oppure può progredire senza fluttuazione.
• Lateralità: l’ipoacusia bilaterale si verifica nella maggior parte dei pazienti (79%). Di tanto in tanto, solo un orecchio è coinvolto inizialmente, con successiva perdita dell'udito nell'orecchio controlaterale . In casi bilaterali, le soglie audiometriche possono essere simmetriche o asimmetriche.
• Punteggio di discriminazione vocale: Spesso i punteggi di discriminazione vocale sono poveri nelle malattie dell'orecchio interno immuno-mediate. Pertanto, nei casi di malattia unilaterale o bilaterale-asimmetrica, bisogna includere la diagnostica per immagini e gli studi sierologici nel workup per escludere malattie retrococleare e la lue, malattia dell'orecchio interno.
• Sintomi vestibolari: Circa il 50% dei pazienti si lamentano di avere sintomi vestibolari tipici della malattia Ménière. I sintomi vestibolari possono includere squilibrio, atassia, movimento intolleranza, vertigini posizionali, e vertigini episodica.
• Acufene e la pienezza sonora: Ben il 25-50% dei pazienti presentano anche sintomi di tinnitus e pienezza sonora, che può oscillare in gravità.
• Malattia sistemica autoimmune: Coesistenza malattia autoimmune sistemica si verifica nel 15-30% dei pazienti. Le diagnosi sono l'artrite reumatoide, la colite ulcerosa, il lupus eritematoso sistemico, e poliarterite nodosa.
Le sordità di origine autoimmune possono raggrupparsi in tre categorie principali:
• quelle che sono note per avere un sostegno immunologico quasi certo: sindrome di Cogan, policondrite atrofizzante, malattia di Vogt-Koyanagi-Harada. Esse sono rare, ma presentano un modello di studio interessante nell'uomo;
• quelle associate a una malattia disimmunitaria o autoimmune e in cui l'orecchio non è che un bersaglio tra altri organi attraverso meccanismi non specifici dell'orecchio interno;
• quelle che sono totalmente isolate o associate a una malattia autoimmune specifica di organo, ma a evoluzione indipendente. I pazienti con una sindrome disimmunitaria possono presentare una sordità di percezione scoperta di solito durante il follow-up della loro patologia, il che rende talvolta difficile chiamare in causa la responsabilità del disturbo disimmunitario nella sordità, a causa delle terapie spesso ototossiche già iniziate, o legata all'età o ai precedenti del paziente, che possono far sospettare una banale presbiacusia. La loro patogenesi rimane incerta senza poter affermare il tipo di mediazione immunitaria a livello dell'organo di Corti.
Classificazione delle malattie autoimmuni
• Malattie autoimmuni specifiche di organo:
○ lesioni limitate a un tessuto o a un organo
○ lesioni secondarie a una risposta immune diretta contro un antigene la cui distribuzione è limitata a questo tessuto
• Malattie autoimmuni non specifiche di organo:
○ lesione sistemica
○ lesione secondaria a una risposta immune diretta contro un antigene la cui distribuzione è ubiquitaria
La sordità colpisce il più delle volte il soggetto tra i 30 e i 50 anni, con una predominanza femminile. La sordità è, di solito, bilaterale, spesso asimmetrica, ed evolve in alcune settimane o in alcuni mesi, talvolta associata a vertigini e ad acufeni. La sordità evolve spesso piuttosto rapidamente ed è, a volte, reversibile con o senza trattamento. Questa evoluzione rapida della sordità è un elemento diagnostico importante a favore di una causa autoimmune, ma non deve far escludere alcune cause genetiche. L'esistenza di una malattia autoimmune nella famiglia o dei precedenti personali disimmunitari devono essere ricercati e sarebbero presenti nel 12-30% dei casi, a seconda degli autori. L'esame clinico otorinolaringoiatrico (ORL) è, di solito, normale. Occasionalmente, è osservata un'otite sierosa, che può condurre a dei dubbi diagnostici. L'audiometria non ha caratteristiche specifiche, benché le curve più spesso riscontrate siano a plateau con caduta sui suoni acuti. La lesione è di tipo endococleare. L'evoluzione può avvenire in maniera fluttuante, spesso con un miglioramento significativo della sordità sotto terapia corticosteroidea.
Dati essenziali della sordità autoimmune
• Patologia rapidamente invalidante
• Diagnosi difficile, di esclusione e, il più delle volte, incerta
• Assenza di test di laboratorio specifici: test di presunzione diagnostica
• Diagnostica per immagini: risonanza magnetica (RM) (con o senza tomografia computerizzata [TC] delle rocche)
• Fondo dell'occhio
• Trattamento non causale, mal codificato, basato sulla terapia corticosteroidea
• Terapia a dosi elevate
• Necessità di discutere con il paziente di rischi, benefici e alternative dei vari trattamenti
• Riabilitazione uditiva in caso di assenza di miglioramento o di aggravamento uditivo: apparecchi acustici, impianto cocleare
• Follow-up del paziente: sviluppo o aggravamento della patologia sistemica associata e conservazione della funzione dell'orecchio controlaterale
|
Tabella 1 - Principali patologie autoimmuni che colpiscono il labirinto. |
|
Reumatismi infiammatori |
Poliartrite reumatoide |
|
Connettiviti |
Sclerodermia sistemica |
|
Vasculiti sistemiche |
Panarterite nodosa |
|
Quadro nosologico mal definito |
Sindrome di Cogan |
|
Malattia di Ménière? |
|
Lesioni dell'orecchio interno nel corso delle malattie sistemiche (Tabella 1)
La prevalenza della sordità autoimmune nel corso di una malattia sistemica è valutata pari a circa il 15-30% [Bovo et al.2006]18, ma può essere sovrastimata a causa dell'assenza di test diagnostici specifici.
Essa è stata descritta inizialmente nel 1934 da Mogan e Baumgartner 19 poi da Cogan nel 1945 20.
Nella forma tipica, presente nel 70% dei casi, essa comporta una cheratite interstiziale non sifilitica e una sordità progressiva bilaterale associata a vertigini, realizzando un quadro simile alla malattia di Ménière. A volte, la cheratite interstiziale si associa o fa seguito a delle lesioni oculari come congiuntivite, uveite, episclerite o sclerite. La lesione è, il più delle volte, bilaterale durante l'evoluzione e può anche comportare fotofobia, lacrimazioni, dolori oculari e riduzione dell'acuità visiva, il più delle volte transitoria. L'evoluzione verso la sordità è piuttosto rapida, in un periodo di 1-3 mesi. L'importanza dello spostamento cronologico tra i sintomi uditivi e oculari rende a volte difficile la diagnosi, poiché esso può arrivare a 2 anni [Haynes et al.,1980] 21 (Tabella 2 ).
Nella forma atipica, la lesione dell'occhio e/o dell'orecchio è di natura differente, come una cheratite interstiziale o un'emorragia sottocongiuntivale, oppure i sintomi audiovestibolari non hanno le caratteristiche di una sindrome di Ménière o compaiono più di 2 anni prima dei sintomi oculari o dopo. La malattia interessa soprattutto gli adulti giovani, colpisce un altro organo in due casi su tre e dà un vero e proprio quadro di malattia sistemica, richiamando una vasculite, in un caso su tre. I sintomi più frequenti sono cardiovascolari, muscoloscheletrici, neurologici, digestivi e mucocutanei.
L'incidenza della sindrome di Cogan è sconosciuta. Trenta casi sono stati descritti su un periodo di 15anni in Francia, e il numero di casi clinici pubblicati nella letteratura internazionale è di circa 200 [Vinceneux P. 2005].
La sindrome di Cogan colpisce soprattutto l'adulto giovane, con un esordio, una volta su due, tra i 20 e i 30 anni (età media: 30 anni) in soggetti caucasici senza predominanza sessuale. Non è stata riscontrata in modo formale alcuna prevalenza di gruppo HLA nei pazienti affetti.
Una lesione vestibolare isolata o associata immediatamente o secondariamente a una lesione uditiva realizza di solito un quadro di malattia di Ménière con vertigini, instabilità, sindrome delle nausee e acufeni. L'evoluzione è fluttuante e intermittente per alcuni giorni. I disturbi vestibolari regrediscono di solito al momento della comparsa di un deficit uditivo, spesso bilaterale fin dall'inizio, con evoluzione piuttosto rapida verso una sordità grave e, quindi, totale, che evolve il più delle volte per crisi. La prognosi è dominata dal rischio di sordità definitiva e dalle complicanze cardiovascolari, in particolare dall'insufficienza aortica. Così, al termine dell'evoluzione, l'80% dei pazienti è cofotico. Sono stati descritti anche una sordità di trasmissione con effetto on/off e dei disturbi vestibolari di tipo centrale.
Tabella 2 - Frequenza delle manifestazioni cliniche nella sindrome di Cogan secondo Vinceneux 2005.
|
Febbre |
39% |
|
Vasculite (grossi e/o piccoli vasi) |
28% |
|
Segni neurologici |
27% |
|
Manifestazioni digestive |
26% |
|
Perdita di peso |
26% |
|
Cute-mucose |
19% |
|
Manifestazioni urogenitali |
16% |
|
Adenopatie |
8%
|
Se i segni oculari e audiovestibolari fanno parte della definizione della sindrome di Cogan e sono indispensabili per la diagnosi, sono abituali altri sintomi, con, in almeno due terzi dei casi, una lesione di un altro organo che può simulare una malattia sistemica autoimmune in un terzo dei casi. Queste malattie sistemiche devono essere ipotizzate come diagnosi differenziale, così come una sifilide congenita (criterio di esclusione della sindrome di Cogan), una sindrome di Vogt-Koyanagi-Harada e la sindrome di Susac che colpisce le arteriole retiniche cocleari e cerebrali e che si manifesta in puntate, con riduzione dell'acuità visiva, sordità e disturbi neurologici centrali.
L'eziologia e i meccanismi fisiopatologici non sono chiaramente spiegati. Il ruolo favorente di un'infezione nelle settimane che precedono i sintomi è ipotizzato nel 30% dei casi. Il ruolo di un meccanismo tipo vasculite o infezione da Chlamydiae trachomatis o altri agenti infettivi resta da dimostrare. Degli anticorpi diretti contro la coclea e la cornea sono stati evidenziati in maniera occasionale, facendo ipotizzare l'intervento dell'immunità umorale. Più recentemente, Lunardi et al.,2002 hanno identificato un peptide Cogan che presenta delle omologie con degli antigeni fortemente espressi sull'endotelio vascolare e nell'orecchio interno.
Benché alcuni esami laboratoristici complementari possano essere alterati nel corso della sindrome di Cogan, in particolare al momento delle puntate, nessuno è specifico.
Una sindrome infiammatoria è abituale. Varie anomalie di tipo immunologico possono essere osservate in maniera occasionale, ma l'indagine non apporta, di solito, alcun elemento determinante [Lejeune J.M., Charachon R.,2002] .Un innalzamento di autoanticorpi della HSP-70 è stato segnalato in tutti i casi adulti[ Bonaguri et al.,2007]. Sono stati osservati anche degli autoanticorpi anticoclea e anticornea [Arnold et al.,1984]. Sono stati evidenziati degli Ac anticonnessina 26 che potrebbero rappresentare un elemento diagnostico interessante, poiché si sa che una mutazione del gene che codifica per questa proteina porta ad ipoacusie neurosensoriali gravi [Lunardi et al.,2002].
È necessario un esame oftalmologico approfondito, alla ricerca di una cheratite interstiziale associata a un'uveite anteriore e/o posteriore più completa. Un bilancio cardiovascolare, in particolare una diagnostica per immagini aortica, è indispensabile a causa di una vasculite associata che può mettere in forse la prognosi vitale.
Il trattamento si basa sulla somministrazione di corticosteroidi che agiscono spesso in maniera favorevole sui segni oculari, vascolari o viscerali, ma il cui l'effetto sull'udito è molto più aleatorio, soprattutto quando si è instaurata la sordità.
Il trattamento deve essere instaurato precocemente e inizia con un bolo di 1 g di prednisolone. Quindi, è raccomandata una dose orale di 1-1,5 mg/kg/die di metilprednisolone, con una riduzione progressiva della dose alla ricerca di una dose di mantenimento minima.
In assenza di efficacia, può essere discussa un'alternativa con un trattamento immunosoppressivo, in particolare con il metotrexate, senza, comunque, che abbia dimostrato la sua efficacia.
Malattia di Vogt-Koyanagi-Harada
Questa malattia associa una sindrome meningea di tipo virale, un'uveite bilaterale e una sordità neurosensoriale bilaterale nel 50-80% dei casi, il più delle volte simmetrica e associata a volte a delle vertigini e a una vitiligine seguita da un'alopecia[ Yamaki et al., 2000].
La malattia di Vogt-Koyanagi-Harada, chiamata anche malattia di Harada, colpisce soprattutto le giovani donne e le persone di pelle scura (asiatici, ispanici, indiani d'America), con un'incidenza annuale stimata a 1/400 000. L'età media di esordio è di 30anni.
I criteri diagnostici sono stati precisati nel 1999 e hanno permesso di separare tre forme: completa, incompleta e probabile [Read et al.,2001]. La forma completa comprende una lesione multiviscerale, la forma incompleta comprende una lesione oculare con segni neurologici o uditivi o cutanei e la forma probabile è una forma oculare isolata.
La malattia evolve secondo quattro fasi cliniche:
• la fase prodromica associa febbre, cefalee, nausea e vertigini e, poi, dei sintomi neurologici (debolezza muscolare, emiparesi, emiplegia, disartria, dolori orbitari);
• la fase oftalmologica si presenta alcuni giorni dopo con fotofobia, dolori oculari e, spesso, un distacco retinico bilaterale sieroso. A questo stadio, possono anche essere presenti, in un terzo dei casi, una perdita uditiva e dei segni vestibolari;
• la fase di convalescenza compare nei tre mesi che seguono l'esordio della malattia e si caratterizza per dei segni cutanei come poliosi (che interessa le ciglia e le sopracciglia), caduta di capelli e vitiligine;
• l'ultima fase è ricorrente, cronica e con la comparsa di uveite ricorrente e di complicanze oculari. La patogenesi è collegata a un disordine immunologico di IgG contro i melanociti, che induce una citotossicità e un'apoptosi mediata dai linfociti T, ma l'eziologia rimane incerta.
Non esistono indicatori specifici attuali di una lesione disimmunitaria dell'orecchio interno.
La diagnosi è clinica e, in caso di comparsa di una sindrome meningea monolinfocitaria fugace, l'esame del liquido cerebrospinale rivela una pleiocitosi che conferma la diagnosi. L'esame oculistico è fondamentale, alla ricerca di un'iridociclite e di un'uveite posteriore.
La sindrome infiammatoria laboratoristica è poco alterata. Si riscontrano più frequentemente i gruppi HLA DRB0405, DR4 e DRW53. Degli anticorpi (Ac) antigangliosidi sono stati evidenziati nel 70% dei casi [Yokoyama et al.,1981] e sono stati descritti degli anticorpi (Ac) antimelanina o un'autoimmunità cellulare contro i melanociti [Moorthy et al.,1995] . È necessario escludere con esami sierologici una borreliosi, una sifilide, una toxoplasmosi, una rosolia, una lesione da citomegalovirus o herpes e, con gli indicatori specifici, una malattia di Wegener o una sarcoidosi.
Un trattamento precoce mediante terapia corticosteroidea a forti dosi è, in genere, efficace. La sordità può regredire all'inizio dell'evoluzione, mentre i segni oculari progrediscono. L'evoluzione a più lungo termine è segnata di solito da un'alterazione grave dell'udito e della vista. Nelle forme gravi, può anche essere proposto un trattamento immunosoppressivo [Rao et al.,2006]. L'evoluzione della malattia è segnata da complicanze oftalmiche, come glaucoma, cataratta, neovascolarizzazione della membrana coroidea, fibrosi subretinica e cecità [Read RW. 2002]. In caso di evoluzione verso una sordità profonda bilaterale, è indicato l'impianto cocleare.
Policondrite cronica atrofizzante
Una policondrite cronica atrofizzante è segnata da una condrite asettica ricorrente dei padiglioni auricolari e delle cartilagini del naso che conduce alla loro progressiva scomparsa. Essa interessa tutti i tipi di cartilagine: fibrosa, elastica o ialina.
La diagnosi segue o i criteri di McAdam et al.,1976 (associazione a tre dei seguenti criteri: condrite recidivante delle due orecchie, poliartrite non erosiva, condrite del naso, infiammazione oculare, condrite laringea o tracheale e lesione cocleare) o i criteri di Mac Caffrey et al.,1978 (esistenza di una condrite recidivante di due elementi cartilaginei differenti). Può essere presente una lesione cutanea e cardiovascolare.
L'età media è di 50 anni, e questa associazione può incontrarsi con un'altra sindrome disimmunitaria nel 25% dei casi. La sordità è progressiva o improvvisa, mono- o bilaterale e, a volte, con un fattore trasmissivo associato per lesione tubarica.
L'eziogenia e la patogenesi di questa lesione restano sconosciute.
Il meccanismo causale sembra essere una malattia immunitaria anticollagene di tipo II e di tipo IX 35, con depositi di collagene di tipo II all'interno della membrana tettoria e nella capsula otica [Nair et al.,1999].
Il bilancio laboratoristico mostra una sindrome infiammatoria non specifica al momento dell'evoluzione iniziale acuta, con innalzamento della velocità di sedimentazione (VS), della proteina C reattiva (PCR) e del complemento CH 50 e C3 e un'ipergammaglobulinemia [Kumakiri et al.2005]. Degli Ac antinucleari sono presenti nel 5-20% dei casi, mentre il gruppo HLA DR4 è presente nel 56% dei casi [Bachor et al.,2006]. Si possono riscontrare degli Ac anticollagene II nativi, ma solo nel 30% dei casi all'esordio della malattia [Yoo et al.,2002] e dei test di trasformazione linfoblastica (TTL) positivi diretti contro proteoglicani della cartilagine [Lejeune et al.,1991]. La migliore prova diagnostica è l'analisi istologica di una cartilagine infiammatoria dove un infiltrato di linfociti macrofagi è concomitante alla distruzione della matrice cartilaginea con necrosi. Possono essere evidenziati con una tecnica di immunofluorescenza dei depositi di Ig e di complemento all'interno delle cartilagini colpite, più frequentemente su una cartilagine auricolare.
Il trattamento utilizza una terapia corticosteroidea alla dose di 0,5 mg/kg al giorno, con un miglioramento prevedibile dell'udito in circa un terzo dei casi.
Sindrome di Gougerot-Sjögren
La sindrome di Gougerot-Sjögren primitiva associa una cheratocongiuntivite a xerostomia e a disturbi sistemici, di eziologia sconosciuta [Manoussakis et al.,2004]. Le ghiandole salivari e lacrimali sono le più colpite e realizzano la sindrome sicca, potendo provocare una sordità di trasmissione con otite sierosa per alterazione della mucosa tubarica. Nessun segno o sintomo è patognomonico, e la diagnosi positiva è posta in presenza di diversi segni clinici, istopatologici e laboratoristici (consensus conference internazionale nel 2001) [Vitali et al.,2002]. È frequente una lesione reumatoide moderata a evoluzione lenta e cronica. La biopsia delle ghiandole salivari accessorie è un elemento essenziale, ma non è indispensabile quando la sintomatologia risponde ai criteri della malattia. La sordità di percezione è riscontrata in una percentuale di casi che arriva fino al 40% [Tumiati et al.,1997]. La presenza di anticorpi anticardiolipina sembra essere un fattore prognostico infausto per l'udito, mentre né l'età né la gravità né l'antichità della malattia né i precedenti di trattamento con corticosteroidi sembrano essere correlati allo stato uditivo [Tumiati et al.,1997]. Le diagnosi differenziali responsabili di una sindrome di Gougerot-Sjögren « like » sono numerose: cause farmacologiche, infettive (in particolare virus dell'immunodeficienza umana [HIV], epatite C), tumorali (linfomi, amiloidosi), metaboliche (iperlipidemie di tipo II, IV e V) o post-irradiazione. Una sindrome di Gougerot-Sjögren, detta secondaria, compare spesso in numerose malattie autoimmuni (poliartrite reumatoide, lupus eritematoso, sclerodermia, cirrosi biliare primitiva, connettivite mista).
La lesione colpisce preferenzialmente le donne (rapporto 9/1), suggerendo il ruolo degli ormoni sessuali [Yamamoto K. 2003]. Essa compare nel quarto o nel quinto decennio senza predilezione geografica, con una prevalenza dell'1-3%; è la seconda lesione reumatologica autoimmune in ordine di frequenza dopo il lupus eritematoso sistemico [Dafni et al.,1997].
Il trattamento è essenzialmente sintomatico sulla sindrome sicca e sul trattamento specifico di organo in caso di interessamento di diversi grandi organi. Il trattamento della sordità con terapia corticosteroidea non ha dimostrato la sua efficacia in questa patologia.
La malattia di Behçet associa un'aftosi bipolare (orale e genitale) e una lesione della retina (uveite, irite), della cute (eritema nodoso, acne, fenomeno di patergia), delle articolazioni, del sistema nervoso e, più raramente, di altri organi.
Questa malattia di causa sconosciuta, denominata anche malattia o sindrome di Adamantiadès-Behçet, secondo il nome dei medici che l'hanno riconosciuta e descritta, compare di solito verso l'età di 30 anni e colpisce in pari misura gli uomini e le donne ed è più frequente in Medio Oriente e in Asia, con una predisposizione dei gruppi HLAB5 (Medio ed Estremo Oriente) e HLAB51 (israeliti). La diagnosi è clinica. Il test di patergia, che consiste nel pungere l'avambraccio del paziente con un piccolo ago e che provoca una pustola con areola infiammatoria, è specifico della malattia di Behçet, ma la reazione non è presente in tutti i pazienti [Ozdemir et al.,2007]. Le diagnosi differenziali da ipotizzare in caso di afte sono la sindrome di Reiter, il lupus eritematoso, l'aftosi idiopatica, l'herpes recidivante, l'HIV e, in caso di manifestazioni cutanee e articolari, la sarcoidosi o la spondilite anchilosante.
La lesione audiovestibolare, segnalata per la prima volta da Alajouanine nel 1961 , è piuttosto frequente, con un deterioramento progressivo dell'udito.
Malattia di Wegener
La granulomatosi di Wegener è una granulomatosi dell'apparato respiratorio nel suo insieme, associata a una vasculite necrotizzante dei vasi di piccolo e medio calibro, che può manifestarsi con un ampio ventaglio di segni clinici. L'età media si situa intorno ai 45 anni, ma tutte le età della vita possono essere colpite, con una leggera predominanza maschile. Si tratta di una malattia rara, la cui prevalenza è dell'ordine di due-tre per 100 000. La formazione di granulomi (pansinusiti destruenti, lesione otologica), la vasculite pauci-immune (noduli polmonari parenchimatosi) e le glomerulonefriti (vasculite renale) sono la testimonianza istologica della granulomatosi di Wegener e possono essere associate nel corso di una forma completa, costituendo la triade della malattia di Wegener (manifestazioni ORL, polmonari, renali), oppure essere presenti separatamente nella fase iniziale della malattia. Si distinguono, così, le forme diffuse (segni generali, lesione renale, emorragia alveolare importante ed evolutiva, lesione di uno o di più organi) e le forme localizzate (soprattutto respiratorie ORL e/o polmonari senza emorragia alveolare, senza lesione renale, ma, talvolta, anche cutanee, senza alterazioni dello stato generale). Il passaggio da una forma localizzata a una forma generalizzata e viceversa è possibile durante l'evoluzione della malattia e testimonia lo spettro clinico continuo della malattia.
L'orecchio è colpito diversamente, dal 19% al 61% dei casi[ Yildirim et al.,2008], e l'eziologia è sconosciuta. La caratteristica della lesione otologica nella malattia di Wegener è una sordità mista con l'associazione di un'otite media molto infiammatoria, dall'aspetto otoscopico spesso evocatore, e di una lesione neurosensoriale dell'udito. La lesione isolata dell'orecchio è rara.
La ricerca di anticorpi anticitoplasma dei polimorfonucleati neutrofili (ANCA) ha un valore diagnostico certo (sensibilità e specificità elevate). Gli ANCA che producono una fluorescenza perinucleare (p-ANCA), il cui antigene principale è la mieloperossidasi, sono meno specifici e possono essere osservati nel corso di altre vasculiti sistemiche (Churg e Strauss, poliangite microscopica, poliartrite reumatoide, lupus), delle glomerulonefriti a semiluna o, ancora, delle enteropatie infiammatorie. La prova istologica può essere difficile da ottenere, il che può giustificare dei prelievi multipli. Le biopsie nasali, sinusali o bronchiali mostrano tipicamente delle zone di necrosi circondate da un granuloma a palizzata a cellule giganti, associate a un'angioite necrotizzante acuta circonferenziale.
Il trattamento d'attacco si basa sull'associazione corticosteroidi-ciclofosfamide. Le forme limitate possono essere trattate meno aggressivamente con corticosteroidi e metotrexate a basse dosi. L'evoluzione, segnata da un elevato rischio di recidiva, giustifica il fatto che il trattamento sia di solito prescritto per una durata di 1 anno dopo l'ottenimento di una remissione completa e che sia interrotto progressivamente.
La malattia di Horton (MDH) è definita come una panarterite infiammatoria, subacuta gigantocellulare segmentaria e plurifocale. Essa può colpire l'insieme del sistema arterioso di piccolo e medio calibro, con una predilezione per i rami della carotide esterna e oftalmici della carotide interna. Essa colpisce i soggetti di età superiore ai 50 anni e tipicamente oltre i 70 anni e la sua incidenza aumenta con l'età. Colpisce i due sessi con una preponderanza femminile (due uomini per sette donne). La diagnosi della malattia di Horton è, prima di tutto, clinica e si basa, in un soggetto anziano, sull'esistenza di segni cefalici associati a un'importante sindrome infiammatoria (Tabella 3 ). Le cefalee sono generalmente lancinanti e, talvolta, pulsanti, permanenti o inframmezzate, a volte, da fasi di quiescenza molto lunghe. Esse sono tipicamente temporali o frontotemporali, talvolta diffuse. L'ipersensibilità dolorosa del cuoio capelluto al tatto (segno del cuscino) è caratteristica, così come il suo aumento al contatto (segno del pettine). Sono a volte associati dei dolori masseterici che sono molto suggestivi (claudicatio intermittente della mandibola per lesione dell'arteria mascellare interna). Il dolore può, infine, essere cervico-occipitale, simulando un torcicollo febbrile (lesione dell'arteria occipitale). Le manifestazioni oculari di origine ischemica sono frequenti e rappresentano tutta la gravità della malattia, potendo portare alla cecità. La sua diagnosi formale si basa sull'analisi anatomopatologica della biopsia dell'arteria temporale, ma questa deve essere di una lunghezza sufficiente, dato il carattere segmentario abituale delle lesioni. La sua sensibilità varia dal 60% al 97% ed è legata in gran parte al carattere segmentario di questa arterite. Caratteristicamente, sono colpite le tre tuniche della parete (panarterite) con delle lesioni variabili tipo arterite gigantocellulare, distruzione delle fibre muscolari lisce della media, variabile e, talvolta, associata a una necrosi fibrinoide, distruzione della limitante elastica interna, indispensabile alla diagnosi, e assenza di fibrosi avventiziale. La negatività di un prelievo non permette, quindi, di escludere la diagnosi e la biopsia dell'arteria temporale controlaterale deve essere discussa, anche se, nei quadri caratteristici e, soprattutto, quando sono associate delle complicanze oculari o neurologiche, la sua realizzazione non deve far ritardare l'inizio del trattamento. L'esplorazione laboratoristica oggettiva una sindrome infiammatoria generalmente importante (velocità di sedimentazione [VS] superiore a 80 mm). Una colestasi anitterica è osservata con notevole frequenza. Le indagini immunologiche contribuiscono alla diagnosi solo per la loro negatività e hanno soltanto un interesse limitato. La lesione uditiva nella malattia di Horton è rara e pone il problema della diagnosi differenziale con la presbiacusia. Tuttavia, un'evoluzione rapida della sordità lascia pochi dubbi rispetto a una presbiacusia e deve far sospettare la malattia di Horton come fattore causale o aggravante della sordità. In assenza di trattamento, la malattia di Horton causa un rischio funzionale essenzialmente legato alle lesioni oculari (in un caso su due, con rischio di cecità nel 20% dei casi) e vitale legato alle lesioni vascolari dei grossi vasi. La terapia corticosteroidea è il trattamento essenziale della malattia di Horton, come della maggior parte delle vasculiti. La possibilità di comparsa di complicanze vascolari (infarto del miocardio, accidenti vascolari cerebrali, occlusioni arteriose in genere) secondarie all'introduzione della terapia corticosteroidea, senza che la sua imputabilità sia certa, giustifica, per alcuni, l'associazione di un trattamento anticoagulante o antiaggregante al momento dell'inizio della terapia corticosteroidea. Sotto trattamento, l'evoluzione è favorevole in modo spettacolare: i sintomi clinici regrediscono in alcune ore o in alcuni giorni e i segni laboratoristici in alcuni giorni (PCR) o in alcune settimane (VS).
|
Tabella 3 - Criteri diagnostici della malattia di Horton secondo i criteri dell'American College of Rhumathology .
|
|
Inizio della malattia dopo i 50anni Cefalee recenti Sensibilità o diminuzione delle pulsazioni di un'arteria temporale Velocità di sedimentazione superiore a 50 mm alla prima ora Biopsia dell'arteria temporale che mostra dei segni di vasculite con infiltrato di cellule a mononucleate o granuloma con presenza di cellule giganti |
Malattia di Lyme
Anche se causato dalle spirochete Borrelia burgdorferi, molti dei suoi sintomi possono essere mediati da autoimmunità attraverso la produzione di anticorpi anti-fosfolipidi (APLA). Altre infezioni associate alla produzione di APLA sono HIV, EBV, parvovirus, epatite A, B, e C, rosolia, parotite e, la sifilide.
Periarterite nodosa
La periarterite (o panarterite) nodosa (PAN) è una vasculite necrotizzante che colpisce preferenzialmente le arterie di medio calibro dirette ai visceri (renali, epatiche, coronarie, il tronco celiaco e le arterie mesenteriche) e le piccole arterie che corrispondono alle arterie intraparenchimali che si connettono alle arteriole 49. Il 70% ha una malattia renale. In questi vasculiti, perdita dell'udito è spesso abbastanza rapido, coerente con una patogenesi vascolare. Paralisi del nervo facciale risultante dalla vasculite all'interno del canale facciale è una manifestazione ben descritto di PAN.
Le arteriole sono poco o per nulla interessate. L'incidenza annuale è di 5-10 per 100 000 abitanti, uguale nei due sessi [Pettigrew et al.,2007]. Essa interessa tutte le età, con una prevalenza tra i 40 e i 60anni.
La gravità della PAN è definita dalla presenza di una proteinuria superiore a 1 g/24 h; di un'insufficienza renale con creatininemia superiore a 140 μmol/l, di una cardiomiopatia, di una lesione digestiva grave e di una lesione del sistema nervoso centrale. La lesione audiovestibolare è segnalata raramente.
Sarcoidosi
La localizzazione della sarcoidosi è principalmente polmonare e linfonodale. Essa è caratterizzata dalla formazione di ammassi cellulari chiamati granulomi sarcoidei, che svolgono un ruolo nell'infiammazione. Questi ammassi si formano soprattutto nei polmoni, ma possono interessare qualunque organo [Baughman et al.,2001; Nunes et al.,2007]. L'esame oculistico è necessario, alla ricerca di un'uveite [Baughman et al.,2010; Takase et al.,2010].
La lesione uditiva si manifesta con acufeni e, più raramente, con una sordità, di cattiva prognosi [Cama et al.,2011;, Fusconi et al.,2011].
Lupus sistemico
Il suo altro nome è il lupus eritematoso acuto disseminato. È una malattia infiammatoria cronica, che colpisce numerosi organi come la cute, i reni, le articolazioni, i polmoni e il sistema nervoso, da cui il termine di sistemico. La parola lupus (lupo in latino) fa riferimento all'aspetto caratteristico a forma di maschera della lesione del volto. Sono descritti delle sordità lentamente progressive o a instaurazione improvvisa [Sugiura et al.,2006] e, diversamente, degli acufeni e delle vertigini [Karatas et al.,2007] . Sono state ipotizzate delle lesioni della stria vascolare e del legamento spirale con microinfarti capillari o arteriolari [Veldman et al.,1988], in particolare per la presenza di anticorpi anticardiolipici (sindrome degli antifosfolipidi) all'origine di microtrombi della vascolarizzazione labirintica [Green L., Miller E.B. 2001]. La risposta alla terapia corticosteroidea è incostante.
Sono state pubblicate delle associazioni, in un piccolo numero di casi, tra sordità e malattia di Crohn, dermatomiosite e polimiosite, sindrome di Susac, sindrome degli antifosfolipidi [Kang K.T., Young Y.H.2008; Wang et al.,2009]], sclerosi sistemica progressiva [Crawley et al.,2009], malattia di Takayasu [Smith et al.,2004] e malattia di Kawasaki [Magalhaes et al.,2010;Kara et al.,2007].
La presenza di una ricca rete linfatica in vicinanza del sacco endolinfatico e la presenza delle cellule immunocompetenti (linfociti T e macrofagi) hanno portato a ipotizzare un'origine immunitaria per la malattia di Ménière [Semaan MT, Megerian CA 2011]. Si ammette che il termine di malattia di Ménière possa applicarsi alle forme semplicemente cocleari o vestibolari della malattia [Committee on Hearing and Equilibrium guidelines 1995], che sono sospettate di avere una causa autoimmune in una proporzione che arriva a un terzo dei casi [Hughes et al.,1983]. L'ipotesi autoimmune nella malattia di Ménière è suffragata da numerosi indizi sperimentali e clinici:
• possibilità di indurre un'idrope sperimentale con iniezione di antigene o di autoanticorpo monoclonale [Yoo T.J. 1984];
• presenza di numerosi antigeni dell'orecchio interno testati nella malattia di Ménière: collagene III [Yoo T.J. 1984], IV, proteina PO [Hefeneider et al.,2004], beta-tubulina [Yoo et al.,2002], beta actina [Boulassel et al.,2001] Raf-1 [Yoo et al.,2002], proteina 68 kDa [Kawaguch et al.,2008];
• deposito di complessi immuni circolanti nel 21-96% dei pazienti affetti da malattia di Ménière [Brookes G.B. 1986];
• presenza di anticorpi antivirali [Yoo et al.,2002];
• più alta percentuale di lesioni sistemiche autoimmuni nei pazienti affetti da malattia di Ménière rispetto a un gruppo controllo;
• associazione all'allele CW7 del complesso maggiore di istocompatibilità (CMH) [Xenellis et al.,1986] ;
• presenza di un'idrope endolinfatica come indicatore istologico nell'osso temporale di pazienti affetti da malattia di Ménière [Merchant et al.,2005; Sajjadi H., Paparella M.M. 2008];
• efficacia del trattamento corticosteroideo [Ozer et al.,2008].
Tuttavia, la diagnosi è essenzialmente clinica e la presenza di indicatori immunologici quali gli anticorpi anti-heat shock protein 70 (HSP-70), il tumor necrosis factor alpha (TNF-α), gli ANCA e gli anticorpi antifosfolipidi [Yehudai et al.,2006] non sembra essere positivamente correlata alla malattia di Ménière, né essere predittiva dell'efficacia del trattamento corticosteroideo Suslu et al.,2009.
La sordità improvvisa è una sindrome definita da un' ipoacusia neurosensoriale monolaterale di almeno 30 dB su almeno tre frequenze audiometriche contigue, comparsa o instaurata in meno di 24-72 ore e di eziopatogenesi sconosciuta. La sordità brusca rappresenta circa l'1% delle ipoacusie neurosensoriali. Se ne contano circa 15 000 nuovi casi ogni anno nel mondo. Sono proposte numerose ipotesi eziopatogenetiche, tra cui l'infezione virale e le cause vascolari, neurologiche e traumatiche. Una causa tumorale benigna (schwannoma, meningioma) o maligna (linfoma, multiplo, metastasi) deve essere ricercata di principio attraverso un bilancio di diagnostica per immagini. Benché una sordità brusca possa essere associata a una malattia autoimmune, realizzando una delle manifestazioni cliniche della malattia, non è dimostrato che una sordità brusca isolata al di fuori di ogni contesto disimmunitario possa presentare una fisiopatologia autoimmune. Inoltre, i bilanci immunologici realizzati nel quadro di una sordità brusca non forniscono elementi di orientamento diagnostico a favore di un'origine autoimmune.
Sordità neurosensoriale rapidamente progressiva
L'ipotesi della natura autoimmune di una sordità neurosensoriale rapidamente progressiva rispetto a una sordità improvvisa è suffragata da una presentazione clinica differente: comparsa rapidamente progressiva (alcune settimane o mesi) piuttosto che brusca (poche ore), bilaterale (contro monolaterale), asimmetrica e, talvolta, fluttuante. Essa realizza, a volte, un'evoluzione alternante. Alla sordità possono essere associate delle vertigini, con un deficit vestibolare spesso bilaterale, che può arrivare fino all'areflessia vestibolare bilaterale. Talvolta, si riscontra una sensazione di pienezza dell'orecchio e la presentazione clinica può simulare in ogni punto una malattia di Ménière. La presenza di acufeni è variabile. Essa interessa tutte le fasce di età, con una leggera predominanza femminile 81. L'audiometria non ha alcun carattere specifico. Le curve possono essere ascendenti. Il tipo più frequente è una curva a plateau con caduta sugli acuti, ma sono stati descritti tutti i profili. Si ricordano due elementi di orientamento supplementare: la sordità mono- o bilaterale è migliorata dal trattamento immunosoppressivo e una malattia autoimmune, di qualunque tipo, è, a volte, riscontrata nell'anamnesi familiare o personale del paziente, in modo che la sordità sarebbe, così, la manifestazione iniziale della malattia autoimmune sistemica.
Vi è poca specificità clinica, ma la lesione bilaterale fin dall'inizio o la lesione controlaterale, la rapidità di evoluzione e il miglioramento a volte spettacolare con un trattamento corticosteroideo devono far ricercare una causa immunologica.
Come è diagnosticata la malattia autoimmune dell'orecchio interno?
La diagnosi si basa sull’anamnesi ( storia), sui risultati dell’ esame fisico, sugli esami del sangue, sui risultati dell’esame audiometrico e vestibolare, la risonanza magnetica, e la risposta ai farmaci immunosoppressivi. Il quadro clinico usuale è una subacuta bilaterale progressiva perdita dell'udito neurosensoriale .

Paziente con una perdita uditiva che in parte ha risposto agli steroidi per diverse settimane.
§ Perdita progressiva dell'udito bilaterale o progressiva vestibolare (equilibrio) perdita
§ Audiometria documentare progressiva sordità neurosensoriale bilaterale
§ ABR (se l'udito è abbastanza buono), o il test delle emissioni otoacustiche
§ Test CON sedia Rotatoria
§ ECOG (elettrococleografia)
§ Gli esami del sangue per la malattia autoimmune generale
§ ANA (per il lupus)
§ Velocità di sedimentazione eritrocitaria
§ Raji-Cell
§ Fattore reumatoide
§ Complemento C1Q
§ Anticorpo del muscolo liscio
§ Malattie della tiroide [ormone stimolante la tiroide (TSH), anti-microsomiale
anticorpi tireoglobulina]
§ Gli anticorpi anti-gliadina e anti-endomisio (per la malattia celiaca)
§ Anticorpi anti-citoplasma neutrofili
§ Anticorpo cellula Antiendoteliali
§ Antifosfolipidi / anticorpo anticardiolopina
§ antigeni dei leucociti umani testing (HLA)
I medici possono ordinare alcuni o tutti questi test, che non sono specifici per AIED, ma possono dare evidenza di malattia autoimmune nel paziente (Garcia-Berrocal et al 2005).
§ Gli esami del sangue per specifiche patologie dell'orecchio interno
§ Test degli anticorpi anti-cocleare
§ Test di trasformazione dei linfociti
§ Immunofluorescenza della coclea animali (solo ricerca)
Questi anticorpi non sono presenti in tutti i pazienti con AIED, e possono essere presenti in alcuni pazienti senza evidenza di perdita dell'udito.
§ Gli esami del sangue per i disturbi che possono imitare AIED
· FTA (per sifilide )
· HBA1C (per il diabete, che è spesso anche autoimmune )
· HIV (HIV è associato a neuropatia uditiva nonché sifilide )
· Titolo di Lyme
· Risposta alla terapia steroidea per via orale (Ruckenstein, 2004)
Recentemente è stato suggerito che i livelli ematici di TNF, fattore di necrosi tumorale, è sia diagnostico e predittivo di risposta al trattamento (Svarkic, 2012). Come TNF è una citochina infiammatoria aspecifica, siamo dubbia in quanto riteniamo che il TNF dovrebbe logicamente essere elevata in molte condizioni.
Test di risonanza magnetica è fatto principalmente per escludere altre entità, ma di tanto in tanto il miglioramento è visto della coclea.
Diagnosi differenziale della malattia autoimmune dell'orecchio interno
· meningite compresa la sifilide
· Menieres (anche se è spesso AIED comunque di Meniere forse bilaterale).
· carcinosi (incredibilmente raro)
· ototossicità (compresi aminoglicosidi, nonsteroidals, chemioterapia)
· fonti genetiche della perdita dell'udito
· forme bilaterali di perdita dell'udito neurosensoriale prevalentemente unilaterale
· rumore
· tumori bilaterali come in neurofibromatosi
Per la maggior parte, questa è la diagnosi differenziale della progressiva sordità neurosensoriale bilaterale. (Kishimoto et al, 2013)
Non vi è attualmente nella pratica corrente un test abbastanza affidabile per confermare la diagnosi di lesione cocleovestibolare autoimmune, cioè che permetta di evidenziare delle cellule immunocompetenti o degli anticorpi circolanti diretti contro delle strutture del labirinto Frachet B,ed Al.,2008. La sensibilità (Se) e la specificità (Sp) dei vari test proposti in letteratura sono discutibili e devono essere interpretate con cautela, in quanto, in assenza di comparatori standard o gold standard, esistono numerose distorsioni metodologiche, distorsione di reclutamento, di controllo e di logica circolare, conducendo a una sovrastima probabile della Se e della Sp dei test, il che si manifesta, in particolare in letteratura, con una grande variabilità in funzione degli studi Hughes G.B.,1986 .
La realizzazione del bilancio complementare, in particolare laboratoristico, è in funzione dell'anamnesi (precedenti personali e familiari, ricerca di un trauma anche antico, sindrome virale recente, vaccinazione recente e assunzione di un farmaco ototossico) e della clinica. L'esame otoscopico e vestibolare è completato con delle misure audiologiche soggettive (audiometria) e, a volte, oggettive (potenziali evocati uditivi, otoemissioni evocate acustiche provocate) e con delle prove vestibolari strumentali. Quando una lesione cocleovestibolare accompagna un'altra malattia disimmunitaria conosciuta, il bilancio sarà quello di quest'ultima (Tabella 4 ) e l'iter clinico è, di solito, simile a quello del medico internista Papo T.,2006 . Tabella 5
|
Tabella 4 - Indagine autoimmune: principali esami complementari di prima intenzione (secondo [84]). |
|
EMS-piastrine, PCR, ionogramma ematico, creatinina, test epatici Latex-Waaler Rose, anticoagulante circolante, anticardiolipina, C3, C4, CH50 Esame oftalmologico (compresi fondo dell'occhio e ricerca di una sindrome sicca) Capillaroscopia b Biopsia delle ghiandole salivari accessorie c Radiografia delle mani d |
|
Didascalia :
|
|
Tabella 5 - Indagine autoimmune: principali esami complementari di seconda intenzione. |
||
|
||
|
||
|
Didascalia : |
[a] Gli anticorpi anti-ENA possono essere presenti mentre la ricerca globale di fattori antinucleari è negativa. Gli antigeni nucleari solubili sono soprattutto Sm, SSA oppure Ro, SSB o La e RNP.
[b] Soprattutto in caso di sindrome di Raynaud, alla ricerca di megacapillari presenti nella sclerodermia, ma anche nella dermatomiosite, nella connettivite mista o, più raramente, nel lupus.
[c] Da discutere, anche in assenza di sindrome sicca, alla ricerca di un infiltrato linfoide (Gougerot-Sjögren) o di un granuloma (tenendo presente che la sarcoidosi non è «autoimmune»).
[d] Ricerca di calcinosi o di artrite.
Test non specifici dell'orecchio interno
Un bilancio infiammatorio (VS, PCR) è realizzato sistematicamente. Secondo il risultato, è richiesto un bilancio complementare che comprenda delle sierologie virali, della sifilide o della malattia di Lyme, un'elettroforesi delle proteine sieriche, le immunoglobuline sieriche e dei dosaggi sanguigni alla ricerca di diverse stimmate di malattia autoimmune: crioglobuline, complessi immuni circolanti, dosaggio del complemento, fattore reumatoide, fattori antinucleari, anticorpi anticitoplasma dei polimorfonucleati neutrofili (ANCA), anticorpi non specifici (antinuclei, antitireoglobulina, antimitocondrio, antimuscolatura liscia e striata, antimicrosomi tiroidei, anticellule parietali gastriche, antiendotelio, antifosfolipidi, antimicrosoma epatico e renale, antireticolo) Lobo D., ed Al.,2008. Uno studio recente retrospettivo Hervier B, ed Al.,2010, su 49 pazienti che presentavano una sordità progressiva idiopatica non mostra alcun valore predittivo della positività degli Ac non specifici sull'efficacia di una terapia corticosteroidea. Nella malattia di Ménière che si presenta sotto forma di sordità fluttuante si riscontrano più spesso rispetto a dei soggetti normali dei complessi immuni circolanti Brookes G.B., Newland A.C. ed Al., ,1986. La ricerca di un gruppo HLA particolare può rinforzare gli argomenti a favore di una patologia autoimmune, in particolare se vari esami precedenti orientano verso una lesione disimmunitaria. La presenza isolata di un autoanticorpo non è sufficiente a definire una malattia autoimmune e l'ipotesi diagnostica di sordità autoimmune deve essere avanzata solo su un insieme di elementi clinici e paraclinici.
Test specifici dell'orecchio interno
I test di trasformazione linfoblastica (TTL), che esplorano l'immunità cellulare, e i test di Western blot, che esplorano l'immunità umorale, sono dei test antigenici specifici dell'orecchio interno. I test di inibizione di migrazione leucocitaria, di affidabilità insufficiente, sono stati abbandonati.
Test di immunità cellulare (TTL)
Dopo aver posto in incubazione dei linfociti di pazienti con antigeni (Ag) dell'orecchio interno di origine umana, si può misurare la loro stimolazione se sono stati sensibilizzati precedentemente in occasione di un processo autoimmune. La realizzazione di questi test richiede di raccogliere degli estratti di labirinto membranoso umano nel corso di un intervento per via translabirintica. I risultati forniti sono su un numero limitato di pazienti e la relazione con un miglioramento sotto corticosteroidi è molto variabile. È stato segnalato un aumento della produzione di interferone γ da parte delle cellule T poste in presenza di antigeni dell'orecchio interno umano Lorenz R.R., ed Al., 2002. La realizzazione pratica di questo esame richiede sangue fresco trasferito rapidamente al laboratorio ed è stata condotta solo da un numero molto ristretto di equipe [Lejeune J.M., Charachon R.,1991 , Hughes G.B., ed Al., 1986]. Hughes et Al. riferivano una Se stimata tra il 50% e l'80%, una Sp del 93% e un valore predittivo positivo del 56-73% in funzione della prevalenza della malattia testata nella popolazione 83. Nessun test è specifico. È difficile attribuire un valore diagnostico. Il trattamento corticosteroideo crea più falsi positivi con il TTL che in Western blot Harris J.P., ed Al.,.,1989.
Test di immunità umorale
Immunofluorescenza indiretta (IFI)
Il principio si basa sulla visualizzazione, a partire da sezioni di osso temporale umano o animale, della fissazione di anticorpi umani prelevati dal siero dei pazienti, che permette di confermare che il siero contiene gli anticorpi specifici diretti contro le strutture dell'orecchio interno o non specifici (altri tessuti). La sensibilità è variabile, secondo gli studi, così come la soglia di positività, che si situa tra il 50% e il 75% Zeitoun H., ed Al.,2005 ,. Anche la specificità è mediocre e dipende in particolare dal supporto tissutale usato per evidenziare la presenza degli anticorpi sierici del paziente Disher M.J., ed Al., 1997. Le tecniche di immunofluorescenza indiretta non sono di realizzazione agevole e forniscono indicazioni solo sulla sede di fissazione degli autoanticorpi e, quindi, sulla loro presenza o meno, senza aspetti quantitativi. La loro interpretazione è delicata e dipende dalla tecnica utilizzata, dall'utilizzo di osso temporale umano o animale, dall'assenza di valori standard e dall'esistenza di falsi positivi.
Western blot
Il principio del test si basa sulla localizzazione e sull'individuazione degli autoanticorpi circolanti specifici rispetto a diversi Ag presenti nel labirinto umano seguendo la loro migrazione su un supporto a seconda della loro dimensione e del loro peso. È il test attualmente più utilizzato. Sono stati studiati numerosi antigeni candidati come bersagli nella sordità autoimmune: collagene tipo II, Po-mielina, β-actina, β-tubulina e diverse proteine di peso molecolare di 30, 32, 33, 34, 35 58, 68, 220 kDa [Yehudai D., ed Al.,2006, Suslu N., ed Al.,2009, Lobo D., ed Al.,2005, Garcia-Berrocal J.R., ed Al.,2010 ] (Tabella 6 ).
|
Tabella 6 - Algoritmo nella prescrizione degli autoanticorpi disponibili fuori laboratorio di ricerca in funzione della diagnosi sospettata (secondo [84]). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Didascalia FAN: fattori antinucleari; DNA: acido desossiribonucleico; PR3: antiproteinasi 3; ANCA: antineutrophil cytoplasmic antibodies; MPO: mieloperossidasi; CCP: citrullinated protein antibodies. 1: in prima intenzione; 2: in seconda intenzione; x: facoltativo. [a]La ricerca di anticardiolipina è associata a quella di un anticoagulante circolante, con due determinazioni a 6 settimane di intervallo
|
Alcuni autoanticorpi non specifici dell'orecchio interno sono stati inizialmente incriminati. È il caso degli anticorpi anticollagene II Yoo T.J.,2003 si è, infine, dimostrato che essi non avevano alcun ruolo nella sordità autoimmune Lopez-Gonzalez M.A., 1999 . Altri antigeni sono stati oggetto di studi complessivamente concordanti: gli Ac diretti contro una proteina di 68 kDa sono stati frequentemente riscontrati in Western blot fino nel 60% circa dei casi di ipoacusie neurosensoriali evolutive isolate, ma anche in altre patologie infiammatorie extralabirintiche [Agrup C., ed Al.,2006, Park S.N., ed Al.,2006]. Questa proteina corrisponderebbe, per alcuni autori, alla proteina di shock termico (HSP-70), proteina cellulare liberata in caso di stress cellulare Bonaguri C., ed Al.,2007 , mentre, per altri, alla choline transporter-like protein 2 (CTL2) Mogan R.F., ed Al.,1934 .
La proteina HSP-70 è stata oggetto del più grande numero di studi, nella sordità improvvisa Park S.N., ed Al. 2006 e progressiva Zeitoun H., ed Al. 2005 e nella malattia di Ménière Rauch S.D., ed Al. 2000, ed è stato posto in commercio un kit di dosaggio. Il suo dosaggio non è, tuttavia, di pratica corrente e richiede un laboratorio di biologia altamente specializzato.
Gli autoanticorpi responsabili delle sordità autoimmuni bloccherebbero questo trasportatore CTL2, il che avrebbe per effetto una degenerazione delle cellule dell'organo di Corti Hervier B., ed Al.,2010 . La distribuzione del CTL2 non sarebbe, tuttavia, limitata soltanto alle cellule dell'organo di Corti, e la sua vicinanza a isoforme della coclina fa sospettare una cofunzione nel trasporto di molecole dall'ambiente extra- all'ambiente intracellulare delle cellule dell'orecchio interno Kommareddi P.K., ed Al.,2010 . Sono così state prodotte delle sordità autoimmuni sperimentali nell'animale Billings P.,2010 . Si sa, d'altra parte, che una mutazione del gene che codifica per la coclina porta a una sordità neurosensoriale ereditaria isolata (DFNA9). Sono state evidenziate delle cellule immunocompetenti sensibilizzate nei confronti della coclina in alcune ipoacusie neurosensoriali di aspetto autoimmune Baek M.J., 2006, ma non vi sono ancora studi su un numero sufficiente di casi in diverse patologie cocleovestibolari per poter giungere a una conclusione. Inoltre, il carattere immunogeno del CTL2 resta da dimostrare nell'animale. Tuttavia, questa proteina specifica dell'orecchio interno sembra una pista di ricerca interessante, ma non è ancora stata realizzata la messa a punto di un esame a scopo diagnostico.
Punto importante
• I test di laboratorio non hanno né la sensibilità né la specificità sufficienti per confermare la diagnosi e sono solo degli argomenti di presunzione che orientano verso una sordità autoimmune.
• Gli esami di laboratorio e immunologici completi con lo scopo di «cercare di orientarsi» sono da proscrivere.
• Un'esplorazione laboratoristica mirata, basata sui profili di rischio dei pazienti e orientata dall'indagine diagnostica, sembra fornire un'efficacia diagnostica equivalente a quella di un bilancio completo cinque volte più costoso 102.
Altri test
È richiesto un fondo dell'occhio con esame della camera anteriore (esame alla lampada a fessura) e posteriore, alla ricerca di segni infiammatori quali uveite, sclerite ed episclerite.
Una capillaroscopia mira a osservare, a livello della microvascolarizzazione dei capillari ungueali, dei segni di vasculite con alterazione della microvascolarizzazione, quali degli aggregati di emazie (sludge), un microaneurisma, una vasculite e un'acrocianosi Lejeune J.M.,Charachon R. ed Al.,1992 . Il suo interesse è limitato.
La realizzazione di una RM cerebrale della fossa posteriore e dell'orecchio interno è sistematica in prima intenzione di fronte a qualsiasi sordità neurosensoriale asimmetrica, alla ricerca di una patologia retrococleare Saliba I. ed Al.,,2009 . La metodica RM ad alta risoluzione dovrebbe permettere in futuro una migliore risoluzione spaziale dei compartimenti endococleari 104. L'infiammazione della membrana labirintica nella sordità autoimmune permette un accumulo di gadolinio negli spazi liquidi intralabirintici, ma non è specifica.
L'utilità della tomografia per emissione di positroni nei pazienti con sordità autoimmune è incerta Morita N.,2 ed Al.,2009 . Il ruolo dei potenziali evocati uditivi del tronco cerebrale è limitato. La TC delle rocche conserva un ruolo importante, in particolare nel bambino, alla ricerca di anomalie morfologiche del labirinto.
La diagnosi si basa sulla storia, i risultati su esame fisico, esami del sangue, ed i risultati di ascolto e prove vestibolari. Come neuropatia uditiva può presentare con una ipoacusia neurosensoriale bilaterale progressiva, test ABR dovrebbe essere fatto in persone con sufficiente udienza per la prova di essere pratici. Prove delle emissioni otoacustiche può essere fatto in quelli in cui il test ABR non può essere fatto a causa di udienza gravemente compromessa. ECOG (elettrococleografia) test può anche essere utile.
Mentre i test specifici per l'autoimmunità all'orecchio interno sarebbe auspicabile, a partire dal 7/2012, non ce ne sono che sono disponibili in commercio e ha dimostrato di essere sempre utile. Questo è un settore che si sta evolvendo rapidamente comunque. E 'generalmente ritenuto che anticorpi anti-cocleare (detta anche anti-HSP70) analisi del sangue non sono sensibili o abbastanza specifico per essere molto utile. Anticorpi anti-HSP 70 si possono trovare anche nella malattia di Lyme, colite ulcerosa, tumori e in circa il 5% di individui sani. Uno studio ha suggerito che tutti i test anti-HSP sono diretti contro il substrato sbagliato (Yeom et al 2003).
Se questo è vero o no, a causa della scarsa specificità di anti-HSP 70 test, la diagnosi si basa generalmente su prove di test più ampi di autoimmunità o di una risposta positiva agli steroidi. Immunofluorescenza di cellule di supporto di organi cavia del Corti è stato anche dimostrato di correlare con la malattia e la reattività di steroidi. Secondo Gray e altri, immunofluorescenza è più sensibile e specifico (86%, 41%) che è Western Blot (59%, 29%) (Gray e altri, abstract ARO, 1999 # 246). La specificità di entrambe le prove a noi sembra inaccettabilmente bassi.
Anche se ci sono alcuni individui con AIED che sembrano avere in primo luogo una presentazione bilaterale vestibolare (vertigini, atassia, oscillopsia), molto poco si sa circa il meccanismo così come se o non esami del sangue sono utili in questa popolazione. Questo potrebbe essere un argomento interessante per ulteriori ricerche (vedi sotto).
Come ci sono attualmente test specifici per AIED, un approccio comune è quello di cercare altre prove di un coinvolgimento autoimmune. Un gran numero di questi sono elencati sopra, e la ricerca ha successo tra il 20 e il 30% del tempo. Non è generalmente ritenuto che le persone con AIED bisogno di ognuno di questi esami del sangue. Generalmente un tasso sed e ANA sono fatti in tutti. Gli altri sono selezionati sulla base di sospetto clinico.
Ci sono anche condizioni che somigliano malattie autoimmuni, che a volte è prudente escludere (vedi sopra).Generalmente un FTA (per escludere l'infezione da sifilide) è fatto in tutti i casi in cui vi sia un ragionevole sospetto di AIED e altre prove sono effettuate sulla base di sospetto clinico.
Come è trattata la malattia autoimmune dell'orecchio interno?
Trattamento per AIED sembra essere in rapida evoluzione. Si consiglia di non fare affidamento sulle informazioni qui come corrente, come sembra molto probabile che ci possono essere progressi dal momento che questa pagina è stata aggiornata.
Terapia corticosteroidea(da EMC 2012)
È il solo trattamento validato che dimostra un'efficacia nella sordità autoimmune ed è spesso proposto in prima intenzione come test terapeutico, in assenza di test diagnostici specifici. La sua efficacia almeno parziale è presente in circa un caso su due Broughton S.S., ed Al.,2004 , con tanto più successo se la presunzione diagnostica in base agli elementi clinici e paraclinici è forte. Non esiste, tuttavia, alcuna correlazione tra la risposta terapeutica nella sordità improvvisa idiopatica e la presenza di anticorpi diretti contro l'orecchio interno Hervier B., ed Al.,2010 . I protocolli di trattamento variano secondo gli autori. Nell'adulto, la dose raccomandata varia tra 1 e 2 mg/kg al giorno di equivalente metilprednisolonico per 4 settimane.
Il trattamento è instaurato per via orale, poiché la terapia corticosteroidea per boli endovenosi non è stata valutata al di fuori del quadro delle sordità improvvise. Il grado di urgenza dell'instaurazione del trattamento è discutibile. Se, in teoria, un trattamento precoce mira ad agire prima che le lesioni dell'orecchio interno siano irreversibili, l'iter diagnostico richiede spesso un periodo di diversi giorni, in particolare per le indagini di laboratorio. Inoltre, i meccanismi fisiopatologici della sordità autoimmune non sono indubbiamente gli stessi della sordità improvvisa, mentre, in quest'ultima, è anche rimessa in questione la gestione terapeutica urgente Tran Ba Huy P., Sauvaget E., ed Al.,2007 . La durata di steroidi necessarie per accertare vera risposta steroide rimane incerta. Mentre molto brevi corsi (ad esempio, Medrol Dosepack) sono a volte efficaci, che molti considerano meno di un mese troppo breve per permettere ripartizione delle immunoglobuline. Harris e Ryan consiglia una prova di 1 mese di steroidi, che potrebbe essere proseguita per altri 1 - 2 mesi, a seconda della risposta.In assenza di una risposta ai corticosteroidi durante le prime quattro settimane, l'interruzione della terapia corticosteroidea è realizzata in un periodo di almeno 7 giorni a dosi progressivamente decrescenti. Nei pazienti che rispondono, può essere proposta una dose di mantenimento di 20-30 mg/die per diverse settimane 19 fino a un massimo di 6 mesi [Hervier B., ed Al.,2010, Hervier B., ed Al.,2010 ]. Né i trattamenti di breve durata (per esempio, 5 giorni in cura breve) né quelli istaurati a lungo corso per numerosissimi mesi sembrano efficaci Mogan R.F., Baumgartner C.J. ed Al., ed Al.,1934 . Un nuovo ciclo di corticosteroidi è somministrato in caso di recidiva, ma le ricadute rapide e iterative si scontrano con il problema della terapia corticosteroidea prolungata (effetti collaterali e inibizione dell'asse ipotalamoipofisario).
Gli steroidi possono essere somministrati per via transtimpanica. Parnes, et al., Ha riferito l'uso di desametasone o metilprednisolone somministrato a 37 pazienti. Ha trovato notevole miglioramento in diversi casi di sordità improvvisa, ma nessun beneficio nei pazienti con idrope cocleare o quelli con un improvviso peggioramento di una perdita uditiva preesistente. 8% ha sviluppato una otite media transitori ma nessuno ha sviluppato la perdita di udito indotta dal trattamento o perforazioni timpanica permanenti.
Nel bambino, l'instaurazione del trattamento deve prendere in considerazione i rischi specifici della terapia corticosteroidea su un organismo in crescita.
Un trattamento alternativo alla terapia corticosteroidea con ciclofosfamide (Endoxan ® ) Huang N.C., Sataloff R.T.,2011 è stato proposto da Mac Cabe 109 o nei soggetti che non rispondono più ai corticosteroidi o quando una terapia corticosteroidea non è più possibile a causa degli effetti secondari o quando essa è rapidamente abbandonata a causa della sua elevata tossicità (cistite emorragica, mielosoppressione, tossicità polmonare, rischio di sterilità) o, per alcuni, dopo la terapia corticosteroidea, per stabilizzare il risultato funzionale acquisito nei soggetti che rispondono. Sono state sperimentate altre terapie farmacologiche immunomodulatorie, come il metotrexate [Matteson E.L., ed Al.,2003, Harris J.P., ed Al.,2003 ], Questi Anti-metaboliti, come il metotrexato e la ciclofosfamide vengono utilizzati per risparmiare ai pazienti il rischio di uso di steroidi a lungo termine. Per i pazienti senza controindicazioni, il metotrexato è prescritto a 7,5 mg / settimana come una singola dose. L'acido folico, 1mg / die è dato anche per ridurre al minimo la stomatite. Tuttavia, questi farmaci presentano i propri rischi e devono essere attentamente monitorati, di solito con l'assistenza di un reumatologo. Alcuni dei rischi di metotrexato includono anemia e trombocitopenia, epato- e nefrotossicità, e problemi polmonari. Alcuni dei rischi di ciclofosfamide (Cytoxan) includono soppressione del midollo, la sterilità, cistite emorragica, il cancro della vescica, e aumento del rischio di linfoma.l'etanercept (anti-TNF-α; Enbrel ® ) Lobo D., ed Al., ed Al.,2003 , Etanercept (Enbrel) è un promettente agente per il trattamento di AIED (Rahmen et al, 2001; Wang et al, ed Al.,2003). Enbrel è un farmaco anti-TNF (fattore di necrosi tumorale). TNF è una citochina infiammatoria (vedi sopra). Wang et al ha recentemente riferito che etanercept data acutamente in sterile labirintite sperimentale portato a risultati molto migliori di udito in un modello animale. D'altra parte, Cohen et al (2005) hanno riportato che Enbrel non era migliore del placebo in persone con AIED cronica a ripristinare l'udito perso alla malattia. Non riteniamo che questo è sorprendente o molto significativo, in quanto non ci si aspetterebbe che Enbrel può causare cellule ciliate di tornare alla vita dalla morte. Nella pratica clinica , abbiamo avuto in genere risultati molto buoni nei nostri pazienti con steroidi reattivi, procedendo AIED e riteniamo che a causa del disegno dello studio (perdita di udito cronica, nessun obbligo di risposta steroide), che Enbrel è ancora la pena di provare.
Enbrel è somministrato per iniezione sottocutanea una volta / settimana, di solito tra 25 e 50 unità. Enbrel è stata generalmente ben tollerata, ma in base alle informazioni del produttore, i pazient trattati con Enbrel hanno sviluppato infezioni gravi (2%), disturbi del sistema nervoso e disturbi di depressione / personalità (1%). l'infliximab (Remicade ® ), anticorpo chimerico monoclonale anti-TNF-α Liu Y.C., ed Al.,2011, Un agente correlato, (infliximab) Remicade, non è stato trovato utile per AIED, ma questo studio si è basato solo su pochi casi (Pyykkö et al, 2002). Inflixamab è stata trovata utile in un altro studio (Heywood, 2013). l'asatiopirina (Imurel ® ) Saracaydin A., ed Al.,1993 , la ciclosporina A (Neoral ® )Daneshi A., ed Al.,2002, il micofenolato sodio (Cellcept ® ) Rennebohm R.M., ed Al.,2006 e il rituximab (Mabthera ® ) Deane K.D. ed Al.,,2011 . È anche stata proposta un'associazione che utilizza metotrexate ed etanercept Street I., ed Al.,2006 . La conduzione del trattamento richiede un monitoraggio stretto (ematologico, biologico e radiologico) svolto da internisti e deve in ogni momento essere pronta a discutere il rapporto beneficio/rischio. Nessuno di questi trattamenti è stato oggetto di una validazione nell'indicazione della sordità autoimmune, che compare in modo isolato o nel quadro di una malattia sistemica. Solo il metotrexate è stato valutato in un recente ampio studio prospettico randomizzato controllato e non sembra un'alternativa terapeutica efficace ai corticosteroidi Harris J.P., ed Al.,2003 . La loro prescrizione non è, inoltre, esente da inconvenienti importanti: comparsa o riacutizzazione della tubercolosi, menopausa precoce e comparsa di neoplasie. Farmaci già disponibili nel mondo che sono anche agenti anti-TNF sono talidomide, pentossifillina (un vasodilatatore utilizzato per la cattiva circolazione), e rolipram (un antidepressivo disponibile in Giappone ed Europa). Questi farmaci non sono stati provati in AIED.
Nessuno di questi farmaci ha un'indicazione ufficiale di FDA per AIED. Recentemente c'è stata una certa preoccupazione in merito a questi farmaci che colpiscono altri problemi di salute come il modo in cui il corpo combatte l'infezione o uccide le cellule tumorali. In studi controllati di tutti i farmaci che bloccano il TNF-alfa, più casi di linfoma sono stati notati nei pazienti trattati rispetto ai controlli . I linfomi sono spesso visti con l'uso di altri immunosoppressori compresi azathiprine e / o mercaptopurina. Inoltre, è generalmente ritenuto che quando questi farmaci sono utilizzati ci dovrebbe essere una maggiore vigilanza per la riattivazione della tubercolosi.
La colchicina, utilizzata soprattutto in terapia per il suo effetto antinfiammatorio nella crisi di gotta, nella condrocalcinosi articolare, nella malattia periodica, nella malattia di Behçet, nella sclerodermia o in alcune forme cliniche di sarcoidosi e nella malattia da siero, è stata proposta anche nella sordità autoimmune. È un alcaloide estratto dalla colchica, che appartiene alla famiglia dei veleni del fuso e che impedisce la polimerizzazione dei microtubuli bloccando le cellule in metafase. La dose raccomandata è di 1 mg/die. Nell'animale, la colchicina modifica la regolazione dei fluidi del labirinto da parte del sacco endolinfatico Takumida M., ed Al.,1989 . La sua utilità nel trattamento delle sordità autoimmuni è incerta.
Attualmente, al di fuori di casi molto particolari e salvo la necessità di curare una patologia sistemica associata, il trattamento immunosoppressivo non ha, a nostro parere, alcun ruolo nel trattamento della sordità autoimmune.
Scambi plasmatici
Lo scambio plasmatico (o plasmaferesi) è fondato sul principio della depurazione del siero dalle gammaglobuline attraverso un procedimento simile a quello della dialisi per depurazione extrarenale. Esso è riservato, per alcuni, agli insuccessi di tutti gli altri trattamenti 120, senza, tuttavia, essere stato validato a tutt'oggi Luetje C.M., Berliner K.I. 1997. E 'stato anche riportato recentemente che plasmaferesi può essere utile nelle AIED (Bianchin et al 2010).Plasmaferesi è costoso, deve essere effettuata periodicamente (di solito mensilmente), è adatta solo per disturbi mediati da anticorpi.
Le immunoglobuline endovenose sono state proposte in quanto agenti immunoregolatori nel trattamento di patologie autoimmuni e infiammatorie, con un'efficacia paragonabile alle plasmaferesi, ma senza i loro inconvenienti Graff-Dubois S., ed Al.,2007 . La loro modalità d'azione è poco nota. Esse regolano le funzioni effettrici di numerose cellule del sistema immunitario, interagendo con un ampio spettro di attori del sistema immunitario, come le citochine, il complemento, i recettori Fc, nonché delle molecole di superficie. In Francia, esse non hanno alcuna indicazione nel trattamento della sordità autoimmune.
L'iniezione locale transtimpanica di agenti farmacologici, in primo luogo i corticosteroidi, ha diversi vantaggi: facilità di somministrazione sotto anestesia locale in visita ambulatoriale, costo modesto, diffusione passiva nell'orecchio interno di grandi concentrazioni della molecola Bird P.A., ed Al.,2011 , assenza di passaggio sistemico, eventuale trattamento sequenziale tra l'orecchio destro e sinistro e trattamento di seconda intenzione dopo l'insuccesso di un trattamento per via sistemica.
La somministrazione sistemica espone, infatti, a una grande variabilità di concentrazione del farmaco, che dipende dal suo profilo farmacocinetico. Gli effetti collaterali possibili sono legati al disagio che può essere sperimentato dal paziente al momento dell'iniezione, alla comparsa di vertigini, all'infezione, alla degradazione uditiva e alla perforazione timpanica residua. Diversi studi prospettici randomizzati nella sordità improvvisa mostrano un'efficacia paragonabile del trattamento locale in confronto con la terapia corticosteroidea per via sistemica Spear S.A., Schwartz S.R.,2004 . Non esiste attualmente alcuna prova di un'efficacia superiore della somministrazione transtimpanica, nel trattamento di prima intenzione, nel trattamento combinato oppure nel trattamento adiuvante di seconda intenzione. È, tuttavia, possibile, almeno in teoria, sperare in un'efficacia almeno equivalente nella sordità autoimmune rispetto alla sordità improvvisa. Buoni risultati sono stati descritti nel trattamento della sordità autoimmune, ma in piccole serie macchiate da distorsioni metodologiche Parnes L.S., ed Al.,1999 . Le terapie locali aprono delle prospettive nuove e promettenti le cui modalità esatte e i cui protocolli terapeutici sono un vasto campo di studio: iniezione intratimpanica, MicroWick™ di
Silverstein, diffusione mediante microcatetere asservito o meno a micropompe osmotiche, idrogel e trasportatori per nanoparticelle McCall A.A., ed Al.,2011 . Analogamente alla sordità improvvisa, il trattamento della sordità autoimmune è, almeno in teoria, molto adatto alla terapia locale. I suoi maggiori svantaggi sono legati ai fattori anatomici (copertura della nicchia della finestra rotonda da parte di mucosa o di tessuto connettivo in un terzo dei casi McCall A.A., ed Al.,2011 ), alla variabilità della diffusione per la perdita del principio attivo attraverso la tuba di Eustachio, alla variabilità delle condizioni fisiologiche e farmacocinetiche dell'orecchio medio (clearance attraverso la finestra rotonda, distribuzione nei compartimenti dell'orecchio interno), alla dose e alla concentrazione della molecola attiva da erogare determinate in maniera empirica
L'impianto cocleare è indicato [come ultima risorsa (Wang et al, 2010)], in caso di evoluzione verso una sordità profonda bilaterale, secondo le raccomandazioni ufficiali della gestione della sordità profonda. Esso può essere ipotizzato a uno stadio variabile della malattia, al termine dell'evoluzione rapida della sordità in alcune settimane o in alcuni mesi, oppure dopo un periodo più o meno lungo in cui il trattamento corticosteroideo, talvolta con immunosoppressori, ha permesso un recupero uditivo di qualità sufficiente, con o senza apparecchio, ma transitorio. L'indicazione non è, in linea di principio, da ipotizzare in urgenza, ma è opportuno valutare caso per caso, in funzione della causa, se esiste un rischio di fibrosi e/o di osteoneogenesi con il progressivo riempimento della rampa timpanica. I risultati dell'impianto cocleare nei pazienti con una sordità autoimmune sono simili a quelli ottenuti nelle altre eziologie Aftab S., ed Al. 2010 . Gli impianti cocleari sono estremamente costosi. A nostro parere, la gestione medica (vale a dire immunosoppressori) dovrebbe essere tentata prima.
La ricerca è necessaria per l’AIED
Le malattie autoimmuni dell'orecchio interno sono rare, il che rende difficile lo studio. Si può ipotizzare che ci potrebbero essere trattamenti efficaci che semplicemente non sono stati scoperti. Per esempio, ci sono numerosi trattamenti potenziali che non sono state provate in modo formale. Infusioni di gamma globulina, sono utili in numerosi disturbi autoimmuni. Questo trattamento è molto costoso, il che limita il suo utilizzo. Farmaci immunomodulatori quali vengono utilizzati per il trattamento della sclerosi multipla (beta-interferone, alfa-interferon, Copaxone) non sono stati provati nell’ AIED. Altri farmaci che hanno una soppressione delle risposte immunitarie, come la minociclina, o altri farmaci anti-TNF (vedi sopra), potrebbero essere processati.
CONCLUSIONI
In assenza di una prova diagnostica formale, clinica, laboratoristica e anatomopatologica, la sordità autoimmune non è, a tutt'oggi, un'entità nosologica ben definita. La capacità dell'orecchio interno di reagire a meccanismi immunitari è, tuttavia, ben dimostrata. È una forma rara di sordità neurosensoriale, di difficile indagine, la cui diagnosi è spesso di esclusione, al di fuori dei casi in cui si inserisce in un contesto autoimmune poliviscerale ricco e conclamato, a volte secondariamente confortata dopo una risposta positiva alle terapie corticosteroidee o immunosoppressive. Occorre ipotizzarla nelle forme isolate quando il bilancio eziologico di una sordità definita improvvisa o neurosensoriale progressiva è negativo. I test di laboratorio non hanno né la sensibilità né la specificità sufficienti per confermare la diagnosi e sono soltanto degli argomenti di presunzione che orientano verso una sordità autoimmune. La messa a punto di test specifici e accessibili in un laboratorio non specializzato resta una speranza ed è un filone importante della ricerca nell'autoimmunità. Una visita oculistica, così come un bilancio di diagnostica per immagini, sono richiesti al minimo dubbio durante l'iter diagnostico. Se il trattamento in prima intenzione con corticosteroidi è ampiamente accettato, anche se non chiaramente codificato nelle sue modalità, l'instaurazione di un trattamento immunosoppressivo, in seconda intenzione dopo l'insuccesso o l'insufficienza della terapia corticosteroidea, rimane molto discutibile e, a nostro parere, non giustificata. Le terapie locali, in pieno sviluppo, suscitano speranza nella sordità autoimmune come in altre malattie del labirinto. La gestione dei pazienti affetti da sordità autoimmune richiede in tutti i casi una collaborazione stretta tra ORL e internista. In caso di evoluzione verso la sordità profonda, l'impianto cocleare è una buona indicazione
BIBLIOGRAFIA
Aftab S., Semaan M.T., Murray G.S., Megerian C.A. Cochlear implantation outcomes in patients with autoimmune and immune-mediated inner ear disease Otol Neurotol 2010 ; 31 : 1337-1342 [cross-ref]
Agrup C., Luxon L.M. Immune-mediated inner-ear disorders in neuro-otology Curr Opin Neurol 2006 ; 19 : 26-32
Alajouanine T., Castaigne P., Lhermitte F., Cambier J., Gautier J.C. The meningoencephalitis of Behcet's disease Presse Med 1961 ; 69 : 2579-2582
Alexander TH, Weisman MH, Derebery JM, Espeland MA, Gantz BJ, et al. Safety of high-dose corticosteroids for the treatment of autoimmune inner ear disease. Otology & neurotology : official publication of the American Otological Society, American Neurotology Society [and] European Academy of Otology and Neurotology 2009;30: 443-8
Alles MJ, der Gaag MA, Stokroos RJ. Intratympanic steroid therapy for inner ear diseases, a review of the literature. Eur Arch Otorhinolaryngol 2006;263: 791-7
Arenberg I.K., Rask-Andersen H., Wilbrand H., Stahle J. The surgical anatomy of the endolymphatic sac Arch Otolaryngol 1977 ; 103 : 1-11
Arnold W., Altermatt H.J., Gebbers J.O. Qualitative detection of immunoglobulins in the human endolymphatic sac Laryngol Rhinol Otol 1984 ; 63 : 464-467 [cross-ref]
Bachor E., Blevins N.H., Karmody C., Kuhnel T. Otologic manifestations of relapsing polychondritis. Review of literature and report of nine cases Auris Nasus Larynx 2006 ; 33 : 135-141 [cross-ref]
Baek M.J., Park H.M., Johnson J.M. Increased frequencies of cochlin-specific T cells in patients with autoimmune sensorineural hearing loss J Immunol 2006 ; 177 : 4203-4210
Baughman R.P., Teirstein A.S., Judson M.A. Clinical characteristics of patients in a case control study of sarcoidosis Am J Respir Crit Care Med 2001 ; 164 : 1885-1889
Baughman R.P., Lower E.E., Kaufman A.H. Ocular sarcoidosis Semin Respir Crit Care Med 2010 ; 31 : 452-462 [cross-ref]
Bianchin G, Russi G, Romano N, Fioravanti P. Treatment with HELP-apheresis in patients suffering from sudden sensorineural hearing loss: a prospective, randomized, controlled study. The Laryngoscope 2010;120: 800-7
Billings P. Experimental autoimmune hearing loss J Clin Invest 2004 ; 113 : 1114-1117 [cross-ref]
Bird P.A., Murray D.P., Zhang M., Begg E.J. Intratympanic versus intravenous delivery of dexamethasone and dexamethasone sodium phosphate to cochlear perilymph Otol Neurotol 2011 ; 32 : 933-936 [cross-ref]
Bonaguri C., Orsoni J.G., Zavota L. Anti-68kDa antibodies in autoimmune sensorineural hearing loss: are these autoantibodies really a diagnostic tool? Autoimmunity 2007 ; 40 : 73-78 [cross-ref]
Boulassel M.R., Deggouj N., Tomasi J.P., Gersdorff M. Inner ear autoantibodies and their targets in patients with autoimmune inner ear diseases Acta Otolaryngol 2001 ; 121 : 28-34
Bovo R., Aimoni C., Martini A. Immune-mediated inner ear disease Acta Otolaryngol 2006 ; 126 : 1012-1021 [cross-ref]
Bovo R, Ciorba A, Martini A.. The diagnosis of autoimmune inner ear disease: evidence and critical pitfalls. Eur Arch Otorhinolaryngol 2009;266: 37-40
Brookes G.B., Newland A.C. Plasma exchange in the treatment of immune complex-associated sensorineural deafness J Laryngol Otol 1986 ; 100 : 25-33
Brookes G.B. Circulating immune complexes in Meniere's disease Arch Otolaryngol Head Neck Surg 1986 ; 112 : 536-540
Broughton S.S., Meyerhoff W.E., Cohen S.B. Immune-mediated inner ear disease: 10-year experienceSemin Arthritis Rheum 2004 ; 34 : 544-548 [cross-ref]
Buniel M.C., Geelan-Hansen K., Weber P.C., Tuohy V.K. Immunosuppressive therapy for autoimmune inner ear disease Immunotherapy 2009 ; 1 : 425-434 [cross-ref]
Cai Q, Du X, Zhou B, Cai C, Kermany MH, Yoo T. Induction of tolerance by oral administration of beta-tubulin in an animal model of autoimmune inner ear disease. ORL; journal for oto-rhino-laryngology and its related specialties 2009;71: 135-41
Cama E., Santarelli R., Muzzi E. Sudden hearing loss in sarcoidosis: otoneurological study and neuroradiological correlates Acta Otorhinolaryngol Ital 2011 ; 31 : 235-238
Cogan D.G. Syndrome of non-syphilitic intersticial keratitis and vestibuloauditory symptoms Arch Ophtalmology 1945 ; 33 : 144-149
Cohen S, Roland P, Shoup A, Lowenstein M, Silverstein H, et al. . A pilot study of rituximab in immune-mediated inner ear disease. Audiology & neuro-otology 2011;16: 214-21
Committee on Hearing and Equilibrium guidelines for the diagnosis and evaluation of therapy in Meniere's disease American Academy of Otolaryngology-Head and Neck Foundation Inc. Otolaryngol Head Neck Surg 1995 ; 113 : 181-185
Couloigner V., Teixeira M., Sterkers O., Rask-Andersen H., Ferrary E. The endolymphatic sac: its roles in the inner ear Med Sci 2004 ; 20 : 304-310 [cross-ref]
Crawley B.K., Close A., Canto C., Harris J.P. Susac's syndrome: intratympanic therapy for hearing loss and a review of the literature Laryngoscope 2009 ; 119 : 141-144 [cross-ref]
Dafni U.G., Tzioufas A.G., Staikos P., Skopouli F.N., Moutsopoulos H.M. Prevalence of Sjogren's syndrome in a closed rural community Ann Rheum Dis 1997 ; 56 : 521-525 [cross-ref]
Daneshi A., Farhadi M., Asghari A., Emamjomeh H., Abbasalipour P., Hasanzadeh S. Three familial cases of Michel's aplasia Otol Neurotol 2002 ; 23 : 346-348 [cross-ref]
Dayal VS, Ellman M, Sweiss N. Autoimmune inner ear disease: clinical and laboratory findings and treatment outcome. J Otolaryngol Head Neck Surg. 2008 Aug. 37(4):591-6. [Medline]
Deane K.D., Tyler K.N., Johnson D.W. Susac syndrome and pregnancy: disease management J Clin Rheumatol 2011 ; 17 : 83-88
Disher M.J., Ramakrishnan A., Nair T.S. Human autoantibodies and monoclonal antibody KHRI-3 bind to a phylogenetically conserved inner-ear-supporting cell antigen Ann N Y Acad Sci 1997 ; 830 : 253-265 [cross-ref]
Ebringer R., Rook G., Swana G.T., Bottazzo G.F., Doniach D. Autoantibodies to cartilage and type II collagen in relapsing polychondritis and other rheumatic diseases Ann Rheum Dis 1981 ; 40 : 473-479 [cross-ref]
Frachet B, Moine A, Giocanti A. Surdités auto-immunes. In: Brasnu D, editor. Traité d'ORL: Flammarion Médecine Sciences; 2008. p. 100-7.
Fusconi M., Ralli G., de Vincentiis M. Sarcoidosis of the middle ear and chronic suppurative otitis media: coexisting conditions? Otol Neurotol 2011 ; 32 : e61-e62
Garcia-Berrocal J.R., Trinidad A., Ramirez-Camacho R., Lobo D., Verdaguer M., Ibanez A. Immunologic work-up study for inner ear disorders: looking for a rational strategy Acta Otolaryngol 2005 ; 125 : 814-818 [cross-ref]
Garcia-Berrocal JR, Ibanez A, Rodriguez A, Gonzalez-Garcia JA, Verdaguer JM, et al. Alternatives to systemic steroid therapy for refractory immune-mediated inner ear disease: A physiopathologic approach. Eur Arch Otorhinolaryngol 2006; 263: 977-82
Garcia-Berrocal J.R., Nevado J., Gonzalez-Garcia J.A. Heat shock protein 70 and cellular disturbances in cochlear cisplatin ototoxicity model J Laryngol Otol 2010 ; 124 : 599-609 [cross-ref]
Graff-Dubois S., Siberil S., Elluru S. Use of intravenous polyclonal immunoglobulins in autoimmune and inflammatory disorders Transfus Clin Biol 2007 ; 14 : 63-68 [inter-ref]
Greco A, Gallo A, Fusconi M, Marinelli C, Macri GF, de Vincentiis M. Meniere's disease might be an autoimmune condition? 2012.;Autoimmunity reviews
Green L., Miller E.B. Sudden sensorineural hearing loss as a first manifestation of systemic lupus erythematosus: association with anticardiolipin antibodies Clin Rheumatol 2001 ; 20 : 220-222 [cross-ref]
Guillevin L. Vasculitides: nosological classification and targeted therapies Rev Prat 2008 ; 58 : 479
Güttich A. Pathologische Anatomie der sympathischen Labyrinthitis Passow-Schaefer-Beiträge Anat Physiol Pathol Ther Ohres 1927 ; 27 : 6-9
Haynes B.F., Kaiser-Kupfer M.I., Mason P., Fauci A.S. Cogan syndrome: studies in thirteen patients, long-term follow-up, and a review of the literature Medicine 1980 ; 59 : 426-441
Harris J.P., Ryan A.F. Immunobiology of the inner ear Am J Otolaryngol 1984 ; 5 : 418-425 [cross-ref]
Harris J.P. Autoimmunity of the inner ear Am J Otol 1989 ; 10 : 193-195
Harris J.P., Heydt J., Keithley E.M., Chen M.C. Immunopathology of the inner ear: an update Ann N Y Acad Sci 1997 ; 830 : 166-178 [cross-ref]
Harris J.P., Weisman M.H., Derebery J.M. Treatment of corticosteroid-responsive autoimmune inner ear disease with methotrexate: a randomized controlled trial JAMA 2003 ; 290 : 1875-1883 [cross-ref] Haynes B.F., Kaiser-Kupfer M.I., Mason P., Fauci A.S. Cogan syndrome: studies in thirteen patients, long-term follow-up, and a review of the literature Medicine 1980 ; 59 : 426-441
Hefeneider S.H., McCoy S.L., Hausman F.A., Trune D.R. Autoimmune mouse antibodies recognize multiple antigens proposed in human immune-mediated hearing loss Otol Neurotol 2004 ; 25 : 250-256 [cross-ref]
Hervier B., Bordure P., Masseau A., Calais C., Agard C., Hamidou M. Auto-immune sensorineural deafness: physiopathology and therapeutic approach Rev Med Interne 2010 ; 31 : 222-228 [cross-ref]
Hervier B., Bordure P., Audrain M., Calais C., Masseau A., Hamidou M. Systematic screening for nonspecific autoantibodies in idiopathic sensorineural hearing loss: no association with steroid responseOtol Neurotol 2010 ; 31 : 687-690
Huang N.C., Sataloff R.T. Autoimmune inner ear disease in children Otol Neurotol 2011 ; 32 : 213-216 [cross-ref]
Hughes G.B., Kinney S.E., Barna B.P., Calabrese L.H. Autoimmune reactivity in Meniere's disease: a preliminary report Laryngoscope 1983 ; 93 : 410-417
Hughes G.B., Barna B.P., Kinney S.E., Calabrese L.H., Nalepa N.L. Predictive value of laboratory tests in “autoimmune” inner ear disease: preliminary report Laryngoscope 1986 ; 96 : 502-505 [cross-ref]
Hughes GB, Barna BP, Calarese LH. Immunologic Disorders of the Inner Ear. Bailey BJ, ed. Head and Neck Surgery-Otolaryngology. Philadelphia, Pa: Lippincott; 1993. 1833-1842.
Hughes G.B., Moscicki R., Barna B.P., San Martin J.E. Laboratory diagnosis of immune inner ear diseaseAm J Otol 1994 ; 15 : 198-202
Joglekar S., Morita N., Cureoglu S. Cochlear pathology in human temporal bones with otitis media Acta Otolaryngol 2010 ; 130 : 472-476 [cross-ref]
Kang K.T., Young Y.H. Sudden sensorineural hearing loss in a patient with primary antiphospholipid syndrome J Laryngol Otol 2008 ; 122 : 204-206
Kara A., Besbas N., Tezer H., Karagoz T., Devrim I., Unal O.F. Reversible sensorineural hearing loss in a girl with Kawasaki disease Turk J Pediatr 2007 ; 49 : 431-433
Karatas E., Onat A.M., Durucu C. Audiovestibular disturbance in patients with systemic lupus erythematosus Otolaryngol Head Neck Surg 2007 ; 136 : 82-86 [cross-ref]
Kawaguchi S., Hagiwara A., Suzuki M. Polymorphic analysis of the heat-shock protein 70 gene (HSPA1A) in Meniere's disease Acta Otolaryngol 2008 ; 128 : 1173-1177 [cross-ref]
Kikuchi M. On the “sympathetic otitis” Zibi Rinsyo Koyto 1959 ; 52 : 600
Kindler W. Sympathische Otitis Arch Klin Exp Ohren Nasen Kehlkopfheilkd 1943 ; 152 : 222-227 [cross-ref]
Kommareddi P.K., Nair T.S., Vallurupalli M. Autoantibodies to recombinant human CTL2 in autoimmune hearing loss Laryngoscope 2009 ; 119 : 924-932 [cross-ref]
Kumakiri K., Sakamoto T., Karahashi T., Mineta H., Takebayashi S. A case of relapsing polychondritis preceded by inner ear involvement Auris Nasus Larynx 2005 ; 32 : 71-76 [cross-ref]
Lejeune J.M., Charachon R. New immunobiological tests in the investigation of Meniere's disease and sensorineural hearing loss Acta Otolaryngol 1992 ; 112 : 174-179
Lobo D., Trinidad A., Garcia-Berrocal J.R., Verdaguer J.M., Ramirez-Camacho R. TNF alpha blockers do not improve the hearing recovery obtained with glucocorticoid therapy in an autoimmune experimental labyrinthitis Eur Arch Otorhinolaryngol 2006 ; 263 : 622-626 [cross-ref]
Lobo D., Lopez F.G., Garcia-Berrocal J.R., Ramirez-Camacho R. Diagnostic tests for immunomediated hearing loss: a systematic review J Laryngol Otol 2008 ; 122 : 564-573
Lorenz R.R., Solares C.A., Williams P. Interferon-gamma production to inner ear antigens by T cells from patients with autoimmune sensorineural hearing loss J Neuroimmunol 2002 ; 130 : 173-178 [cross-ref]
Lunardi C., Bason C., Leandri M. Autoantibodies to inner ear and endothelial antigens in Cogan's syndrome Lancet 2002 ; 360 : 915-921 [cross-ref]
Magalhaes C.M., Magalhaes Alves N.R., Oliveira K.M., Silva I.M., Gandolfi L., Pratesi R. Sensorineural hearing loss: an underdiagnosed complication of Kawasaki disease J Clin Rheumatol 2010 ; 16 : 322-325
Manoussakis M.N., Georgopoulou C., Zintzaras E. Sjogren's syndrome associated with systemic lupus erythematosus: clinical and laboratory profiles and comparison with primary Sjogren's syndromeArthritis Rheum 2004 ; 50 : 882-891 [cross-ref]
Matteson E.L., Fabry D.A., Strome S.E., Driscoll C.L., Beatty C.W., McDonald T.J. Autoimmune inner ear disease: diagnostic and therapeutic approaches in a multidisciplinary setting J Am Acad Audiol 2003 ; 14 : 225-230
Mazlumzadeh M., Lowe V.J., Mullan B.P., Fabry D.A., McDonald T.J., Matteson E.L. The utility of positron emission tomography in the evaluation of autoimmune hearing loss Otol Neurotol 2003 ; 24 : 201-204 [cross-ref]
McAdam L.P., O'Hanlan M.A., Bluestone R., Pearson C.M. Relapsing polychondritis: prospective study of 23 patients and a review of the literature Medicine 1976 ; 55 : 193-215 [cross-ref]
McCabe B.F. Autoimmune sensorineural hearing loss Ann Otol Rhinol Laryngol 1979 ; 88 : 585-589
McCabe B.F. Autoimmune inner ear disease: therapy Am J Otol 1989 ; 10 : 196-197
McCaffrey T.V., McDonald T.J., McCaffrey L.A. Head and neck manifestations of relapsing polychondritis: review of 29 cases Otolaryngology 1978 ; 86 : 473-478
McCall A.A., Swan E.E., Borenstein J.T., Sewell W.F., Kujawa S.G., McKenna M.J. Drug delivery for treatment of inner ear disease: current state of knowledge Ear Hear 2011 ; 31 : 156-165
Merchant S.N., Adams J.C., Nadol J.B. Pathophysiology of Meniere's syndrome: are symptoms caused by endolymphatic hydrops? Otol Neurotol 2005 ; 26 : 74-81 [cross-ref]
Mogan R.F., Baumgartner C.J. Meniere's disease complicated by recurrent intersticial keratitis: excellent results following cervical ganglionectomy West J Surg 1934 ; 42 : 628-631
Mondain M. Les affections de l'oreille interne à médiation immunitaire. Apport d'une technique d'immunofluorescence indirecte sur coupe de cochlée de cobaye. [thèse de Médecine]. Montpellier: Université de Montpellier I, 1991.
Moorthy R.S., Inomata H., Rao N.A. Vogt-Koyanagi-Harada syndrome Surv Ophthalmol 1995 ; 39 : 265-292 [cross-ref]
Mora R, Jankowska B, Passali GC, Mora F, Passali FM, et al. Sodium enoxaparin treatment of sensorineural hearing loss: an immune-mediated response? The international tinnitus journal 2005;11: 38-42
Morita N., Kariya S., Farajzadeh Deroee A. Membranous labyrinth volumes in normal ears and Meniere disease: a three-dimensional reconstruction study Laryngoscope 2009 ; 119 : 2216-2220 [cross-ref]
Nakagawa T, Ito J.. Application of cell therapy to inner ear diseases. Acta oto-laryngologica.Supplementum: 2004;6-9
Nair T.S., Prieskorn D.M., Miller J.M., Dolan D.F., Raphael Y., Carey T.E. KHRI-3 monoclonal antibody-induced damage to the inner ear: antibody staining of nascent scars Hear Res 1999 ; 129 : 50-60[cross-ref]
Nunes H., Bouvry D., Soler P., Valeyre D. Sarcoidosis Orphanet J Rare Dis 2007 ; 2 : 46 [cross-ref]
Ozdemir M., Balevi S., Deniz F., Mevlitoglu I. Pathergy reaction in different body areas in Behcet's disease Clin Exp Dermatol 2007 ; 32 : 85-87
Ozer F., Unal O.F., Atas A., Tekin O., Sungur A., Ayas K. Evaluation of the effect of dexamethasone in experimentally induced endolymphatic hydrops in guinea pigs Am J Otolaryngol 2008 ; 29 : 88-93 [cross-ref]
Palva T., Raunio V., Nousiainen R., Forsen R. Glutamate-hydroxybutyrate and succinate dehydrogenases in post mortem inner ear fluids Acta Otolaryngol 1972 ; 73 : 151-159 [cross-ref]
Parnes L.S., Sun A.H., Freeman D.J. Corticosteroid pharmacokinetics in the inner ear fluids: an animal study followed by clinical application Laryngoscope 1999 ; 109 : 1-17 [cross-ref]
Paparella M.M., Oda M., Hiraide F., Brady D. Pathology of sensorineural hearing loss in otitis media Ann Otol Rhinol Laryngol 1972 ; 81 : 632-637
Papo T. Comment ne pas manquer une maladie systémique auto-immune? Rev Mal Respir 2006 ; 23 : 754-756 [inter-ref]
Park S.N., Yeo S.W., Park K.H. Serum heat shock protein 70 and its correlation with clinical characteristics in patients with sudden sensorineural hearing loss Laryngoscope 2006 ; 116 : 121-125 [cross-ref]
Parnes L.S., Sun A.H., Freeman D.J. Corticosteroid pharmacokinetics in the inner ear fluids: an animal study followed by clinical application Laryngoscope 1999 ; 109 : 1-17 [cross-ref]
Pau H, Clarke RW. Advances in genetic manipulations in the treatment of hearing disorders.Clinical otolaryngology and allied sciences 2004; 29: 574-6
Pettigrew H.D., Teuber S.S., Gershwin M.E. Polyarteritis nodosa Compr Ther 2007 ; 33 : 144-149 [cross-ref]
Rao N.A. Treatment of Vogt-Koyanagi-Harada disease by corticosteroids and immunosuppressive agents Ocul Immunol Inflamm 2006 ; 14 : 71-72 [cross-ref]
Rauch S.D., Zurakowski D., Bloch D.B., Bloch K.J. Anti-heat shock protein 70 antibodies in Meniere's disease Laryngoscope 2000 ; 110 : 1516-1521 [cross-ref]
Rauch SD. Intratympanic steroids for sensorineural hearing loss. Otolaryngologic clinics of North America 2004;37: 1061-74
Read R.W., Holland G.N., Rao N.A. Revised diagnostic criteria for Vogt-Koyanagi-Harada disease: report of an international committee on nomenclature Am J Ophthalmol 2001 ; 131 : 647-652[inter-ref]
Read RW. Vogt-Koyanagi-Harada disease. Ophthalmol Clin North Am 2002;15:333-41, vii.
Rennebohm R.M., Egan R.A., Susac J.O. Treatment of Susac's Syndrome Curr Treat Options Neurol 2008 ; 10 : 67-74 [cross-ref]
Rahman MU, Poe DS, Choi HK. Etanercept therapy for immune-mediated cochleovestibular disorders: preliminary results in a pilot study. Otology & neurotology : official publication of the American Otological Society, American Neurotology Society [and] European Academy of Otology and Neurotology 2001; 22: 619-24
Rennebohm R.M., Egan R.A., Susac J.O. Treatment of Susac's Syndrome Curr Treat Options Neurol 2008 ; 10 : 67-74[cross-ref]
Ruckenstein MJ. Autoimmune inner ear disease. Current opinion in otolaryngology & head and neck surgery 2004; 12: 426-30
Sajjadi H., Paparella M.M. Meniere's disease Lancet 2008 ; 372 : 406-414 [cross-ref]
Saliba I., Martineau G., Chagnon M. Asymmetric hearing loss: rule 3,000 for screening vestibular schwannoma Otol Neurotol 2009 ; 30 : 515-521 [cross-ref]
Saracaydin A., Katircioglu S., Katircioglu S., Karatay M.C. Azathioprine in combination with steroids in the treatment of autoimmune inner-ear disease J Int Med Res 1993 ; 21 : 192-196
Schuknecht H.F. Ear pathology in autoimmune disease Adv Otorhinolaryngol 1991 ; 46 : 50-70
Semaan MT, Megerian CA. Meniere's disease: a challenging and relentless disorder. Otolaryngol Clin North Am 2011;44:383-403, IX.
Sismanis A, Thompson T, Willis HE. Methotrexate therapy for autoimmune hearing loss: a preliminary report. The Laryngoscope 1994;104: 932-4
Sismanis A, Wise CM, Johnson GD. Methotrexate management of immune-mediated cochleovestibular disorders. Otolaryngology–head and neck surgery : official journal of American Academy of Otolaryngology-Head and Neck Surgery 1997;116: 146-52
Smith J.C., Peck J.E., Ray L.I., Smith E.C. Aortoarteritis and sensorineural hearing loss in an adolescent black male Am J Otolaryngol 2004 ; 25 : 370-376 [cross-ref]
Spear S.A., Schwartz S.R. Intratympanic steroids for sudden sensorineural hearing loss: a systematic review Otolaryngol Head Neck Surg 2011 ; 145 : 534-543 [cross-ref]
Srikumar S, Deepak MK, Basu S, Kumar BN. . Sensorineural hearing loss associated with psoriatic arthritis. The Journal of laryngology and otology 2004;118: 909-11
Stearns G.S., Keithley E.M., Harris J.P. Development of high endothelial venule-like characteristics in the spiral modiolar vein induced by viral labyrinthitis Laryngoscope 1993 ; 103 : 890-898
Street I., Jobanputra P., Proops D.W. Etanercept, a tumour necrosis factor alpha receptor antagonist, and methotrexate in acute sensorineural hearing loss J Laryngol Otol 2006 ; 120 : 1064-1066
Sugiura M., Naganawa S., Teranishi M., Sato E., Kojima S., Nakashima T. Inner ear hemorrhage in systemic lupus erythematosus Laryngoscope 2006 ; 116 : 826-828 [cross-ref]
Suslu N., Yilmaz T., Gursel B. Utility of immunologic parameters in the evaluation of Meniere's diseaseActa Otolaryngol 2009 ; 129 : 1160-1165 [cross-ref]
Takase H., Shimizu K., Yamada Y., Hanada A., Takahashi H., Mochizuki M. Validation of international criteria for the diagnosis of ocular sarcoidosis proposed by the first international workshop on ocular sarcoidosis Jpn J Ophthalmol 2010 ; 54 : 529-536 [cross-ref]
Takumida M., Bagger-Sjoback D., Rask-Andersen H. The effects of glycerol on vestibular function and the endolymphatic sac after pre-treatment with colchicine Acta Otolaryngol [suppl] 1989 ; 468 : 59-63 [cross-ref]
ten Cate W.J., Bachor E. Autoimmune-mediated sympathetic hearing loss: a case report Otol Neurotol 2005 ; 26 : 161-165 [cross-ref]
Tran Ba Huy P., Sauvaget E. Idiopathic sudden sensorineural hearing loss is not, at this time, an otologic emergency Ann Otolaryngol Chir Cervicofac 2007 ; 124 : 66-71 [cross-ref]
Tumiati B., Casoli P., Parmeggiani A. Hearing loss in the Sjogren syndrome Ann Intern Med 1997 ; 126 : 450-453
Van Wijk F, Staecker H, Keithley E, Lefebvre PP. . Local perfusion of the tumor necrosis factor alpha blocker infliximab to the inner ear improves autoimmune neurosensory hearing loss. Audiology & neuro-otology 2006;11: 357-65
Veldman J.E. The immune system in hearing disorders Acta Otolaryngol [suppl] 1988 ; 458 : 67-75 [cross-ref]
Vinceneux P. Le syndrome de Cogan. Encyclopédie Orphanet; 2005.
Vitali C., Bombardieri S., Jonsson R. Classification criteria for Sjogren's syndrome: a revised version of the European criteria proposed by the American-European Consensus Group Ann Rheum Dis 2002 ; 61 : 554-558 [cross-ref]
Wang J.G., Xie Q.B., Yang N.P., Yin G. Primary antiphospholipid antibody syndrome: a case with bilateral sudden sensorineural hearing loss Rheumatol Int 2009 ; 29 : 467-468 [cross-ref]
Xenellis J., Morrison A.W., McClowskey D., Festenstein H. HLA antigens in the pathogenesis of Meniere's disease J Laryngol Otol 1986 ; 100 : 21-24 [cross-ref]
Yamaki K., Gocho K., Hayakawa K., Kondo I., Sakuragi S. Tyrosinase family proteins are antigens specific to Vogt-Koyanagi-Harada disease J Immunol 2000 ; 165 : 7323-7329
Yamamoto K. Pathogenesis of Sjogren's syndrome Autoimmun Rev 2003 ; 2 : 13-18 [cross-ref]
Yehudai D., Shoenfeld Y., Toubi E. The autoimmune characteristics of progressive or sudden sensorineural hearing loss Autoimmunity 2006 ; 39 : 153-158 [cross-ref]
Yeom K, Gray J, Nair TS, Arts HA, Telian SA, et al. Antibodies to HSP-70 in normal donors and autoimmune hearing loss patients. The Laryngoscope 2003;.113: 1770-6
Yildirim N., Arslanoglu A., Aygun N. Otologic and leptomeningeal involvements as presenting features in seronegative Wegener granulomatosis Am J Otolaryngol 2008 ; 29 : 147-149 [cross-ref]
Yokoyama M.M., Matsui Y., Yamashiroya H.M. Humoral and cellular immunity studies in patients with Vogt-Koyanagi-Harada syndrome and pars planitis Invest Ophthalmol Vis Sci 1981 ; 20 : 364-370
Yoo T.J. Etiopathogenesis of Meniere's disease: a hypothesis Ann Otol Rhinol Laryngol 1984 ; 113 : 6-12
Yoo T.J., Floyd R.A., Sudo N. Factors influencing collagen-induced autoimmune ear disease Am J Otolaryngol 1985 ; 6 : 209-216 [cross-ref]
Yoo T.J., Shea J., Ge X. Presence of autoantibodies in the sera of Meniere's disease Ann Otol Rhinol Laryngol 2001 ; 110 : 425-429 [cross-ref]
Yoo T.J., Du X., Kwon S.S. Molecular mechanism of autoimmune hearing loss Acta Otolaryngol [suppl] 2002 ; 548 : 3-9 [cross-ref]
Zeitoun H., Beckman J.G., Arts H.A. Corticosteroid response and supporting cell antibody in autoimmune hearing loss Arch Otolaryngol Head Neck Surg 2005 ; 131 : 665-672 [cross-ref]
Zhou Y, Yuan J, Zhou B, Lee AJ, Ghawji M, Jr., Yoo TJ. The therapeutic efficacy of human adipose tissue-derived mesenchymal stem cells on experimental autoimmune hearing loss in mice. Immunology 2011;133: 133-40
Zhou B, Kermany MH, Cai Q, Cai C, Zhou Y, et al. . Experimental autoimmune hearing loss is exacerbated in IL-10-deficient mice and reversed by IL-10 gene transfer. Gene therapy 2012; 19: 228-35
Cos’è la malattia di Ménière? 2-8- (9/10 approfondimento)
Quali sono i criteri per porre diagnosi di Malattia di Ménière? 2- (9/10 approfondimento)
Esistono manifestazioni particolari della malattia di Ménière? 2-18- (47/48)
Con che frequenza si manifesta? 2- (11/13 I° approfondimento) 46- (114/116 II° approfondimento )
Cosa causa la malattia di Ménière ? 2 - 10 -19 (27/31)
Come si fa diagnosi di malattia di Ménière? 4 -12 (32/37 approfondimento)
Come si cura la malattia di Ménière? (3/6) - Scuola Italiana 69-Scuola Francese-72-Scuola Americana-Timothy 78
Trattamento farmacologico : 4/5 (18/19)
I trattamenti chirurgici :4
· Decompressione del sacco endolinfatico 5 110/111
· Labirintectomia chimica con gentamicina 5 68-(86/98 I° approfondimento) (79/103-II°approfondimento)
· Labirintectomia chirurgica 5
· Sezione (neurotomia) del nervo vestibolare 5 112/113
1) Riassunto 6
2) Cenni Storici 6 - (7/8 approfondimento)
3) Definizione: Che cos'è la malattia di Meniere? 9 - (10/11 approfondimento)
4) Epidemiologia 2-10-(11/12 I° approfondimento) (114/116 II°approfondimento)
5) Quali sono i criteri per porre diagnosi di Malattia di Ménière? 13
6) Stadiazione 13 68
7) Quadro Semeiologico 14
8) Etiologia: Che cosa causa la malattia di Meniere? 2-15/19 - (19/23 approfondimento)
Etiologia autoimmune 14 19/23-(31/34)- infettiva-19- allergica 20- genetica 23- traumatica 23
9) Fisiopatologia ed anatomia patologica(24/27)
10) Patogenesi (27/31):Teoria della rottura di membrana (32/33);Teoria dell'alterata permeabilità di membrana 34;Teoria meccanica (34/35)
11) Come si fa diagnosi di malattia di Ménière? 3-13 (35/40 approfondimento)
12) Sintomi : Crisi vertiginose Ipoacusia Acufeni Sintomi associati (41/43)
13) Storia Naturale :Fase iniziale- attiva- di defervescenza- Fase finale- Bilateralizzazione (43/44)
14) Esistono Manifestazioni Particolari della Malattia di Ménière?:44:Sindrome di Lermoyez.44, Catastrofi otolitiche di Tumarkin 44,la sindrome di Ohresser 45,La MdM cocleare 44,la MdM vestibolare 43,L'idrope endolinfatica ritardata 45
15) Forme cliniche 45/47
16) Con che frequenza si manifesta? 2 - (11/12 I° approfondimento) 47-(114/116 II° approfondimento )
17) Terapia: Come si cura la malattia di Ménière? 3/6 Trattamento generale della malattia 47/50
18) Esami Diagnostici: 51/67 Audiometria tonale 13-50 vocale 13-54,sopraliminari 53,automatica 53 Impedenzometria 54 Altri test cocleari Elettrococleografia (55/58);Potenziali evocati acustici 58, Otoemissioni acustiche 54/55 ;Altri test meno utilizzati. Prove vestibolari 60/61 Potenziali evocati vestibolari VEMPs 61/63 -Test al glicerolo acetazolamide furosemide (59- 63/65) ,Diagnostica per immagini 66 ,Esami di laboratorio 67
19) Diagnosi Differenziale (68/70)
20) Terapia medica: Come si cura la malattia di Ménière? (3/6)- (18/21) Scuola Italiana (70/72) ;Scuola Francese (72-104);; 62,Dieta italiana (73/77),(Scuola Americana Timothy)78/84;Trattamento generale della malattia: 27-29-67/104 -Trattamento dell’attacco acuto: 80- Come si fa a gestire un attacco? (81/84);Farmaci usati tra gli attacchi (Stati Uniti) 81; Labirintectomia chimica (78/79) (85/88) APPROFONDIMENTO :Trattamento Intratimpanico/Transtimpanico con Gentamicina per la Malattia di Ménière 88;Le due principali varianti 89:Risultati della variante a basso dosaggio (90/91);Alte dosi 91/93;Altre procedure di variante di gentamicina intratympanic 94;Streptomicina /Streptomicina-desametasone /Titolazione 94;Modalità di somministrazione 95;Gentamicina vs steroidi vs sezione del nervo vestibolare 97; Gentamicina autogestita 98;Informazioni Supplementari Sulle Iniezione Intra/Transtimpaniche Di Gentamicina 102/103: Trattamento Steroideo Intratimpanico per la Malattia di Meniere (104/107); Varianti nella procedura degli steroidi intratimpanici 106 RISULTATI 106 Steroidi per perdita dell’udito o vertigini (108/109);
21)Terapia chirurgica: Chirurgia del Sacco Endolinfatico 111; Sacculotomie 112; Labirintectomia 113,Neurectomia Vestibolare 113
22) Evoluzione 114
23) Bibliografia Generale 116
Cos’è la malattia di Ménière?
È una malattia dell’orecchio interno che si manifesta con crisi vertiginose periodiche, acufene e sensazione di orecchio ovattato e diminuzione dell’udito nell’orecchio interessato che inizialmente è in genere fluttuante. Tipicamente la crisi vertiginosa è preceduta dalla sensazione di ovattamento, da una modificazione o aumento dell’acufene e si manifesta con vertigine oggettiva (l’ambiente ruota intorno al paziente), disequilibrio, nausea e vomito. Gli occhi durante la crini si muovono aritmicamente in senso laterale (nistagmo). La durata della crisi è di alcune ore ma può essere molto variabile al pari della frequenza di manifestazione. In alcune persone l’instabilità persiste anche dopo l’attacco acuto.
Quali sono i criteri per porre diagnosi di Malattia di Ménière?
La sindrome è caratterizzata da una tipica triade sintomatologica:
· Vertigini oggettive (rotatorie di durata oscillante, violente, a crisi, della durata tra 20 minuti e alcune ore giorni) Fig.1.1
·  Ipoacusia percettiva (perdita di udito dovuta a danni dell'orecchio interno)
Ipoacusia percettiva (perdita di udito dovuta a danni dell'orecchio interno)
· Acufeni soggettivi e senso di orecchio pieno nell’orecchio interessato.
Segni e sintomi associati:
· ipoacusia fluttuante
· interessamento iniziale delle basse frequenze
· cadute improvvise (Drop attacks)
· Diplacusia (sensazione di rimbombo o eco)
· iporeflessia vestibolare nell’orecchio interessato
· elevato rapporto SP/AP all’elettrococleografia nell’orecchio interessato
La diagnosi di Malattia di Ménière non è sempre facile soprattutto nelle fasi iniziali della malattia per la variabilità con la quale i diversi sintomi si presentano. La monolateralità dei disturbi aiuta la diagnosi in fase iniziale mentre non è raro nelle fasi avanzate l’interessamento dell’altro orecchio. Durante le crisi il nistagmo batte sul lato dell’orecchio malato, dopo la crisi batte sull’altro lato. Le vertigini sono accompagnate da segni neurovegetativi quali nausea e vomito e si possono verificare con una frequenza molto variabile da diverse volte a settimana a solo una volta all’anno.
Esistono manifestazioni particolari della malattia di Ménière?
In rari casi l’attacco si manifesta come una caduta improvvisa, la cosiddetta “crisi otolitica di Tumarkin” attribuita ad una deformazione meccanica della porzione otolitica dell’orecchio interno (utriculo e sacculo). Ménière cocleare: talvolta l'idrope si localizza prevalentemente al labirinto cocleare (devoluto alla funzione uditiva) configurando la Ménière cocleare o blocco cocleare acuto. In questi casi i sintomi uditivi prevalgono su quelli vertiginosi.
Con che frequenza si manifesta?
Interessa approssimativamente lo 0,2% della popolazione inizia in genere da un lato ed esiste una probabilità che interessi l’altro orecchio del 50%, ma in un periodo di 30 anni. La Malattia di Ménière ha un’incidenza che varia da 7,5 a 157 soggetti su 10.000 e nella nostra esperienza rappresenta la quarta causa di vestibolopatia dopo la vertigine parossistica posizionale da litiasi canalare ,la vestibolopatia emicranica e la neurite della componente superiore del ramo vestibolare del nervo ottavo.
Cosa causa la malattia di Ménière ? Fig.1. 2

La causa della malattia è sconosciuta. Esistono varie ipotesi che trovano riscontro in tutta una serie di rilievi anatomopatologici (autopsia) e clinici (esame del paziente).
• Idiopatica: possibile predisposizione genetica (familiarità , Morrison AW, Johnson KJ 2002; Arweiler DJ e coll; 1995, associazione con HLA-A3, B7, CW7, DR26”).
• Embriopatica (come nella displasia di Mondini).
• Acquisita: patologie autoimmuni 81, infezioni virali Schuknecht HF and Igarashi, M 1986 ’ Gacek, RR and Gacek, MR 2002 , microvasculopatia, Gacek, RR and Gacek, MR (2002) frattura dell’osso temporale. In tali forme secondarie si parla di Sindrome di Menière.
La manifestazione principale è l’idrope endolinfatica cioè la dilatazione del labirinto membranoso, sistema di membrane dell’orecchio interno ripiene di liquidi di cui si ritiene esista una eccessiva produzione oppure un ridotto riassorbimento.
Va detto che mentre non esiste malattia di Ménière senza idrope endolinfatica (0,2/100 persone) si può avere idrope endolinfatica senza malattia di Ménière (0,6/100 ossa temporali di persone decedute).
Tre meccanismi patologici alla base dell’idrope endolinfatica sono emersi dagli studi anatomopatologici: fibrosi del sacco endolinfatico e dell’epitelio vestibolare, alterato metabolismo delle glicoproteine e infezione virale dell’orecchio interno.
Da un punto di vista fisiopatologico il ridotto riassorbimento di endolinfa da parte del sacco endolinfatico, supportata dalle ridotte dimensioni dell’acquedotto vestibolare nei pazienti menierici.
La predisposizione genetica è supportata dalla prevalenza di alcuni antigeni leucocitari (Cw*07). Le alterazioni del sistema immunitario dall’aumento del rapporto OKT 4/8 e dalla diminuzione delle cellule OKT8-positive.
Le alterazioni metaboliche da aumentati livelli di fibrinogeno, D-dimero, leucociti e riduzione dei folati che indicano un generico stato infiammatorio.
Le infezioni virali, supportate da elevati livelli di immunoglobuline G del virus herpes simplex nella perilinfa dei pazienti menierici.
È peraltro verosimile che molte siano le cause che possono determinare idrope endolinfatica che in alcuni casi si manifesta come malattia di Ménière conclamata. Verosimilmente esiste una predisposizione genetica e fattori scatenanti autoimmunitari, virali e metabolici cui si aggiunge una componente psicosomatica e ansiogena universalmente riconosciuta.
Come si fa diagnosi di malattia di Ménière?
La diagnosi di malattia di Ménière è clinica cioè è fatta dal medico sulla base della storia clinica raccolta con il malato (anamnesi) oltre che dell'esame obiettivo (la visita) che evidenzia il tipico nistagmo spontaneo (movimento anomalo involontario degli occhi) e dei dati ottenuti con l’esame audiometrico. . Altri esami che spesso si richiedono al malato (impedenzometrico, potenziali evocati uditivi, risonanza magnetica cerebrale) servono ad escludere altre ben più gravi (neurinoma dell'acustico, sclerosi multipla, tumori e disturbi circolatori ischemici endocranici). mentre l’esame elettrococleografico può, se eseguito correttamente quando la malattia è in fase attiva, esprimere la presenza dell’idrope labirintica (aumento di pressione dei liquidi dell’orecchio interno). L’esame audiometrico nelle fasi iniziali della malattia mostra una diminuzione dell’udito limitata alle basse frequenze spesso fluttuante, cioè che presenta variazioni nel tempo con udito che dopo le prime crisi torna a valori normali.
Come si cura la malattia di Ménière? Scuola Italiana 69/Scuola Francese-72-Scuola Americana- 78
TERAPIA
• Preventiva: dieta moderatamente iperidrica e iposodica, glicerolo, betaistina dicloridratoa (Tighilet et al.,2005: . Lacour et al.,) cortisonici, antitrombotici eparinosimili (sulodexide) (Barbara , et al.,2007), 42, “antiossidanti con QTer’ (ACUVAL9) Khan e Coll.2007; Fetoni e Coll. 2009; cortisone intratimpanico (Philiips JS, Westerberg B., 2011; Casani e Coll., 2011).
• Della crisi: vestibolosoppressori, procinetici.
• Ablativa: gentamicina (Wu IC, Minor LB ,2003; Casani et al., 2011), chirurgica.
• Rieducativa.
Bisogna distinguere un trattamento dell’attacco acuto da tutte le terapie e norme di igiene alimentare e di vita che sono utili per il controllo della malattia. Parleremo poi dei trattamenti medici e chirurgici che permettono di evitare il ripetersi delle crisi acute.
Nei protocolli terapeutici tradizionali si utilizzano farmaci che appartengono a quattro categorie:
Diuretici osmotici (mannitolo, glicerolo): si somministarno mediante fleboclisi ed agiscono richiamando liquidi dall'interno degli organi del labirinto; nelle vertigini, infatti, è frequentemente presente un "accumulo" di liquidi nel labirinto (idrope labirintica).
Sedativi della funzione labirintica (bloccano gli impulsi anomali generati dal labirinto ammalato).
Antiemetici (agiscono contro il vomito).
Cortisonici (agiscono contro l'infiammazione e l'edema)
Trattamento dell’attaco acuto: si basa sull’uso di farmaci che deprimono la funzione vestibolare come alcuni antistaminici che si somministrano per via intramuscolare o endovenosa; farmaci anti-emetici che sopprimono i sintomi dovuti all’attivazione del sistema neurovegetativo (nausea, vomito, malessere generale); farmaci ansiolitici che oltre che ridurre l’ansia associata alla crisi hanno anche un’azione antivertiginosa diretta.
Esistono peraltro degli accorgimenti che permettono di ridurre l’intensità dei disturbi se si viene colti da una crisi e non si hanno a disposizione farmaci antivertiginosi. È consigliabile stendersi su una superficie piana e stabile sul fianco dell’orecchio sano e fissare un punto fermo. Evitare di bere per non stimolare il vomito. Se se ne ha la possibilità può essere utile fare un lavaggio dell’orecchio malato con acqua fredda (dai 20 ai 30 gradi), può essere usatoa per questo una siringa da 20cc (senza l’ago naturalmente) o una peretta che contenga la stessa quantità d’acqua. Lo scopo di questa irrigazione è di inibire l’attività del labirinto malato che in fase acuta presenta un’aumentata attività.
Trattamento generale della malattia: si basa su una serie di norme di igiene soprattutto alimentare che consistono principalmente nel mantenere un buon equilibrio idrosalino dell’organismo. Sebbene i liquidi dell’orecchio interno abbiano un metabolismo separato da quello dei liquidi del resto dell’organismo con concentrazioni specifiche di sodio, potassio e altri elettroliti, sono comunque influenzati dallo stato di equilibrio idrosalino dell’organismo. Le norme principali da seguire per evitare questo squilibrio sono:
· Rimanere a riposo con il capo fermo.
· Stazionare in un ambiente non molto luminoso e il più silenzioso possibile.
· Evitare qualunque sforzo ,gli stress siano essi lavorativi o per attività ludiche.
· Assumere alimenti e liquidi in modo regolare e ben distribuito nella giornata
· Limitare in modo drastico il consumo di sale riducendo anche il consumo di alimenti ad alto contenuto salino (meno di un grammo al giorno)
· Consumare almeno tre porzioni di frutta e due di verdura al giorno
· Bere almeno 2 litri di acqua al giorno o di succhi di frutta a basso contenuto di zuccheri e reintrodurre subito i liquidi persi con l’esercizio fisico o a causa del caldo.
· Prestare attenzione all’assunzione di latte che in alcuni pazienti può accentuare la frequenza delle crisi per motivi di allergia ad esso
· Limiti l’assunzione di caffeina (caffè, tè, cioccolato) che tra l’altro ha un effetto di scatenamento dell’emicrania (alcune forme di idrope sono degli equivalenti emicranici)
· Limitare l’assunzione di alcol ad un bicchiere di vino ai pasti
· Limitare/evitare gli alimenti che contengono monogluttamato di sodio (contenuto sopratutto nella cucina cinese)
Trattamento farmacologico: sono innumerevoli i farmaci usati nel trattamento della malattia di Ménière. Istaminosimili, diuretici risparmiatori di potassio, calcioantagonisti, vasoattivi di varia natura, sedativi e ansiolitici e innumerevoli terapie non convenzionali.
Qualunque trattamento venga proposto è consigliabile che il paziente chieda al medico che effetto vuole ottenere con quella specifica terapia, che effetti collaterali potrebbero presentarsi e se esiste dimostrazione scientifica che quella terapia ha un effetto positivo sulla malattia oppure si tratta di un trattamento sperimentale.
I trattamenti chirurgici sono indicati qualora la terapia dietetica e farmacologica non permetta un ottimo controllo della malattia cioè non si abbiano più crisi violente di vertigini. Essi possono essere di tipo funzionale oppure mirano alla distruzione più o meno completa delle cellule del sistema dell’equilibrio che inviano il segnale al sistema nervoso centrale. I principali sono:
A) Decompressione del sacco endolinfatico
B) Terapie intratimpaniche conservative (steroidi) e ablative:labirintectomia chimica (gentamicina)
(Fig.1.3a);
C) Labirintectomia chirurgica
D) Sezione (neurectomia) del nervo vestibolare ( Fig.1. 3b)
|
|
|
Fig.1.3a-b |
A)La decompressione del sacco endolinfatico110/111 è stato il primo intervento chirurgico “funzionale” per la cura della malattia di Meniere. Consiste nel rimuovere l’osso posto dietro il labirinto che ricopre il sacco endolinfatico dove “scaricano” la pressione i liquidi labirintici. Le procedure descritte sono diverse, semlice decompressione, applicazione di una valvola dal sacco alla mastoide o ai liquidi cerabrali, asportazione completa del sacco e tutti hanno percentuali di successo simili nel controllo della malattia. Essi oscillano nei vari studi dal 60% all’80%. Si tratta di un intervento che si esegue in anestesia generale e, in mani esperte, ha un rischio di complicazioni molto basso. Il principale vantaggio di questi interventi è che non sono distruttivi della funzione vestibolare e quindi non provocano uno squilibrio tra i due lati che, soprattutto nelle persone anziane, può essere difficile da compensare.
B1) La labirintectomia chimica con gentamicina 88/103 rappresenta uno dei trattamenti attualmente più diffusi oltre che per i buoni risultati per la relativa semplicità di applicazione. Infatti può essere eseguito ambulatoriamente iniettando la gentamicina, che è un antibiotico tossico per il sistema otovestibolare, nell’orecchio medio dove viene assorbito a livello della membrana della finestra rotonda. Si sfrutta il fatto che essendo più tossico per le cellule vestibolari che per quelle acustiche può essere applicato in modo da essere tossico solo per le prime lasciando intatta la funzione uditiva. La gentamicina può essere applicata direttamente nell’orecchio con un ago che attravversa la membrana timpanica oppure si posiziona prima un tubicino di ventilazione nel timpano attraverso il quale si inietta il farmaco. La capacità e l’esperienza del medico sta nell’applicare il farmaco in modo da distruggere le cellule vestibolari lasciando intatte quelle uditive. Il trattamento è ambulatoriale ed i risultati nel controllo delle vertigini, in mani esperte, raggiungono il 90%.
C) La labirintectomia chirurgica si esegue solo quando il paziente ha una sordità totale dal lato della malattia ed è l'intervento di emi - slabirintazione.
Attraverso la demolizione della regione mastoidea si giunge all'interno dell'orecchio medio e si asporta il labirinto responsabile della malattia si possono rimuovere chirurgicamente le cellule vestibolari. È un intervento da eseguire in anestesia generale che dà un controllo della vertigine in oltre il 95% dei casi. È raramente eseguito perchè è raro che si abbia una sordità totale dal lato della malattia.
D)La sezione o neurotomia del nervo vestibolare112 si esegue, ormai molto raramente, quando gli altri trattamenti non hanno dato il risultato sperato è il paziente continua ad avere violente crisi vertiginose. Si tratta infatti di un intervento delicato, otoneurochirgico, che consiste nella sezione intracranica del nervo vestibolare (dell’equilibrio) lasciando inatto quello cocleare (dell’udito). È risolutivo in oltre il 95% dei casi.
La nostra esperienza nel trattamento della malattia di Ménière ci ha portato ad impostare una strategia terapeutica che liberi il paziente al più presto dalla dipendenza della malattia. Infatti il problema principale di chi ne soffre è rappresentato dalla imprevedibilità delle crisi oltre che il pericolo intrinseco ad essa (caduta, incidente stradale) ne consegue che se la terapia medica e dietetica non ha raggiunto i risultati sperati nell’arco di tre mesi consigliamo il trattamento chirurgico nelle sue versioni funzionale (decompressione del sacco endolinfatico) e di deafferentazione (interruzione degli stimoli) vestibolare rappresentata dal trattamento con gentamicina. Altri trattamenti “funzionali” quali il trattamento pressorio dell’orecchio con il Meniett non hanno dimostrato, negli studi pubblicati di confronto, un successo superiore a quello dell’applicazione di un semplice tubicino di ventilazione nella membrana timpanica e di conseguenza non riteniamo il loro uso giustificato.
Un aspetto particolare del trattamento della malattia di Ménière è rappresentato dal trattamento della malattia di Ménière bilaterale. In questo caso laddove la terapia medica risulti insufficiente a controllare le crisi non è consigliabile, per la grave inabilità che provoca, un trattamento distruttivo bilaterale, ne consegue che il trattamento dovrà trovare un equilibrio portando ad una riduzione parziale della funzione vestibolare. La streptomicina che è un farmaco tossico per il sistema vestibolare usata per via parenterale (iniezioni intramuscolari) controllando clinicamente la funzione vestibolare ci permette di abbassare gradualmente la funzione labirintica senza danneggiare la funzione uditiva e senza arrivare ad una totale perdita della funzione vestibolare.
Come si curano gli acufeni, il senso di ovattamento auricolare e l’ipoacusia?
Gli acufeni e l’ovattamento possono trarre beneficio da procedure mediche e chirurgiche. La TRT ottiene nel trattamento degli acufeni legati alla malattia di Ménière gli stessi risultati che ottiene nelle altre forme di acufene con miglioramenti ottenibili nell’80% dei casi. L’ovattamento può trarre beneficio da procedure chirurgiche quali la decompressione del sacco endolinfatico, l’applicazione di gentamicina e talora la semplice applicazione di un tubicino di ventilazione. Per quanto concerne l’ipoacusia essa va trattata con apparecchi e protesi acustiche in tutti i casi in cui insorge difficoltà nel capire la provenienza dei suoni e nel capire il discorso in ambiente rumoroso. La protesizzazione può essere complessa a causa del recruitment (che genera fastidio per i rumori intensi) ma è sempre possibile.
Come può la malattia di Ménière condizionare la mia vita?
Il maggiore condizionamento della malattia è rappresentato dalla imprevedibilità delle crisi, dal fastidio legato agli acufeni e al senso di ovattamento auricolare. La collaborazione di chi ci circonda nella vita di tutti i giorni è molto utili nelle fasi iniziali della malattia quando si stanno valutando i risultati di terapie mediche e della dieta. Il prepararsi ad affrontarla secondo i suggerimenti della sezione trattamento della fase acuta ed il preparare e attrezzare l’ambiente familiare in modo da non trovarsi in gravi difficoltà è altrettanto utile. Il semplice mantenimento di una luce di bassa intensità accesa nella stanza da letto evita di trovarsi in difficoltà in caso di crisi notturna. In alcune persone la malattia può determinare l’insorgenza di una sindrome ansioso-depressiva che va adeguatamente riconosciuta e trattata affinchè non incida ulteriormente sulla salute generale del “menierico”.
1) Riassunto
La malattia di Ménière, archetipo della malattia vertiginosa invalidante, è una patologia a eziologia ancora sconosciuta, sebbene sia stata descritta nel XIX secolo e sia stata oggetto di una vasta produzione medico scientifica. Frequente, è caratterizzata da un'idrope endolinfatica che è all'origine della caratteristica e patognomonica triade clinica; questa triade associa un acufene simile ad un ronzio, unilaterale, dal lato dell'orecchio colpito, un'ipoacusia omolaterale di tipo recettivo, tipicamente più evidente sulle frequenze gravi, e una violenta vertigine rotatoria di tipo periferico, accompagnata da nausea e vomito. La triade sintomatologica si presenta in modo parossistico con crisi che durano alcune ore, la cui periodicità è casuale. Nel periodo intercritico, il paziente non accusa disturbi e i dati di laboratorio sono normali. Fare la diagnosi della malattia di Ménière lontano dalla crisi è difficile. Il decorso della malattia è molto variabile. Anche se essa ha un carattere benigno, può diventare gravemente invalidante. Attualmente, il trattamento della malattia di Ménière è decisamente più efficace che negli anni passati; tuttavia se oggi si possono controllare e prevenire le crisi vertiginose, in particolare con la sezione selettiva del nervo vestibolare, non sempre si può prevedere l'evoluzione dell'ipoacusia.
2) Cenni Storici
Nel 1861 Prospero Meniere (1799-1861), successore di Itard come medico capo dell’Istituto Imperiale dei sordomuti a Parigi, descrisse per primo l’entità clinica alla quale venne da allora attribuito il suo nome.
Egli definì una condizione patologica caratterizzata da improvvise e recidivanti crisi vertiginose, spesso accompagnate da nausea e vomito, associate ad ipoacusia e ad acufeni, intervallate da periodi di remissione durante i quali, almeno inizialmente, i pazienti godevano di buona salute Dopo la descrizione di Itard dell'associazione caratteristica di vertigine, ipoacusia e acufene nel 1821 Prospero Ménière descrisse, all'Accademia imperiale di medicina nel 1861, la presenza di una linfa plastica rossastra nel labirinto di due malati che avevano presentato sintomi e segni di congestione cerebrale apoplettiforme .Nonostante la malattia descritta allora non corrispondesse presumibilmente a quella oggi chiamata malattia di Ménière, Prospero Ménière ebbe il grande merito di associare, per la prima volta, all'orecchio interno una sintomatologia che a quei tempi veniva sistematicamente attribuita a un disordine del sistema nervoso centrale. Nella stessa occasione egli convalidò le leggi della fisiologia vestibolare proposte da Flourens nel 1842.
Ménière fece conoscere una patologia destinata a sollevare appassionate discussioni nel mondo medico. Nel fiorire di questi studi scientifici, tre eventi meritano di essere ricordati:
1)nel 1921, Portmann dimostrò sui pesci il possibile ruolo del sacco endolinfatico nella genesi dell'ipertensione endolinfatica
2)Hallpike C,Cairns H nel 1938,scoprirono una dilatazione del labirinto membranoso sulle ossa temporali di due pazienti affetti dalla malattia sulla scorta dei lavori di Guild, che, nel 1927, con esperimenti su animali, aveva dimostrato che un colorante iniettato nell'endolinfa cocleare si ritrovava concentrato nel sacco endolinfatico, nel 1959 Naito fu in grado, di indurre un'idrope endolinfatica nella cavia distruggendo chirurgicamente il canale e il sacco endolinfatici. Questo metodo, migliorato da Kimura e Schuknecht nel 1965 , è tuttora il modello sperimentale più usato per lo studio dell'idrope endolinfatica. Nel 1952, Tasaki e Fernandez dimostrarono che la riduzione reversibile dei potenziali uditivi e dei potenziali d'azione cocleari poteva essere ottenuta iniettando nello spazio perilinfatico della coclea una soluzione di Ringer® allo 0,25% di cloruro di sodio. Nel 1954, Smith, Lowry e Wu documentarono che l'endolinfa presentava una bassa concentrazione di sodio (3 - 5 mmol/l) e un'alta concentrazione di potassio (130 a 145 mmol/l), mentre questi valori si invertivano nella perilinfa. Nel 1959, Lawrence e McCabe postularono che la base dei sintomi della malattia di Ménière dovesse essere attribuita alla rottura delle membrane endolinfatiche distese dall'idrope, con conseguente mescolamento dell'endolinfa ricca di potassio e della perilinfa ricca di sodio. Questa ipotesi fu sperimentalmente testata provocando le crisi tipiche della malattia di Ménière, attraverso l'iniezione in animali da esperimento di una soluzione ricca di potassio nello spazio perilinfatico, fino al raggiungimento di un'alta concentrazione di potassio anche nell'endolinfa. Il concetto dell'intossicazione potassica delle fibre demielinizzate dell'epitelio sensoriale della coclea e del vestibolo fu quindi adottato come meccanismo base delle crisi. Studi successivi hanno posto maggiore attenzione alla struttura e alle alterazioni patologiche del sacco endolinfatico, visto che l'ipotesi più accreditata sulla patogenesi dell'idrope endolinfatica è basata sul difettoso riassorbimento dell'endolinfa a livello del sacco. Nel 1983, Schuknecht osservando le rocche petrose di pazienti affetti dalla malattia di Ménière ha riscontrato non solo la presenza di un'idrope endolinfatica, ma anche di una fibrosi e di un'obliterazione ossea del canale e del sacco endolinfatici. Infine, va ricordato anche che al sacco endolinfatico viene attribuito un ruolo immunologico. Tuttavia, come si vedrà in seguito, nonostante siano state avanzate numerose ipotesi al riguardo, la patogenesi della malattia di Ménière resta inspiegabile.
 2)CENNI STORICI(approfondimento) La malattia prende il nome di Prospero Ménière al quale viene universalmente riconosciuta la paternità della scoperta. (Figura1.4). Dopo la descrizione di Itard dell'associazione caratteristica di vertigine, ipoacusia e acufene nel 1821. Prospero Ménière sviluppò le sue ricerche durante gli anni (dal 1839 al 1862) in cui lavorò come medico presso l’Institut Imperial des Sourds et Muet di Parigi.
2)CENNI STORICI(approfondimento) La malattia prende il nome di Prospero Ménière al quale viene universalmente riconosciuta la paternità della scoperta. (Figura1.4). Dopo la descrizione di Itard dell'associazione caratteristica di vertigine, ipoacusia e acufene nel 1821. Prospero Ménière sviluppò le sue ricerche durante gli anni (dal 1839 al 1862) in cui lavorò come medico presso l’Institut Imperial des Sourds et Muet di Parigi.
Fig.1.4
Prosper Ménière 1861 ;descrisse, all'Accademia imperiale di medicina nel 1861, la presenza di una linfa plastica rossastra nel labirinto di due malati che avevano presentato sintomi e segni di congestione cerebrale apoplettiformePrima della sua scoperta,esposta nel 1861 nella seduta dell’8 gennaio dell’Accademia Imperiale di Medicina, i pazienti con idrope endolinfatico sintomatologico non venivano considerati malati di competenza otorinolaringoiatrica. Prospero Ménière ebbe il grande merito di associare, per la prima volta, all'orecchio interno una sintomatologia che a quei tempi veniva sistematicamente attribuita a un disordine del sistema nervoso centrale. Prospero Ménière invece per primo interpretò i sintomi della vertigine e della ipoacusia osservati in una serie di pazienti come conseguenza di una alterazione patologica dall’apparato labirintico. Nonostante la

Fig.1.5.a Fig.1. 5.b
malattia descritta allora non corrispondesse presumibilmente a quella oggi chiamata malattia di Ménière, Nella stessa occasione egli convalidò le leggi della fisiologia vestibolare proposte da Flourens nel 1842 Ménière fece conoscere una patologia destinata a sollevare appassionate discussioni nel mondo medico. Le tesi di Ménière furono subito recepite con particolare interesse dal mondo scientifico medico del tempo e, già nel 1867, il quadro clinico veniva descritto come Malattia di Ménière.Appena qualche anno dopo, Goltz prima e successivamente Knapp ipotizzarono che la causa della malattia fosse un aumento di pressione intralabirintica analogamente a quanto avveniva nel già noto glaucoma Nel fiorire di questi studi scientifici, tre eventi meritano di essere ricordati: nel 1921, Portmann dimostrò sui pesci il possibile ruolo del sacco endolinfatico nella genesi dell'ipertensione endolinfatica .Solo nel 1938 gli inglesi Hallpike e Cairns e il giapponese Yamakawa fornirono la dimostrazione istologica dell’esistenza dell’idrope endolinfatico nei pazienti con sintomatologia menierica. Hallpike e Cairns (Fig 1.5.a e 1.5.b) scoprirono una dilatazione del labirinto membranoso sulle ossa temporali di due pazienti affetti dalla malattia; sulla scorta dei lavori di Guild, che, nel 1927 con esperimenti su animali ,aveva dimostrato che un colorante iniettato nell'endolinfa cocleare si ritrovava concentrato nel sacco endolinfatico, nel 1959 Naito fu in grado di indurre un’ e idrope endolinfatica nella cavia distruggendo chirurgicamente il canale e il sacco endolinfatici. Questo metodo, migliorato da Kimura e Schuknecht nel 1965 , è tuttora il modello sperimentale più usato per lo studio dell' idrope endolinfatica.
Nel 1952, Basai e Fernandez dimostrarono che la riduzione reversibile dei potenziali uditivi e dei potenziali d'azione cocleari poteva essere ottenuta iniettando nello spazio perilinfatico della coclea una soluzione di Ringer® allo 0,25% di cloruro di sodio. Nel 1954, Smith, Lowry e Wu documentarono che l'endolinfa presentava una bassa concentrazione di sodio (3 - 5 mmol/l) e un'alta concentrazione di potassio (130 a 145 mmol/l), mentre questi valori si invertivano nella perilinfa. Nel 1959, Lawrence e McCabe postularono che la base dei sintomi della malattia di Ménière dovesse essere attribuita alla rottura delle membrane endolinfatiche distese dall’ idrope con conseguente mescolamento dell'endolinfa ricca di potassio e della perilinfa ricca di sodio. Questa ipotesi fu sperimentalmente testata provocando le crisi tipiche della malattia di Ménière, attraverso l'iniezione in animali da esperimento di una soluzione ricca di potassio nello spazio perilinfatico, fino al raggiungimento di un'alta concentrazione di potassio anche nell'endolinfa. Il concetto dell'intossicazione potassica delle fibre demielinizzate dell'epitelio sensoriale della coclea e del vestibolo fu quindi adottato come meccanismo base delle crisi. Studi successivi hanno posto maggiore attenzione alla struttura e alle alterazioni patologiche del sacco endolinfatico, visto che l'ipotesi più accreditata sulla patogenesi dell' idrope endolinfatica è basata sul difettoso riassorbimento dell'endolinfa a livello del sacco. Nel 1983, Schuknecht osservando le rocche petrose di pazienti affetti dalla malattia di Ménière ha riscontrato non solo la presenza di un' i idrope endolinfatica, ma anche di una fibrosi e di un'obliterazione ossea del canale e del sacco endolinfatici. Infine, va ricordato anche che al sacco endolinfatico viene attribuito un ruolo immunologico. Tuttavia, come si vedrà in seguito, nonostante siano state avanzate numerose ipotesi al riguardo, la patogenesi della malattia di Ménière resta inspiegabile
3)Definizione: Che cos'è la malattia di Ménière ?
È una malattia dell’orecchio interno che si manifesta con crisi vertiginose periodiche, acufene e sensazione di orecchio ovattato e diminuzione dell’udito nell’orecchio interessato ,che inizialmente è in genere fluttuante. Tipicamente la crisi vertiginosa è preceduta dalla sensazione di ovattamento, da una modificazione o aumento dell’acufene e si manifesta con vertigine oggettiva (l’ambiente ruota intorno al paziente), disequilibrio, nausea e vomito. Nella figura 1, la superficie dell'orecchio colpito è il labirinto intero, che include sia i canali semicircolari e la coclea.
Un tipico attacco di malattia di Ménière è preceduta da pienezza in un orecchio. Hearing fluctuation or changes in tinnitus may also precede an attack. Fluttuazione udito o cambiamenti di tinnito può anche precedere un attacco. A Meniere's episode generally involves severe vertigo (spinning), imbalance, nausea and vomiting. Un episodio di Ménière comporta generalmente gravi vertigini (spinning), squilibrio, nausea e vomito. The average attack lasts two to four hours. L'attacco ha una durata media di 2-4 ore. Following a severe attack, most people find that they are exhausted and must sleep for several hours. A seguito di un grave attacco, maggior parte delle persone che sono esausti e devono dormire per diverse ore. There is a large amount of variability in the duration of symptoms. C'è una grande quantità di variabilità nella durata dei sintomi. Some people experience brief "shocks", and others have constant unsteadiness. Alcune persone breve esperienza "shock", e altri hanno instabilità costante. High sensitivity to visual stimuli ( ) is common. Alta sensibilità agli stimoli visivi (visual dependence). (Lacour, 1997). (Lacour, 1997). During the attack the eyes jump (this is called "nystagmus"). Durante l'attacco è comune che gli occhi si muovino spontaneamente (questo fenomeno è chiamato "nistagmo").
![]() Supplemental material on the : Movie of Materiale supplementare sul sito DVD : film di nistagmo durante la malattia di un attacco di Ménière
Supplemental material on the : Movie of Materiale supplementare sul sito DVD : film di nistagmo durante la malattia di un attacco di Ménière
|
|
Fig.1.6 Caduta a causa di crisi otolitici di Tumarkin. This is a very dangerous variant of Meniere's disease, which can result in abrupt falls. Questa è una variante molto pericolosa della malattia di Meniere, che può provocare brusche cadute
A particularly disabling symptom is a sudden fall.Un sintomo particolarmente invalidante è una caduta improvvisa. These typically occur without warning. Questi si verificano in genere senza preavviso. These falls are called "otolithic crisis of Tumarkin", from the original description of Tumarkin (1936). Queste cadute sono chiamati "crisi otolitici di Tumarkin", dalla descrizione originale di Tumarkin (1936). They are attributed to sudden mechanical deformation of the (utricle and saccule), causing a sudden activation of vestibular reflexes. Sono attribuiti a improvvisi deformazione meccanica della organi otolitici otolith organs (utricolo e sacculo), causando una improvvisa attivazione di riflessi vestibolari. Patients suddenly feel that they are tilted or falling (although they may be straight), and bring about much of the rapid repositioning themselves. I pazienti che improvvisamente si sentono inclinati o in diminuzione (anche se possono essere dritto), e portare gran parte del riposizionamento rapido se stessi. This is a very disabling symptom as it occurs without warning and can result in severe injury. Questo è un sintomo molto invalidante in quanto si verifica senza preavviso e può causare lesioni gravi.Often (eg labyrinthectomy or ) is the only way to manage this problem. Spesso il trattamento distruttivo destructive treatment (ad esempio la labirintectomia o sezione del nervo vestibolare vestibular nerve section) è l'unico modo per gestire questo problema. Other otologic conditions also occasionally are associated with Tumarkin type falls (Black et al, 1982; Ishiyama et al, 2003). Altre condizioni otologiche anche occasionalmente sono associate con cadute di tipo Tumarkin (Black et al, 1982; Ishiyama et al, 2003). See here for more information about .
Meniere's episodes may occur in clusters; that is, several attacks may occur within a short period of time.Gli episodi di Ménière possono verificarsi a grappoli , cioè, diversi attacchi possono verificarsi entro un breve periodo di tempo. However, years may pass between episodes. Tuttavia, gli possono passare degli anni tra gli episodi. Between the acute attacks, most people are free of symptoms or note mild imbalance and . Tra un attacco acuto e l'altro , la maggior parte le persone sono libere dai sintomi o notano un lieve squilibrio ed acufeni tinnitus .
3) DEFINIZIONE (APPROFONDIMENTO)
La malattia di Ménière può essere definita come una patologia dell'orecchio interno a eziologia sconosciuta, il cui substrato anatomopatologico è un'idrope endolinfatica. È caratterizzata dall'associazione di ipoacusia fluttuante con sensazione di pienezza auricolare, di crisi vertiginose accompagnate da marcati segni neurovegetativi e di un acufene. Questi sintomi si manifestano con crisi parossistiche e imprevedibili, a frequenza variabile; nella fase iniziale sono monolaterali e tendono ad attenuarsi nel periodo intercritico mentre con la progressione della malattia possono diventare bilaterali.
Il termine «malattia di Ménière» va preferito agli appellativi più comunemente usati come «vertigine di Ménière» o «sindrome di Ménière». Il termine «vertigine» conferisce un ruolo predominante al sintomo vestibolare che, sebbene sia il più eclatante, non è né il più duraturo né il più preoccupante nella storia della malattia. È, in effetti, l'ipoacusia a creare i maggiori problemi terapeutici e a rappresentare il criterio più tangibile di efficacia terapeutica. Il termine di «sindrome» sottintende l'esistenza di una possibile eziologia all'associazione dei sintomi caratteristici della malattia. Ora, se gli stessi possono essere osservati nel corso di malattie autoimmuni, della sindrome di Cogan o della sifilide, la malattia di Ménière è, per definizione, idiopatica e deve dunque essere caratterizzata come tale. Il termine di «malattia di Ménière» sembra dunque il più adatto e assicura una definizione di insieme della malattia e un'identità di linguaggio con la comunità scientifica anglosassone.
Altre patologie del sistema cocleo-vestibolare, del nervo cocleo-vestibolare o del sistema nervoso centrale possono provocare sintomi simili a quelli della malattia di Ménière. La diagnosi differenziale di questa malattia si rivela spesso difficile, anche per uno specialista, fino a quando non compaia la triade tipica e non sia stata esclusa una patologia retrococleare. Per questo, un'ipoacusia fluttuante isolata e crisi isolate di vertigine oggettiva non dovrebbero essere riferite alla malattia di Ménière e, con riserva, possono essere considerate solo una variante, cocleare o vestibolare, della malattia.
Tra le definizioni proposte per la malattia di Ménière, occorre ricordare quella dell’American Medical Association che, nell’indeterminatezza del fattore causale, si basa su caratteristiche cliniche e semeiologiche di accertato o supposto valore discriminante:la malattia di Ménière è una malattia dell’orecchio interno membranoso caratterizzata da ipoacusia, vertigine e abitualmente acufene che ha il suo corrispettivo patologico nella distensione idropica del sistema endolinfatico. L’ipoacusia è di tipo neurosensoriale fluttuante, generalmente unilaterale e progressiva. La vertigine è episodica; dura da 20 minuti a 24 ore ed è accompagnata da nausea, vomito e si associa ad un nistagmo vestibolare. Sono assenti i segni neurologici e la perdita di coscienza
Solo nel 1995 il Commitee ad hoc della American Academy of Otolaryngology-Head an Neck Surgery (AAO-HNS) ha pubblicato delle linee guida (i criteri )per la diagnosi di MdM Malattia di Ménière (tabella 1-1) .
|
Tabella 1-1 - Scala diagnostica della sindrome di Ménière secondo l'American Academy of Otolaryngology-Head and Neck Surgery (AAO-HNS). |
|
|
Malattia di Ménière certa |
Malattia di Ménière accertata con conferma istopatologica. |
|
Malattia di Ménière definitiva |
Due episodi o più di vertigini di durata non inferiore a 20 minuti Ipoacusia documentata da un audiogramma in almeno un'occasione Acufene o sensazione di pienezza auricolare |
|
Malattia di Ménière probabile |
Un episodio certo di vertigine Ipoacusia documentata da un audiogramma in almeno un'occasione Acufene o sensazione di pienezza auricolare |
|
Malattia di Ménière possibile |
Vertigine episodica senza ipoacusia documentata Ipoacusia neurosensoriale, fluttuante o stabile, con alterazioni dell'equilibrio ma senza episodi parossistici certi. |
prima di questa data una accurata descrizione dei valori di prevalenza ed incidenza di questa affezione risulta estremamente difficoltosa a causa delle diverse metodologie di selezione dei pazienti e della mancanza di criteri diagnostici e di stadiazione definiti e condivisi.
4) Epidemiologia delle Malattie di Ménière
La malattia diMeniere's affects roughly 0.2% of the population (click details about the epidemiology). Ménière colpisce circa lo 0,2% della popolazione. LaMeniere's disease usually starts confined to one ear but it often extends to involve both ears over time so that after 30 years, 50% of patients with Meniere's have bilateral disease (Stahle et al, 1991). Malattia di Ménière comincia solitamente interessando un solo orecchio, ma spesso si estende e coinvolge entrambe le orecchie nel tempo, in modo che dopo 30 anni, il 50% dei pazienti ha una malattia di Ménière bilaterale (Stahle et al, 1991). There is some controversy about this statistic however -- some authors, for example Silverstein, suggest that the prevalence of bilaterality is as low as 17% (Silverstein, 1992). Vi è una certa polemica circa questa statistica tuttavia alcuni autori, ad esempio Silverstein, suggeriscono che la prevalenza della bilateralità sia più bassa 17% (Silverstein, 1992). We suspect that this lower statistic is due to a lower duration of follow up and that the 50% figure is more likely to be correct. Sia ha il sospetto che questa statistica sia più bassa a causa di una minore durata del follow up e che la cifra del 50% è probabile che sia la più corretta. Other possibilities, however, are selection bias and different patterns of the disease in different countries. Altre possibilità, tuttavia, sono il tipo di selezione e diversi modelli di classificazione della malattia nei ad avere una malattia di maniera bilaterale diversi paesi. Silverstein suggested that 75% of persons destined to become bilateral do so within 5 years. Silverstein ha suggerito che il 75% delle persone destinate ad avere una malattia di Ménière bilaterale la raggiunge entro 5 anni.
In most cases, a progressive hearing loss occurs in the affected ear(s).Nella maggior parte dei casi, una perdita progressiva della funzionalità uditiva si verifica nell'orecchio colpito . Inizialmente si ha un ipoacusia neurosensoriale per le bassa frequenza, ma col passare del tempo, di solito si trasforma in una perdita uditiva sia piatta o con caduta delle frequenze acute . Anche se un attacco acuto può essere invalidante, la stessa malattia non è mortale.
Gli occhi durante la crisi si muovono aritmicamente in senso laterale (nistagmo). La durata della crisi è di alcune ore ,ma può essere molto variabile al pari della frequenza di manifestazione. In alcune persone l’instabilità persiste anche dopo l’attacco acuto.
Per malattia di Menière (MdM) si intende un'affezione idiopatica che interessa l’orecchio interno il cui sottostante meccanismo fisiopatologico è un aumento della pressione a carico dei liquidi endolinfatici, contenuti nella coclea e nel labirinto (Idrope endolinfatica).
L'esistenza dell'idrope può essere accertata solo "post mortem" dai dati istopatologici relativi all'osso temporale.
4) Epidemiologia delle malattia di Ménière (MdM) (I °approfondimento)
c'è notevole disaccordo nella letteratura mondiale circa l'incidenza (nuovi casi/anno) e la prevalenza (tutti i casi nella popolazione) della malattia di Ménière probabilmente a causa di bias metodologici e, in particolare, per l'assenza di criteri clinici o diagnostici univoci. Per riassumere, sembra che LA MdM abbia una incidenza di circa 200 casi su 100.000 persone negli Stati Uniti, o in altre parole, circa lo 0,2% della popolazione ha la malattia di Ménière. La prevalenza può variare a livello internazionale. La prevalenza aumenta con l'età, piuttosto lineare, fino all'età di 60 anni. Anche a proposito della ripartizione per sesso, si segnala una di scordanza tra le varie statistiche: alcuni Autori indicano una leggera prevalenza maschile ( Watanabe, 1981), altri femminile ( Wladislavosky,Wasserman et al , 1984). All’opposto esiste un accordo pressoché unanime sul ritenere la MdM una patologia della mezza età; l’età di esordio appare perlopiù intorno alla quarta decade di vita. Un aspetto epidemiologico ancor più controverso è costituito dal possibile coinvolgimento bilaterale dell’orecchio interno (OI) sia all’esordio che nella naturale evoluzione della malattia. In letteratura sono riportate percentuali variabili dal 2 al 78% (House et al,, 2006); l’estrema etei oeneira di questo dato dipende anche da cosa si intende per coinvolgimento bilaterale, dato che sono stati i riscontrati trequentemente nell’orecchio controlaterale anomalie uditive senza tuttavia la comparsa di una sintomatologia menierica conclamata (Perez e et al., 2004). Nella esperienza di Casani et al., 2005,.raramente hanno registrato forme ad esordio bilaterale e ad un follow-up di circa 20 anni, la percentuale dei casi bilaterali non supera il 7%
Per l'Inghilterra, Cawthorne e Hewlett (1954) segnalano, 157 casi su 100.000 casi basati su i dati di 8 medici di base in Inghilterra sino al marzo 1952. Non è chiaro nella loro relazione se tali cifre riflettono incidenza o prevalenza, sebbene Arenberg et al hanno suggerito che è una figura di incidenza (1980). Se la prevalenza, questa cifra potrebbe essere molto simile a una figura segnalato per gli Stati Uniti da Wadislowvsky e soci, più tardi). Se si intende l’incidenza, questa cifra potrebbe suggerire che la prevalenza è maggiore (approssimativamente.16-25%, o circa il 4% della popolazione). Riteniamo che questo dato sia altamente improbabile. 160/100.000 casi in Inghilterra Carlborg BI, 1983 ; Mentre altri hanno suggerito un tasso di prevalenza alto come 1% (es. Morrison, 1995; Harrison e Naftalin, 1968), sembra che le prove per questa asserzione,siano poco attendibili. Goodman (1957) ha presentato dati che suggeriscono una prevalenza dello 0.56%, che è simile ai dati trovati negli Stati Uniti da Wadislowvsky e soci. In Giappone ci sono stati diversi grandi studi epidemiologici. 50/100.000 casi in Giappone Shojaku H, 1997 ;secondo Watanabe (1988), malattia di Ménière era rara fino al 1950. Dopo la fine della seconda guerra mondiale, c'è stato un rapido aumento del numero di pazienti con malattia di Ménière. In questi studi sono definiti Menierici i pazienti con ripetuti attacchi di vertigine, sintomi cocleari fluttuanti e vertigini, con esclusione di altre malattie (Watanabe et al., 1995). Hanno riferito che l'età media di esordio era di 41-42 anni , con una picco di incidenza nell’ età tra i 30 ed i 39. La prevalenza è stata di 16-17 casi x 100.000. Questa cifra viene valutata bassa. In uno studio più recente Shojaku e Watanabe (1997)hanno trovato una incidenza tra 21,4 e 36,6 casi x100.000, che può essere considerata ancora una stima bassa.
Ci sono stati diversi studi della popolazione statunitense. Nello studio di Framingham, (Framingham, messa, USA)l’ 1,48% della popolazione ha dichiarato di avere avuto una malattia di Ménière (Moscicki et al., 1985). Queste percentuali elevate derivano probabilmente dalla tendenza di molti medici a trattare, tutti i casi di vertigine ricorrenti ,come malattia di Ménière (Slater, 1988). Wladislavosky e soci, alla Mayo Clinic hanno riferito, nel 1980 ,una prevalenza di su 218.2 casi x 100.000, nella popolazione di Rochester ,Minnesota e un tasso di incidenza di 153nuovi casi x100,000 x anno. Hanno anche riferito di un tasso di diagnosi fondamentalmente proporzionale all'età fino all'età di 60, con un successivo declino. Nel 34% della loro coorte è stato trovato una Ménière bilaterale. Questi AA hanno commentato che i tassi ,riscontrati in Rochester MN, appaiono più bassi rispetto a quelli segnalati in Inghilterra e Svezia. Da 15 a 21/100.000 casi negli USA 1991,Kitahara M, Futaki T, Nakano K hanno dimostrato l'assenza di differenze significative nell'insorgenza della malattia di Ménière tra diversi gruppi etnici negli USA e, fino a oggi, non è stato possibile dimostrare nessuna predisposizione legata al sesso, alla razza o all'area geografica di residenza.
In Finlandia, la è stata segnalata una frequenza di 43casi x 100.000 abitanti, l’incidenza era del 4.3x100.000 (Kotimaki et al., 1999). Questa cifra appare bassa rispetto a quanto segnalato negli Stati Uniti ed in Inghilterra.
In Svezia, Stahle et al. Hanno segnalato nel 1973 un'incidenza di Menierici ad Uppsala di 45x100.000 abitanti. Questo studio ha utilizzato per la diagnosi criteri più severi rispetto agli altri studi e pertanto è generalmente ritenuto una sottostima .La malattia di Ménière, per i loro criteri, è circa 4 volte più comune rispetto all’ otosclerosi. L'incidenza sarebbe pari a 46/100.000 casi in Svezia, escludendo la forma cocleare pura (ipoacusia fluttuante isolata Spoendlin H,)1992.
In Italia, Celestino e Ralli hanno riportato un tasso di incidenza di 8 x 100,000, e stimano che la prevalenza era di circa lo 0,4% della popolazione. Ciò presuppone che la maggior parte delle persone convivere con la malattia di maniera in media cinquant'anni. La distribuzione dei loro caso, non è normalizzata per l'età della popolazione, ha raggiunto un picco a 41-50 anni.
L’incidenza, cioè il numero di nuovi pazienti diagnosticati ogni anno, è stata calcolata in Italia nel 1988 ed è risultata pari a 82 nuovi casi per milione di abitanti mentre la prevalenza, cioè il numero totale di casi presenti in una popolazione, è risultata di 116.850 casi.Ricerche simili in varie aree del mondo hanno dato risultati discordanti (vedi tabella 1-2).
|
Autori (tabella 1-2) |
Anno |
CASI |
NAZIONE |
|
Cawthorne e Hewlett |
1954 |
157 |
USA |
|
Goodmann |
1956 |
37 |
INGHILTERRA |
|
Michel e coll |
1975 |
75 |
FRANCIA |
|
Stahke e coll |
1978 |
460 |
SVEZIA |
|
Watanabe |
1980 |
40 |
GIAPPONE |
|
Celestino e Ralli |
1988 |
82 |
ITALIA |
|
Muzukoschi |
1993 |
161 |
GIAPPONE |
La sensazione generale è che entrambi i sessi sono ugualmente colpiti. Tuttavia ci può essere una differenza nella distribuzione dei pazienti gravemente disabili. Stahle (1976) ha osservato che il numero di maschi superano le femmine (206:150) in questo gruppo.
pochi dati riguardo alla predisposizione razziale sono disponibili per la malattia di Ménière. Nel 1972 Nsamba ha segnalato che la malattia di Ménière era rara in Uganda. CaparaosaA(1963) ha riferito che la malattia di Ménière è stata prevalentemente una malattia della razza bianca e si è verificato solo raramente nella popolazione nera. D'altra parte, Futaki e Kitahara (1974) hanno trovato che l'incidenza della malattia di Meniere è rimasta sostanzialmente invariata tra bianchi e neri americani americano. malattia di Ménière è rara nel sud-ovest degli indiani d'America (Wiet, 1979). In sintesi, al momento non è chiaro se vi siano predisposizioni razziali alla malattia di Meniere.
La condizione sociale sembra invece influenzare la comparsa della patologia, dato che essa colpisce più frequentemente le classi sociali medio-alte Tran Ba Huy P 1989.
Nonostante possa manifestarsi a qualsiasi età, la malattia di Ménière compare più spesso tra la quarta e la sesta decade di vita; è un evento piuttosto raro prima dei 20 anni Brette MD, 1989; ed eccezionale nel bambino McClure JA, 1981 ; Inoltre, gran parte dei bambini colpiti dalla malattia di Ménière può in realtà essere classificata come affetta da sindrome di Ménière «secondaria o sintomatica», dato il riscontro anamnestico di ipoacusie conseguenti a parotite, a meningiti da “Haemophilus influenzae”, a una frattura del temporale, a patologie otologiche congenite o embriopatiche, evolute in una classica triade di Ménière alcuni anni più tardi Hausler R, 1987 ; La predominante lateralità sinistra osservata nel corso della malattia di Ménière non è stata spiegata Heermann J. 1993 ; Infine, la frequente insorgenza di casi multipli nella stessa famiglia lascia supporre la presenza di fattori genetici predisponenti Bernstein J 1965 ; Birgerson L, 1987 ;
5) QUALI SONO I CRITERI PER PORRE DIAGNOSI DI MALATTIA DI MÉNIÈRE?
Crisi di vertigine rotatoria di durata oscillante tra 20 minuti e alcune ore.
La diagnosi di Malattia di Ménière non è sempre facile soprattutto nelle fasi iniziali della malattia per la variabilità con la quale i diversi sintomi si presentano. La monolateralità dei disturbi aiuta la diagnosi in fase iniziale mentre non è raro nelle fasi avanzate l’interessamento dell’altro orecchio. Durante le crisi il nistagmo batte sul lato dell'orecchio malato, dopo la crisi batte sull'altro lato. Le vertigini sono accompagnate da segni neurovegetativi quali nausea e vomito e si possono verificare con una frequenza molto variabile da diverse volte a settimana a solo una volta all'anno
La sintomatologia della MdM è caratterizzata da un insieme di sintomi quali:
Attacchi spontanei e ricorrenti di vertigine oggettive (rotatorie, violente, a crisi, della durata di ore/giorni, cadute improvvise (Drop attacks iporeflessia vestibolare nell’orecchio interessato));
Ipoacusia percettiva(perdita di udito dovuta a danni dell'orecchio interno ipoacusia fluttuante, interessamento iniziale delle basse frequenze, elevato rapporto SP/AP all’elettrococleografia nell’orecchio);
Ovattamento auricolare [fullness Diplacusia (sensazione di rimbombo o eco) ];
Acufeni soggettivi e senso di orecchio pieno.
L'ipoacusia, l'ovattamento auricolare e gli acufeni (sintomi cocleari) e la vertigine (sintomo vestibolare) devono essere contemporaneamente presenti durante la crisi ed interessare l'orecchio colpito .
La vertigine, accompagnata da nausea e vomito, deve durare non meno di 20 minuti, sino a qualche ora (in media 4 - 5 ore) e deve presentarsi in almeno due episodi.
Durante la crisi, è presente un movimento oculare patologico (nistagmo - Ny) spontaneo, orizzontale-rotatorio, il cui movimento rapido è diretto in un primo momento (fugace) verso l'orecchio patologico e successivamente verso l'orecchio sano.
L'ipoacusia è di tipo percettivo (neurosensoriale) e abitualmente fluttuante nelle fasi precoci della malattia, anche se tali oscillazioni dell'udito non sono sempre presenti né necessarie per la diagnosi. Inizialmente coinvolge le frequenze gravi (250Hz-500Hz), estendendosi in seguito alle frequenze medie (1000Hz-2000Hz) ed acute (4000Hz-8000Hz) con curva piatta (pantonale).
6) STADIAZIONE
L'entità dell'ipoacusia consente la stadiazione della malattia in 4 gradi (Tabella 1-3) e deve essere accertata strumentalmente in almeno una occasione.
|
STADIO |
PTA (dB) |
|
1 |
25 |
|
2 |
26-40 |
|
3 |
41-70 |
|
4 |
>70 |
Tab. 1. Stadiazione della MdM. La stadiazione è basata sulla media di 4 toni (media aritmetica arrotondata al numero intero più vicino) della soglia uditiva tonale a 0.5, 1, 2, e 3 kHz. del peggiore audiogramma rilevato nei sei mesi precedenti l'inizio della terapia.
L'acufene e la fullness devono essere presenti nell'orecchio patologico e rivestono carattere variabile da soggetto a soggetto.
È molto importante che tutte le patologie in grado di manifestarsi con un quadro clinico simile alla MdM siano escluse: in particolare, i disturbi immunitari dell'orecchio interno, le neoformazioni dell'ottavo nervo cranico, le alterazioni metaboliche sistemiche e le patologie vascolari.
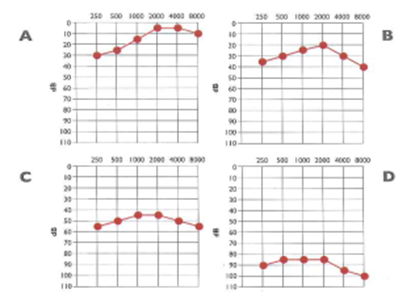
Fig.1.7 A-D
TIPOLOGIA DI CURVA AUDIOMETRICA NELLE DIVERSE FASI EVOLUTIVE DELLA MALATTIA DI MENIERE
L’ipoacusia neurosensoriale della \IdM rappresenta uno degli elementi cardine ai fini diagnostici. Pui con notevoli variazioni inrerindividuali, all’inizio l’ipoacusia si presenta frequentemente con un prevalente interessamento sui toni gravi (curva audiometrica in salita) (Figura 7a), per poi colpire i toni aci.iti (aspetto a V rovesciata) (Figura 7b) ed infine assumere un aspetto pantonale (Figura 7c) (Staljle et al., 1991).
Raramente in fase avanzata si assiste ad una anacusia forse perché il danno istopatologico interessa solo parzialmente le cellule ciliare interne o per una maggiore protezione offerta dalle terminazioni nervose a calice presenti nelle cellule ciliare di tipo I nei confronti dell’intossicazione da potassio (Figura 7d) .Sulla base dell’entità dell’ipoacusia (calcolata sulla media delle frequenze 0.5, 1, 2, 3 KHz, pure tone average, PTA) è stata proposta una stadiazione della MdM ((Tabella 1-3).
La fluttuazione, intesa come variazione di almeno 10 dB del valore di soglia, è elemento distintivo dell’ipoacusia della MdM, specialmente nelle fasi iniziali laddove il calo uditivo può frequentemente risol ersi del tutto. Nella maggioranza dei pazienti l’ipoacusia tende a stabiliz— zarsi mediamente dopo 5 anni dall’esordio della sintomatologia assumendo un aspetto pantonale senza più flumiazioni Uno speciale comitato internazionale ha codificato con precisione i sintomi che devono essere presenti nella sindrome per poter essere classificata come tale. Ciò rappresenta uno sforzo medico per ridurre la confusione nella terminologia ma non ha prodotto, apparentemente, un granché di benefici tra i pazienti
STADI SINDROMICI
Prodromico: sintomi audio-vestibolari sfumati.
Florido: sintomi cocleari fluttuanti, che si accentuano prima della crisi vestibolare.
Inveterato: sintomi cocleari stabili e cronici; instabilità.
7) QUADRO SEMEIOLOGICO
● Stadio Prodromico
- Segni cocleo-vestibolari incostanti: lieve deficit uditivo fluttuante, possibile asimmetria dinamica del guadagno del riflesso vestibolo-oculomotore.
● Stadio Conclamato
- In fase acuta:
Skew deviation, ciclotorsione e tilt della verticalità omolaterali alla lesione.
Asimmetria statica e dinamica del guadagno del riflesso vestibolo oculomotore: nistagmo irritativo e quindi deficitario Bance et al., (1991); Xia et aI., (2002) , test di Halmagyi positivo, inversione della direzione del nistagmo alla prova termica simultanea ghiacciata, inversione della direzione del nistagmo indotto daUo stimolo vibratono (recruitment vestibolare) alterazione dell acuita visiva dinamica
Asimmetria del guadagno statico e dinamico del rifleso vestiboIo-pinale: Romberg, Romberg sensibilizzato, Unterberger patologici.
- In fase intercritica:
Possibile asimmetria dinamica e ad alta frequenza del guadagno del riflesso vestibolo-oculomotore: head-shaking test, test di rotazione rapido di Gufoni, test di Halmagyi patologici. Test vibratorio positivp (in genere, recruitment).
● Stadio inveterato
- Asimmetria a bassa e alta frequenza del guadagno del riflesso vestibolo-oculomotore: iporeflettività omolesionale alle prove di stimolazione binaurale bitermica alternata, head-shaking test, test di Halmagyi positivi.
8) ETIOLOGIA: CHE COSA CAUSA LA MALATTIA DI MÉNIÈRE ?
|
|
|
|
Fig.1.8a: Labirinto membranoso Normale |
Fig.1.8b: Dilated membranous labyrinth in Meniere's disease (Hydrops) (Idrope)Dilatativa del labirinto membranoso nella malattia di Ménière |
L'origine della malattia di Ménière è attualmente controversa. Mentre in passato, si è ritenuto che i problemi idraulici (idrope) nell'orecchio erano responsabili della malattia, l'opinione più corrente è che i problemi idraulici sono solo un marker per la malattia del Ménière , piuttosto che necessariamente essere responsabili dei sintomi .
L’lE(idrope endolinfatica), in base alle diverse eziologie, può essere classificato in:
— embriopatico, generalmente secondario alla displasia tipo Mondini;
— acquisito, laddove sia possibile identificare con precisione la causa del danno a carico dell’ 01, ad esempio virale (come accade nel Delayed Endolvmphatic Hvdrops, DEH), batterica, luetica o post-traumatica;
— idioparico laddove non sia riconoscibile un fattore eziopatogenerico noto; a tale proposito sono state avanzate molte ipotesi, nessuna delle quali realmente convincente e scientificamente provata (Fig. 1.9c ).
Etiologia (tradizionale) della malattia di Ménière : L'opinione più diffusa è che un attacco acuto di malattia di Ménière risultati da fluttuazioni di pressione del fluido all'interno dell'orecchio interno. Un sistema di membrane, chiamato labirinto membranoso, contenente un liquido chiamato endolinfa. Le membrane può diventare dilatata come un pallone, quando aumenta la pressione. Questo si chiama "idrope". Dal momento che l’idrope è stato documentato non solo in tutte le ossa temporali di pazienti menierici ma anche in soggetti asintornatici, è ipotizzabile che l’idrope di per sé non generi il quadro clinico della MdM, ma che uno o più fattori debbano intervenire a produrre il quadro istopatologico e la relativa sintomatologia (Merchant et al., 2005).

fig 1.9c ipotesi avanzate per spiegare le forme di MdM AD ETIOLOGIA IDIOPATICA
(VESTIBOLOGIA CLINICA CASANI-NUTI PAGNINI ED EUREKA 2014)
Un modo perché questo avvenga è quando il sistema di drenaggio, chiamato il dotto endolinfatico o uscita è bloccata. In alcuni casi, il dotto endolinfatico può essere ostruito da tessuto cicatriziale, o può essere stretto dalla nascita. In alcuni casi ci può essere troppo liquido secreto dalla stria vascularis.
Oltre ad una interruzione delle vie di drenaggio, un allargamento abnorme delle vie dei fluidi nell'orecchio interno come l'acquedotto vestibolare o l'acquedotto cocleare possono e essere associata con i sintomi della MdM. Recenti evidenze sono contro una relazione tra l'acquedotto cocleare e MD (Yilmazer et al, 2001). Un acquedotto vestibolare allargato è una delle malformazioni più comunemente identificate nell’orecchio interno osseo nei bambini affetti da ipoacusia neurosensoriale da causa sconosciuta (Oh et al, 2001). L'acquedotto vestibolare si estende dalla parete mediale del vestibolo alla superficie posteriore della rocca petrosa dell'osso temporale. La maggior parte delle persone con acquedotti allargata i con disturbi vestibolari dell'orecchio presentano una perdita uditiva , ma a volte c'è una associazione con problemi vestibolari (Shessel e Nedzelski, 1992). Ci può essere un collegamento genetico tra un acquedotto vestibolare allargato e la sindrome di Pendred, che è un disturbo congenito della tiroide .
Teorie più recenti sull'origine della malattia di Ménière . D'altra parte, l’idrope non si trova in tutte le persone con la malattia di Ménière e l’idrope si riscontra anche comunemente (6%) su studi autoptici di persone che non avevano i sintomi tipici della malattia di Ménière (Honrubia, 1999; Rauch et al, 2001). Perché la malattia di Ménière si verifica in circa 0.2/100 persone , e l’idrope si trova nel 6% delle ossa temporali, c'è un ordine di grandezza in più rispetto ai pazienti con idrope da malattia di Ménière. Così logicamente, ci deve essere qualcosa di più ,della semplice idrope, coinvolti nell'origine della malattia di Ménière
Malattia Autoimmune Dell'orecchio Interno .
Recentemente l'attenzione è stata focalizzata sulla funzione immunologica del sacco endolinfatico ,le malattie immunitarie immune disease immune disease possono contribuire su una sostanziale percentuale di pazienti con malattia di Ménière . Queste affermazioni in parte si basano su uno studio in cui i pazienti con malattia di Meniere avevano una prevalenza molto elevata (circa del 25%) di malattie autoimmuni della tiroide (Brenner et al, 2004). D'altra parte, Ruckenstein e altri recentemente ottenuto in un grande numero di test di autoimmunologia del sangue ,in un gruppo di 40 pazienti con malattia unilaterale di Ménière, che comprendevano CBC, ANA, anti-Sjoegren, RF, complemento, anticorpi antifosfolipidici, Western Blot per le proteine da shock termico (HSP ) Una proteina da shock termico è una sostanza proteica sintetizzata quando le cellule sono esposte alle alte temperature oppure ad alte condizioni di stress.,  MHA (test per la sifilide), e di Lyme. Solo nel test degli anticorpi antifosfolipidi, sono stati trovati valori aumentati, nel 27% dei pazienti, invece del 6-9% atteso. Proteina anti shock termico è stato trovata nel 6%. Questi autori hanno concluso che è improbabile che un eziologia autoimmune abbia svolto un ruolo significativo nella loro popolazione di Ménière unilaterale (Ruckenstein, 2002). Un'altra interpretazione dei dati è che questi autori potrebbe semplicemente non avere utilizzato un indicatore appropriato per un coinvolgimento autoimmunologico, così come la malattia di Ménière unilaterale possa avere meno cause auto immunologiche rispetto alla malattia di Ménière bilaterale.
MHA (test per la sifilide), e di Lyme. Solo nel test degli anticorpi antifosfolipidi, sono stati trovati valori aumentati, nel 27% dei pazienti, invece del 6-9% atteso. Proteina anti shock termico è stato trovata nel 6%. Questi autori hanno concluso che è improbabile che un eziologia autoimmune abbia svolto un ruolo significativo nella loro popolazione di Ménière unilaterale (Ruckenstein, 2002). Un'altra interpretazione dei dati è che questi autori potrebbe semplicemente non avere utilizzato un indicatore appropriato per un coinvolgimento autoimmunologico, così come la malattia di Ménière unilaterale possa avere meno cause auto immunologiche rispetto alla malattia di Ménière bilaterale.
Si può anche pensare ragionevolmente che l'emicrania (Migraine) sia la causa di (alcuni) casi di malattia di Ménière . L'emicrania è più comune della malattia di Ménière ,di almeno un ordine di grandezza e ciò può consentire la possibilità che le varianti di emicrania siano simili per frequenza , alla malattia di Ménière . I pazienti con Ménière hanno anche emicrania, circa il 50% del tempo. La perdita dell'udito nella malattia di Ménière ( MdM) non segue lo schema previsto per una malattia dell'orecchio interno (ovvero la perdita prima alle alte frequenze, e la perdita delle OAE’s). Il trattamento non farmacologico della MdM (malattia di Ménière) cioè la dieta, è quasi identico a quello dell’ emicrania.
Così, alla fine è che, nella maggior parte dei pazienti con MdM nel 2011, la causa della malattia di Ménière è sconosciuta. E 'più spesso attribuita a infezioni virali dell'orecchio interno, trauma cranico, una predisposizione ereditaria, o ad allergie. L'emicrania può causare sintomi che si sovrappongono con la malattia di Ménière . La causa della malattia è sconosciuta. Esistono varie ipotesi che trovano riscontro in tutta una serie di rilievi anatomopatologici (autopsia) e clinici (esame del paziente).Con il progredire della ricerca, si è stabilito con chiarezza il meccanismo che causa questi sintomi: è un'alterazione dei liquidi labirintici. La manifestazione principale dell’idrope endolinfatica è la dilatazione del labirinto membranoso, che è un sistema di membrane dell’orecchio interno ripiene di liquidi in cui si ritiene esista od una eccessiva produzione, oppure un ridotto riassorbimento. Va detto che mentre non esiste una malattia di Ménière senza idrope endolinfatica (0,2/100 persone) si può avere idrope endolinfatica senza malattia di Ménière (0,6/100 ossa temporali di persone decedute)
Tre meccanismi patologici alla base dell’idrope endolinfatica sono emersi dagli studi anatomopatologici: fibrosi del sacco endolinfatico e dell’epitelio vestibolare, alterato metabolismo delle glicoproteine e infezione virale dell’orecchio interno. Da un punto di vista fisiopatologico il ridotto riassorbimento di endolinfa da parte del sacco endolinfatico, presuppone una ridotta dimensione dell’acquedotto vestibolare nei pazienti menierici.
La predisposizione genetica è supportata dalla prevalenza di alcuni antigeni leucocitari (Cw*07). Le alterazioni del sistema immunitario dall’aumento del rapporto OKT 4/8 e dalla diminuzione delle cellule OKT8-positive
Le alterazioni metaboliche da aumentati livelli di fibrinogeno, D-dimero, leucociti e riduzione dei folati che indicano un generico stato infiammatorio.
Le infezioni virali, sostenute da elevati livelli di immunoglobuline G del virus dell’ herpes simplex nella perilinfa dei pazienti menierici.È peraltro verosimile che molte siano le cause che possono determinare idrope endolinfatica che in alcuni casi si manifesta come malattia di Ménière conclamata. Verosimilmente esiste una predisposizione genetica e fattori scatenanti autoimmunitari, virali e metabolici
L'endolinfa , ma in qualche caso si ipotizza che anche la perilinfa, nei pazienti affetti dalla malattia abbia la tendenza ad accumularsi all'interno del labirinto. Dato che questo ha delle pareti ossee, e quindi inestensibili, un aumento del contenuto provoca un aumento della pressione dei liquidi. Le cellule ciliate dei “sensori” uditivi e dell'equilibrio, che vivono immerse nell'endolinfa ne risultano schiacciate. Il loro funzionamento è compromesso, questo provoca la vertigine e l'instabilità, l'ipoacusia e l'acufene, che possono comparire contemporaneamente o in sequenza casuale. L'accumulo di endolinfa viene definito idrope endolinfatica e può interessare tutto il labirinto oppure solo la parte anteriore o la posteriore. Inoltre, soprattutto nelle fasi iniziali, l'idrope è fluttuante, così come i sintomi. Questo è il motivo del nefasto impatto psicologico della malattia sul paziente. Quando questa è stabilizzata, infatti, è vissuta più facilmente. La sequenza di eventi descritta, estremamente semplificata, sembrerebbe aver risolto il grosso problema relativo alla diagnosi ed alla terapia della malattia di Menière. In realtà esiste ancora una grande zona d'ombra relativa alla causa che provoca il ristagno dell’ endolinfa. Negli ultimi anni si è sottolineato con estrema enfasi il ruolo delle Aquaporine . Con questo nome si identificano delle sorta di canali sulla superficie delle cellule fondamentali per la distribuzione dei liquidi, dentro e fuori le cellule e quindi, nell'organismo. L'apertura e la chiusura di questi canali è regolata da un ormone, prodotto dalla nostra Ipofisi, che è detto Antidiuretico (ADH) . Quando particolari sensori cerebrali, si accorgono che c'è una diminuzione della quantità di acqua, parte un impulso a produrre Ormone Antidiuretico, così che le Aquaporine si chiudono e trattengono acqua

Struttura molecolare della Aquaporine
Anche questo modello di funzionamento, estremamente studiato, non trova però un consenso uniforme e probabilmente non è l'unico con cui si realizza l'idrope. Inoltre, nei casi in cui è possibile studiarne il funzionamento (ed è estremamente raro e difficile da realizzare), si osserva anche un quadro di idrope a carico della perilinfa, e non dell'endolinfa. Tutto ciò rende molto interessante l'ulteriore terreno di ricerca, ma ancora una volta non modifica di molto le possibilità di guarire dalla malattia.
In realtà la scoperta dell'importante ruolo delle Aquaporine e del ADH, ha modificato radicalmente l'atteggiamento terapeutico. I farmaci e la dieta, sono indirizzati in senso opposto a quello che si faceva in passato. Ad esempio l'eccesso di liquidi (l'idrope) può dare origine a reazioni paradosse se trattato per lungo termine con diuretici, considerati per anni il cardine della terapia.
La possibilità di disporre di un numero sempre crescente di esami strumentali permette di identificare chiaramente la causa della sintomatologia. E' fondamentale infatti identificare le fasi iniziali dell'instaurarsi dell'idrope endolinfatica, quando è fluttuante. Infatti durante i primi episodi della malattia, si suppone che non si produca un danno permanente dei recettori. Risolto l'idrope, la pressione scende e questi possono riprendersi. E' importante fare attenzione a quali possono essere i sintomi d'esordio. Spesso è la sensazione di pressione auricolare, la fullness, a presentarsi per prima, frequentemente inosservata, sottovalutata ed erroneamente attribuita ad una disfunzione dell'orecchio medio o della tuba di Eustachio . Purtroppo non è usuale osservare il paziente in questa fase, spesso si è verificato un episodio vertiginoso in seguito alla semplice fullness e quindi si determina un nesso con la malattia di Ménière .
Alla luce di queste considerazioni è necessario riprogrammare l'atteggiamento diagnostico nei confronti degli acufeni, non raramente sintomo di esordio della malattia. Anche se l’acufene è l'unico segno isolato per lungo tempo è necessario sottoporre l'individuo ad un iter esaustivo per la ricerca dell'idrope endolinfatico.
|
|
|
|
Figure 1a: Normal membranous labyrinth Fig.1-10a: labirinto membranoso normale |
1b. Fig.1-10b: Dilated membranous labyrinth in Meniere's disease (Endolymphatic Hydrops) labirinto membranoso dilatato nella malattia di Ménière (Idrope endolinfatica) |
8) ETIOLOGIA: COSA CAUSA LA MALATTIA DÌ MÉNIÈRE ?approfondimento
|
|
|
|
Fig.1-11a:labirinto membranoso normale della Malattia di Ménière ( idrope endolinfatica)
|
Fig.1.11b : labirinto membranoso dilatato
|
Oggetto ancor oggi di discussione è invece l’eziopatogenesi dell’idrope. La causa della malattia è sconosciuta. Secondo alcuni, esso dipenderebbe da una sregolazione vasomotoria caratterizzata inizialmente da una vasocostrizione dei capillari labirintici e successivamente da una vasodilatazione con aumento della permeabilità vasale e iperproduzione di endolinfa. Secondo altri, l’ idrope endolinfatico potrebbe dipendere invece da un difettoso riassorbimento dell’endolinfa a causa di una alterazione strutturale del dotto e/o del sacco endolinfatico oppure da modificazioni biochimiche della perilinfa o da un aumento delle proteine nell’endolinfa, ecc. Tra le cause vengono citate quella virale, traumatica, tossica, allergica, dismetabolica, ormonale, ecc. Esistono varie ipotesi che trovano riscontro in tutta una serie di rilievi anatomopatologici (autopsia) e clinici (esame del paziente).Con il progredire della ricerca, si è stabilito con chiarezza il meccanismo che causa questi sintomi: è un'alterazione dei liquidi labirintici. La manifestazione principale è l’idrope endolinfatica cioè la dilatazione del labirinto membranoso, sistema di membrane dell’orecchio interno ripiene di liquidi di cui si ritiene esista una eccessiva produzione oppure un ridotto riassorbimento. Va detto che mentre non esiste malattia di Ménière senza idrope endolinfatica (0,2/100 persone) si può avere idrope endolinfatica senza malattia di Ménière (0,6/100 ossa temporali di persone decedute).
Tre meccanismi patologici alla base dell’idrope endolinfatica sono emersi dagli studi anatomopatologici: fibrosi del sacco endolinfatico e dell’epitelio vestibolare, alterato metabolismo delle glicoproteine e infezione virale dell’orecchio interno. Da un punto di vista fisiopatologico il ridotto riassorbimento di endolinfa da parte del sacco endolinfatico, supportata dalle ridotte dimensioni dell’acquedotto vestibolare nei pazienti menierici.
La predisposizione genetica è supportata dalla prevalenza di alcuni antigeni leucocitari (Cw*07). Le alterazioni del sistema immunitario dall’aumento del rapporto OKT 4/8 e dalla diminuzione delle cellule OKT8-positive
Le alterazioni metaboliche da aumentati livelli di fibrinogeno, D-dimero, leucociti e riduzione dei folati che indicano un generico stato infiammatorio.
Le Infezioni Virali, supportate da elevati livelli di immunoglobuline G del virus herpes simplex nella perilinfa dei pazienti menierici.È peraltro verosimile che molte siano le cause che possono determinare idrope endolinfatica che in alcuni casi si manifesta come malattia di Ménière conclamata. Verosimilmente esiste una predisposizione genetica e fattori scatenanti autoimmunitari, virali e metabolici .
L'endolinfa , ma in qualche caso si ipotizza anche la perilinfa, nei pazienti affetti dalla malattia ha tendenza ad accumularsi all'interno del labirinto. Dato che questo ha delle pareti ossee, e quindi inestensibili, un aumento del contenuto provoca l'aumento della pressione dei liquidi. Le cellule ciliate dei “sensori” uditivi e dell'equilibrio, che vivono immerse nell'endolinfa ne risultano schiacciate. Il loro funzionamento è compromesso, questo provoca la vertigine e l'instabilità, l'ipoacusia e l'acufene, che possono comparire contemporaneamente o in sequenza casuale. L'accumulo di endolinfa viene definito idrope endolinfatico , e può interessare tutto il labirinto, solo la parte anteriore o la posteriore. Inoltre, soprattutto nelle fasi iniziali, l' idrope è fluttuante, così come i sintomi. Questo è il motivo del nefasto impatto psicologico della malattia sul paziente. Quando questa e stabilizzata, infatti, è vissuta più facilmente. La sequenza di eventi descritta, estremamente semplificata, sembrerebbe aver risolto il grosso problema relativo alla diagnosi ed alla terapia della malattia di Menière. In realtà esiste ancora una grande zona d'ombra relativa alla causa che provoca il ristagno di endolinfa. Negli ultimi anni si è sottolineato con estrema enfasi il ruolo delle Aquaporine . Con questo nome si identificano delle sorta di canali sulla superficie delle cellule fondamentali per la distribuzione dei liquidi, dentro e fuori le cellule e quindi, nell'organismo. L'apertura e la chiusura di questi canali è regolata da un ormone, prodotto dalla nostra Ipofisi, che è detto Antidiuretico (ADH) . Quando particolari sensori cerebrali, si accorgono che c'è una diminuzione della quantità di acqua, parte un impulso a produrre Ormone Antidiuretico, così che le Aquaporine si chiudono e trattengono acqua.

Fig.1-5
Struttura molecolare della Aquaporine
Anche questo modello di funzionamento, estremamente studiato, non trova però un consenso uniforme e probabilmente non è l'unico con cui si realizza l'idrope. Inoltre, nei casi in cui è possibile studiarne il funzionamento (ed è estremamente raro e difficile da realizzare), si osserva anche un quadro di idrope a carico della perilinfa, e non dell'endolinfa. Tutto ciò rende molto interessante l'ulteriore terreno di ricerca, ma ancora una volta non modifica di molto le possibilità di guarire dalla malattia.
In realtà la scoperta dell'importante ruolo delle Aquaporine e del ADH, ha modificato radicalmente l'atteggiamento terapeutico. I farmaci e la dieta, sono indirizzati in senso opposto a quello che si faceva in passato. Ad esempio l'eccesso di liquidi (l'idrope) può dare origine a reazioni paradosse se trattato per lungo termine con diuretici, considerati per anni il cardine della terapia.
Di seguito è riportato l'ipotesi centrale che la sindrome di Meniere è causata da idrope fetale.
Ipotesi centrale della malattia di Meniere (Merchant et al., 2005 fig.1.12).
|
|
|
Central hypothesis of Meniere's disease (Merchant et al, 2005) |
Recentemente, più generalmente l’idea accettata che la malattia di Ménière e l’idrope endolinfatica siano sempre associate è stata messa in discussione.L’ idrope non si trova in tutte le persone con malattia di Ménière ed anche comunemente si trovano l’idrope nel 6% negli studi autoptici di persone che non avevano alcun sintomi tipico della malattia di Ménière(Honrubia, 1999; Rauch et al., 2001). Perché la malattia di Ménière si verifica in circa 0,2/100 persone e l’ idrope è presente nel 6/% delle ossa temporali, non c'è più di un ordine di grandezza più persone con idrope di malattia di Ménière . Così logicamente, ci deve essere qualcosa di più che semplicementel’ idrope coinvolta nell'origine della malattia di Ménière
La possibilità di disporre di un numero sempre crescente di esami strumentali permette di identificare chiaramente la causa della sintomatologia. E' fondamentale infatti identificare le fasi iniziali dell'instaurarsi dell'idrope endolinfatico, quando è fluttuante. Infatti durante i primi episodi della malattia, si suppone che non si produca un danno permanente dei recettori. Risolto l'idrope, la pressione scende e questi possono riprendersi. E' importante fare attenzione a quali possono essere i sintomi d'esordio. Spesso è la sensazione di pressione auricolare, la fullness, a presentarsi per prima, frequentemente inosservata, sottovalutata, erroneamente attribuita ad una disfunzione dell'orecchio medio o della tuba di Eustachio . Purtroppo non è usuale osservare il paziente in questa fase, spesso si è verificato un episodio vertiginoso in seguito alla semplice fullness e quindi si determina un nesso.
Alla luce di queste considerazioni è necessario riprogrammare l'atteggiamento diagnostico nei confronti degli acufeni, non raramente sintomo di esordio della malattia. Anche se questo è isolato per lungo tempo è necessario sottoporre l'individuo ad un iter esaustivo per la ricerca dell'idrope endolinfatico.
Molti autori ritengono che la sindrome di Ménière, che è di solito è attribuita all’ idrope endolinfatico (vedi figura 1 in alto), abbia diverse cause (eziologia). possibilità ragionevoli sono l'ostruzione di deflusso endolinfatico, a livello del dotto endolinfatico, aumento della produzione di endolinfa, o ridotto assorbimento di endolinfa causato da un sacco endolinfatico disfunzionale.
Recentemente, l’etiologia più diffusa , che la malattia di Ménière e l’ idrope endolinfatica siano sempre associate è stata messa in discussione .L’ Idrope non si riscontra in tutte i pazienti con la malattia di Ménière , e l’idrope si riscontra comunemente (6%) su studi autoptici anche di persone che non avevano sintomi di tipo Menieriforme (Honrubia, 1999; Rauch et al, 2001). Perché la malattia di Ménière si verifica in circa 0.2/100 persone, e l’Idrope si trova in 6 / 100 ossa temporali, vi è più di un ordine di grandezza maggiore di pazienti con idrope, rispetto a quelli con malattia di Ménière . Così logicamente, ci deve essere qualcosa di più ,che semplicemente l’ idrope, coinvolti nella genesi della malattia di Ménière.
La spiegazione che la Ménière dipenda, da lesioni unilaterale di un orecchio, come ad esempio un blocco di un "tubo di drenaggio" nelle orecchie, sembrano anche difficile da sostenere in vista che gli studi conosciuti, a lungo termine, indicano che la Ménière diventa bilaterale in circa il 50% di tutte i pazienti, dopo 15 anni (Stahle et al, 1991). Sebbene rotture delle membrane(dell’orecchio interno) si trovano in post-mortem, non vi è alcuna prova di quando queste si verificano. Le rotture potrebbero essere determinate periodicamente, durante i periodi di interessamento uditivo e vestibolare della malattia di Ménière , si dovrebbe accettare l'idea che ci siano fratture multiple delle sottili membrane ,dell’orecchi interno,e che queste membrane vengono riparati più e più volte. Questo ipotesi sembra molto plausibile. E 'anche dubbio che, anche se si dovesse verificare una rottura , la miscela di endolinfa e perilinfa sia sufficiente a creare i sintomi della malattia di Ménière. (Honrubia, 1999)
Di recente si è pure parlato di una etiologia autoimmune considerando che nelle fasi iniziali di alcune malattie sistemiche del connettivo si osservano episodi di sofferenza cocleo-vestibolare a carattere ricorrente del tutto sovrapponibili a quelli che compaiono nella malattia di Ménière. Che all’origine dell’idrope endolinfatico vi possa essere uno stato disreattivo del paziente su base autoimmune, lo confermano i referti istologici di specimen operatori prelevati, durante interventi otochirurgici, su malati affetti da connettiviti sistemiche. Tali prelievi bioptici hanno dimostrato la presenza nel labirinto membranoso di linfociti, plasmacellule e macrofagi, di IgA e IgG nell’epitelio neurosensoriale e nel lume del sacco endolinfatico e di IgG negli elementi plasmacellulan. Recentemente l'attenzione si è concentrata principalmente sulla funzione immunologica del sacco endolinfatico – la malattia immunitaria può contribuire ad una percentuale sostanziale di malattia di Meniere. Continuano ad emergere evidenze che il sacco endolinfatico è parte del sistema immunitario dell’orecchio, e che è coinvolto con le risposte infiammatorie. Vedere nella sezione successiva di questa pagina per ulteriori dettagli. Queste reperti istologici fanno supporre che il sacco endolinfatico non sia soltanto deputato all’assorbimento dell’endolinfa ma svolga anche un’attività di difesa locale di tipo immunologico indipendentemente da quella sistemica. Fattori favorenti sarebbero gli stress psicofisici.
Qualunque sia l’origine dell’idrope, la comparsa della sintomatologia cocleo-vestibolare dipenderebbe. sec. Schuknecht, dalla rottura della parete del dotto cocleare a livello della membrana di Reissner. La fuoriuscita di endolinfa ricca di potassio nello spazio perilinfatico altera i caratteri fisico- chimici della perilinfa che “bagna” la porzione amielinica delle fibre dell’Vili e il tratto laterale delle cellule acustiche determinando una caduta del potenziale di membrana con conseguente improvvisa riduzione degli input cocleari e vestibolari. Secondo Dohlman e Silverstein, una volta che la breccia della parete del labirinto membranoso spontaneamente si è richiusa e la pressione dell’endolinfa ha raggiunto di nuovo i valori normali, il contenuto ionico dei due liquidi labirintici riacquista il corretto equilibrio. Ogni sintomo scompare e, almeno nelle fasi iniziali della malattia, si può anche assistere al recupero totale della funzione recettoriale. Secondo altri Autori, la comparsa del deficit cocleare dipenderebbe dalla deformazione, per l’effetto meccanico dell’idrope, della m. basilare mentre la comparsa della crisi vertiginosa sarebbe conseguenza della dislocazione della cupula dei canali semicircolari a causa della cospicua distensione del dotto cocleare, del sacculo e, in misura minore anche dell’utricolo. Altri Autori sono invece dell’idea che la sintomatologia dipenda da modificazioni del flusso ematico nella rete capillare del labirinto dovuto all’idrope endolinfatico (Andrews J.C. et all., 1991).
Si incomincia a credere che la malattia di Ménière e l'emicrania siano due facce indistinguibili della stessa condizione. Questo può essere il caso che ricorre in alcune persone. Circa il 50% delle persone con la Ménière soddisfano i criteri per l'emicrania, e per questo motivo, è spesso una buona idea per provare il vasto repertorio di trattamenti di emicrania nelle persone con malattia di Ménière
Una sintesi del pensiero attuale è che la sindrome di Ménière sembra essere la via finale comune che l'orecchio interno risponde a quasi tutte le lesioni, e che la genesi della malattia di Ménière abbia molte cause, alcune delle quali riflettono i traumi ed altre che riflettono processi metabolica più generalizzati o genetica che colpiscono entrambe le orecchie in maniera abbastanza simmetricamente.
Le cause specifiche includono:
Virus
- gli anticorpi dell’Herpes virus (HSV) si trovano più comunemente in pazienti con la Ménière (Arnold e Niedermeyer, 1997). E’stato trovato DNA virale ,da herpes simplex nel ganglio vestibolare di persone con Meniere da Vrabec (2003), ma non da Welling, che inoltre non ha trovato CMV o varicella-zoster (Welling et al, 1997). Antigene HSV e HSV DNA si trovano anche nel sacco endolinfatico e dell'epitelio di persone sane. Ci sono alcuni dati recenti patologici che sostengono una causa virale (Gacek e Gacek, 2001). Linthicum ha riferito recentemente che l'herpes simplex DNA si trova nei sacchi endolinfatico di 12 dei 16 casi di Meniere, contro i 2 di 26 controlli (Linthicum, 2001). Ricercatori giapponesi hanno segnalatori avere trovato varicella-zoster in 7 / 10 sacche endolinfatiche di pazienti con Meniere, 4 con Epstein Barr Virus, e 1 con citomegalovirus (Yazawa et al, 2003). Stranamente, nei loro casi ,non dei avevano trovato nel sacco endolinfatico HSV-1 o 2 int. Studi sul trattamento con farmaci antivirali raramente hanno dimostrato un effetto positivo, e ci sono dubbi su su una relazione di riferisce una risposta (ad esempio, Gacek, 2008) Queste scoperte sono interessanti, si è un po 'perplessi in qualche caso, e c’è bisogno di ulteriori indagini.
L’otosifilide è in grado di produrre un quadro clinico identico a Ménière . Pulec ha indicato che la sifilide è la causa della malattia di Ménière nel 6% dei casi (1997). Questo dato molto più alto di quanto trovano dall'autore che ha riscontrato meno dell'1% in tutti i pazienti che hanno un test FTA positivo per la sifilide
Predisposizione ereditaria
L’ipotesi da alcuni avanzata sul carattere famigliare della malattia fino a qualche anno fa molto controversa per le scarse conoscenze delle alterazioni genetiche che sottendono la ventilata trasmissibilità di questa lesione labirintica, sembra trovar oggi conferma dalle recenti ricerche di Fransen e Coll. (1999). Da uno studio eseguito sui componenti di tre nuclei famigliari affetti da una forma ricorrente di cocleovestibolopatia del tutto simile a quella della m. di Ménière, risulterebbe la presenza di un’alterazione genica (COCH gene) a livello del cromosoma 14. Secondo gli Autori, tale riscontro potrebbe aprire nuove prospettive per la precisazione eziologica della malattia. Pertanto, l’analisi della mutazione di tale gene dovrebbe venir condotta nei pazienti affetti da m. di Ménière.
L’unico dato sul quale da tempo tutti concordano è la presenza dell’ idrope che inizialmente interessa il dotto cocleare e il sacculo e successivamente l’intero spazio endolinfatico labirintico. Circa uno su tre pazienti con la malattia di Ménière hanno un parente di primo grado con malattia di Ménière. In teoria, la predisposizione ereditaria potrebbero essere connessa alle differenze anatomiche dei canali per i liquidi endolinfatici all'interno dell'orecchio o a differenze nella risposta immunitaria (vedi più avanti).
Allergia
Per quanto riguarda l'allergia, Derebery (1966) ha suggerito che il 30% dei pazienti con malattia di Meniere hanno allergia alimentare, e ha suggerito che l'allergia può giocare tre ruoli:
1)Il sacco può essere l "organo bersaglio" dei mediatori rilasciati da inalanti sistemici o reazioni agli alimenti.
2)La deposizione di complessi immuni circolanti può produrre l'infiammazione e interferire con capacità di filtraggio del sacco;
3)Una infezione virale predisponenti può interagire con le allergie in età adulta e causare uno scompenso del sacco endolinfatico , con conseguente idrope endolinfatica (Derebery, 1996).
Tutte queste ipotesi riguardano il sacco endolinfatico, ma alcuni autori ritengono che il sacco non è necessariamente il colpevole. In vista dell’idea attuale che l’idrope non può essere la chiave nella patologia di tutte le malattie di Ménière, questo concetto deve essere rivisto. Nella nostra l'esperienza la Ménière e l’allergia non sono intimamente legate. L’immunoterapia per l'allergia, nella nostra esperienza , non è quasi mai un trattamento vitale per la malattia di Meniere.
Disordini autoimmuni
c’è una considerevole evidenza che la malattia Ménière è causata da meccanismi autoimmuni, almeno qualche volta. Un tipo di patologia a cui ultimamente è stato attribuito un ruolo non trascurabile come causa o concausa di forme di sordità o disordine uditivo, è la patologia autoimmunitaria.
Il sistema immunitario è complesso e ci sono diversi modi che possono danneggiare l’ orecchio interno. La causa di malattia autoimmune dell’orecchio interno è presumibilmente connessa al danno di quest’organo da parte di un anticorpo o di cellule immunitarie.
A riguardo esistono diverse teorie su come questi anticorpi potrebbero indurre disturbi autoimmuni:
Danno da citochine: quest’ultime dopo essere rilasciate provocano ulteriori reazioni immunitarie. L’attivazione dei linfociti T, iniziata dal complesso immunogeno,è avviata e completata da fattori solubili. Le citochine costituiscono un network molecolare complesso,infatti nell’economia del sistema immunitario esse agiscono amplificando le capacità proliferative e differenziative delle cellule immunocompetenti, contribuendo a modulare e regolare la risposta immunitaria.
Le ipoacusie autoimmuni, più correttamente definibili “immuno-mediate”, sono neurosensoriali a localizzazione elettiva cocleare; possono essere improvvise o progressive, monolaterali ma più spesso bilaterali; possono
essere caratterizzate da una soglia di audiometria atipica ma spesso sovrapponibile al classico quadro della Malattia di Ménière; sono spesso accompagnate da acufeni e/o disturbi vertiginosi.
Insorgono più frequentemente nell’età giovanile ed in quella adulta.
Possono essere forme isolate, cioè non accompagnate ad altri disturbi o patologie in altri apparati, ma in un terzo di casi si tratta di forme sindromiche o sistematiche in cui coesistono altre manifestazioni patologiche di origine autoimmune, quali tireopatie, lupus eritematoso, sclerodermia, artite reumatoide,poliartrite nodosa, malattia di Behcet, granulomatosi di Wegener.
Nella patologia autoimmune dell’orecchio interno è coinvolta sia l’immunità umorale che cellulare. La disfunzione dell’orecchio interno può cominciare da un lato ma può evolvere colpendo anche l’altro, conducendo ad una perdita bilaterale completa della funzione uditiva e vestibolare a meno che non venga iniziata una terapia specifica.
Sono state identificate tre sindromi cliniche caratteristiche:
1. l’orecchio interno viene colpito unitamente ad altri organi in corso di patologia autoimmune sistemica(poliarterite,artrite reumatoide, rettocolite ulcerosa).
2. coinvolgimento dell’orecchio interno unitamente a cheratite interstiziale (sindrome di Cogan)
3. coinvolgimento del solo orecchio interno.
4. Spesso i pazienti possono passare da una categoria ad un’altra; la tipica progressione è (3),(2),(1).
5. I segni clinici spesso cominciano con ipoacusia fluttuante, senso di pressione auricolare, acufeni e vertigine,sintomi caratteristici dell’idrope endolinfatica la cui diagnosi si basa sul riscontro dei segni clinici caratteristici, unitamente agli esami di laboratorio che confermano il deficit immunitario.
A tal proposito il riconoscimento dell’ auto-anticorpo nel siero del paziente è fondamentale per confermare la diagnosi di malattia di Meniere ad etiologia autoimmune. L’autoimmunità è un errore che l’organismo fa nel riconoscere come estranee delle cellule che invece sono sue.
La conseguenza è la produzione di auto-anticorpi con danni ai tessuti e agli organi. Questa è la dinamica del “war game” biologico che caratterizza le malattie autoimmuni.
Anche se le cause non sono ancora conosciute, numerosi sono gli studi che puntano dritto ad un problema che affligge molte persone .
Il midollo osseo e gli organi linfatici maggiori producono e modulano la funzione di alcune cellule che si trovano nel sangue.Si tratta dei globuli bianchi o linfociti.
Al momento della nascita il sistema immunitario esegue una sorta di “inventario” di tutti i tessuti, cellule e sostanze del nostro organismo riconosciute come proprie (il “self”). Normalmente il sistema immunitario si auto- regola attraverso stimoli di attivazione e di inibizione, garantendo la tolleranza immunologia.
Come tutti i sistemi biologici, anche il sistema immunitario può impazzire. Nelle malattie autoimmuni prevalgono aberranti stimoli di attivazione ed i linfociti iperstimolati perdono la capacità di riconoscere sostanze proprie sane (il “self”) provocando una anomala reazione di distruzione autoimmune rivolta verso tessuti e cellule sane dell’organismo che vengono trattati come se fossero sostanze estranee.
Le malattie autoimmunitarie sono malattie multifattoriali, dove di fondamentale importanza è la presenza di una predisposizione genetica a sviluppare la malattia. Questa predisposizione può evolvere in malattia quando il paziente viene in contatto con determinati fattori ambientali (virus, batteri, farmaci, etc, etc.) che attivano in maniera irreversibile e progressiva la malattia.
Tuttavia queste malattie non sono ereditarie nel senso stretto della parola ma esiste sicuramente una predisposizione di alcune famiglie a sviluppare malattie autoimmuni.
Un altro fattore causale di queste malattie sono gli ormoni femminili. Infatti le donne sono maggiormente colpite da malattie autoimmuni rispetto ai pazienti di sesso maschile. Inoltre si ha un picco di comparsa intorno ai 15/20 anni o nell’età pre- menopausale 45/50, e tutto ciò suggerisce un importante ruolo ormonale nella genesi delle malattie.
Ogni malattia autoimmune è quindi caratterizzata dalla presenza nel siero di auto-anticorpi circolanti.
Oltre ai comuni test di laboratorio oggi impiegati per la diagnosi generica di malattia autoimmune (Ab anti-nucleo, anti-tireoglobulina, anti-perossidasi, anti-muscolo liscio, anti-cardiolipina, ecc.) è stato recentemente introdotto un test di laboratorio assai più specifico per l’apparato uditivo. Si tratta del cosiddetto “OTOblot”: esso ricerca ed identifica nel siero del soggetto affetto gli anticorpi diretti verso un antigene da 68 KDa (hsp-70) associato a perdite uditive autoimmuni.
Il test ha una sensibilità del 42%, una specificità del 90% ed un valore predittivo del 91% ai fini di una risposta positiva ai corticosteroidi. La malattia di Meniere su base autoimmunitaria e le ipoacusie autoimmunitarie non possono ancora giovarsi di terapie molto specifiche ma possono comunque avvalersi del trattamento corticosteroideo o immuno-soppressivo mediante metotrexate o citoxan.
Le linee guida per la terapia delle patologie autoimmuni dell’orecchio interno sono controverse. Sono stati tentati molti schemi terapeutici con risultati contrastanti. C’è un generale accordo, comunque, che il trattamento iniziale dev’essere condotto con steroidi ad alte dosi per i primi giorni. Segue poi una terapia a scalare, fino ad arrivare ad una dose di mantenimento che viene somministrata per alcuni mesi. La terapia è tanto più efficace quanto più precocemente viene iniziata. Dopo la sospensione della terapia, normalmente vi è un periodo di stabilità, ma non è eccezionale la ripresa della malattia anche dopo un lungo periodo di quiescenza . Se la terapia steroidea fallisce alcuni studiosi hanno proposto l’uso di farmaci citotossici. Recentemente la plasmaferesi è stata utilizzata con buoni risultati in paziente non responsiva alla terapia steroidea e citotossica. In realtà la plasmaferesi rimuove la fase acuta degli immunocomplessi ma non incide sull’evoluzione della patologia di base. Perciò non dovrebbe sostituire la terapia steroidea o citotossica, ma dovrebbe essere utilizzata in combinazione ad essa.

Fig 1.13
Concludendo studi appositamente condotti indicano chiare correlazioni tra alterazioni del sistema vascolare cocleare e compromissione metabolica dell’orecchio interno a seguito di formazioni di immunocomplessi, fattore che sembra sottendere il determinismo patogenetico di specifiche patologie dell’orecchio interno, quali la malattia di Meniere .
Per poter evidenziare il ruolo degli autoanticorpi nella malattia di Meniere o nella ipoacusia autoimmune e quindi stilare un protocollo terapeutico specifico per queste patologie, negli ultimi dieci anni molti studiosi si sono avvalsi per la titolazione dell’autoanticorpo Hsp-70 dell’orecchio interno, responsabile delle ipoacusie neurosensoriali e della malattia di Meniere ad etiologia autoimmune, del test OTOblot, al fine di chiarire la funzione immunitaria dell’orecchio interno e il suo coinvolgimento in alcune malattie sistemiche.
Quindi per i pazienti affetti da malattia di Meniere o da ipoacusia autoimmune si aprono nuovi scenari sia in ambito diagnostico, con l’esame di laboratorio su prelievo ematico venoso OTOblot, che terapeutico, tramite ausili terapeutici ed elettronici , tra cui la laser terapia a basso livello energetico, che possono migliorare la loro qualità di vita.
Circa il 60% dei pazienti con malattia di Meniere hanno anticorpi per le proteine dell'orecchio interno. Circa nel 10% dei pazienti con Ménière sono ben documentate patologie autoimmuni (ma anche la popolazione generale ha un'alta prevalenza di questi disturbi). Una percentuale elevata di pazienti affetti da Ménière hanno anche un tiroidite autoimmune (Brenner et al, 2004). Alcuni pazienti con Ménière mostrano un cambiamento nella loro immunità durante gli attacchi (Mamikoglu et al, 2002).
Vi è evidenza di citochine nella coclea compresa l'interleuchina-1A, TNF-alfa, P65 e P50 NFkB, e IkBa (Adams, 2002). I farmaci che bloccano il TNF come l'etanercept, sembrano essere potenzialmente efficace nella malattia autoimmune dell'orecchio interno (AIED), (autoimmune inner ear disease (AIED)che ricordano alcune forme della malattia di Ménière (Rahmen et al, 2001).
Attualmente l'ipotesi migliore è che il percorso immunologico per la malattia di Meniere coinvolga il sacco che è l'organo immunitario, o "linfonodo" dell'orecchio. La stimolazione immunitaria del sacco può disturbare la sua funzione di regolamentazione dei fluidi, o può causare idrope attraverso meccanismi indipendenti come la produzione dei mediatori infiammatori. Clicca qui per maggiori dettagli (Click here for more detail )circa la malattia autoimmune dell'orecchio interno.
Fattori genetici: c'è prova che gli aspetti geneticamente controllati del sistema immunitario possono aumentare o altrimenti essere associato con l'aumento della suscettibilità Ai comuni disturbi dell'udito, come la malattia di Meniere. Bernstein e associati ha riferito che il 44% dei pazienti con Meniere, otosclerosi e presbiacusia striatale aveva una particolare esteso MHC aplotipo (Dqw2-Dr3-c4Bsf-C4A0-G11: 15-Bf:0.4-C2a-HSP70:7.5-TNF), rispetto a solo il 7% dei controlli. La perdita improvvisa dell'udito nei coreani che non si recupera è anche associato con HLA-DRB1 * 04, DQA1 03 e 05 (Yeo et al, 1999; Yeo et al, 2001). L'autore ha anche trovato un'associazione (negli USA) con alcuni tipi di HLA (Human leukocyte antigen) - antigene umano leucocitario, cioè il complesso maggiore di istocompatibilità della specie umana e varianti di vertigine in caucasici (inedito). D'altra parte, un recente studio di Lopez-Escamez e altri eseguiti in Spagna non ha trovato alcuna differenza di antigeni HLA tra 54 pazienti con definita MdD e 534 controlli normali (Lopez Escamez et al, 2002). Lo sfondo genetico degli studi HLA è importante ed è possibile che un gruppo potrebbe trovare differenze HLA, che non si trovano in altre patologie .
Questi dati sono così in conflitto. Se c'è infatti un'associazione con HLA, almeno in alcune popolazioni, si vorrebbe suggerire che della malattia di Ménière ed altre sindromi progressive potrebbero essere causate da disfunzioni immunitarie che è ciò che attualmente in genere si crede. È importante ricordare che la tipizzazione HLA è rilevante quando considerato nel contesto genetico di fondo del paziente. In altre parole, gli studi su pazienti coreani , ad esempio, come riportato da Yeo, potrebbero non essere applicabili al pazienti di etnia non coreana.
Traumi cranici ed acustici
Questo è un argomento controverso a causa della natura altamente litigiosa dei sintomi dopo le lesioni alla testa. Da una visione d'insieme i dati della letteratura non sono definitivi circa la connessione tra la malattia di Ménière e traumi. Ciò è probabilmente dovuto alla mancanza di una chiara definizione della malattia di Ménière ed anche la difficoltà intrinseca di quantificare i traumi cranici. Sembra molto ragionevole per noi che la malattia di Ménière, che ha un gran numero di potenziali meccanismi e delle cause e "definizioni" molto inclusiva l'esigenza che solo un unica anormalità obiettiva (perdita dell'udito), potrebbe essere causata da un trauma cranico.
Ci sono certamente dei casi di sindrome post-traumatica di Ménière. Questi casi sono attribuiti ai cambiamenti idrodinamici causate da cicatrici da sanguinamento nell'orecchio interno. Ci sono anche casi riportati di Ménière dopo frattura dell'osso temporale, e anche semplicemente dopo lesioni da accelerazione-decelleratione (Dibiase e Arriaga, 1997).
Esposizione a rumore impulsivo intenso(come lo sparo di una pistola) è stato suggerito da alcuni come causa di malattia dell'orecchio interno e sintomi simili a quelli della malattia di Ménière. Vi è una certa polemica qui però, in uno studio molto grande di 17.245 veterani israeliani viene suggerito che non vi era alcun effetto per una malattia di Ménière (Segal e Avitar, 2003). A nostro parere, il rumore forte impulso non causa la malattia di Meniere.
9) FISIOPATOLOGIA ED ANATOMIA PATOLOGICA
La fisiopatologia della malattia di Ménière è ancora imprecisa, a dispetto di numerosi lavori sperimentali che in questa sede non è possibile sintetizzare in modo esauriente; per questo ci si limiterà a illustrare i più importanti, differenziando gli studi istopatologici sull'uomo (casistiche autoptiche) dai modelli sperimentali. Prima di tutto, si impone un breve richiamo anatomico
Cenni di anatomia
L'acquedotto del vestibolo è un canale osseo molto stretto (0,5 mm di diametro per gran parte del suo decorso), che si estende dal vestibolo alla cavità cranica. Esso si diparte dalla parete mediale del vestibolo, all'estremità superiore della doccia sulciforme, al di sotto e davanti all'orifizio non ampollare dei canali semicircolari superiore e posteriore. Da lì, si dirige in direzione posteriore, medialmente e in basso, descrivendo una curva a concavità infero-laterale, per andare ad aprirsi sulla parete postero-superiore della rocca, a livello della fossetta ungueale, 1 cm circa dietro al foro del meato acustico interno
Il condotto endolinfatico origina dall'unione di due sottili canalicoli, che si distaccano dalle pareti mediali dell'utricolo e del sacculo. Questo canale si impegna nell'aquedotto del vestibolo e termina sotto la dura madre dell'angolo ponto-cerebellare, a livello della fossetta ungueale, con un rigonfiamento, il sacco endolinfatico. Il grado di vascolarizzazione di questa regione è probabilmente finalizzato a possibili e numerosi scambi di liquidi.
Studi istopatologici sull'uomo
Idrope endolinfatica
Il primo passo verso la comprensione della patogenesi della malattia di Ménière fu il riscontro istologico di un'idrope endolinfatica per merito di Hallpike e Cairns nel 1938. Questi Autori descrissero, sulle rocche di pazienti deceduti per postumi di neurotomia vestibolare, l'esistenza di una distensione del labirinto membranoso, che chiamarono «idrope endolinfatica». Rauch, nel 1989, constatò, in uno studio in doppio cieco condotto su 119 pazienti e basato su rilievi clinici e sullo studio istopatologico dell'osso temporale, che 13 pazienti con malattia di Ménière clinicamente evidente avevano un'idrope endolinfatica; al contrario, l'idrope endolinfatica era stata riscontrata solo su 6 di 106 pazienti appartenenti al gruppo di controllo, privi di sintomatologia clinica suggestiva per malattia di Ménière ( Rauch S.,1989).
Queste considerazioni conferiscono all'idrope un ruolo patogenetico centrale
Il principale aspetto istopatologico della MdM è rappresentato da un incremento di volume dell’endolinfa associato ad una dilatazione dell’intero sistema endolinfatico (Figura 1) con prevalenza del dotto cocleare e del sacculo, che presenta pareti molto meno spesse rispetto a quelle dell’utricolo (Schuknecht, 1993).
Tuttavia, è doveroso precisare che la IE non è sinonimo di MdM: è dimostrata la presenza di segni istopatologici
di idrope in ossa temporali di soggetti che in vita mai hanno evidenziato sintomi cIinici compatibili con MdM (Merchant et al,, 2005). La dilatazione del sacculo può determinarne un’estroflessione nel canale semicircolare laterale ed un contatto anomalo con la superficie interna della platina della staffa definito “vestibolofibrosi” (Nadol, 1977), aspetto che può giustificare il fenomeno di Tullio e/o il segno di Hennebert osservabili in alcuni pazienti.
Tipico è il prolasso verso la scala vestibolare della membrana di Reissner con frequente rottura della stessa da cui una commistione tra endolinfa e perilinfa con una grave alterazione della loro composizione ionica. Anche a livello canalare si possono evidenziare simili distensioni come ad esempio una erniazione dell’utricolo nella crus comune ed un (distacco della cupola dal suo attacco a livello del tetto ampollare (Rizvi 1986),
Nonostante questi reperti, spesso le cellule recettoriali della coclea e delle strutture vestibolari conservano una relativa integrità Schuknecht, et al, 1962). Con tecniche di microscopia più avanzate si è evidenziata una perdita specifica di cellule ciliare vestibolari di tipo lI(Tsuji et al., 2000). Nelle fasi avanzate della malattia si osservano anomalie fino all’atrofia delle cellule sensoriali e di sostegno dell’organo del Corti e delle strutture vestibolari, in associazione con analoga atrofia delle fibre nervose (Albers et al., 1988). Di frequente riscontro una marcata atrofia della stria vascolare ed anomalie del sistema di drenaggio dell’endolinfa (Ikeda e Sando, 1985): fibrosi perisacculare, ipoplasia del dotto e del SE, ridotta vascolarizzazione ed ipoplasia dell’acquedotto del vestibolo e ridotta pneumatizzazione periduttale, reperti confermati da studi radiologici ( Valvassori e Dobben, 1984).
L'idrope si osserva costantemente nel canale cocleare, dove si manifesta con una deformazione della membrana vestibolare che, a seconda dello stadio della malattia, può risultare localizzata o estesa (Antoli-Candela F 1976). In pratica esso inizia sempre all'apice, per poi estendersi al resto della coclea. La membrana vestibolare si distende progressivamente e, nelle fasi avanzate, può riempire tutta la scala vestibolare e coinvolgere la scala timpanica attraverso l'elicotrema. Alla base, il cieco vestibolare del canale cocleare disteso, aggetta nel vestibolo. La gravità dell'idrope sembra correlata a quella dell'ipoacusia: sotto i 70 dB di perdita, resta moderato e prevale all'apice, fatto che probabilmente spiega l'interessamento iniziale delle frequenze gravi; sopra i 70 dB di perdita, è più cospicuo e prevale alla base ( Antoli-Candela F, 1976 ).
L'idrope è spesso riscontrata anche nel sacculo. Quest'ultimo, una volta dilatato, viene a contatto con l'utricolo, con i canali semicircolari e con la base della staffa (platina della staffa), sulla quale si modella in circa il 60% dei casi ( Paparella MM, 1984 ) e con la quale a volte sviluppa aderenze, di cui si illustreranno successivamente le ripercussioni cliniche. L'utriculo e i canali semicircolari sono interessati in modo incostante dall'idrope (Antoli-Candela F, 1976 ; Hilding DA, 1964) , fatto che potrebbe essere imputabile all'azione della valvola utriculo-endolinfatica che protegge a lungo la parte superiore dall'idrope formatosi a valle (Schuknecht HF,1975).
Rotture, fistole e collasso
Le rotture del labirinto membranoso sono state descritte con frequenza variabile in tutte le zone del labirinto a eccezione dell'utricolo e del sacculo
Antoli-Candela(1976 ne distingue due tipi
· il tipo I si osserva solo nel labirinto cocleare e a livello del segmento inferiore del labirinto posteriore, ossia nel punto in cui le pareti membranose sono più sottili, e quindi più suscettibili di artefatti durante la preparazione istologica. I margini, infatti, non sembrano essere oggetto di rimaneggiamento e non presentano alterazioni delle strutture neurosensoriali contigue;
· il tipo II, al contrario, sembra corrispondere a vere rotture ante mortem, che sopraggiungono nel punto massimo di distensione e sono caratterizzate sui loro margini da segni di atrofia o, più spesso, di cicatrizzazione ipertrofica. Talvolta il danno è riparato da un sottile monostrato cellulare. Altrove, questo tipo di rottura porta alla formazione di una fistola organizzata e permanente tra gli spazi endo- e perilinfatico, addirittura tra le stesse strutture endolinfatiche, con frequente collasso delle pareti o delle strutture adiacenti.
Nonostante ciò, le rotture non sono state riscontrate da tutti gli Autori (Antoli-Candela F,1980 ; Paparella MM,1984),fatto che rimette in discussione questa teoria e che fornisce un argomento di un certo peso alla teoria dell'intossicazione potassica, che verrà descritta più avanti
Lesioni fibrotiche
In molti casi, è stata osservata una proliferazione di tessuto fibroso all'interno del labirinto, tra membrana vestibolare ed endostio cocleare della scala vestibolare o tra le membrane vestibolari e le pareti del vestibolo osseo. Fasci fibrosi attraversano così la cavità labirintica, ancorando in particolare la base della staffa alle strutture vestibolari profonde (Schuknecht HF,1993).
Organi sensoriali
L'organo spirale (o del Corti) la cresta ampollare e le macule acustiche non presentano lesioni significative. Le alterazioni osservate a questo livello sembrano indipendenti dalla malattia e, piuttosto, in rapporto all'età (Altman F 1943 ; Kristensen HK 1962).
Nell'organo del Corti può essere osservata una perdita di cellule ciliate, un'atrofia delle cellule di sostegno, una distensione o un'atrofia della membrana tectoria. Queste diverse lesioni sono più frequenti all'apice e si accompagnano talvolta a una perdita dei neuroni corrispondenti. Il ganglio spirale non presenta anomalie di rilievo. Nel vestibolo, le creste sono compresse dalle pareti vestibolari dilatate, fatto che ne altera il movimento (Rivzi SS, 1986).
Le macule otolitiche utricolari e sacculari sono a volte scompaginate, ma è molto raro osservare un danno delle fibre nervose vestibolari (Tran Ba Huy P,1989).
Stria vascolare e tessuti secretivi
Anche se nella loro prima descrizione Hallpike e Cairns avessero segnalato una degenerazione della stria vascolare, ciò non ha trovato conferme negli studi successivi. Le aree di atrofia eventualmente osservate, come per le strutture sensoriali, sembrerebbero essere spiegate da un comune processo di invecchiamento
Al contrario, formazioni papillari coroidee sono state descritte nel ductus reuniens (Schuknecht HF, 1993). Tali strutture sono caratteristiche dei tessuti impegnati nei fenomeni di trasporto e di produzione di liquidi.
Sacco endolinfatico
Al ruolo del sacco linfatico sono stati dedicati numerosi studi istologici, visto che esso sembra essere il sito elettivo in cui l'endolinfa viene riassorbita. Gli Autori che hanno lavorato su questo distretto hanno descritto sia le sue modificazioni, sia quelle dell'acquedotto del vestibolo. Il tessuto fibroso perisacculare e la scomparsa del connettivo subepiteliale sembrano costituire i segni istopatologici più costanti, anche se il loro ruolo patogenetico è tuttora oggetto di discussione. Già descritte da Hallpike e Cairns nel 1938, sono state successivamente riportate da numerosi Autori ( Altman F, 1943 ;Schindler RA,1979 ; Schuknecht HF, 1993). Allo stesso modo, è stata descritta l'esistenza di un processo degenerativo dell'epitelio del sacco con fibrosi e aderenze intraluminali identiche a quelle osservate dopo una infezione virale (Arenberg IK, 1970).
Altri Autori hanno riscontrato segni riferibili a un danno ischemico, potenzialmente riferibile a una marcata riduzione dell'apporto vascolare (Ikeda M, 1985). Queste evidenze confermano i dati del lavoro di Shambaugh 1966 ; che, negli anni Sessanta, constatarono in sede perioperatoria un'ischemia del sacco e l'ostruzione endoluminale dell'acquedotto del vestibolo, immediatamente supportate da osservazioni radiologiche (Clemis JD,1968). Infine, a latere, è stata descritta l'esistenza di lesioni potenzialmente in grado di generare un'idrope, ma non di giustificare la malattia di Ménière: agenesia (Ikeda M, 1985 ; o atrofia Arenberg IK, 1970) ; del sacco, ostruzione o obliterazione del canale endolinfatico da osteoma o esostosi (Altman F, 1965 ) , persino aree di reazione perineoplastica Hallpike C, 1938 ; Nel 1982, Kodama e Sando hanno studiato la morfologia dell'acquedotto del vestibolo e del sacco endolinfatico su 79 rocche petrose di individui senza malattia di Ménière precedentemente diagnosticata. Essi osservarono 17 ipoplasie a carico di queste due strutture (21,5%), 38 normoplasie (48,1%) e 24 iperplasie (30,4%). Nel 1984, Sando e Ikeda studiarono le rocche di 27 soggetti affetti dalla malattia di Ménière; 16 di esse erano ipoplasiche, ossia il 59,3%. Come già descritto nel capitolo della diagnostica per immagini, scansioni della rocca dimostrano nei pazienti con Ménière un'ipoplasia della regione retrolabirintica (Sando I, 1984 ; Yazawa Y1994). Nel 1997, Takeda et al hanno dimostrato, con piani di scansione obliqui, che i pazienti portatori di Ménière hanno un'ipoplasia dell'acquedotto del vestibolo e un orifizio esterno stretto Da qualche anno la RMN, che ha permesso la visualizzazione del canale e del sacco endolinfatici, ha dimostrato che essi sono meno frequentemente visualizzati nei pazienti affetti dalla malattia di Ménière rispetto ai soggetti (Takeda T,1997 ; Schmalbrock P, 1996 ; Tanioka H,1997 ; Welling DB, 1996 ). Questi riscontri radiologici sono stati confermati anche dopo esplorazione chirurgica una casistica di 41 pazienti (Kobayashi M, 2000). Nonostante ciò, tutte queste lesioni non sono né costanti, né specifiche (Fraysse B, 1980). La possibilità di osservare la «fibrosi perisacculare» potrebbe essere influenzata dalle tecniche di scansione impiegate (vedi sotto).
Lesioni vascolari
Oltre all'ischemia perisacculare già ricordata, è stata descritta l'assenza congenita della vena satellite dell'acquedotto del vestibolo, associata allo sviluppo di un circolo collaterale di drenaggio (Gussen R, 1980). Dunque, questo sistema venoso assicura il drenaggio della parte non sensitiva del vestibolo e in particolare delle cellule scure che controllano la secrezione di endolinfa (essendo il resto del sistema cocleo-vestibolare drenato dalla vena cocleare inferiore, satellite dell'acquedotto cocleare).
Modelli sperimentali
Modelli sperimentali Su queste basi istopatologiche, molti studi si sono proposti di sviluppare un modello animale di idrope endolinfatica (IE) e di analizzarne gli aspetti istologici, biochimici, elettrofisiologici e terapeutici. Portmann, fin dal 1921, aveva osservato alterazioni del comportamento natatorio in alcuni elasmobranchi, ai quali aveva cauterizzato il canale e il sacco endolinfatico. Ne concludeva, quindi, che il sacco endolinfatico poteva avere un ruolo nel mantenimento dell'omeostasi dei liquidi labirintici e che un suo danneggiamento poteva indurre un IE . A partire da questi lavori storici, Naito riuscì nel 1950 a provocare un IE nella cavia per mezzo dell'obliterazione diretta del sacco e del dotto endolinfatici Questa esperienza fu riprodotta con lo stesso successo da Kimura nel 1965 sulla cavia e da Schuknecht nel 1968 nel gatto (Kimura RS,1965 ; Schuknecht HF, 1968). Questa procedura, capace di indurre un IE nel 100% delle cavie, fu utilizzata per tentare di determinare l'efficacia dei trattamenti terapeutici dell'idrope. Tuttavia, questo modello è specie specifico. Se si ottiene un IE nel 100% delle cavie trattate e interessa, pertanto, i labirinti cocleare e vestibolare, così come nel ratto e nel coniglio, nel gatto esso può essere ottenuto meno costantemente; in tal caso riguarda esclusivamente la regione cocleare (Kimura RS,1999). Infine, con questo metodo è molto difficile provocare l'IE nel cincillà e nella scimmia. D'altronde, cavie e gatti non presentano nistagmo dopo l'obliterazione dell'acquedotto del vestibolo, mentre coniglio e gerbillo ne soffrono per svariati giorni dopo l'intervento. La spiegazione più probabile è dovuta al blocco della vena dell'acquedotto del vestibolo, assente nella cavia e nel gatto e presente nel gerbillo e nel coniglio. Dunque, l'obliterazione selettiva di questa vena induce in maniera incostante il nistagmo nel gerbillo, probabilmente per l'esistenza di un circolo venoso collaterale presente solo in alcuni animali (Kimura RS, 1996). La principale conseguenza dell'obliterazione del sacco endolinfatico consiste nella distensione della membrana di Reissner e delle pareti delle cavità membranose vestibolari. Questo IE compare rapidamente, spesso entro 24 ore, ma in modo variabile a seconda della specie. La dilatazione della membrana di Reissner si effettua a spese delle cellule esistenti, ma non attraverso la proliferazione cellulare Shinozaki N, 1980 Identici riscontri sono in contrasto con alcune osservazioni effettuate su rocche umane, che fanno cenno di una proliferazione cellulare in risposta a uno stiramento (Gussen R 1971 ; Johnson LG 1971). Infine, le giunzioni serrate tra le cellule epiteliali sono simili a quelle osservate negli animali normali (Shinozaki N,1980), ciò depone a favore di un'aumentata permeabilità di membrana, evocata come possibile meccanismo di fuga ionica (Shinozaki N,1980). Infine, le giunzioni serrate tra le cellule epiteliali sono simili a quelle osservate negli animali normali Kimura RS .Peraltro, si osserva spesso un'atrofia delle cellule ciliate, che colpisce sia le cellule esterne, sia quelle interne. Danni a carico delle cellule del ganglio spirale e delle cellule della stria vascolare sono osservati nella stessa misura. Tutte queste lesioni predominano all'apice, fatto che suggerisce un meccanismo lesionale diverso da quello dei traumi sonori o dei farmaci ototossici (Albers FW, 1987). . Inoltre, esse vengono osservate solo 1-2 mesi dopo l'obliterazione del sacco o molto più tardi rispetto all'IE. Del resto, fistole a livello delle pareti dei sacculi sono state osservate in alcune specie (scimmia, cincillà, ratto) e, in questo caso, non è stata evidenziata alcuna idrope. Al contrario, nella cavia, dove non sono state riscontrate fistole, si osserva quasi costantemente un'idrope (Kimura RS, 1984) . Una tale discordanza è senza dubbio spiegabile con le differenze tra specie riguardo all'elasticità della membrana o alla diversa fisiologia dei liquidi vestibolari. In ogni caso, queste fistole sembrano prevenire lo sviluppo dell'IE ed essere la conseguenza di un aumento di pressione all'interno del labirinto membranoso, anche se la loro sede sacculare, prossima al canale e al sacco endolinfatici, suggerisce che esse non possano essere altro che la conseguenza di fenomeni infiammatori postchirurgici. Esse non provocano, almeno così sembrerebbe, nessuna lesione significativa delle cellule sensoriali, il che suggerisce che la contaminazione dell'endolinfa da parte della perilinfa è limitata. Le fistole indotte sperimentalmente, contemporaneamente all'obliterazione del sacco, si ripercuotono in modo variabile sullo sviluppo dell'IE. Effettuate nel canale cocleare, sembrano ridurne la gravità mentre, se realizzate nel vestibolo, non sembrano sortire alcun effetto. Esse cicatrizzano peraltro molto rapidamente, in particolare nel vestibolo (Kimura RS 1984). Da queste osservazioni sperimentali, si può ritenere che:il modello di IE sperimentale si basa sull'obliterazione del sacco o del canale endolinfatico. L'IE compare rapidamente, prevale all'apice, ma può essere generato solo in alcune specie, rendendo difficile un'estrapolazione all'uomo, tanto più che gli animali con idrope solo raramente manifestano i sintomi vestibolari tipici della malattia di Ménière (Andrews JC, 1988),le alterazioni sensoriali predominano, come nell'uomo, all'apice, ma non possono giustificare da sole i sintomi cocleari osservati nella le fistole provocate arginano lo sviluppo dell'IE solo se effettuate nel canale cocleare e ciò potrebbe pratica clinica. Esse compaiono in ritardo rispetto all'IE;
le fistole provocate arginano lo sviluppo dell'IE solo se effettuate nel canale cocleare e ciò potrebbe rappresentare un argomento a favore degli shunt chirurgici endococleari.
Recentemente è stata ridimensionata l’importanza del flusso longitudinale dell’endolinfa, Secondo la teoria del flusso radiale (Salt e Plontke, 2010), è piuttosto un’anomalia del trasporto ionico il fattore principale che conduce ad un aumento di volume dell’endolinfa. Secondo questa teoria è la stria vascolare che provvede localmente a riassorbire l’endolinfa in presenta di un suo aumento volumetrico; Solo in casi di grande incremento volumetrico dell’endolinfa il flusso endolinfatico si muove in senso longitudinale verso il SE. L’osservazione che, dopo ablazione del SE, l’incremento della pressione perilinfatica è modesto e la composizione endolinfatica rimane costante, conferma quest’affermazione (Mateijsen et al., 2001). Un’alterazione dei meccanismi di trasporto attivo può indurre un’anomalia del contenuto ionico dell’endolinfa da cui deriverebbe un richiamo di liquidi nello spazio endolinfatico e quindi l’insorgenza dell’idrope.
Le acquaporine, adeguatamente rappresentate anche nell’OI (Ishiyama et al., 2006), così come alcuni ormoni (vasopressina, aldosterone) (Juhn et al., 1991), possono svolgere un ruolo di rilievo nella regolazione dell’equilibrio idro-elettrolitico dell’Ol. Un recente studio ha dimostrato che il SE di pazienti menierici esprime alti livelli di recettore di tipo 2 per la vasopressina (ADH) (Kitahara et al., 2008). Un incremento dei suddetti ormoni, causato da stress o alterazioni dietetiche, potrebbe quindi rappresentare un fattore scatenante la crisi menierica.
10) PATOGENESI
Sulla scorta dei dati istopatologici ottenuti sull'uomo e sull'animale da esperimento, sono state avanzate diverse ipotesi patogenetiche, che saranno successivamente descritte a seconda che esse riguardino l'IE o i sintomi clinici. In entrambi i casi, tuttavia, queste ipotesi hanno come punto cardine l'idrope endolinfatica, della quale si propongono di spiegare i meccanismi di comparsa o di cui si servono per chiarire la sintomatologia clinica. Ora, il concetto stesso di idrope come substrato istopatologico della malattia non può essere accettato incondizionatamente, poiché:
· non è costante nei pazienti che hanno presentato tutti i sintomi classici della patologia (risulta assente su 10 dei 22 pazienti di Paparella 1984)
· a partire dalla sua descrizione iniziale nel 1938, l'osservazione dell'idrope si basa in tutto e per tutto sull'esame di circa 150 rocche petrose umane, un numero che non autorizza certezze assolute
· infine, oltre che nella malattia di Ménière, l'idrope è stata descritta anche in altre patologie
Patogenesi dell'idrope endolinfatica
Nessuno studio ha potuto stabilire con certezza la composizione biochimica dell'endolinfa accumulata nel labirinto idropico o, ancora, mostrare se questa endolinfa fosse normale (Bremond G, 2000;Rauch S,1968).La dilatazione del labirinto membranoso rileva a priori, sia un'iperproduzione di endolinfa, sia una disfunzione dell'epitelio del labirinto, che regola le concentrazioni degli elettroliti e l'osmolarità dell'endolinfa e della perilinfa, sia un insufficiente riassorbimento di endolinfa da parte del sacco endolinfatico.
Un'iperproduzione può teoricamente risultare da tre fenomeni:
a)un aumento della pressione idrostatica nel segmento arterioso della stria vascolare, con successivo aumento della perdita di liquidi dal versante capillare in direzione della scala media, o una riduzione della pressione oncotica plasmatica, che riduce il ritorno dei liquidi extravascolari nel distretto venoso. Questa ipotesi non tiene conto che l'endolinfa è il frutto di una secrezione attiva e non di una ultrafiltrazione;
b)una stimolazione del processo di secrezione. Feldman e Brusilow hanno anche riferito che l'iniezione di tossina colerica nella scala media comportava un IE (Feldman AM, 1976). Tuttavia, quest'ipotesi fu abbandonata, poiché non è stato più possibile riprodurre questo esperimento;
c)un aumento della pressione osmotica endolinfatica per accumulo di detriti cellulari o di macromolecole, dovuto alla perdita della funzione fagocitaria del sacco endolinfatico (Dohlman GF, 1965) o per deficit in ialuronidasi, con conseguente accumulo di grosse molecole idrofiliche (Godlowski Z,1972). La conferma di questa ipotesi non è stata possibile (Tran Ba Huy, 1984).
Fino a oggi l'ipotesi più comunemente accreditata prevede un insufficiente riassorbimento di endolinfa da parte del sacco endolinfatico. Essa si basa sulla teoria del flusso longitudinale, suggerita già da più di 60 anni dagli esperimenti di Portmann(1921) e Guild(1927). Quest'ultimo, dopo aver iniettato inchiostro nella scala media, lo ritrovava nel sacco qualche giorno più tardi. Questa teoria è in seguito stata suffragata da studi di microscopia elettronica (Lundquist PG,1976), che hanno mostrato che il sacco dispone dell'attrezzatura cellulare tipica dell'epitelio impegnato nei fenomeni di trasporto e di scambio di liquidi e metaboliti. Così, il flusso longitudinale porta al sacco acqua e soluti endolinfatici, in particolare le proteine penetrate nello spazio endolinfatico.
Purificazione e riassorbimento verrebbero effettuati in seguito secondo tre possibili meccanismi
1)diffusione passiva transcellulare di acqua. La matrice sub-epiteliale priva di collagene crea un elevato gradiente osmotico transepiteliale in corrispondenza di alcune zone atrofiche, che attira l'acqua verso vasi che circondano il sacco e che determina la concentrazione dell'endolinfa;
2)trasporto attivo transcellulare di ioni verso gli spazi intercellulari, che aumenta l'osmolarità e induce secondariamente un richiamo passivo di acqua;
3)pinocitosi attiva transcellulare che trasporta l'endolinfa dal lume del sacco ai vasi periferici (Wackym PA, 1987).
Questa teoria del difetto di riassorbimento di endolinfa è stata rafforzata da studi istopatologici condotti sull'uomo, che hanno evidenziato l'esistenza di fibrosi perisacculare (Hallpike C, 1938), ipoplasia o atrofia del sacco. Va anche notato che se il sacco è ipofunzionante, nei pazienti affetti da malattia di Ménière l'acquedotto del vestibolo potrebbe sembrare ipoplasico; ciò potrebbe spiegare la frequente impossibilità di visualizzare l'acquedotto del vestibolo con le tecniche di imaging (Welling DB, 1996).
Sul piano eziologico, l'IE è attualmente classificato in congenito o acquisito (Shuknecht HF ,1983).
· Il tipo congenito è comunque raro e potrebbe essere conseguente alla displasia di Mondini (Schuknecht HF,1980).
· Il tipo acquisito potrebbe essere dovuto a una lesione labirintica infiammatoria (virale o batterica) o traumatica(Shuknecht HF ,1983). Si può mettere in relazione la «delayed vertigo» con l'IE ritardato, che compare nei pazienti che hanno presentato una grave ipoacusia unilaterale, di origine infettiva o traumatica, e che, dopo un lungo periodo di tempo, sviluppano o una vertigine episodica omolaterale, o una ipoacusia fluttuante dal lato controlaterale, associata a volte a una vertigine recidivante (Gulya AJ, 1978). Una lesione autoimmune dell'orecchio interno è stata sospettata, in particolare dopo il riscontro di immunocomplessi circolanti (Derebery MJ, 1991) e di autoanticorpi anti-sacco endolinfatico(Alleman AM, 1997).
D'altro canto, un IE può essere presente senza dare sintomi:
· quando la funzione cocleovestibolare è scomparsa;
· se si è già creata una fistola spontanea (Schuknecht HF, 1976);
La constatazione che l'emicrania risulti spesso associata alla malattia di Ménière e che il suo trattamento possa attenuare la sintomatologia (Parker W, 1995) non è sufficiente per dimostrare che la causa della malattia di è Ménière vascolare. Tuttavia, Oliveira et al hanno riportato nel 1997 la presenza di queste due patologie nella stessa famiglia e ciò potrebbe testimoniare la medesima origine autosomica dominante
PATOGENESI DEI SINTOMI
Teoria della rottura di membrana
L'ipotesi più classica per spiegare i sintomi della malattia di Ménière è quella descritta da Larence e McCabe nel 1959 ripresa e sviluppata da Schuknecht nel 1974 la rottura del labirinto membranoso e l'intossicazione potassica. Sotto l'effetto della progressiva distensione, il labirinto membranoso finisce per rompersi, liberando in questo modo il potassio endolinfatico che, a seconda della sede della rottura, può diffondere nella perilinfa della cisterna vestibolare o in quella della scala vestibolare del canale cocleare da cui può guadagnare, attraverso l'elicotrema, la scala timpanica (fig. 1.14).
Fig.1.14 Teoria della rottura della membrana.
Sotto l'effetto della distensione progressiva il labirinto membranoso finisce per rompersi, liberando in tal modo il potassio endolinfatico che, secondo la sede della rottura, diffonde nella perilinfa della cisterna vestibolare o in quella della scala vestibolare del canale cocleare da cui guadagna, in seguito, la scala timpanica attraverso l'elicotrema.
Il labirinto membranoso e i nervi sono bagnati dalla perilinfa, la cui composizione elettrolitica è simile a quella del liquor (Na+ = 143 mmol/l, K+ = 8 mmol/l). Al contrario, la concentrazione di potassio nell'endolinfa (K+ = 150 mmol/l, Na+ = 15 mmol/l) è sufficientemente alta per provocare una depolarizzazione assonale all'origine di un blocco della conduzione nervosa (Smith CA, 1954).È stato anche dimostrato che il rilascio nello spazio perilinfatico di una soluzione ricca di potassio è in grado di bloccare le risposte cocleari (Tasaki I,1952)o di causare nistagmo paralitico( Dohlman GF, 1965).
Quando nella perilinfa la concentrazione di potassio aumenta, le fibre nervose afferenti che attraversano quest'ultima sono le prime a essere interessate. Queste fibre vengono improvvisamente eccitate, poiché il loro potenziale di membrana si avvicina al potenziale di attivazione dei canali del sodio( Bance M,1991). Se la concentrazione di potassio continua a salire, i potenziali d'azione vengono bloccati, con riduzione dell'attività spontanea, legata al blocco dei canali assonali del sodio. Questo aspetto è stato riprodotto nella cavia, infondendo endolinfa artificiale negli spazi perilinfatici (Bretlau P,1994). Tale meccanismo spiegherebbe perché il nistagmo all'inizio dell'attacco acuto è di tipo irritativo, per poi cambiare senso e diventare di tipo deficitario. Infine, quando l'eccesso di potassio viene rimosso, il nistagmo batte di nuovo verso l'orecchio malato (nistagmo di recupero), prima di scomparire del tutto. La durata di questo ciclo varia a seconda del tempo necessario per il rinnovamento del liquido.
La direzione del nistagmo e della vertigine potrebbe dipendere anche dal punto in cui si crea la rottura della membrana. Recenti analisi tridimensionali del nistagmo spontaneo hanno tuttavia mostrato, su quattro pazienti affetti da malattia di Ménière, che nei movimenti oculari di questi pazienti esistevano solo due componenti: orizzontale e rotatoria (Toshiaki Y,1997).Queste osservazioni hanno portato a supporre che nel corso della crisi erano stimolate le fibre afferenti di tutti i canali semicircolari. Quando i due canali verticali vengono stimolati predomina la componente rotatoria, mentre le componenti verticali opposte si annullano.
Così, Schuknecht,(1993) ha formulato «un concetto logico del meccanismo della sordità fluttuante e delle vertigini parossistiche nella malattia di Ménière »:
· riduzione del riassorbimento dell'endolinfa. Un'ipoplasia dell'orecchio interno, un trauma o una labirintite virale alterano la funzione di riassorbimento del sacco endolinfatico;
· idrope. Ne consegue un lento accumulo di endolinfa, che origina l'idrope e la distensione della membrana labirintica;
· rotture. L'incremento di volume di endolinfa provoca rotture ripetute del sistema endolinfatico e una contaminazione della perilinfa che blocca temporaneamente sia la funzione cocleare che vestibolare, causando vertigine e/o ipoacusia;
· cicatrizzazione delle rotture. Le lacerazioni cicatrizzano, dando all'intero processo la possibilità di ripetersi;
· dilatazione e atrofia. In una fase avanzata, il labirinto membranoso presenta deformità permanenti, responsabili dell'ipoacusia e delle alterazioni dell'equilibrio, anche permanenti, nonostante la cavità vestibolare sia occupata da zone di tessuto fibroso denso, esiti di molti processi di fistolizzazione e di cicatrizzazione intercorsi lungo il decorso della patologia. Queste connessioni fibrose assicurano la trasmissione degli stimoli meccanici tra le diverse strutture che esse uniscono, in particolare tra base della staffa e le strutture vestibolari. Si spiega in questo modo il classico segno di Hennebert (vedi sopra).
La teoria dell'intossicazione potassica secondaria a una rottura membranosa solleva, tuttavia, numerose obiezioni: non sempre le rotture sono riscontrate all'esame autoptico delle rocche petrose umane; il processo ciclico dilatazione-rottura-cicatrizzazione presuppone un certo lasso di tempo difficilmente compatibile con le crisi che si ripetono a ritmo talvolta giornaliero; i dosaggi effettuati sui liquidi prelevati da labirinti umani non mostrano nella perilinfa concentrazioni di potassio significativamente elevate, così come vorrebbe il concetto di intossicazione permanente (Tran Ba Huy P,1984).
Teoria dell'alterata permeabilità di membrana
La teoria dell'alterata permeabilità di membrana è stata contrapposta a quella dell'improvviso aumento di permeabilità del compartimento endolinfatico(Jahnke K,1981).Le giunzioni intracellulari, che assicurano per la perfetta tenuta elettrochimica di questo distretto, perderebbero improvvisamente le loro proprietà e provocherebbero una fuga di potassio che, a causa di un gradiente elettrochimico altamente favorevole, avverrebbe in modo massivo in direzione degli spazi perilinfatici. Tuttavia, in seguito non è stato possibile confermare questa ipotesi (Morgenstern C,1979), che è stata pertanto abbandonata(Brandt T,1991).
Teoria meccanica
In una serie di esperimenti condotti su un modello cocleare, Tonndorf ha proposto una teoria detta «meccanica», dei sintomi della malattia di Ménière (Tonndorf J,1976;1983).Dato che le membrane limitanti, Reissner e basilare, conservano le loro proprietà elastiche, un aumento di volume dell'endolinfa, causato dall'idrope, determina un aumento di pressione che riduce la sensibilità vibratoria della membrana basilare laddove essa è più elastica, ossia all'apice, e sposta la sede della massima risposta, cioè della frequenza di risonanza, in direzione della base, da dove originano le distorsioni del suono. Il grado di queste alterazioni sarebbe direttamente proporzionale all'aumento di volume. Quando queste membrane diventerebbero flaccide, perdendo elasticità, l'aumento di volume interesserebbe a quel punto la capacità vibratoria dell'intero canale cocleare, a causa dell'eccesso di massa che gli verrebbe imposto.
Tali conclusioni possono ben spiegare i principali sintomi osservati: sordità fluttuante che colpisce le frequenze gravi con ipoacusia disarmonica e distorsione nella fase iniziale, quindi ipoacusia costante, non fluttuante, con ipoacusia disarmonica nelle fasi avanzate. Nel momento in cui fosse predominante l'effetto della rigidità, lo spostamento delle frequenze di risonanza sarebbe diretto verso le alte frequenze, mentre il contrario accadrebbe in presenza di un predominante effetto massa.
Successivamente, Tonndorf ha ipotizzato un disaccoppiamento tra stereociglia e membrana tectoria provocato da un aumento della pressione intralabirintica. L'ipoacusia potrebbe in tal caso essere spiegata da un'alterata trasduzione elettromeccanica. La sua intensità varia con il grado di disaccoppiamento e col numero di cellule coinvolte. La scarsa capacità di discriminazione vocale del paziente con la malattia di Ménière dipende dal silenzio periodico legato al disaccoppiamento che interessa la struttura delle formanti. Quanto a loro, gli acufeni sono legati all'agitazione spontanea delle stereociglia che, isolate dall'ancoraggio tectoriale, sono animate da movimenti spontanei «browniani». Questo meccanismo spiega inoltre come gli acufeni possano essere mascherati da un suono incidente che ricongiunge stereociglia e membrana tectoria e come siano direttamente funzione della sede di disaccoppiamento: durante le prime crisi, l'ipoacusia è predominante sulle gravi ed è accompagnata da acufeni di tonalità grave.
La correlazione tra pressione dei liquidi e udito è confermata da recenti studi condotti su pazienti affetti da malattia di Ménière. Autori svedesi (Konradsson KS, 1999) hanno misurato le soglie uditive ed eseguito un'elettrococleografia prima e dopo permanenza nella camera ipobarica, al fine di ottenere un'ipertensione timpanica relativa. L'ipertensione timpanica, probabilmente per compressione della finestra rotonda, migliora in modo statisticamente significativo le soglie uditive e le registrazioni elettrococleografiche. Va sottolineato che lo sviluppo del test di Marchbanks,(1997) lascia aperta la possibilità di misurare la pressione perilinfatica in modo non invasivo nei pazienti con malattia di Ménière . Sfortunatamente, i risultati di questo test sembrano poco probanti (Bagger-Sjobak D,1997; Rosingh HJ,1997).
Il rapporto tra volumi liquidi e pressione si correla ai sintomi vestibolari, da un lato perché le manifestazioni vertiginose osservate durante un attacco possono essere frenate ponendo il paziente in una camera a pressione, che riduce il gradiente di pressione tra endo- e perilinfa (Densert B,1987) dall'altro perché l'aumento sperimentale di volume nei canali della rana determina un aumento proporzionale della pressione endolabirintica, che provoca essa stessa un aumento dell'attività elettrica del nervo ampollare e che cessa con esso. Esiste dunque una relazione diretta tra aumento di pressione e attività elettrica. Allo stesso modo, un continuo aumento di pressione induce una corrente liquida ampullipeta (perché l'aumento di pressione si diffonde più rapidamente nello stretto canale semicircolare piuttosto che nell'ampia cavità utricolare). Al contrario, un abbassamento della pressione induce una corrente ampullifuga. Questi dati spiegano la direzione del nistagmo spontaneo osservato nel corso della crisi, all'inizio omolaterale, quindi controlaterale (Henriksson NG, 1966 ; Gleissner L, 1966).
Tuttavia, né l'aumento della pressione endolinfatica né una contaminazione potassica possono spiegare il carattere prolungato del nistagmo e della vertigine durante la crisi e quello permanente e non fluttuante della iporeflessia vestibolare che si mantiene quasi costante durante l'evoluzione della malattia. Questa teoria, che si applica ai sintomi ma non all'idrope, non esclude la possibilità di rotture del labirinto membranoso, che possono essere responsabili delle crisi.
Altre ipotesi
Per spiegare la comparsa della crisi, sono state proposte numerose altre ipotesi che attualmente non sono ritenute valide: squilibrio neurovegetativo con ipersimpaticotonia (Cawthorne T, 1954),allergia (Clemis JD,1967) da danno immunomediato, (Yoo TJ, 1982) sbalzi di osmolarità, che provocherebbero uno spostamento d'acqua verso il labirinto membranoso (Johnstone BN, 1981)vascolari, una lesione primitiva, congenita o di altra natura, del sistema venoso dell'acquedotto del vestibolo che, originando un'ipertensione venosa a monte, si ripercuoterebbe sulle zone secretorie vestibolari e sui meccanismi di trasporto dei liquidi (Gussen R,1980).
REFERENCES
Most authors feel that , which is usually attributed to endolymphatic hydrops (see figure 1 above), has several causes (etiologies). 11) Come si fa diagnosi di malattia di Ménière?
La diagnosi di malattia di Ménière è clinica cioè è fatta dal medico sulla base della storia clinica raccolta con il malato (anamnesi) e dei dati ottenuti con l’esame audiometrico. e l'esclusione di altre cause. La diagnosi differenziale è ampia e comprende fistola perilinfatica , labirintiti ricorrenti , emicrania , malformazioni congenite dell'orecchio di vario tipo , la sifilide , malattia di Lyme, tumori come il neuroma acustico , sclerosi multipla, cisti aracnoidea della fossa posteriore, e altre entità rare. Sintomi simili a quelli della malattia di Ménière (udito fluttuante, acufeni, vertigini) può anche essere causato da ictus incombente nella distribuzione dei anteriore arteria cerebellare inferiore (Lee e Cho, 2003). Bilateralità di fluttuazione dell'udito suggerisce una causa vascolare come l'emicrania . Di tanto in tanto il nistagmo nella malattia di Ménière è visto in " modo sbagliato ". Questo è un risultato altamente specifico per la malattia di Ménière , in quanto poche altre condizioni hanno una fase eccitatoria. Gli altri esami che spesso si richiedono al malato sono: l’esame impedenzometrico,l’elettrococleografia , le otoemissioni, i potenziali evocati uditivi, l’esame vestibolare,i potenziali Vestibolari Miogeni (VEMP's), i vari esami del sangue ( ANA ,FTA ) la risonanza magnetica cerebrale ,che servono ad escludere altre malattie; mentre l’esame elettrococleografico può, se eseguito correttamente quando la malattia è in fase attiva, esprimere la presenza dell’idrope labirintica (aumento di pressione dei liquidi dell’orecchio interno). L’esame audiometrico nelle fasi iniziali della malattia mostra una diminuzione dell’udito limitata alle basse frequenze spesso fluttuante, che presenta variazioni nel tempo e che dopo le prime crisi torna a valori normali.
La conferma otologica si basa sui seguenti test clinici:
L' esame audiometrico tonale e vocale (quest'ultimo valuta la capacità di comprendere una lista di parole e non solo i suoni puri), sono importanti ai fini di una stadiazione funzionale della malattia. Così come l' esame impedenzometrico , dirimente per lo studio dell'orecchio medio e della tuba, allo scopo di escludere un loro coinvolgimento.
|
|
Fig.1.15a: Audiogramma (esame dell’udito) tipica della malattia di Ménière sul lato destro (x = sinistra, destra = o). C'è un ipoacusia neurosensoriale. per le basse frequenze. |
|
|
Fig.1.15b: Audiogramma tipico della malattia di Ménière nella fase intermedia , sempre sul lato destro. L'udito è ridotto su tutte le frequenze, ma più per le frequenze alte e basse. |
A questi fanno seguito tutta la serie di esami elettroacustici come i Potenziali Evocati del Tronco Encefalico (ABR) , i quali vengono eseguiti spesso, ma in questo caso ,hanno più che altro valore di esclusione per le patologie retrococleari.
L' Elettrococleografia (Fig.1-4a/b)che assume un'importanza fondamentale nell'idrope endolinfatica. L'esame misura le micro-correnti elettriche prodotte dalle cellule acustiche, ma le difficoltà di esecuzione con le tecniche tradizionali (presso il nostro studio viene utilizzata la tecnica peritimpanica) lo rende assai scarsamente diffuso. L'aspetto della risposta registrata è notevolmente modificato quando c'è un aumento della pressione endolinfatica . Viene quindi ritenuto di estrema rilevanza nella diagnosi di idrope endolinfatica, fondamentale quindi quale prova della genesi di uno o più sintomi che essendo incompleti non possono essere classificati come malattia di Ménière .
|
|
Fig. 1-16a: ECochG normale.
Fig.1-16b l’ECochG è interpretato confrontando l’altezza del SP,con l’AP
|
The ECochG is interpreted by comparing the height of the SP to the AP.
|
|
Fig. 1-17a: Le attrezzature utilizzate per registrare un ECochG, un ICS
|
|
|
Fig. 1-17b: Elettrodo per ECochG - la punta blu è posizionato in modo che sia vicino al timpano dopo che viene effettuata una ECochG, è spesso presente del gel azzurro che rimane nel condotto uditivo.
|
In questo modo si realizza uno studio approfondito di tutte le componenti del labirinto e si ottengono informazioni sulla possibile natura della sintomatologia
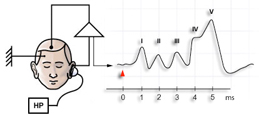
|
|
Fig. 1-18a: Potenziali acustici Cocleari (EChocG)
Fig. 1-18b: Potenziali Acustici del Tronco Encefalico ( ABR) |
|
|
|
|
|
|
POTENZIALI EVOCATi studio tanzariello Fig. 1-18. c-d-e-f-g
Esame vestibolare:la valutazione continua con lo studio VideoNistagmoGrafico.Fig.1-19.a-b
Si registrano, con speciali telecamere ad infrarossi, i movimenti oculari anomali (nistagmo). In fase acuta questi movimenti sono spontanei, oppure possono essere rivelati da manovre appropriate. Durante le fasi silenti della malattia e necessario provocarli con stimoli idonei (esempio acqua calda o fredda nelle orecchie). La presenza di un nistagmo anomalo è l'evidenza di un cattivo funzionamento dei canali semicircolari. Fig. 1-19a-b
|
|
|
Fig. 1-19.a-b PROVE TERMICHE :Perdita unilaterale sul lato destro dopo 3 iniezioni di gentamicina
I Potenziali Vestibolari Miogeni (VEMP'S) Fig.1.20 , che registrano l'attività elettrica dei sensori del Sacculo, e possono dare spiegazione dei disturbi come il disequilibrio e l'instabilità

Fig. 1.20 VEMP normale utilizzando unICS Il potenziale principale, P1, si trova a circa 13 msec. Ogni lato è di circa 250 microvolt di dimensioni (che è molto al di sopra del limite inferiore del normale, circa 70). Vi è un artefatto elettrico visto a 0 msec per il lato sinistro. Questo può essere ignorato
Nel tentativo di cercare eventuali fattori predisponenti lo sviluppo dell'idrope, vengono via via proposti esami ematochimici sulla funzionalità tiroidea, ipofisaria (soprattutto ormoni sessuali della donna) piuttosto che sulla presenza di allergie o intolleranze alimentari. Questi hanno valore, comunque, se prescritti in maniera circostanziata, dopo una valutazione anamnestica che orienti verso una direzione, piuttosto che sottoporre routinariamente ad una valutazione ematica, a tappeto, di tutto le variabili via via messe in ipotetica relazione con lo sviluppo dell'idrope
EVOLUZIONE
L'evoluzione, la cui durata è imprevedibile e imprognosticabile, è caratterizzata da una progressiva riduzione delle crisi vertiginose che vengono sostituite da una instabilità continua.
L'ipoacusia raggiunge gradi elevati, senza più fluttuazioni e si associa ad una povera discriminazione vocale, con abbassamento della soglia del fastidio (recruitment). La MdM è generalmente monolaterale, ma in una percentuale variabile tra il 5 e il 46% dei casi può diventare bilaterale
Epidemiologicamente, l'incidenza varia tra i 3,7 e i 46 nuovi casi ogni 100.000 abitanti per anno, differendo molto nelle casistiche per disomogeneità diagnostica. In Italia l'incidenza calcolata è di 8,2 per 100.000, cifra che pecca per difetto . Non sembra esservi una differenza statisticamente significativa tra i sessi, mentre l'età maggiormente colpita varia tra i 40 e i 60 anni .
12) SINTOMI SINDROME CLINICA
Il quadro clinico della malattia di Ménière è caratterizzato dalla comparsa, scaglionata nel tempo o simultanea, di una triade sintomatologica che associa crisi di vertigine rotatoria, ipoacusia fluttuante e acufene monolaterale intermittente.
Questi sintomi possono non essere presenti contemporaneamente specie nelle fasi iniziali della malattia laddove l’associazione ipoacusiavertigine si rileva solo nel .50% dei casi, mentre un 19% dei pazienti manifesta solo vertigine e un 26% solo ipoacusia (Kitaliara et al., 1984). Le cosiddette varianti cocleari e vestibolari della ÌvldM non sono quindi altro che particolari modalità di esordio della malattia non essendo mai stati dimostrati casi di idrope selettivo. Per questo, nel sospetto di MdM, uno stretto follow-up è fondamentale poiché solo l’evidenza di una documentata ipoacusia in associazione con la crisi vertiginosa può portare alla diagnosi, resa difficile nella fase iniziale dal ritorno alla norma della funzione uditiva e vestibolare.
Accanto a periodi piuttosto lunghi di apparente remissione della malattia, possono seguire momenti in ciii le crisi assumono carattere ricorrente tipo cluster: in generale le crisi vertiginose, indubbiamente il sintomo più invalidante, tendono a ridursi fino a scomparire spontaneamente dopo 8 anni dall’esordio nel 71% dei casi (Silverstein et al., 1989). Generalmente nella fase iniziale le crisi verriginose sono piuttosto violente e di più lunga durata (anche se di iado superano le 24 ore per poi lasciare una sensazione di instabilità che permane per alcuni giorni) ma isolate pci poi divenire un po’ più frequenti ma di intensità e durata minore nella fase florida della malattia. In fase avanzata di solito si assiste alla scomparsa pressoché totale degli attacchi acuti che lasciano il posto ad una sensazione subcontinua di instabilità spesso associata a brevi episodi di lareropulsione (da non confondere con le crisi orolitiche di Tumarkin).
Ancora più specificamente, il paziente racconta di vere e proprie crisi che si dipanano secondo il seguente schema:
![]() iniziale senso di pienezza auricolare;
iniziale senso di pienezza auricolare;
![]() quindi comparsa di ipoacusia o peggioramento di una vecchia ipoacusia omolaterale;
quindi comparsa di ipoacusia o peggioramento di una vecchia ipoacusia omolaterale;
![]() comparsa o aggravamento di un acufene, sempre dallo stesso lato;
comparsa o aggravamento di un acufene, sempre dallo stesso lato;
![]() seguiti da una crisi vertiginosa rotatoria, con difficoltà a mantenere la stazione eretta, nausea e vomito.
seguiti da una crisi vertiginosa rotatoria, con difficoltà a mantenere la stazione eretta, nausea e vomito.
Normalmente questi sintomi possono essere raccolti con l'anamnesi, anche se non è raro osservarli durante la crisi. L'esame obiettivo è pertanto essenziale, mentre gli esami audio-vestibolari non servono che a confermare la diagnosi
Tuttavia, la malattia non esordisce sempre con la triade classica, sviluppandosi spesso, a volte anche per un anno, in modo monosintomatico con caratteristiche vestibolari o cocleari. La diagnosi può essere confermata solo dopo diverse crisi e la comparsa della triade classica Brandt T 2000;1991; Hamann KF, 1999 ; Tran Ba Huy P, 1989;
Crisi vertiginose
Le crisi vertiginose rappresentano il sintomo più eclatante della malattia di Ménière e sono in genere il motivo per cui il paziente si rivolge allo specialista. Esse sono eminentemente variabili nelle loro modalità di comparsa, nel loro decorso, nella loro durata, intensità e frequenza.
Possono insorgere in ogni ora del giorno: in piena notte, risvegliando il paziente, in concomitanza di uno stress, di uno sforzo fisico o di una variazione di pressione atmosferica. Sono generalmente precedute, da 15 a 60 minuti prima, da segni uditivi, isolati o associati, ma monolaterali: comparsa o cambiamento di acufeni o di un'ipoacusia, sensazione di pienezza o di pressione auricolare. Questi segni premonitori, vere aure della vertigine, permettono al paziente che ha già avuto una crisi, di predisporre alcune misure di sicurezza: sedersi, sdraiarsi, scendere da una scala, fermare l'automobile, ecc. Successivamente, compare una violenta vertigine rotatoria, che impedisce la stazione eretta, accompagnata da importanti segni neurovegetativi: malessere, lipotimia, sudorazione, nausea, vomito, diarrea, cefalea. Ciò sottolinea il valore localizzante dei segni uditivi, che permettono di riferire all'orecchio una sintomatologia digestiva e anche di definire il lato colpito dalla malattia. Normalmente non si osserva perdita di coscienza, anche se a volte sono stati descritti eventi sincopali.
La vertigine raggiunge il suo acme in qualche minuto e dura per due o tre ore per poi sfumare in seguito, lasciando il paziente esausto, che finisce spesso per addormentarsi. Se nella crisi inaugurale la vertigine può continuare anche per 24 ore, essa non va mai oltre questa durata. Allo stesso modo, non dura mai meno di un minuto. Una volta passata la crisi, il paziente può recuperare immediatamente il pieno benessere o lamentare nei giorni successivi una sensazione di malessere, di astenia e/o di instabilità nei movimenti.
Talvolta, spesso nelle fasi più tardive, la crisi compare senza alcun segno premonitore e può manifestarsi con una sensazione di beccheggio, di rollio, di ascesa, di discesa o di lateralizzazione.
La frequenza delle crisi vertiginose varia considerevolmente da un individuo all'altro e anche nello stesso paziente e va da diversi accessi alla settimana a crisi distanziate di parecchi mesi o anni. Teoricamente, la frequenza delle crisi si riduce col progredire della patologia, sebbene alcuni Autori ritengono che sia indipendente dalla durata della malattia.
Ipoacusia
L'ipoacusia fluttuante dell'orecchio affetto, che compare o peggiora durante le crisi è, con la vertigine, uno dei due sintomi che compare più spesso. Allo stadio iniziale, può anche essere isolata e indirizzare verso la diagnosi di ipoacusia improvvisa. Essa ha una valenza localizzante e diagnostica.
All'inizio, interessa le frequenze gravi e presenta caratteristiche fluttuazioni, con ritorno alla normalità nell'arco di qualche ora o di alcuni giorni. Si associa spesso a una sensazione di orecchio tappato, di pienezza o pressione, che in genere si risolve dopo l'attacco; può anche associarsi a una riduzione della capacità discriminatoria, a un fastidio per i suoni forti, a una distorsione sonora o a una paracusia disarmonica, segni che indicano un danno endococleare. Altri importanti sintomi uditivi sono rappresentati dall’iperacusia, dalla diploacusia, dall’acufene e dall’autofonia. L’iperacusia è l’espressione soggettiva del fenomeno del recruirmenr particolarmente accentuato nella MdM in virtù del prevalente danno a carico delle cellule ciliare esterne Pertanto le strutture neurosensoriali (cellule ciliare e neuroni) risponderanno ad un più ampio spetti o di frequenze rispetto a quanto accade in condizioni normali e, considei ando che uno (lei meccanismi con cui iene codihcara I’inrensita dei suoni si basa sul numero delle fibre nervose arrivare, si capisce come nella MdM i suoni di intensità elevata creino una marcata sensazione di disconfoit. Questo sintomo tende ad accentuarsi con l’evoluzione della malattia e spesso assume un carattere invalidanre visto che l’ipersensibilità ai suoni può portare ad una vera e propria fonofobia.
La diplacusia, che consiste nella percezione di diversa altezza tonale di uno stesso suono, si riscontra spesso nei pazienti menierici ed esprime anch’essa la lesione a carico delle cellule ciliate esterne da cui deriva la perdita dei fini meccanismi di tuning della membrana basilare: le cellule ciliate residue rispondono ad un più ampio raggio di frequenze. L’acu[ene raramente si presenta come sintomo iniziale (meno del 5%), di solito non ha carattere pulsante e la sua intensità è variabile. In fase inziale/fiorida di malattia la sua intensità è equa- mente divisa tra lieve, moderata e forte; tipico è l’incremento o la comparsa sotto forma di forte frastuono a precedere l’attacco acuto ed il suo carattere intermittente (talora in parallelo con le fiuttuazioni uditive). Diviene quindi costante ed assume tonalità acuta nella fasi avanzate, laddove rappresenta un sintomo così invalidante che il paziente preferirebbe perdere l’udito residuo pur di ottenerne la scomparsa o la riduzione.
L’autofonia compare spesso al momento dell’attacco e di solito tende a regredire con la progressione della malattia. Dal momento che appare poco probabile che la minima quantità di endolinfa che si accumula durante la crisi idropica possa distendere la membrana della finestra rotonda in modo da simulare la sintomatologia tipica delle flogosi dell’orecchio medio, è stato ipotizzato, visto il prevalente interessamento dei toni gravi, che tale sensazione derivi da un fenomeno psicologico di associazione con precedenti esperienze in cui l’autofonia era realmente riconducibile a fenomeni di fiogosi catarrale (Ruckenstein, 2010).
Nel decorso, l'ipoacusia si aggrava, diviene pantonale, perde il caratteristico andamento fluttuante e si stabilizza su perdite di 50-70 dB. La cofosi rimane comunque un evento eccezionale.
Acufeni
Nella malattia di Ménière, gli acufeni simulano tipicamente il rumore di conchiglia marina, ma possono anche presentarsi con i caratteri di un fischio acuto, di rombo o ronzio. Costanti o intermittenti, mai pulsanti, compaiono o si accentuano generalmente nei minuti che precedono la crisi vertiginosa; Presentano, dunque, il vantaggio di segnalare al paziente la crisi imminente, cosa che consente la messa in atto di comportamenti di sicurezza.
Il secondo aspetto rilevante è dato dal fatto che la loro comparsa, come nel caso dell'ipoacusia, permette di riferire la vertigine a una patologia dell'orecchio interno, fatto che evita al paziente di consultare inutilmente altri specialisti. Il terzo aspetto interessante è che l'acufene indica il lato affetto dalla patologia.
L'intensità degli acufeni può essere valutata in tre gradi:
![]() grado 1: acufeni percepibili solo in ambiente silenzioso;
grado 1: acufeni percepibili solo in ambiente silenzioso;
![]() grado 2: acufeni percepibili in qualsiasi ambiente ma che si riducono di intensità durante le attività mentali;
grado 2: acufeni percepibili in qualsiasi ambiente ma che si riducono di intensità durante le attività mentali;
![]() grado 3: acufeni permanenti che condizionano la vita del paziente.
grado 3: acufeni permanenti che condizionano la vita del paziente.
Questa classificazione, anche se soggettiva, permette di valutare le ripercussioni psicologiche degli acufeni e di valutare l'efficacia della terapia intrapresa.
Gli acufeni possono persistere a lungo dopo che la vertigine e l'ipoacusia si siano risolti. A lungo termine, sono destinati a diventare permanenti e invalidanti.
Da non trascurare è infine la valutazione dell’assetto psicologico nell’ambito del quadro clinico della MdM. La qualità di vita di questi pazienti è fortemente compromessa ed è ampiamente documentata l’elevata incidenza nei menierici di fenomeni depressivi di entità direttamente proporzionale al numero delle crisi vertiginose (Eckhartd-Henn et al., 2008). D’altro canto, l’osservazione che la malattia si manifesta con sintorni più severi in soggetti con tratti ansioso-depressivi, ha portato ad ipotizzare un’origine psicosomatica della stessa ( Wexler e Crary, 1986).
Sintomi associati
Alla classica triade della malattia di Ménière possono associarsi altri sintomi aspecifici:
talvolta cefalea ed emicrania sono riferite dal paziente, senza che sia stato possibile stabilire una chiara relazione patogenetica tra queste manifestazioni e la malattia di Ménière. D'altro canto, è stato accertato come nel corso o tra le crisi di emicrania basilare autentica possano anche comparire sintomi oto-neurologici e, in particolare, la vertigine rotatoria
Kayan A, 1984 ;
talvolta accompagnata da segni uditivi. Al cospetto di un quadro clinico evocatore della malattia di Ménière, è quindi importante riconoscere la presenza di un'eventuale emicrania, che può giovarsi di un trattamento adeguato;
il contesto psicologico costituisce, in alcuni casi, uno degli elementi essenziali del quadro clinico. Numerose pubblicazioni hanno evocato il ruolo dello stress, dell'affaticamento, delle preoccupazioni familiari o professionali o anche di shock emotivi nella comparsa delle crisi
I pazienti colpiti dalla malattia di Ménière presentano spesso un particolare profilo psicologico, sono colti e intelligenti, ma anche meticolosi, perfezionisti o, addirittura, ossessivi. Alcuni Autori fanno di questo profilo uno degli elementi indispensabili alla diagnosi Altri hanno parlato di malattia psicosomatica, «di ulcera dell'orecchio interno». Andersson, tuttavia, in una metanalisi, non ha trovato elementi statisticamente significativi in grado di suffragare il ruolo dello stress nella genesi della malattia di Ménière. Allo stesso modo, lo stesso moltiplicarsi delle crisi è in grado di scatenare una condizione di stress, che si manifesta conseguentemente come sintomo secondario
13) STORIA NATURALE
Imprevedibile, misteriosa e in grado di diventare bilaterale: questi sono senza dubbio i termini più appropriati per definire e riassumere la storia della malattia di Ménière. Tali aspetti devono essere immediatamente sottolineati per dare al paziente un'informazione chiara e per ottenere un'affidabile e lucida valutazione dei risultati terapeutici.
Tutti gli Autori concordano nell'affermare che, nella stragrande maggioranza dei casi, la malattia è inizialmente monolaterale. Possono essere descritte quattro fasi evolutive.
Fase iniziale
La malattia compare in genere nella quarta-sesta decade di vita, generalmente in modo monolaterale e monosintomatico, anche se può ovviamente esordire con la triade completa. Non è importante quale dei tre sintomi maggiori possa dare origine alla patologia e precedere, per un lasso di tempo indeterminato, la comparsa degli altri. Secondo alcuni, l'acufene e l'ipoacusia precedono il più delle volte la vertigine di molti mesi o anni, in quanto il canale cocleare viene ritenuto l'iniziale sito di sviluppo dell'idrope Brandt 1991; Malgrado ciò, la malattia può esordire con crisi di vertigine in assenza di segni cocleari. Di regola, il quadro clinico si completa entro un anno dalla comparsa dei primi sintomi
Fase attiva
A questo stadio, la lesione cocleo-vestibolare diventa irreversibile. Le crisi di vertigine perdono di intensità, la funzione uditiva si altera È durante questa fase che la malattia assume il suo aspetto più classico. La triade si instaura in modo parossistico, con periodi di remissione completa. Questa fase può durare per 5-20 anni.
Fase di defervescenza
A questo stadio, la lesione cocleo-vestibolare diventa irreversibile. Le crisi di vertigine perdono di intensità, la funzione uditiva si altera progressivamente Friberg U.1984;Hulshof J.H.1981.Le fluttuazioni scompaiono, le remissioni diventano rare e il paziente lamenta una sensazione di instabilità più o meno permanente L'ipoacusia è piatta e fluttuante e si instaura un'iporeflessia vestibolare
Fase finale
Nella sua fase finale, la malattia di Ménière realizza il classico quadro del «Ménière anziano». Le vertigini scompaiono, ma il paziente, gravemente ipoacusico, è afflitto a permanenza da un intenso ronzio. La perdita uditiva è tale da configurare un quadro di sub-cofosi (60-70 dB), la reflettività vestibolare è minima, ma cofosi e areflessia sono rare.
Tuttavia, questa descrizione della storia naturale della malattia è soltanto schematica e la sua divisione in quattro fasi empirica. In effetti, si può osservare di tutto lungo il decorso e una stabilizzazione o una ripresa possono sopraggiungere in ogni momento.
Bilateralizzazione
Elemento essenziale nell'evoluzione clinica della malattia, il riscontro della bilateralizzazione aumenta percentualmente in modo proporzionale alla durata del follow-up del paziente
L'alta variabilità dei tassi di incidenza riportati in diverse pubblicazioni non dipende solo dalla durata del periodo di osservazione, ma anche dalla diversità dei criteri diagnostici adottati. Su una casistica di 67 esami autoptici, in cui era stata segnalata la presenza di idrope endolinfatica a livello della rocca petrosa, Kitahara ha osservato il 30% di patologie bilaterali Morrison AW,1996.
L'analisi della letteratura permette di osservare che, a due anni dall'esordio della malattia, il 15% dei casi diventano bilaterali (Fig. 18babighian). e che dopo 10 o 20 anni questa percentuale aumenta fino al 30 e addirittura al 60%(Fig. 19 BABIGHIAN). Sembra, infine, che la bilateralizzazione sia indipendente dallo stadio della lesione controlaterale.La bilateralizzazione, che grava pesantemente sulla futura capacità funzionale del paziente, pone anche un problema terapeutico, perché una qualsiasi decisione, in particolare di chirurgia distruttiva, deve essere considerata in rapporto a questa minaccia evolutiva.
14) ESISTONO MANIFESTAZIONI PARTICOLARI DELLA MALATTIA DI MÉNIÈRE?: È possibile identificare alcune varianti cliniche in base a criteri sintomatologici o alla successione temporale della comparsa dei sintomi.
Esse comprendono:
15) FORME CLINICHE
|
|
|
Fig. 1.21 - B.A. a. 44 - M. di Ménière bilaterale. I controlli audiometrici del deficit dell’udito all’or, destro iniziano nel marzo del 1993; nell’agosto del 1993 il danno uditivo interessa anche l’orecchio sinistro. Le crisi menieriche si sono ripetute fino al 2000 provocando un grave deficit bilaterale dell’udito; es. imped: timpanogramma tipo A; RCS nella norma bilateralmente (presenza del test di Metz bilaterale); ABR: tracciato normale.(BABIGHIAN-OTONEUROLOGIA PICCIN 2008).
|
|
|
|
Fig.1.22 - M. di Ménière bilaterale. Col trascorrere degli anni, aumenta la percentuale dei casi nei quali l’idrope labirintica interessa anche l’altro orecchio. .(BABIGHIAN-OTONEUROLOGIA PICCIN 2008).
|
· Sindrome di Lermoyez
Nel 1919, Lermoyez medico francese - Cambrai, 1858 - Parigi, 1929) descrisse una vertigine parossistica recidivante associata al miglioramento di un'abituale ipoacusia ed alla scomparsa dell’acufene; era «la vertigine che fa comprendere»(le vertige qui faut entendre ed ipotizzò che alla base di questa condizione vi fosse un processo ischemico a carico dell’ OI tanto che si è parlato di “fenomeno di Raynaud” del labirinto.) . L’improvviso miglioramento della sintomatologia cocleare si manifesta con la risoluzione dello spasmo dell’ a. ud. int. che l’aveva provocata .La sintomatologia evolve a crisi della durata di 2-3 ore con irregolare frequenza.Questa sindrome fu classificata come una variante clinica della malattia di Ménière. Lermoyez stesso attribuiva l'origine dell'ipoacusia e dell'acufene a uno spasmo dei vasi labirintici e alla sua improvvisa risoluzione nel corso della crisi vertiginosa il miglioramento della funzione uditiva e la lieve attenuazione della vertigine. È possibile osservare questa forma nell'1% circa dei pazienti con malattia di Ménière ed essa potrebbe non essere altro che una variante cronologica e temporanea della malattia stessa Lermoyez M Tran Ba Huy P,1989; secondo Pagnini questa sarebbe una modalità di esordio della Ménière e non una sindrome autonoma in quanto tulle le Lermoyez diventano poi delle Ménière .
· Catastrofi otolitiche di Tumarkin
Nel 1936, Tumarkin segnalò il caso di tre pazienti colpiti da cadute improvvise senza prodromi o«drop attacks» Si trattava di improvvise sensazioni di cedimento delle ginocchia, che portavano il paziente alla caduta; Esse sopraggiungevano senza prodromi, non si accompagnavano alla perdita di coscienza, non erano scatenate da spostamenti e potevano provocare ferite o fratture tanto erano improvvise. Le crisi di Tumarkin sono brevi, di durata inferiore al minuto; si verificano spesso nelle ultime fasi della malattia e nel 10% dei pazienti affetti Schuknecht HF 1993 .Tumarkin stesso riteneva che l'origine di queste crisi fosse vestibolare. Secondo l’A., l’improvvisa caduta dipenderebbe dall’ effetto pressorio dell’idrope sui recettori maculari dell’utricolo. Da alcuni, il quadro viene infatti definito come “otholithic attack” o “otholithic catastrofe”. L”otholithic attack” è molto simile al “drop attack” manifestazione clinica che generalmente si osserva in alcuni casi di patologia del SNC (neoplasie, lesioni vascolari acute, ecc.) o internistica (ipertensione arteriosa, diabete, scompenso cardiaco acuto, ecc.). La diagnosi differenziale con la crisi otolitica di Tumarkin si basa sul fatto che nel “drop attack” vi è perdita della coscienza e mancano i segni anamnestici e clinici di una pregressa lesione cocleare e/o vestibolare.
Attualmente, data questa sintomatologia clinica, si ritiene che in questi pazienti l'idrope endolinfatica sia localizzata nell'utricolo e non nei canali semicircolari, da cui il nome di «catastrofi otolitiche». Su una casistica di 11 pazienti affetti, Black et al hanno dimostrato che un pieno recupero era impossibile con il solo trattamento medico alla fine tutti i pazienti sono stati sottoposti a labirintectomia o a neurotomia. Al contrario, altre casistiche segnalano una remissione spontanea nel corso di qualche mese Black FO,1982 ; Effron MZ, Baloh RW, 1990 ; Jansen VD,1988 ;
Secondo Pagnini rappresenta una potenziale fase evolutiva della Meniere, è caratterizzata da una violenta pulsione, come una enorme spinta laterale che costringe il paz. ad afferrare qualcosa per nona cadere. L’episodio critico ha una durata non superiore alle poche decine di secondi, generalmente si realizza in pazienti con forma avanzate di malattia di Méniere ed appare con maggior frequenza nei pazienti con malattia insorta dopo la sesta decade. E' un fenomeno otolitico da non confondere con i drop attacks che si realizzano nelle forme vascolari come l'IVB, in cui si realizza un improvvisa perdita del tono antigravitario agli arti inferiori. l'origine è otolitica (otriculo e sacculo infatti sarebbero interessati in un secondo tempo perchè più resistenti all'idrope). E' una crisi estremamente pericolosa in quanto avviene all'improvviso, magari in una fase di relativa quiescenza della malattia per il realizzarsi dell'iporeflessia vestibolare (riduzione della funzione vestibolare), senza dare alcun segno premonitore di se, come la fullness della crisi Menierica. Tale crisi spaventa così tanto il malato che spesso sviluppa una paura di uscire di casa. Il nome di "Sindrome otolitica" deriverebbe da un aumento della pressione a livello dei recettori otolitici. Si ritiene che il fattore scatenante sia rappresentato da una grave deformazione meccanica delle strutture maculari del sacculo e dell’utricolo con rottura delle membrane, indotta da un’improvvisa ed intensa variazione della pressione endolinfatica. Sebbene queste crisi mostrino la tendenza a risolversi spontaneamente in pochi mesi, in virtù del loro carattere fortemente invalidante, si pone spesso l’indicazione a trattamenti con ablazione chimica o neurectomia vestibolare,
● L’idrope endolinfatica ritardata (DEH):
è una condizione patologica caratterizzata da crisi vertiginose ricorrenti e/o ipoacusia fluttuante indotte da lE a carico di uno dei 2 orecchi, in soggetti con un pregresso grave danno neurosensoriale cocleare monolaterale non progressivo (Schuknecht , 1978). Quest’ultimo rappresenta l’evento precoce, causato da una infezione vitale/batterica oppure da un evento traumatico, che viene poi seguito, con una latenza che va da pochi anni fino a molti decenni, da un evento tardivo caratterizzato da sintomi tipici dell’lE o nell’orecchio ipsilaterale (DEH ipsilaterale), con crisi vertiginose che non si accompagneranno all’ipoacusia fluttuante data l’assenza di funzione cocleare, o, più frequentemente, nell’orecchio controlaterale (DEH controlaterale), con un quadro clinico caratterizzato da crisi di vertigine ricorrente associate ad ipoacusia fluttuante. Si può ipotizzare che nel corso dell’evento precoce l’insulto virale abbia provocato, oltre che la grave ipoacusia neurosensoriale monolaterale, anche un danno subclinico a carico dei meccanismi di produzione e di riassorbimento dell’endolinfa che, aggravandosi con il tempo, può indurre l’insorgenza di lE (Casani et al., 1993). Il DEH potrebbe essere anche la conseguenza di un meccanismo autoimmunitario scatenato dalla liberazione di antigeni dell’Ol durante l’evento precoce (Harris e Aframian, 1994)
16) CON CHE FREQUENZA SI MANIFESTA?
Gli studi hanno dimostrato che la malattia di Meniere colpisce circa 200 su 100.000 persone (o in altre parole, 2 / 1000). inizia in genere da un lato ed esiste una probabilità che interessi l’altro orecchio del 50%, ma in un periodo di 30 anni.
Questo è grosso modo la stessa diffusione che la sclerosi multipla (SM). La maggior parte delle persone con malattia di Meniere sono oltre 40 anni di età, con equa distribuzione tra maschi e femmine. È interessante notare che lo studio Framingham ha rilevato che 2 / 100 persone credono di avere la malattia di Meniere negli Stati Uniti, suggerendo che la diagnosi errata è molto più comune di quanto la diagnosi corretta. (Clicca qui per maggiori )
17) TERAPIA:COME SI CURA LA MALATTIA DI MÉNIÈRE?
Bisogna distinguere un trattamento dell’attacco acuto da tutte le terapie e norme di igiene alimentare e di vita che sono utili per il controllo della malattia. Parleremo poi dei trattamenti medici e chirurgici che permettono di evitare il ripetersi delle crisi acute.
Trattamento dell’attacco acuto: si basa sull’uso di farmaci che deprimono la funzione vestibolare come alcuni antistaminici che si somministrano per via intramuscolare o endovenosa; farmaci anti-emetici che sopprimono i sintomi dovuti all’attivazione del sistema neurovegetativo (nausea, vomito, malessere generale); farmaci ansiolitici che oltre che ridurre l’ansia associata alla crisi hanno anche un’azione antivertiginosa diretta.
Esistono peraltro degli accorgimenti che permettono di ridurre l’intensità dei disturbi se si viene colti da una crisi e non si hanno a disposizione farmaci antivertiginosi. È consigliabile stendersi su una superfice piana e stabile sul fianco dell’orecchio sano e fissare un punto fermo. Evitare di bere per non stimolare il vomito. Se se ne ha la possibilità può essere utile fare un lavaggio dell’orecchio malato con acqua fredda (dai 20 ai 30 gradi), può essere usatoa per questo una siringa da 20cc (senza l’ago naturalmente) o una peretta che contenga la stessa quantità d’acqua. Lo scopo di questa irrigazione è di inibire l’attività del labirinto malato che in fase acuta presenta un’aumentata attività.
Trattamento generale della malattia: si basa su una serie di norme di igiene soprattutto alimentare che consistono principalmente nel mantenere un buon equilibrio idrosalino dell’organismo. Sebbene i liquidi dell’orecchio interno abbiano un metabolismo separato da quello dei liquidi del resto dell’organismo con concentrazioni specifiche di sodio, potassio e altri elettroliti, sono comunque influenzati dallo stato di equilibrio idrosalino dell’organismo. Le norme principali da seguire per evitare questo squilibrio sono:
assumere alimenti e liquidi in modo regolare e ben distribuito nella giornata
Limitare in modo drastico il consumo di sale, riducendo anche il consumo di alimenti ad alto contenuto salino (meno di un grammo al giorno)
Consumare almeno tre porzioni di frutta e due di verdura al giorno
Bere almeno 2 litri di acqua al giorno o di succhi di frutta a basso contenuto di zuccheri e reintrodurre subito i liquidi persi con l’esercizio fisico o a causa del caldo.
Prestare attenzione all’assunzione di latte che in alcuni pazienti può accentuare la frequenza delle crisi per motivi di allergia ad esso
Limitare l’assunzione di caffeina (caffè, tè, cioccolato) che tra l’altro ha un effetto di scatenamento dell’emicrania (alcune forme di idrope sono degli equivalenti emicranici)
Limitare l’assunzione di alcol ad un bicchiere di vino ai pasti
Limitare/evitare gli alimenti che contengono monogluttamato di sodio (contenuto sopratutto nella cucina cinese)
Evitare per quanto possibile gli stress siano essi lavorativi o per attività ludiche
La terapia della MdM si avvale di presidi ortodossi (dietetici, farmacologici e chirurgici) ed eterodossi (agopuntura, psicoanalisi, bio-feedback, training autogeno): tutti sembrano ottenere risultati significativi nei confronti dei singoli sintomi della malattia, ad indicare come tale affezione mostri forti connotati di tipo psicosomatico.
Tradizionalmente, una volta posta diagnosi di MdM, è necessario sottoporre il paziente ad una terapia medica che può essere attuata in due circostanze:
A):durante l'attacco acuto: si impiegano vestibolosoppressori ad azione sedativa centrale come le fenotiazine o le benzodiazepine (Diazepam). Utile anche la somministrazione di diuretici osmotici (Mannitolo e.v.: 1-2 gr. /Kg./ per tre volte die) e di anticolinergici (scopolamina transdermica).
Più discutibile l'impiego di diuretici d'ansa (Furosemide) e dei corticosteroidi.
B)nella fase intercritica: si impiega la dieta iposodica come supporto alla terapia farmacologica che è fondamentalmente rappresentata da alte dosi di Betaistina (16mg. per 3 volte die). Non sembra altrettanto efficace l'alternanza tra Betaistina e corticosteroidi ,né l'uso protratto di diuretici per os.
La terapia dietetica e medica va mantenuta per almeno 6 mesi prima di prendere ulteriori provvedimenti.
Se nonostante il completamento del ciclo terapeutico medico il paziente lamenta ancora sintomi, tali da causare un degrado della propria qualità di vita, occorre prendere in considerazione le seguenti soluzioni:
9)se il sintomo più importante sono le crisi vertiginose si deve optare per una terapia ablativa farmacologica (gentamicina transtimpanica) o chirurgica (neurectomia selettiva). Tale ulteriore decisione è a sua volta condizionata anche da altri parametri quali l'età del soggetto, la funzione uditiva e la mono o bilateralità della patologia (Tab. 2);
I trattamenti chirurgici sono indicati qualora la terapia dietetica e farmacologica non permetta un ottimo controllo della malattia cioè non si abbiano più crisi violente di vertigini. Essi possono essere di tipo funzionale oppure mirano alla distruzione più o meno completa delle cellule del sistema dell’equilibrio che inviano il segnale al sistema nervoso centrale. I principali sono:
A)Decompressione del sacco endolinfatico
B)Labirintectomia chimica con gentamicina
C)Labirintectomia chirurgica
D)Sezione (neurotomia) del nervo vestibolare
A)La decompressione del sacco endolinfatico è stato il primo intervento chirurgico “funzionale” per la cura della malattia di Ménière.(attualmente quasi abbandonata)Consiste nel rimuovere l’osso posto dietro il labirinto che ricopre il sacco endolinfatico dove “scaricano” la pressione i liquidi labirintici. Le procedure descritte sono diverse, semplice decompressione, applicazione di una valvola dal sacco alla mastoide o ai liquidi cerebrali, asportazione completa del sacco e tutti hanno percentuali di successo simili nel controllo della malattia. Essi oscillano nei vari studi dal 60% all’80%. Si tratta di un intervento che si esegue in anestesia generale e, in mani esperte, ha un rischio di complicazioni molto basso. Il principale vantaggio di questi interventi è che non sono distruttivi della funzione vestibolare e quindi non provocano uno squilibrio tra i due lati che, soprattutto nelle persone anziane, può essere difficile da compensare,attualmente è stato sostituito con:.
B)La labirintectomia chimica con gentamicina rappresenta uno dei trattamenti attualmente più diffusi oltre che per i buoni risultati per la relativa semplicità di applicazione. Infatti può essere eseguito ambulatoriamente iniettando la gentamicina, che è un antibiotico tossico per il sistema otovestibolare, nell’orecchio medio dove viene assorbito a livello della membrana della finestra rotonda. Si sfrutta il fatto che essendo più tossico per le cellule vestibolari che per quelle acustiche può essere applicato in modo da essere tossico solo per le prime lasciando intatta la funzione uditiva. La gentamicina può essere applicata direttamente nell’orecchio con un ago che attraversa la membrana timpanica oppure si posiziona prima un tubicino di ventilazione nel timpano attraverso il quale si inietta il farmaco E' anche possibile iniettare direttamente il farmaco attraverso la membrana del timpano con un ago sottile.
La somministrazione viene eseguita molto lentamente e il paziente viene mantenuto in posizione supina con la testa ruotata di 45° verso l'orecchio sano per circa 30 minuti.
Sono sufficienti basse dosi, che implicano cicli di 3 iniezioni a distanza di circa 5 giorni, eventualmente ripetibili in un tempo successivo.
Tale metodica comporta tuttavia la possibilità di un effetto tossico anche sulla coclea, con un peggioramento uditivo significativo che varia dal 3 al 20% dei casi. La capacità e l’esperienza del medico sta nell’applicare il farmaco in modo da distruggere le cellule vestibolari lasciando intatte quelle uditive. Il trattamento è ambulatoriale ed i risultati nel controllo delle vertigini, in mani esperte, raggiungono il 90%
C)La labirintectomia chirurgica si esegue solo quando il paziente ha una sordità totale dal lato della malattia e si possono rimuovere chirurgicamente le cellule vestibolari. È un intervento da eseguire in anestesia generale che dà un controllo della vertigine in oltre il 95% dei casi. È raramente eseguito perchè è raro che si abbia una sordità totale dal lato della malattia.
D)La sezione o neurotomia del nervo vestibolare si esegue, molto raramente, quando gli altri trattamenti non hanno dato il risultato sperato è il paziente continua ad avere violente crisi vertiginose. Si tratta infatti di un intervento delicato, otoneurochirgico, che consiste nella sezione intracranica del nervo vestibolare (dell’equilibrio) lasciando intatto quello cocleare (dell’udito). è un metodo invasivo ma efficace, che consente allo stesso tempo di conservare meglio la funzione uditiva dell'orecchio ammalato. Al nervo vestibolare si può accedere per diverse vie, venendo ciascuna preferita in base alla esperienza personale del chirurgo. È risolutivo in oltre il 95% dei casi
10)Come si curano gli acufeni, il senso di ovattamento auricolare e l’ipoacusia?
se il sintomo più fastidioso è l'ipoacusia, e la malattia è bilaterale anche se di grado differente, l'unico provvedimento terapeutico è la protesizzazione acustica, notevolmente difficoltosa in tali pazienti a causa del recruitment (che genera fastidio per i rumori intensi) ma è sempre possibile; se il sintomo più importante è l'ovattamento auricolare, in certi casi specifici può essere preso in considerazione il posizionamento di un tubo di ventilazione transtimpanico; se il sintomo più invalidante sono gli acufeni, nessun
provvedimento tradizionale è in grado di risolvere il problema. I risultati migliori si ottengono con la TRT ottiene nel trattamento degli acufeni legati alla malattia di Ménière gli stessi risultati che ottiene nelle altre forme di acufene con miglioramenti ottenibili nell’80% dei casi.
Sia in seguito all'evoluzione naturale della malattia che dopo terapia ablativa spesso i pazienti lamentano una instabilità posturale costante che può essere attenuata mediante l'esecuzione di adeguati esercizi riabilitativi vestibolari.
Bisogna impostare una strategia terapeutica che liberi il paziente al più presto dalla dipendenza della malattia. Infatti il problema principale di chi ne soffre è rappresentato dalla imprevedibilità delle crisi oltre che il pericolo intrinseco ad essa (caduta, incidente stradale) ne consegue che se la terapia medica e dietetica non ha raggiunto i risultati sperati nell’arco di tre mesi consigliamo il trattamento minichirurgico di deafferentazione (interruzione degli stimoli) vestibolare rappresentata dal trattamento con gentamicina. Altri trattamenti “funzionali” quali il trattamento pressorio dell’orecchio con il Meniett non hanno dimostrato, negli studi pubblicati di confronto, un successo superiore a quello dell’applicazione di un semplice tubicino di ventilazione nella membrana timpanica e di conseguenza non riteniamo il loro uso giustificato.
Un aspetto particolare del trattamento della malattia di Ménière è rappresentato dal trattamento della malattia di Ménière bilaterale. In questo caso laddove la terapia medica risulti insufficiente a controllare le crisi non è consigliabile, per la grave inabilità che provoca, un trattamento distruttivo bilaterale, ne consegue che il trattamento dovrà trovare un equilibrio portando ad una riduzione parziale della funzione vestibolare. La streptomicina che è un farmaco tossico per il sistema vestibolare usata per via parenterale (iniezioni intramuscolari) controllando clinicamente la funzione vestibolare ci permette di abbassare gradualmente la funzione labirintica senza danneggiare la funzione uditiva e senza arrivare ad una totale perdita della funzione vestibolare.
La terapia della malattia di Ménière richiede, soprattutto nelle fasi iniziali, il controllo dell'idrope endolinfatico che è il responsabile della sintomatologia. Lo sviluppo delle conoscenze sui meccanismi di regolazione dei liquidi labirintici ha permesso di modificare radicalmente l'approccio terapeutico.
I pilastri del personale approccio all'idrope sono rappresentati da un trattamento dietetico e da farmaci che favoriscano la diuresi ed il ricambio di liquidi. Il primo si basa sull'aumento dell'assunzione di liquidi e di alimenti che non inducano ritenzione idrica. In questo modo si agisce sulla composizione idro-salina dell'organismo (osmolarità) così che si inibisce la sintesi dell'ormone antidiuretico. Questo provoca una maggiore permeabilità delle aquaporine e quindi vengono espulsi liquidi, in maniera naturale. La terapia medica si basa sull'uso di tradizionali diuretici (della categoria osmotica) associati a corticosteroidi ed antistaminici. Queste ultime due classi di farmaci svolgono importanti funzioni sul ricambio idro-salino. L'utilizzo di questo genere di protocollo ha dimostrato negli anni un'estrema efficacia ed un'ottima tollerabilità da parte dei pazienti. Per questo motivo è sempre consigliabile intraprendere tale terapia , in qualsiasi fase della malattia si trovi il paziente. Nel senso che l'utilità di ridurre in maniera la pressione dei liquidi labirintici è alle prime manifestazioni della malattia, ma anche nei casi di evidenti deficit della funzione dell'orecchio interno, apparentemente irreversibili. Accade infatti che la riduzione dell'idrope migliori il funzionamento delle cellule cigliate e quindi si possa produrre un recupero della funzionalità.
Nei protocolli terapeutici tradizionali si utilizzano farmaci che appartengono a quattro categorie :
a)Diuretici osmotici (mannitolo, glicerolo): si somministrano mediante fleboclisi ed agiscono richiamando liquidi dall'interno degli organi del labirinto; nelle vertigini, infatti, è frequentemente presente un "accumulo"di liquidi nel labirinto (idrope labirintica).
b)Sedativi della funzione labirintica (bloccano gli impulsi anomali generati dal labirinto ammalato).
c)Antiemetici(agiscono contro il vomito).
d)Cortisonici (agiscono contro l'infiammazione e l'edema).
REFERENCES
18) ESAMI DIAGNOSTICI
Nel caso in cui si sospetti la malattia di Ménière, il paziente deve essere sottoposto a esami audio-vestibolari, radiologici e di laboratorio, nel tentativo di confermare la diagnosi e di escludere altre possibili patologie.
Esame audio-vestibolare
La malattia di Ménière provoca una tipica ipoacusia percettiva, per lo meno nei primi tempi, e un'iporeflessia vestibolare tardiva. Attualmente, una valutazione iniziale di massima prevede l'esecuzione di audiometria tonale, audiometria vocale, impedenzometria, test di stimolazione calorica e test osmotico.
Audiometria tonale
Questo esame permette di evidenziare due delle caratteristiche essenziali dell'ipoacusia percettiva tipica della malattia Ménière: il suo aspetto in salita o piatto e la sua evoluzione fluttuante. Studi clinici basati su ampie casistiche hanno mostrato che questa ipoacusia era di tipo ascendente, con perdite di circa 30-50 dB a carico delle frequenze gravi fino a 1 kHz durante il periodo critico (fig.1-9) . Nella fase iniziale della malattia e per numerosi anni, la capacità uditiva migliora o addirittura si normalizza nel periodo intercritico (fig. 1-10) . In fase avanzata, risultano interessate anche le frequenze acute, con la curva che si stabilizza sui 40-60 dB di perdita a carattere pantonale; infine l'ipoacusia perde il suo carattere reversibile (fig 1-11) . La cofosi, tuttavia, si osserva solo in casi eccezionali.
Quattro punti devono essere segnalati:
![]() il carattere ascendente e fluttuante della curva audiometrica è altamente suggestivo della presenza di idrope endolinfatica; ciò, tuttavia, non è patognomonico della malattia di Ménière;
il carattere ascendente e fluttuante della curva audiometrica è altamente suggestivo della presenza di idrope endolinfatica; ciò, tuttavia, non è patognomonico della malattia di Ménière;
![]() le fluttuazioni tipiche delle fasi iniziali sono meglio dimostrabili con il test osmotico che verrà descritto più avanti;
le fluttuazioni tipiche delle fasi iniziali sono meglio dimostrabili con il test osmotico che verrà descritto più avanti;
![]() un Rinne di 10-15 dB può essere osservato sulle basse frequenze; fatto che sarebbe dovuto a una distorsione armonica che sposta la zona di risonanza verso la base della coclea;
un Rinne di 10-15 dB può essere osservato sulle basse frequenze; fatto che sarebbe dovuto a una distorsione armonica che sposta la zona di risonanza verso la base della coclea;
![]() a volte può essere osservata una caduta sulle frequenze acute, il cui significato non è ben noto.
a volte può essere osservata una caduta sulle frequenze acute, il cui significato non è ben noto.
![]()
Fig 1.24a Aspetto tipico dell'ipoacusia durante una crisi di Ménière; l'ipoacusia è di tipo percettivo o misto, predominante sulle frequenze gravi, fatto che conferisce alla curva audiometrica un aspetto in salita. Il timpanogramma è normale, la curva audiometrica vocale appiattita.
![]()
Fig 1.24. 10 Stesso paziente della figura 1-9 nella fase terminale della crisi: la curva audiometrica e la vocale migliorano
![]()
Fig 1.25. Quadro audiometrico in uno stadio avanzato della malattia. Si osserva una subcofosi con curva audiometrica vocale appiattita.
Prove audiometriche sopraliminari
|
|
|
Fig.1.26 Un esempio di iper-recruitment (over-recruitment).
|
Iper-Recruitment Alcuni pazienti con malattia di Meniere possono mostrare casi speciali di Recruitment , in cui la loudness nell’ orecchio malato(anormali), non solo si raggiunge la loudness dell'orecchio normale ma in realtà viene superata (Dix, Hallpike, e Hood, 1948; Hallpike & Hood, 1959 : Hood, 1977). Questa scoperta si chiama iper-recruitment (o overrecruitment), ed è mostrato in fig. 2-12 L’Iperrecruitment si rivela sul laddergram in cui le linee(scalini) prima si orizzontalizzano e poi si dirigono in direzione inversa. In questo esempio, il suono di 85 dB HL nell’ orecchio patologico in realtà risulta più intenso dei 100 dB HL presentati nell’orecchio normale. Questo fenomeno viene indicato sul diagramma di SteinbergGardner quando la linea che mostra la sensazione uditiva(loudness)del paziente supera la linea diagonale. Si noti che l'iper-recruitment è in qualche modo una questione controversa, e la probabilità di trovarlo sembra essere influenzato dal modo in cui il test ABLB viene eseguito (Hood, 1969, 1977; Coles & Priede, 1976).
Audiometria automatica
L’audiometria automatica evidenzia una curva di II° tipo e l’adattamento risulta patologico senza però raggiungere valori elevati come si osserva nelle lesioni retrococleari. L’audiometria automatica evidenzia una curva di II° tipo e l’adattamento risulta patologico senza però raggiungere valori elevati come si osserva nelle lesioni retrococleari.
|
|
Fig.1.27. B.D. a. 29: nella fase (b) l’audiomertria automatica mette in evidenza una curva audiometrica del II° tipo di Jerger; nella fase (c) quella del I° tipo (BABIGHIAN-OTONEUROLOGIA PICCIN 2008).
|
Impedenzometria
L'impedenzometria permette, attraverso la rilevazione del riflesso stapediale (RS), di precisare la natura endococleare dell'ipoacusia, evidenziando un altro elemento molto caratteristico della malattia: il recruitment. Nessun'altra patologia cocleare è in grado di associarsi a un fenomeno tanto intenso. Così, le soglie del RS restano normali, qualunque sia l'intensità della ipoacusia e non superano mai i 60-70 dB. Il fenomeno del recruitment è altrettanto ben osservato con i potenziali evocati acustici (PEA), Anche se in modo meno semplice e rapido rispetto all'impedenzometria.
Audiometria vocale
L’esame audiometrico vocale rivela una modificazione della curva di intelligibilità che, all’inizio, potrà fluttuare in modo analogo alla curva audiometrica tonale. la discriminazione vocale rimane buona soprattutto nelle fasi iniziali i, tende poi a deteriorarsì in associazione con il progressivo incremento dei fenomeni di diistrsione sopraliminare (recruirment) con alterazione della soglia di per cezione e di massima discriminaiione. Ma, dopo alcuni anni, essa raggiunge valori molto bassi di discriminazione della voce, in media del 53%. L'audiometria vocale mostra spesso una marcata discordanza rispetto agli score ottenuti con l'audiometria tonale. Espressa in decibel di intelligibilità, in percentuale di discriminazione o tramite il semplice aspetto della curva, essa mostra, in effetti, performances peggiori rispetto all'audiometria tonale, cosa che spiega le sue ridotte possibilità diagnostiche in questi pazienti (fig.1-9). Anch'essa oscilla con il progredire della malattia (fig.1-10), ma ben presto nel corso della sua evoluzione, la curva vocale non raggiunge più il 100% di intelligibilità e presenta spesso un aspetto a cupola o a campana (fig.1-11),il fenomeno del roll-over si riscontra nel 20% dei casi.La causa di questo fenomeno potrebbe risiedere in una lesione elettiva del ganglio spirale, secondaria a una degenerazione nervosa retrograda
L’esame impedenzometrico
mostra a un timpanogramma di tipo A e almeno nelle fasi più avanzate, il riflesso stapediale presenta un test di
Metz positivo a conferma del fenomeno del recruitment.
Otoemissioni acustiche Prodotti di distorsione (DPOAEs)
I prodotti di distorsione (DPOAEs) rappresentano un metodo biettivo e non invasivo per misurare la funzione delle cellule acustiche esterne. I movimenti delle ciglia di queste cellule producono una energia meccanica che si trasforma in energia acustica. La sua misura permette di valutare l’effettivo danno di queste cellule. Possono essere misurati in più del 60% degli orecchi con malattia di Ménière e riflettono le differenti fasi della malattia.EOAEs nei pazienti con malattia di Meniere.
I meccanismi fisiologici responsabili della perdita fluttuante dell'udito osservato nelle orecchie con idrope endolinfatica (EH Endolymphatic Hydrops) , o malattia di Meniere, non sono chiare. La teoria prevalente è che l'accumulo di liquido endolinfatico nella coclea altera la meccanica cocleare, ostacolando la mobilità della membrana basilare e sganciando le stereocilia delle cellule acustiche esterne (OHC) dalla membrana tettoria (Braun, 1996). Tali cambiamenti fisiologici determinano una perdita uditiva cocleare e uno si aspetterebbe di vedere le OAE diminuiti o assenti. Nella la maggior parte dei casi di EH (Endolymphatic Hydrops), le misure delle E0AE non sono diverse da quelli di altre eziologie cocleare con perdite similari (de Kleine et al, 2002), tuttavia, sembrano esserci cambiamenti a vari livelli nella coclea dei pazienti con idrope endolinfatica EH, tra cui non solo le cellule ciliate, ma anche l’innervazioni cocleare, così come la composizione chimica dei liquidi cocleari (Nadol, 1989). Come è stato menzionato per ISHL, fino al 30% dei pazienti con EH (Endolymphatic Hydrops) presentano EOAEs misurabile, nonostante perdita dell'udito di 40 dB o superiore (Bonflls et al, 1988b; Cianfrone et al, 2000: Fetterman, 2001: Harris e Probst, 1992; Lonsbury -Martin e Martin, 1990; Martin et al, 1990; Ohlms et al, 1991). Di conseguenza, in molti casi di EH( idrope endolinfatica) l'attività di movimento delle cellule ciliate esterne (OHC outer hair cell) OHC non è compromessa e si è 'osservato che la perdita dell'udito è legata alla disfunzione delle altri componenti meccaniche, sensoriali, o neurali.
Un esempio è mostrato in fig. 1-14 di un adulto di 51anni con diagnosi di malattia di Meniere che mostrava una ipoacusia moderata SNHL per le frequenze basse e medio alte nell’orecchio sinistro. Le TEOAEs erano presenti nel suo orecchio sinistro per le frequenze comprese tra 1-1,5-kHz , nonostante la diagnosi di una patologia cocleare
|
|
|
Fig. 1.28 Audiogramma e tracciati delle otoemissioni acustiche transitorie vocate (TEOAE) i per entrambe le orecchie in un paziente di 51 anni con diagnosi di malattia di Meniere L'orecchio colpito è il sinistro uno ed i sintomi erano presenti 13 mesi prima di questa valutazione. La migliore sensibilità uditiva per l'orecchio sinistro è a 2 kHz, ma i picchi delle TEOAE a circa 1 kHz. Il livello complessivo delle risposte per le TEOAE per le due orecchie è quasi la stessa, nonostante le differenze tra le 2 configurazioni audiometriche Da Harris, FP,, e Probst, R. (2002) Le emissioni otoacustiche e risultati uditiva. da : MS, Robinette, & T, J. Glattke (Eds), otoemissioni acustiche: applicazioni cliniche, 3a edizione,2007 (pp. 250-252). New York: Thieme,.
|
La misurazione della OAE può aiutare a determinare di eziologia diversa dalla idrope endolinfatica (EHs) in base alla presenza o assenza di motilità delle cellule ciliate esterne (OHC outer hair cell) . Un risultato potenziale è la scelta della terapia medica.
Una proposta di applicazione clinica della EOAEs è l’obiettivo di monitorare la funzione cocleare, per esempio, nella diagnosi della idrope endolinfatica (EH) usando i tests al glicerolo, si è riscontrato che le EOAEs sono più sensibili (Cianfrone et al, 2000; e Li Zhong, 1999; Magliulo et al, 2004 ; Sakashita et al, 2001) o ugualmente sensibili (Jablonka et al, 2003) ai cambiamenti della soglia ai tono puri. Sakashita et al, (2001) hanno misurato TEOAEs, DPOAEs, e le soglie ai toni puri prima e 3-ore dopo la somministrazione orale di glicerolo su 22 pazienti con idrope endolinfatica( EH)Le soglie ai toni puri miglioravano da 10 o più dB su una o più frequenze sulla funzionalità uditiva di 11 sui 22 paziente esaminati. I cambiamenti delle TEOAE e DPOAE sono stati considerati significativi qualora superavano di 2 deviazioni standard la media della variabilità del test-retest di un gruppo normativo. Sia le TEOAEs ,che le DPOAEs hanno mostrato livelli di ampiezza significaticativamente maggiori per le 11 orecchie che aveva avuto un migliorato delle soglie ai toni puri. Inoltre, le TEOAEs sono risultati presenti in 14 orecchie e le DPOAEs in 20 su 22 orecchi dei pazienti esaminati. Gli autori concludono che le EOAEs erano più sensibili come test diagnostico delle idrope endolinfatica (EHs) rispetto all’audiometria ai toni puri e la sensibilità del test è stata di gran lunga superiore per le DPOAEs rispetto alle TEOAEs . Altri studi indicano un aumento delle ricerche che utilizzano nelle DPOAE la funzione I/O ,che sono più sensibili ai cambiamenti nella funzione cocleare in pazienti con idrope endolinfatica( EHs) rispetto alle DPOAEs che utilizzano un singolo livello di stimolo (Kusuki et al, 1998; Sakashita et al, 1998).
Elettrococleografia
L’elettrococleografia misura i segnali elettrici dell’orecchio interno in risposta agli stimoli uditivi ed è onsiderato un indicatore dell’idrope.
I parametri chiave sono il rapporto tra l’ampiezza dei potenziali di sommazione (SP) e l’ampiezza dei potenziali di azione (AP).Nell’individuo normale c’è una piccola differenza mentre nel menierico c’è un aumento dell’SP e quindi un alto rapporto SP/AP.
APPLICAZIONI DELL’ECOCHG NELLO STUDIO DELLA MALATTIA DI MÉNIÈRE
Numerosi parametri sono importanti per l’analisi dei risultati:
- è ben documentata l’influenza delF intensità dello stimolo, quella del posizionamento dell’elettrodo (Eggerrnont, 1976) e del livello uditivo sui risultati ottenuti:
- è necessario impiegare una banda passante larga, poichè quella utilizzata abitualmente per l’ABR impedisce la rilevazione dell’SP (fig. 3a-8);
- è necessario altresì tener conto del tempo di salita del tone burst. Infatti questa variabile influenza direttamente l’ampiezza dell’AP (e dell’effetto 0FF). ma non sembra modificare sensibilmente l’ampiezza dell’SP (fig. 3a-8). La costanza dell’SP al variare del tempo di salita del burst è un argomento che depone a favore di un tempo di salita breve per le diverse frequenze, in grado quindi di produrre la nascita di un AP di migliore leggibilità. Non va tuttavia trascurato il fatto che un tempo di salita breve fa perdere a1FAP la sua specificità in frequenza. in quanto il contributo della base della coclea tende a predominare, indipendentemente dalla frequenza dello stimolo.
La principale applicazione dell’SP è quella di facilitare la diagnosi differenziale della malattia di Ménière dalle altre patologie a carico dell’orecchio interno. L’SP è in effetti di maggiore ampiezza nella Ménière (Dauman et al., 1986). E spesso di valore positivo con un tone burst di 8 kHz e negativo a 1 o 2 kHz (fig. 3a-9a e b),
L’elemento più caratteristico resta tuttavia lo studio degli effetti del glicerolo sull’SP (Dauman et al., 1984). Nel 60% dei malati di Ménière si osserva una caduta progressiva, in 3/4 - i ora, dell’SP sulle frequenze basse (Dauman et aL, 1988b), Tale effetto (un esempio è illustrato in fig. 3a-iOa e b) viene generalmente interpretato come un indice indiretto di una distensione reversibile della membrana basilare. La diminuzione delle ampiezze dell’SP sotto l’azione del glicerolo si manifesta elettivamente alle frequenze gravi (1 e 2 kHz). Tale azione selettiva del glicerolo è stata interpretata come una modifica della risposta della base della coclea ai suoni di bassa frequenza (Dauman et al., 1986).
Il test al glicerolo è due volte più sensibile in elettrofisiologia che in audiometria, nonostante che sugli stessi soggetti il miglioramento audiometrico si rilevi solo nel 30% dei menierici.
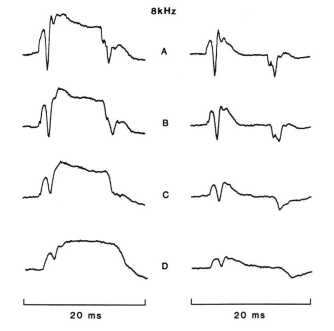
Fig. 1-29. SP e AP nello stesso soggetto e con la stessa stimolazione acustica (un burst di 8 kHz) ma in condizioni di registraziom diverse. Nella colonna di sinistra sono presentate le curve ottenute con banda passante I - 10000 Hz, Nella colonna di destra le curvi con banda passante più stretta, come usualmente impiegata nella misura dell’ABR, 150- ì000 Hz. Le lettere A - D corrispondono nei due tipi dì filtraggio, a valori differenti del tempo di salita dello stimolo, rispettivamente 0.25, 0 5. 1 e 2 ms. L’ampiezza dell’AP è influenzata dal tempo di salita che condiziona la sincronizzazione delle risposte individuali. L’ampiezza dell’SP dipende inven essenzialmente dal filtraggio
![]()
|
|
Fig. 1-30. Test al glicerolo (prova audiometrica) e ECochG di un soggetto con malattia di Ménière. I due test sono entrambi positivi; mostrano un miglioramento dell’udito di meno dii O dB ed una caduta progressiva e selettiva dell’SP alle basse frequenze. (Da Dauman et al.. Am J Otol 9:31-38, Decker Periodicals, I 988b), GRANDORI- MARTINI-I POTENZIALI EVOCATI UDITIVI” ,1955 –PICCIN.
|
A fronte di questi dati clinici, sono tuttora poco chiare le relazioni tra SP, idrope e malattia di Menière, La presenza o l’assenza dell’SP potrà forse diventare in futuro un elemento discriminante tra diverse forme di malattie di Ménière.
A fronte di questi dati clinici, sono tuttora poco chiare le relazioni tra SP, idrope e malattia di Menière, La presenza o l’assenza dell’SP potrà forse diventare in futuro un elemento discriminante tra diverse forme di malattie di Ménière.
|
|
|
Fig. 1-31. Test al glicerolo (prova audiometrica) e ECochG di un soggetto con malattia di Ménière, I due test sono entrambi positivi; mostrano un miglioramento dell’udito di meno di IO dB ed una caduta progressiva e selettiva dell’SP alle basse frequenze. (Da Dauman et aL, Am i Otol 9:31-38, Decker Periodicals, I 988b). F. Grandori-A Martini-“I Potenziali Evocati Uditivi” ,1955 –Piccin.
|
|
|
Fig. 1-32. L’ elettrococleogramma nel soggetto nonnale, Sono visibili 3 picchi positivi (PI. P2 e P3) e 3 picchi negativi (N I. N2 e N3). Il potenziale di sommazione (SP) è visibile nella branca discendente delFNl (click. 80dB HL) F. Grandori-A Martini- “I Potenziali Evocati Uditivi” ,1955 –Piccin. |
F. GRANDORI-A MARTINI”-I POTENZIALI EVOCATI UDITIVI” ,1955 –PICCIN.
In questa condizione, come in altre caratterizzate da idrope, quali sifilide, sordità improvvisa e alcuni casi di neuromi dell’ acustico, il dato più significativo che emerge dall’interpretazione del tracciato è un potenziale di sommazione di grande ampiezza (fig. 3c-3); questo può essere notato sia come una deflessione nella branca discendente dell’ N 1, sia come una pre-onda negativa che si stacca dalla N 1. caratterizzata dalla conservazione di latenza al diminuire dell’intensità. 11 complesso AP-SP è sempre allargato. e questo è dovuto interamente all’aumento relativo della componente SP negativa. Per comprendere tale comportamento dell’SP bisogna rifarsi ai dati della latteratura sulla genesi e fisiopatologia di questo potenziale; Dallos et al. (1972) hanno ritenuto l’SP una risposta a molte componenti, originate da più di una sorgente all’interno della coclea: secondo Withfield e Ross (1965). la maggiore di queste componenti deriva da una fisiologica vibrazione asimmetrica della membrana basilare, tale per cui quest’ultima oscilla maggiormente verso la scala media, e meno verso la scala timpanica. In effetti, si può ipotizzare come questa asimmetria sia responsabile della genesi dell’SP. Infatti, in condizioni caratterizzate da idrope endolinfatica. l’asimmetria di vibrazione verso la scala media viene intensificata, in quanto quest’ultima si trova già in una condizione di stiramento e tensione verso la scala timpanica; tale condizione produrrebbe quindi un potenziale di ampiezza maggiore. Il potenziale di sommazione può essere evidenziato, oltre che come misurazione della sua ampiezza assoluta, anche come rapporto di ampiezza tra SP e AP. Nel normale tale rapporto è di circa 0,27 e può essere ritenuto patologico un rapporto SP/AP maggiore di 0,51.
Per quanto riguarda il potenziale d’azione, a differenza della presbiacusia, in questa condizione recruitante la difasicità dell’AP non è evidente, nel tracciato ottenuto con il click, La difasicità si può dimostrare utilizzando per la registrazione la tecnica di sottrazione. descritta da Gibson e Beagley (1967):
essa si basa sul principio di ottenere un tracciato a bassa cadenza di stimolazione (10 pps) e un altro a rapida cadenza (70 pps); questo permette di separare il complesso AP-SP nei suoi costituenti fondamentali, e il potenziale di azione appare così di ampiezza ridotta e difasico. La condizione di recruitment è riconoscibile anche dalla curva intensità/ampiezza.
|
|
Fig.1-33. Malattia di Ménière Il tracciato tipico è caratterizzato da un ampio potenziale di sommazione (SP) e da un allargamento del complesso AP-SP (click. 80 dB HL) F. Grandori-A Martini: “I Potenziali Evocati Uditivi” ,1955 –Piccin.
|
Test al Glicerolo
F. GRANDORI-A MARTINI”-I POTENZIALI EVOCATI UDITIVI” ,1955 –PICCIN.
In particolare, rapporti di ampiezza SP / AP abnormemente grande (che è semplicemente il rapporto tra l'ampiezza SP rispetto alla ampiezza AP) sono buoni indicatori della malattia di Meniere, in contrasto con i casi di perdita delle cellule acustiche (che hanno un basso rapporto SP / AP). L'SP / AP rapporto ha circa 60-70% di sensibilità per l’ identificazione della malattia di Meniere, ed il 95% di specificità (ad esempio, Sass, 1998; Chung et al, 2004). Una misura potenzialmente più sensibile per la rilevazione di idrope endolinfatico è rapporto tra le aree l'SP / AP, che mette a confronto le aree del SP e il AP invece della loro ampiezza (Devaiah, Dawson, Ferraro, e Ator, 2003).
Potenziali evocati acustici
Al contrario della risonanza magnetica (RMN), la loro utilità è duplice: essi permettono sia di escludere un processo tumorale retrococleare che può mimare clinicamente la malattia di Ménière, sia di mostrare il recruitment specifico di questa malattia 72 pazienti (50 males/22 femmine) con vertigini e / o perdita dell'udito ed acufeni di diversa origine sono state studiate con i potenziali uditivi evocati del tronco encefalico.Il 41,66% dei pazienti era affetto da malattia di Meniere ed il resto (58,33%) da vertigini di origine virale, trauma-cranico, ototossicità, spondiloartrosi cervicale, e di origine vascolare improvvisa-, tra cui la varietà idiopatica.
Il recruitment della malattia di Meniere può essere dimostrata con le risposte evocate uditive del tronco encefalico ,così come le lesione retrococleare potrebbe essere escluso con lo studio dei valori di latenza interpicco, che ha notevolmente contribuito a differenziare una malattia di Meniere unilaterale da un neuroma acustico. I potenziali evocati uditivi del tronco encefalico forniscono quindi informazioni su come funziona la coclea e il nervo 8 a livello del tronco encefalico fino al collicolo inferiore .
Prove vestibolari
I pazienti con malattia di Ménière usualmente presentano un nistagmo spontaneo orizzontale controlaterale all’orecchio malato simile a quello che avviene nei casi con perdita acuta della funzione vestibolare. In questi casi il nistagmo associato con l’idrope riflette una funzione paretica (nistagmo paretico).
Il nistagmo ispsilaterale (nistagmo irritativo) che è diretto verso l’orecchio malato è molto meno frequente ma può essere osservato nelle fasi preparatorie della crisi. (fig. 1-20).Sono r le osservazioni del nistagmo all’inizio e durante un attacco. Bance e coll., McClure e coll. hanno osservato un nistagmo controlaterale durante l’attacco acuto (in alcuni pazienti della durata di più di un giorno) seguito da un nistagmo ipsilaterale durante il periodo di convalescenza (nistagmo recovery) della durata di minuti o molte ore. Quando il nistagmo non è presente,la manovra dello head shaking test può frequentemente far comparire nei pazienti con disfunzione vestibolare.
Eseguite in assenza di terapia antivertiginosa o sedativa, esse sono classicamente rappresentate dalla prova di stimolazione calorica calibrata. Questo esame fornisce, in accordo con la letteratura, una serie di informazioni sulla reflettività vestibolare e la sua prevalenza direzionale. In questa sede si ricordano solo i risultati delle prove effettuate durante la fase intercritica.
La funzione vestibolare resta a lungo anormale ed è caratterizzata da una grande variabilità di risposta alle prove, senza che vi sia un parallelo con le risposte ai test audiometrici (fig.2-4).Nei periodi di intervallo tra un episodio vertiginoso e l’altro, riesce talvolta difficile notare la presenza del nistagmo con l’osservazione diretta. In questi casi, lo si potrà valutare meglio o mediante la registrazione ENG che permette, con la chiusura degli occhi, di eliminare l’effetto inibitorio della fissazione o per mezzo di stimoli (sensitivi o sensoriali, di posizione, otticocinetici) che sono in grado di rendere evidente una condizione di asimmetria vestibolare “latente”.
Negli stadi iniziali della malattia, la stimolazione calorica del labirinto non rileva particolari variazioni dei parametri del riflesso vestibolo-oculare. Ma se l’osservazione del nistagmo avviene con la registrazione ENG è possibile, anche in questo periodo, evidenziare nel lato malato una riduzione dei valori dell’ampiezza e della velocità angolare della fase lenta delle scosse. . Tuttavia, essa si deteriora nel tempo e nel 50-70% dei casi compare un'iporeflessia dal lato colpito
|
|
|
|
Fig.1.34 La crisi di Ménière si accompagna generalmente a iporeflessia vestibolare (A), raramente ad areflessia (B). Nella fase intercritica, la prova calorica calibrata è normale (C).
Infine,Fig. 1.35 l'iporeflessia si stabilizza a valori pari alla metà o a un terzo del suo valore iniziale. come la cofosi, l'areflessia, è all'inizio, eccezionale (nella fase terminale interessa il 5-10% dei casi) e impone, se è riscontrata in diversi esami successivi, di ricercare sempre altre cause, in particolare quella neoplastica
|
|
Fig.1.35 Aspetto tipico della funzione vestibolare nello stadio avanzato della malattia.Si ha iporeflessia dal lato affetto.
|
La prevalenza direzionale, al contrario dell'iporeflessia, non ha valore localizzante, in quanto può risultare diretta sia verso l'orecchio sano che verso quello malato. Al contrario, rivela a volte il fenomeno della iper-compensazione, caratterizzato da una prevalenza direzionale dal lato dell'orecchio affetto, quando essa dovrebbe essere normalmente diretta verso il lato sano. Tale segno si osserva durante un periodo di crisi vertiginose di qualche giorno o settimane e si spiega con un meccanismo centrale: per ridurre lo stato di squilibrio, il nucleo vestibolare centrale controlaterale al lato affetto riduce la sua attività spontanea; quando lo stato di sofferenza del labirinto malato cessa, l'attività del nucleo vestibolare omolaterale si ristabilisce. È quindi il lato sano che sembra ipoeccitabile a spiegare la preponderanza paradossa.
È stato dimostrato nei canali semicircolari posteriori della rana che i recettori ampollari venivano inibiti da un aumento della pressione idrostatica, probabilmente per le variazioni della quantità di neurotrasmettitore a livello del polo sinaptico delle cellule ciliate (Zucca G,1991).La prova rotatoria è eseguita più raramente. Nella fase intercritica è normale solo nel 15% dei casi. Un'asimmetria delle risposte è riscontrata quasi nella metà dei casi (Conraux C, 1982) Nei pazienti affetti da Ménière non è stato osservato recruitment vestibolare dopo la prova rotatoria (Furman JM,1990
L’Head Impulse Test (HIT)
L’Head Impulse Test (HIT) si trova alterato in percentuali nettamente minori rispetto al test calorico, Questo reperto potrebbe indicare che nella MdM ci può essere una sostanziale conservazione della funzionalità dei canali semicircolari tenendo presente che i due test saggiano il sistema utilizzando valori frequenziali estremamente diversi (Carey, 2010). Piuttosto l’HIT (così come l’ice water test) sembra un ottimo indicatore dell’efficacia del trattamento ablativo eseguito con gentamicina intratimpanica (Agrawal e Minor, 2010), Irrilevanti le informazioni ricavabili dai test rotatori e dalla posturografia.;)
VEMP nella malattia di Meniere
Un valido contributo diagnostico viene all’opposto offerto dallo studio dei potenziali evocati vestibolari miogenici cervicali (c-VEMPs) la cui sensibilità per la valutazione della funzione sacculare è paragonabile a quella del rest calorico per la funzione del canale semicircolare laterale.
I pattern di risposta sono estremamente variabili ( Young et al., 2003): i c-VEMPs possono essere assenti, di ampiezza ridotta o con valori di latenza aumentati, mentre in altri casi si può assistere ad un incremento dell’ampiezza dal lato colpito, espressione della dilatazione sacculare che, venendo a contatto con la platina, potrebbe rinforzare la sensibilità del sacculo ai suoni. Un reperto più indicativo è il notevole incremento nei pazienti menierici dei valori di soglia a tutte le frequenze, con uno shift della frequency tuning (frequenza ottimale di stimolo) verso i 1000 Hz (valore normale intorno ai 500 Hz); tale reperto, chiara espressione della distensione sacculare, si riscontra, seppure in modo minore, anche nell’orecchio normale (Rauci, et al., 2004) e potrebbe risultare da un’alterata interazione binaurale del riflesso otolito-cervicale come anche essere segno di una potenziale deriva idropica bilaterale (Raiich et al., 2004). I più elevati valori di shift frequenziale si riscontrano nei pazienti con crisi otolitica di Tumarkin. I c-VEMPs possono avere anche un ruolo nel valutare gli effetti della terapia con gentarnicina e nell’identificazione precoce di evoluzione bilaterale della malattia: fino al 27% dei pazienti con MdM monolaterale presentano anomalie dei c-VEMPs nell’orecchio sano con aspetti intermedi tra orecchio normale e orecchio patologico (Lin et al, 2006).
Alterazioni della tuning curve sono state riscontrate anche utilizzando i VEMPs oculari che non sono tuttavia in grado di fornire chiare indicazioni diagnostiche (Sandhu et aL, 2012).
Questo caso (Fig.1-36/37) illustra una situazione simile:
Prima della somministrazione con gentamicina (basso dosaggio), questo uomo aveva una differenza di 14% tra le orecchie.
|
|
Fig.1.36 Un anno più tardi, egli aveva una differenza del 63% fra le orecchie.
|
|
|
|
|
Fig.1.37 :Così, questo esempio mostra che c'è stata una sostanziale riduzione dell'ampiezza VEMP per questo particolare individuo aveva un ottimo risultato, senza ulteriori attacchi di vertigine
|
|
Il test di deidratazione (con glicerolo o furosemide) è stato eseguito utilizzando come parametro di risposta i potenziali evocati vestibolari miogenici (Seo et al., 2003): il recupero o un incremento dell’ampiezza del potenziale (se ridotta prima del test) può confermare la diagnosi di idrope.Rauch e soci hanno riferito che VEMP mostrano diversi "tuning" nella malattia di Meniere. L'idea sembra essere al fatto che, siccome i pazienti con Meniere hanno un ipoacusia per le frequenze basse, potrebbe anche mostrano alterazione per le frequenze basse con i VEMP. Questa non sembrerebbe un'idea molto logica ,in quanto , la coclea e sacculo hanno un’ organizzazione meccanica molto diversa. Tuttavia, in diversi documenti, Rauch e colleghi hanno dimostrato che a 500 Hz- ton-burst i VEMP hanno una soglia minima, e che questo "favorisca" i 500 hz ,in quanto i 250 ed 1 K in gran parte si perdono nei pazienti con la malattia di Meniere (Rauch et al., 2004). Si ha la sensazione che questo è semplicemente impraticabile. È’ semplicemente troppo difficile ottenere le soglie VEMP a 3 frequenze.
Rauch et al, hanno riferito che le differenze di soglia nei VEMPs, in particolare a 250 hz, erano circa l'80% precisi nel rilevare il lato della lesione in pazienti già noti per avere la malattia di Meniere da dati audiometrici e clinici (Rauch et al., 2004). In mancanza di una diagnosi patologica "gold standard", tuttavia, è difficile sapere come interpretare questa osservazione.
(Osei-Lah et al ,2008) hanno recentemente riferito che il rapporto di differenza media di ampiezza interaurale è significativamente più alto nella malattia di Meniere stabile rispetto alla malattia di Meniere in fase acuta. Soglie e latenze non erano utili
Test al glicerolo
Risultati
Nel 1966 Klockhoff, adattando un test di screening del glaucoma Klockhoff I,1967 ; constatò che l'assunzione di glicerolo, potente agente osmotico, poteva temporaneamente alleviare l'idrope endolinfatica, causando un temporaneo miglioramento della funzione delle cellule ciliate esterne (vedi sotto) e della soglia uditiva. Partendo dall’osservazione che alcuni pazienti menierici presentano fluttuazioni della loro sintomatologia in rapporto all’entità dell’assunzione di liquidi, è stato proposto un test di deidratazione, comunemente definito test al glicerolo, che potrebbe transitoriamente indurre un recupero della perdita uditiva sui toni gravi (Klockhoff e Lindblorn, 1966).I test osmotici hanno acquisito anche un grande interesse diagnostico, perché rappresentano l'unico modo disponibile per dimostrare l'esistenza di un'idrope endolinfatica. Essi hanno, peraltro, sia valore prognostico, dato che la loro positività testimonia che la malattia è ancora in uno stadio reversibile, sia valore terapeutico, perché costituiscono un aiuto nella scelta del trattamento. Tuttavia, un risultato negativo non consente assolutamente di escludere l'esistenza della malattia di Ménière Hamann KF, 1999 ;
Principio Il principio di questi test è basato sull'induzione di un gradiente tra i compartimenti vascolare e labirintico, attraverso un rapido e transitorio aumento dell'osmolalità ematica indotto dall'ingestione o dall'infusione di una sostanza ad alta capacità osmotica. Questo gradiente comporta uno spostamento di liquido fuori dall'orecchio interno, che attenua l'ipertensione labirintica e, conseguentemente, migliora la trasduzione elettromeccanica nell'orecchio interno e, dunque, la funzione uditiva o vestibolare. Questo miglioramento può essere verificato con prove funzionali, eseguite prima e dopo il test. Il fatto che la sottrazione chirurgica di endolinfa possa peggiorare la funzione uditiva, mentre al contrario la somministrazione di glicerolo la migliora, potrebbe indicare che lo spostamento dei liquidi indotto dal test osmotico avviene a carico della perilinfa piuttosto che dell'endolinfa e che l'abbassamento della pressione perilinfatica sarebbe immediatamente trasmesso all'endolinfa Tran Ba Huy P1989; Tuttavia, l'ipotesi di un semplice effetto osmotico diretto non è sufficiente a motivare le differenze che si osservano tra i diversi prodotti utilizzati. Altri meccanismi, come l'aumento del flusso ematico cocleare (Larsen HC, 1982) o l'effetto emodinamico diretto della pressione arteriosa (Carlborg BI,1983)sono stati chiamati in causa
Tecnica Il farmaco più comunemente utilizzato è il glicerolo. Esso viene somministrato per via orale, a digiuno, a riposo assoluto, alla dose di 1,5 g/kg di peso corporeo, mescolato a un pari volume di soluzione salina isotonica e ad alcune gocce di succo di limone, se il suo gusto è sgradito al paziente. Oltre ai suoi effetti sulla funzione uditiva, esso può indurre cefalea (da ipotensione liquorale) o vomito. A volte viene utilizzata anche l'urea per via orale alla dose di 20 g mescolati a 200 ml di succo di frutta. Il mannitolo può essere usato per via venosa con, parrebbe, eccellenti risultati.Gli esami audiometrici vengono effettuati poco prima di iniziare il test e nelle prime due o tre ore che seguono l'ingestione del prodotto. Il glicerolo agirebbe attraverso un incremento dell’osmolarità plasmatica da cui deriva un passaggio di liquidi per osmosi dagli spazi extravascolari, favorendo in tal modo una deidratazione della coclea idropica. Dopo ingestione orale di 1.5 mg/kg/peso di glicerolo, si valuta l’eventuale variazione dell’audiogramma basale a 1 ora e dopo 3 ore. Il test è considerato positivo se si assiste ad un miglioramento della soglia di 10 o più dB su almeno due frequenze da 250 a 2000 Hz o se si assiste ad un miglioramento della discriminazione vocale di almeno il 12%.
Risultati strumentali
L'audiometria tonale è quella eseguita più spesso. Il criterio comunemente fissato per valutare la positività del test è dato dalla comparsa di un miglioramento delle soglie tonali di 10 dB almeno su due frequenze tra 500, 1.000 e 2.000 Hz.
L'audiometria vocale è considerata più sensibile dell'audiometria tonale. Un miglioramento dell'intelligibilità pari al 10% è considerato come significativo.
Per quanto riguarda l'audiometria, il test al glicerolo risulta positivo in circa il 60% dei casi di malattia di Ménière. In realtà, questa positività dipende dallo stadio della malattia. A causa del carattere fluttuante della capacità uditiva, ci si rende conto anche di come il test possa essere negativo al di fuori della crisi. Alcuni Autori hanno proposto di rendere più sensibile il test attraverso un carico di sodio da somministrare nei giorni precedenti, fatto che peggiora momentaneamente la funzione uditiva (Arenberg IK,1974).;
Recentemente la risposta al glicerolo è stata studiata con i DPOAEs. Sono stati segnalati casi in cui il Dp-gramma migliorava dopo l’assunzione del glicerolo ed altri casi in cui, assente prima, compariva dopo.
I test all'urea e al mannitolo sembrano complessivamente meno sensibili del test al glicerolo. Inoltre, l'assunzione di questi prodotti può, in alcuni casi, non provocare un miglioramento ma piuttosto un peggioramento. Sebbene risultato positivo nel 40-60% dei pazienti menierici (Stahle e Klockoff, 1986), questo test non viene considerato di grande utilità diagnostica poiché risulta spesso negativo nelle fasi precoci della malattia e anche nelle fasi avanzate laddove si instaurano variazioni irreversibili delle strutture membranose dell’Ol,
L'elettrococleografia con elettrodo transtimpanico è un metodo di registrazione dei potenziali evocati acustici molto precoci, che hanno, cioè, una latenza massima pari a 2 ms. L'origine di questi potenziali è localizzata a livello della coclea o del nervo coclearie. Il potenziale elettrococleografico è costituito da tre elementi: i potenziali microfonici, che verranno eliminati; i potenziali di sommazione, che riflettono lo spostamento statico della membrana basilare; e i potenziali d'azione, che provengono dall'origine del nervo cocleare. Nella malattia di Ménière, l'ampiezza dei potenziali di sommazione è aumentata in valore assoluto rispetto a quella che si riscontra nei soggetti normali. Questo aumento è correlato alla distensione della membrana basilare verso la scala timpanica. Eggermont ha messo a punto un metodo di valutazione di questi potenziali, calcolando il rapporto ottenuto dalle ampiezze dei potenziali di sommazione su quelle dei potenziali d'azione (PS/PA). Una ratio superiore a 0,35, può indicare l'esistenza di un'idrope endolinfatica (Eggermont JJ 1979).
Sotto l'effetto glicerolo, peraltro, l'ampiezza dei PS si riduce (generando una riduzione della distensione della membrana basilare), mentre quella dei PA aumenta (generando un miglioramento dell'udito). L'elettrococleografia, che mostra un aumento del rapporto PS/PA nell'80% dei casi, appare quindi allo stato attuale come il miglior metodo per documentare un'idrope endolinfatica (Dauman R, 1986). Nonostante ciò, un test negativo non consente di scartare formalmente l'idrope, poiché quest'ultima può ridursi, casualmente, anche poco prima del test (Hamann KF,1999).
D'altra parte, le procedure di esecuzione tecnica devono essere meglio codificate ed esistono tuttora problemi per ottenere registrazioni stabili e riproducibili (Jackler RK, 1994).
Alcuni Autori ritengono che il test al glicerolo consenta di individuare i pazienti con malattia di Ménière allo stadio precoce e usano questo test come indice di risposta terapeutica (Jackler RK,1994).
L'audiometria tonale è quella eseguita più spesso. Il criterio comunemente fissato per valutare la positività del test è dato dalla comparsa di un miglioramento delle soglie tonali di almeno 10 dB su due frequenze tra 500, 1.000 e 2.000 Hz.
L'audiometria vocale è considerata più sensibile dell'audiometria tonale. Un miglioramento dell'intelligibilità pari al 10% è considerato come significativo. Per quanto riguarda l'audiometria, il test al glicerolo risulta positivo in circa il 60% dei casi di malattia di Ménière. In realtà, questa positività dipende dallo stadio della malattia. A causa del carattere fluttuante della capacità uditiva, ci si rende conto anche di come il test possa essere negativo al di fuori della crisi. Alcuni Autori hanno proposto di rendere più sensibile il test attraverso un carico di sodio da somministrare nei giorni precedenti, fatto che peggiora momentaneamente la funzione uditiva (Arenberg IK,1974).
I test all'urea e al mannitolo sembrano complessivamente meno sensibili del test al glicerolo.
Inoltre, l'assunzione di questi prodotti può, in alcuni casi, non provocare un miglioramento ma piuttosto un peggioramento.
L’elettrococleografia(FIG 1-38 )
L'elettrococleografia con elettrodo transtimpanico è un metodo di registrazione dei potenziali evocati acustici molto precoci, che hanno, cioè, una latenza massima pari a 2 ms. L'origine di questi potenziali è localizzata a livello della coclea o del nervo cocleare. Il potenziale elettrococleografico è costituito da tre elementi: i potenziali microfonici, che verranno eliminati; i potenziali di sommazione, che riflettono lo spostamento statico della membrana basilare; e i potenziali d'azione, che provengono dall'origine del nervo cocleare. Nella malattia di Ménière, l'ampiezza dei potenziali di sommazione è aumentata in valore assoluto rispetto a quella che si riscontra nei soggetti normali. Questo aumento è correlato alla distensione della membrana basilare verso la scala timpanica. Eggermont ha messo a punto un metodo di valutazione di questi potenziali, calcolando il rapporto ottenuto dalle ampiezze dei potenziali di sommazione su quelle dei potenziali d'azione (PS/PA). Una ratio superiore a 0,35, può indicare l'esistenza di un'idrope endolinfatica (Eggermont JJ, 1979). Sotto l'effetto glicerolo, peraltro, l'ampiezza dei PS si riduce (generando una riduzione della distensione della membrana basilare), mentre quella dei PA aumenta (generando un miglioramento dell'udito). L'elettrococleografia, che mostra un aumento del rapporto PS/PA nell'80% dei casi, appare quindi allo stato attuale come il miglior metodo per documentare un'idrope endolinfatica (Dauman R., 1986)
Nonostante ciò, un test negativo non consente di scartare formalmente l'idrope, poiché quest'ultima può ridursi, casualmente, anche poco prima del test di Hamann (1999). D'altra parte, le procedure di esecuzione tecnica devono essere meglio codificate ed esistono tuttora problemi per ottenere registrazioni stabili e riproducibili (Jackler RK, 1994). Alcuni Autori ritengono che il test al glicerolo consenta di individuare i pazienti con malattia di Ménière allo stadio precoce e usano questo test come indice di risposta terapeutica (Jackler RK, 1994).
Altri test cocleari
Potenziali evocati acustici
Al contrario della risonanza magnetica (RMN), la loro utilità è duplice: essi permettono sia di escludere un processo tumorale retrococleare che può mimare clinicamente la malattia di Ménière, sia di mostrare il recruitment specifico di questa malattia
Otoemissioni acustiche
Altri test meno utilizzati
Vengono riportati, infine, alcuni esami che, per mancanza di specificità e per la loro complessità, sono poco usati:
test psicoacustici.
La membrana basilare deformata dall'idrope comporta una perdita di selettività e di potere mascherante, che può essere esplorata attraverso questi test
test all'acetazolamide
Questa prova consiste nel praticare un'audiometria tonale poco prima e 45 minuti dopo somministrazione endovenosa in 1 minuto di 500 mg di acetazolamide. Questa sostanza è un inibitore dell'anidrasi carbonica, enzima contenuto in grandi quantità nell'orecchio interno. Il meccanismo del test è poco chiaro; l'acetazolamide potrebbe indurre una transitoria caduta dell'osmolalità sanguigna. Questo test è considerato positivo in presenza di un peggioramento delle soglie acustiche almeno pari a 10 dB. Dotato di alta sensibilità, provocando un peggioramento e non un miglioramento della funzione uditiva, il test potrebbe essere in grado di predire una possibile bilateralizzazione della patologia in presenza di un orecchio controlaterale apparentemente sano;
test vestibolare al furosemide
Stranamente, le sostanze osmotiche summenzionate non esplicano alcun effetto sul vestibolo . La furosemide, al contrario, sembra in grado di modificare la funzione vestibolare nei pazienti affetti dalla malattia Ménière (FutakiT, 1977 ; Futaki T 1975).
Il test consiste nel praticare una prova calorica fredda (50 ml a 30 °C) prima e 1 ora dopo la somministrazione endovenosa di 20 mg. Il test, positivo in presenza di un incremento della velocità massima del nistagmo superiore al 9,4%, risulterebbe positivo nell'80% delle forme tipiche e potrebbe essere positivo anche nelle fasi di ipoacusia stabilizzata, quando il test al glicerolo non è più positivo. A causa dei loro effetti secondari indesiderati (cefalea, diarrea, vomito, aumento della diuresi), i diuretici osmotici (glicerolo, furosemide, ecc.) non vengono comunemente usati. Inoltre, il diabete, la disidratazione, l'insufficienza cardiaca, renale o epatica ne controindicano l'utilizzo;
la camera ipobarica
Nel 1975, Densert descrisse come l'ipoacusia di tre pazienti in piena crisi di Ménière fosse stata stata migliorata da una permanenza di 30-129 minuti in camera ipobarica, a pressioni variabili da -300 a -900 mm di acqua. L'Autore avanzò l'ipotesi che la crisi di Ménière fosse dovuta a un'ostruzione parziale o totale, ma temporanea, del canale endolinfatico, a causa di una stasi venosa. In base a ciò, se l'organismo fosse stato esposto a una riduzione della pressione atmosferica, avrebbe potuto giovarsi del decongestionamento dei vasi dell'orecchio interno e dell'orecchio medio e, conseguentemente, della neutralizzazione dell'ipertensione endolinfatica (Densert B, 1987). I pazienti considerati affetti sono sistemati in una camera ipobarica, all'inizio a pressioni di -500 mm d'acqua, quindi, dopo 5 minuti, a -700 mm d'acqua. La pressione è mantenuta a questo livello durante i 5 minuti successivi, quindi riportata a 0. La procedura è ripetuta per tre volte consecutive, mentre viene chiesto ai pazienti di non effettuare manovre di compensazione dell'orecchio medio quando la pressione è a 0. Un guadagno di 10 dB in almeno due tra le frequenze di 250, 500 e 1.000 Hz è considerato come un effetto positivo del test. La funzione uditiva migliora solo nei pazienti con Ménière (50%) e/o con una forma cocleare pura della malattia (32%). Secondo gli Autori, la positività a questo esame indica la presenza di una malattia di Ménière, anche se, per contro, non riescono a spiegare come una riduzione della pressione atmosferica possa migliorare la funzione uditiva dei pazienti affetti;
Più recentemente, Kitahara et al hanno descritto un altro test diagnostico della malattia di Ménière
altri test. Il Test di Fowler, il SISI test, il Bekesy e il Tone Decay Test confermano la natura endococleare della malattia, ma generalmente sono poco usati.
DIAGNOSTICA PER IMMAGINI
Indagini Nueroradiologiche
• RM encefalo e orecchio interno, senza e con MDC ev Naganawa e coll 2006.
• RM encefalo e orecchio interno con mdc intratimpanico Naganawa e coll 2008.
Nel caso della malattia di Ménière, le tecniche di imaging vengono usate con un duplice scopo:
![]() escludere una patologia in grado di mimare la sintomatologia menieriforme: neurinoma dell'acustico, meningioma dell'angolo ponto-cerebellare, malformazione congenita dell'orecchio interno (sindrome di Mondini), malformazione del tratto cervicale della colonna o della cerniera occipito-atlantoidea;
escludere una patologia in grado di mimare la sintomatologia menieriforme: neurinoma dell'acustico, meningioma dell'angolo ponto-cerebellare, malformazione congenita dell'orecchio interno (sindrome di Mondini), malformazione del tratto cervicale della colonna o della cerniera occipito-atlantoidea;
![]() tentare di evidenziare varianti anatomiche dell'orecchio interno in grado di favorire lo sviluppo della malattia.
tentare di evidenziare varianti anatomiche dell'orecchio interno in grado di favorire lo sviluppo della malattia.
I progressi della radiologia medica, in particolare l'avvento della tomografia computerizzata, hanno permesso di confermare nei pazienti affetti dalla malattia di Ménière le osservazioni istologiche di un acquedotto del vestibolo di piccole dimensioni e di una ridotta pneumatizzazione mastoidea periacqueduttale (Sando I,1985 ) . Così, vari tagli di scansione della rocca petrosa hanno mostrato una ipoplasia della regione retrolabirintica (Yazawa Y ,1994) , e dell'acquedotto del vestibolo (Takeda T, 1997) nei pazienti affetti Tuttavia, altri lavori, basati sulla scansione delle rocche, non hanno permesso di raggiungere conclusioni definitive sulle caratteristiche dell'acquedotto del vestibolo, poiché il diametro del canale endolinfatico non è strettamente correlato a quello dell'acquedotto. (Schmalbrock P ,1996).
Più recentemente, studi di imaging mediante risonanza magnetica (RMN) sembrano dimostrare con buona significatività che l'acquedotto del vestibolo può essere visualizzato con minor frequenza nei pazienti portatori della malattia piuttosto che nei soggeti appartenenti al gruppo di controllo
Si vedrà più avanti che il calibro dell'acquedotto del vestibolo sembra avere un ruolo preponderante nella genesi della malattia. La RMN ha anche dimostrato che, da un lato, la distanza tra la parte verticale del canale semicircolare posteriore e la fossa cranica posteriore era rappresentativa della grandezza del sacco endolinfatico e che, dall'altro, questa distanza era significativamente inferiore nei pazienti affetti da Ménière, rispetto a quella dei soggetti sani (Mateijsen DJ 1999).Nonostante ciò, nella stessa persona, gli stessi Autori non hanno osservato differenze significative tra orecchio affetto e orecchio sano, ed evocano, per concludere, un'anomalia anatomica congenita.
Bisogna dunque diffidare di possibili variazioni interindividuali e della mancanza di studi comparativi, per l'assenza di standardizzazione delle tecniche di imaging utilizzate. La mancata visualizzazione radiologica dell'acquedotto del vestibolo non deve essere considerata come un equivalente della sua lesione funzionale. Le tecniche di imaging servono, per alcuni, solo ad escludere altre patologie e, in particolare, il neurinoma vestibolare (Hamann KF, 1999).
Laddove la sintomatologia tipica compare in età infantile o in giovani adulti sarà inoltre necessario ricorrere ad uno studio TC ad alta risoluzione dell’QI allo scopo di escludere la presenza di anomalie congenite quali l’acquedotto vestibolare largo o quadri di incompleto sviluppo delle strutture labirintiche compatibili con una displasia tipo Mondini. Con la stessa indagine sarà inoltre possibile escludere anche fenomeni di deiscenza del canale semicircolare superiore.
Recentemente con tecniche di MR 3 Tesla è stato possibile visualizzare direttamente l’lE in pazienti menierici a seguito di somministrazione intrarimpanica di gadolinio la cui distribuzione preferenziale nella perilinfa permette di misurare l’area occupata dall’endolinfa idropica rispetto al totale fornendo in tal modo anche dati quantitativi sul grado di idrope (Pyykkö et al, 2010). Questa inno ativa metodica ha permesSo di dimostrare che l’idrope rende a divenii e sempre maggiore con il progredire della malattia, confei mandone in tal modo il carattere progressi amente degenerativo.
Esami di laboratorio
Qualsiasi sospetto di malattia di Ménière impone una valutazione di laboratorio per ricercare l'esistenza di un'anomalia causale o intercorrente, la cui correzione è, teoricamente, in grado di migliorare la storia evolutiva della malattia
Vengono dunque richiesti: un'elettrolitiemia, una glicemia a digiuno e, in casi dubbi, una curva da carico orale di glucosio, osmolalità plasmatica, emocromo, bilancio lipidico e sierologia per la sifilide.
L’esecuzione di test sierologici e immunologici in pazienti con sospetta MCIM può essere utile per evidenziare una forma luetica (Abuzeid , Ruckenstein , 2008) ed escludere la presenza di fenomeni autoimmuni a carico dell’QI. A dispetto dell’entusiasmo suscitato negli anni 90 dall’ipotesi immunologica della MdM, attualmente non disponiamo di test specifici per poter porre questa diagnosi eziologica e al fine di individuare un possibile coinvolgimento del sistema immunitario, è indicato eseguire una limitata batteria di esami che comprende (Ruckenstein et al., 2002): emocromo, VES, PCR, ricerca anticorpi antinucleari (la cui presenza sembra piuttosto elevata in soggetti con MdM bilaterale), ricerca anticorpi antifosfolipidi.
Vengono talvolta richiesti altri esami come: dosaggio degli ormoni tiroidei, prove immunologiche (ricerca di anticorpi antinucleo, elettroforesi proteica, indici di flogosi, studio del sistema degli antigeni umani leucocitari [HLA]). Tuttavia, come si vedrà più avanti, l'ipotesi di una malattia autoimmune non è, al momento, sufficientemente provata.
Alla luce di quanto esposto, è possibile impostare un tentativo di stadiazione della MdM basandoci sulle variazioni del quadro clinico e strumentale che avvengono nel lungo decorso della malattia che viene così suddivisa temporalmente in base al tipo di interessamento vestibolare in una fase iniziale, una fase florida ed una avanzata. I sintomi da interessamento delle strutture cupolari dei canali semicircolari sono evidenti nella fase iniziale e florida della malattia, mentre quadri clinici indotti da un coinvolgimento delle strutture maculari appaiono generalmente nella fase florida o avanzata ( Tabella 1-4).
TABELLA 1-4 - Stadiazione clinica della malattia di Menière
|
MALATTIA DI MENIÉRE: STADIAZIONE CLINICA |
||
|
|
|
|
|
MdM canalare |
INIZIALE |
Ipoacusia monolaterale in salita (toni gravi) |
|
|
|
Fluttuazione uditiva con ritorno alla normalità |
|
|
|
Vertigini oggettive isolate (prolungate) |
|
|
|
Vertigini oggettive isolate (prolungate ) |
|
|
|
Variante di esordio tipo Lermoyez |
|
|
|
Esordio bilaterale (raro) |
|
|
FLORIDA |
Ipoacusia a V rovesciata (gravieacuti) |
|
|
|
Fluttuazione uditiva senza ritorno alla norma |
|
|
|
Vertigini oggettive subentranti |
|
|
|
Deficit labirintico parziale |
|
|
|
|
|
MdM maculare |
|
Ipoacusia pantonale |
|
|
|
Fluttuazione uditiva modesta |
|
|
|
Variazioni precritiche dell’acufene |
|
|
|
Vertigini soggettive (piu brevi) |
|
|
|
Labirintolitiasi episodica |
|
|
|
Fase di Tumarkin (pulaioni otolitiche) |
|
|
|
Deficit labirintico totale o subtotale |
|
|
|
|
|
MdM avanzata |
|
Deficit labirintico totale o subtotale |
|
|
|
lpoacusia pantonale grave stabile |
|
|
|
Instabilità posturale senza crisi |
|
|
|
Deficit labirintico totale |
19) DIAGNOSI DIFFERENZIALE
Il problema della diagnosi differenziale si pone soprattutto quando la triade clinica non è completa.
Sindrome cocleare isolata
In presenza di una sindrome cocleare isolata, bisogna escludere:
![]() una forma cocleare pura della malattia, ancora chiamata ipoacusia fluttuante.
una forma cocleare pura della malattia, ancora chiamata ipoacusia fluttuante.
Il riscontro di una forma cocleare pura di Ménière è comunque messa in discussione da numerosi Autori (AAO-HNS), perché non è affatto dimostrato che il substrato fisiopatologico sia in ogni caso un'idrope endolinfatica. È meglio quindi parlare di «ipoacusia fluttuante», in attesa che l'eventuale comparsa di crisi vertiginose associate possa far sospettare una malattia di Ménière. Questa malattia, in effetti, può evolvere per molti anni in modo monosintomatico;
![]() una ipoacusia improvvisa.
una ipoacusia improvvisa.
![]() Le ipoacusie improvvise, se reversibili nell'arco di alcune ore o giorni, possono evocare la diagnosi di malattia di Ménière allo stadio iniziale. Solamente un controllo a lungo termine del paziente, valutando l'assenza o al contrario l'insorgenza di recidive, può consentire un'esatta diagnosi;
Le ipoacusie improvvise, se reversibili nell'arco di alcune ore o giorni, possono evocare la diagnosi di malattia di Ménière allo stadio iniziale. Solamente un controllo a lungo termine del paziente, valutando l'assenza o al contrario l'insorgenza di recidive, può consentire un'esatta diagnosi;
![]() una labirintite sierosa.
una labirintite sierosa.
![]() Una lesione infiammatoria, acuta o cronica, dell'orecchio medio, può generare un'idrope reattiva (Paparella MM ,1984).
Una lesione infiammatoria, acuta o cronica, dell'orecchio medio, può generare un'idrope reattiva (Paparella MM ,1984).
D'altronde, in questi casi è molto comune notare una sensazione di pienezza auricolare e di lieve instabilità, così come una curva in salita sull'audiogramma di otiti purulente. La diagnosi si basa sull'esame otoscopico e sul quadro clinico;
![]() una sifilide labirintica.
una sifilide labirintica.
![]() La sifilide nella sua fase terziaria dal punto di vista istologico si manifesta con alterazioni infiammatorie del labirinto membranoso, con idrope, che evolvono secondariamente in fibrosi. La diagnosi si basa sulla storia clinica, sui classici segni associati, sul segno di Hennebert (segno della fistola senza fistola), qui particolarmente evidente per la presenza di fibrosi e soprattutto sulla sierologia;
La sifilide nella sua fase terziaria dal punto di vista istologico si manifesta con alterazioni infiammatorie del labirinto membranoso, con idrope, che evolvono secondariamente in fibrosi. La diagnosi si basa sulla storia clinica, sui classici segni associati, sul segno di Hennebert (segno della fistola senza fistola), qui particolarmente evidente per la presenza di fibrosi e soprattutto sulla sierologia;
![]() una sindrome di Cogan o altre malattie autoimmuni.
una sindrome di Cogan o altre malattie autoimmuni.
![]() La sindrome di Cogan è un fenomeno raro che associa ai segni labirintici la cheratite e una vasculite sistemica. La sua diagnosi, affidata in genere all'internista, si basa su stigmate generali, che lasciano ipotizzare l'esistenza di un disordine immunitario, e sull'esecuzione di test laboratoristici che esplorano la funzione immunitaria. La diagnosi, rara, chiama in causa un trattamento che associa a diversi gradi corticosteroidi, immunosoppressori o addirittura la plasmaferesi. A causa della pesantezza di questi trattamenti, questa diagnosi va posta solo con estrema prudenza.
La sindrome di Cogan è un fenomeno raro che associa ai segni labirintici la cheratite e una vasculite sistemica. La sua diagnosi, affidata in genere all'internista, si basa su stigmate generali, che lasciano ipotizzare l'esistenza di un disordine immunitario, e sull'esecuzione di test laboratoristici che esplorano la funzione immunitaria. La diagnosi, rara, chiama in causa un trattamento che associa a diversi gradi corticosteroidi, immunosoppressori o addirittura la plasmaferesi. A causa della pesantezza di questi trattamenti, questa diagnosi va posta solo con estrema prudenza.
Sindrome vestibolare isolata
In presenza di una sindrome vestibolare isolata, bisogna escludere:
una forma vestibolare pura della malattia.
Prima di poter porre tale diagnosi, solo dopo aver escluso ogni altra patologia possibile, bisognerebbe tuttavia attendere nel corso degli anni la comparsa dei segni cocleari;
una neurite vestibolare.
La neurite vestibolare si differenzia dalla malattia di Ménière per la mancanza di sintomi cocleari associati, per l'unicità della crisi vertiginosa, per la sua durata, che supera generalmente alcune ore per durare alcuni giorni, per l'ipo- o l'areflessia unilaterale spesso definitiva alle prove vestibolari e per la presenza di un meccanismo di compensazione centrale che si instaura nel giro di alcuni giorni o settimane;
una vertigine posizionale parossistica benigna (VPPB).
La VPPB è caratterizzata da episodi vertiginosi brevi, dell'ordine di qualche secondo, che si manifestano in concomitanza di alcuni movimenti del capo. Le vertigini sono elicitabili con la manovra di Dix e Hallpike;
una vestibolopatia emicranica,
una vestibular paroxysmia,
una atassia periodica.
una vertigine di origine centrale.
Tre malattie possono accompagnarsi a manifestazioni vetiginose e fanno sospettare un'origine periferica: la sclerosi multipla e la sindrome di Wallenberg, diagnosticabili con la RMN, e l'insufficienza vertebrobasilare.
Segni vestibolari e cocleari
Al cospetto di segni vestibolari e cocleari, devono essere escluse:
una labirintite o ancora un'ipoacusia improvvisa con interessamento labirintico.
Essa è caratterizzata dal calo, improvviso e unilaterale, dell'udito e a volte della funzione vestibolare, associati a un acufene omolaterale. Contrariamente alla malattia di Ménière, la sintomatologia dura parecchi giorni e il recupero è casuale, come per l'ipoacusia improvvisa e la neurite vestibolare;
il neurinoma dell'acustico.
Nella sua forma classica, intracanalare quindi pontocerebellare, il neurinoma può essere diagnosticato con la RMN, che viene richiesta quando dopo la prima crisi c'è assenza di recupero. Al contrario, nella sua variante eccezionale a partenza intralabirintica, esso può simulare a lungo una malattia di Ménière (Tran Ba Huy P, 1989); In questo caso la diagnosi può essere posta spesso solo dopo diversi anni, in presenza della comparsa di sintomi atipici, in particolare con esteriorizzazione della massa neoplastica nell'orecchio medio o addirittura esterno. Questa possibilità diagnostica deve essere tenuta presente in presenza di qualsiasi malattia di Ménière caratterizzata da elementi atipici, in particolare areflessia vestibolare e cofosi;
una fistola labirintica.
Di origine traumatica (trauma cranico, barotraumatismo) o iatrogena (chirurgia otologica), la fistola labirintica si manifesta con sensazioni vertiginose fugaci provocate da sforzo e associate a una riduzione progressiva e graduale dell'udito. Questo quadro clinico può confondersi solo raramente con la malattia di Ménière; tuttavia, è stato riportato che alcune fistole perilinfatiche della finestra cocleare potrebbero mimare tutte le caratteristiche cliniche della malattia di Ménière e che solo un'esplorazione chirurgica potrebbe identificarle e trattarle;
ototossicità da farmaci.
Molte classi di farmaci sono in grado di danneggiare l'orecchio interno (antibiotici come gli aminoglicosidi, per esempio,(Bagger-Sjobak D, 1997 ); Altri possiedono un effetto inibitorio sul labirinto, come gli antiinfiammatori non steroidei, gli antiepilettici e i sedativi (Brandt T,,1991);La raccolta dell'anamnesi, che deve essere rigorosissima, rivela la relazione tra l'assunzione del farmaco e la comparsa dei sintomi. L'attacco dura inoltre più a lungo di una crisi di Ménière
20) TERAPIA (scuola ITALIANA CASANI)
Terapia
Le strategie terapeutiche proposte ed impiegate nella MdM numerose e per lo più basate su criteri empirici, alcune universalmente accettate, altre invece praticate solo in alcuni centri in Italia o all’estero. La difformità di trattamento deriva non solo dall’assenza di una sicura base eziopatogenetica, ma anche dalla difficoltà di effettuare studi cimici di classe A in virtù dell’andamento fluttuante della malattia che può presentare lunghe fasi di remissione della sintomatologia. Le review che hanno analizzato la risposta dei pazienti menierici a tutta una serie di terapie mediche hanno evidenziato che la percentuale di successo si poneva intorno al 70%, non dissimile a quanto ottenibile con il placebo (Torok 1977; Coelho e Lalwani 2008). Partendo da queste premesse, sulla base di un sano pragmatismo clinico e considerando le basi fisiopatologiche, il trattamento medico ha un suo preciso ruolo pur dovendo essere condotto tenendo presente i possibili effetti collaterali e i costi economici, per poi procedere verso trattamenti più specifici qualora non si ottengano risposte positive.
Per la terapia dell’attacco acuto si ricorre generalmente a farmaci ad azione vestibolo-soppressiva in associazione con antiemetici, oppure, anche per i benefici effetti ansiolitici, al diazepam per via endovenosa (5 mg) (Tabella IV). L’uso del cortisone in fase acuta è stato proposto in virtù della ipotetica origine autoimmune della MdM allo scopo di ridurre sia l’entità della crisi sia per favorire il recupero uditivo e vestibolare (Antonio e Friedman, 2005). Il cortisone potrà essere usato sia per via intravenosa che orale con cicli a scalare di 10-14 gg (es prednisone i mglKg). Infine si ricorda l’uso dei diuretici osmotici (mannitolo o glicerolo 10%) per via endovenosa in infusione lenta.
TERAPIA DELLA FASE INTERCRITICA (PROFILASSI)
Lo scopo del trattamento della MdM in fase intercritica è teoricamente quello di:
1. ridurre il numero e la gravità delle crisi vertiginose;
2. alleviare i sintomi cronici (instabilità e acufene);
3. prevenire la progressione della malattia, con particolare riguardo all’ipoacusia e ai disturbi dell’equilibrio.
Le terapie di mantenimento riescono ad ottenere un sufficiente controllo delle crisi vertiginose in almeno 2/3 dei pazienti, soprattutto adottando un adeguato stile di vita (no alcool, no tabacco, no caffè, no stress), misure dietetiche (restrizione sodica) e diuretici (Rauch 2010; Shen e Ruckenstein 2010; ); all’opposto non esiste alcuna terapia che sia efficace nel preservare l’udito a lungo termine.
La misura dietetica principale raccomandata nella MdM da più di 70 anni corrisponde alla restrizione dell’apporto di sodio. In effetti, secondo il già menzionato concetto dell’orecchio fragile, nella MdM viene perduta la capacità di controllare il livello idro-elettrolitico locale e l’orecchio è molto più suscettibile a variazioni di sodio e di liquidi. Più che una dieta povera di sodio, sarà quindi importante che il paziente ne assicuri un costante apporto (0.5-1 gr a pasto). La compliance è migliore con una baseline di sodio non troppo bassa perché se occasionalmente c’è un forte surplus salino, partendo da bassi valori, si può scatenare una crisi. Anche un incremento dell’assunzione di acqua potrebbe avere un ruolo favorevole nel controllo della sintomatologia menierica (Naganuma et al., 2006). La scoperta di recettori per I’ADH nel SE e in altri tessuti dell’QI e la capacità di questo ormone di regolare l’omeostasi idroelettrolitica attraverso il controllo dell’espressione di aquaporine, ha indotto ad ipotizzare che un periodo di disidratazione, inducendo un incremento dell’ADH, possa provocare un lE attraverso l’azione dell’aquaporine 2, molto rappresentata a livello della stria vascolare, fonte principale dell’endolinfa cocleare (Kitahara et al., 2008).
Ad oggi i diuretici rappresentano, almeno negli USA, la categoria farmacologica più ampiamente utilizzata per il trattamento della MdM (Shen e Ruckenstein, 2010), nonostante l’assenza di prove sperimentali e cliniche certe della loro efficacia. Il loro razionale d’utilizzo è puramente empirico e si basa sull’effetto di riduzione del volume plasmatico che potrebbe indurre una deplezione cii fluidi nell’QI tale da prevenire l’idrope, Tra le diverse classi di diuretici i più utilizzati sono l’idroclorotiazide, il triamterene e l’acetazolamide, mentre è da sconsigliare l’uso della furosernide per gli elevati rischi di effetti collaterali (Tabella 1-6 ).
Tabella 1-6 Le categorie di diuretici utilizzati nalle malattia di meniere
|
Classe |
Azione |
Farmaco |
Effetti Collaterali
|
|
TIAZIDICI |
Inibiscono il riassorbi mento renale di NaICl |
Clortalidone Idroclorotiazide |
Ipokaliemia Iperuricemia Intolleranza glucudica |
|
RISPARMIATORI DI POTASSIO |
Inibiscono lo scambio renale Na/K |
Spironolattone |
Iperkalemia |
|
DIURETICI DELL’ANSA |
Inibiscono il cotrasporto renale |
Furosemide |
Ipovolemia, ipotensione lpokaliemia |
|
INIBITORI DELL’ANIDRASI CARBONICA |
Inibisce la secrezione di H+ promuove l’escrezione di Na+ e K+ |
Acetazolamide |
Disturbi gastroenterici Acidosi metabolica nefrolitiasi |
Anche i farmaci ad azione vasoattiva sono stati ampiamente utilizzati nella profilassi della MdM, specialmente in Europa. Di questi il più adottato è indubbiamente la Betaistina, debole agonista per i recettori Ri dell’istamina e contemporaneamente antagonista per i recettori H3 dell’istamina a livello centrale (Mira, 2001). Sebbene una recente review abbia dimostrato che non vi sono prove dell’efficacia di questo farmaco ( james e Burton, 2001), sono stati riportati ottimi risultati utilizzando un dosaggio di betaistina variabile da 288 a 480 mg/die: il numero degli attacchi acuti dopo 12 mesi di trattamento è apparso statisticamente minore rispetto ad un gruppo trattato con dosaggio più basso (Strupp et al., 2008; Lezius et al., 2011). Nel caso in cui vi sia associazione tra MdM ed emicrania potrebbe essere di aiuto l’utilizzo di vasoattivi della categoi ia dei calcio antagonisti ad azione antìistaminica (cinnarizina e flunarizina).
Anche gli steroidi vengono utilizzati nella terapia della fase intercritica della MCIM. Il loro uso si basa sostanzialmente sull’ipotesi allergica e/o autoimmune di questa patologia laddove essi agirebbero per la loro azione antinfiammatoria ed immunosoppressiva; inoltre, in vii tù del ritrovamento di recettori per i mineralcorticoidi nell’Ol, potrebbero entrare in gioco anche meccanismi di controllo dell’omeostasi idroelettroliti ca. Recentemente, l’utilizzo intratimpanico degli steroidi ha sostanzialmente sostituito l’uso orale del cortisone Un solo studio (Morales-Luckie et al,, 2005) ha paragonato l’efficacia dello steroide (prednisone 0.3.5 mg/kg/die per 18 settimane) in associazione con diuretici rispetto ad un gruppo di pazienti trattati solo con diuretici: i i isultati migliori nel controllo della vei tigine sono stati ottenuti nei soggetti trattati con cortisone. Nell’ambito dei trattamenti medici mci ira di essere inserita anche la terapia cosiddetta pn/se pì L’S511)’ attraverso l’utilizzo di uno strumento chiamato Meniett . Il i azionale si basa sull’ipotesi che variazioni della pressione esterna possono essere trasmesse alla perilinfa il cui incremento pressorio potrebbe comprimere il compai timento endolinfatico forzando il drenaggio dell’endolinfa verso il dotto ed il SE con miglioramento dell’idrope (Densert et al., 2000). Il Meniett , attraverso un tubo di ventilazione, applica all’orecchio medio variazioni pressorie che vengono trasferite all’Ol, anche se tale trasmissione e i relativi movimenti dei fluidi non sono mai stati documentati sperimentalmente. Secondo uno studio condotto in doppio cieco (Thomsen et al., 2005) nei pazienti trattati con Meniett si otterrebbe una riduzione della frequenza degli attacchi vertiginosi mentre non sono state trovate differenze per ciò che riguarda l’udito, l’acufene e l’autofonia.
Tabella 1-7 Categorie di farmaci utili nella fase acuta della malattia di Menière CTZ = ChemoreceptorTrigger Zone.
|
Classe |
Azione |
Farmaco |
Effetti Collaterali |
|
FENOTIAZINE |
Anticolinergici con attività sedativa ed antiemetica per azione su CTZ |
Prometazina anche azione antiistaminica Proclorpromazina con spiccata azione antiemetica Tietilpirazina con spiccata azione |
Effetti extrapiramidali |
|
ANTIISTAMINICI AD AZIONE ANTICOLINERGICA |
Forte inibizione centrale:marcati effetti su fenomeni neurovegetativi (nausea e vomito) |
Dimenidrinato Meclizina, ad azione Glaucoma |
Secchezza delle fauci |
|
BENZODIAZEPINE |
Effetto vestibular supressant Azione ansiolitica |
Disazepam |
Marcata sedazione Ritenzione urinaria Glaucoma |
|
ANTIDOPAMINERGICI |
|
Metoclopramide Levosulpiride azione selettiva su CTZ |
Effetti |
(scuola francese)
Il trattamento della malattia di Ménière dovrebbe avere quattro obiettivi:
· trattare la crisi;
· prevenire la comparsa di crisi successive;
· migliorare e/o preservare le funzioni cocleare e vestibolare;
· prevenire lo sviluppo della bilateralizzazione della malattia.
Al momento, le terapie conservative e chirurgiche hanno mostrato la loro efficacia solo sui primi due punti. D'altronde la letteratura internazionale offre un panorama alquanto confuso, che rende arduo stabilire il trattamento medico più efficace. Nessun'altra patologia vestibolare è stata in grado di suscitare un così imponente numero di articoli (circa 1.500 tra 1966 e 1996), fatto che testimonia la complessità del problema.
I pazienti devono essere istruiti sul modo di gestire le crisi e devono essere informati sull'evoluzione complessivamente benigna della malattia, con la comparsa di una remissione spontanea nella maggior parte dei casi o, quanto meno, con la riduzione del numero delle crisi dopo qualche anno.
Trattamento della crisi
Il trattamento della crisi è essenzialmente indirizzato contro la vertigine e prevede:
· Alcune misure generali che il paziente deve conoscere: sospensione di ogni attività, in particolare di quelle potenzialmente rischiose (guidare) fin dai prodromi (in particolare acufeni), sdraiarsi o sedersi per prevenire una caduta, riposo assoluto in ambiente calmo, isolato e nell'oscurità per tutta la durata della crisi;
· Evitare rapidi cambiamenti di posizione della testa, per non aggravare la vertigine;
· La somministrazione parenterale di sedativi, come diazepam (Valium®), 10 mg, dimenidrinato (Xamamina®), 50 mg. Le benzodiazepine determinano una potente azione depressiva vestibolare rinforzando l'inibizione cerebellare sui neuroni vestibolari;
· A questo sedativo si può associare un antistaminico, tipo prometazina, per la sua azione antiemetica e antivertiginosa (Farganesse®), 25 mg e/o un antiedemigeno sistemico cerebrale (solfato di magnesio al 15%, in iniezione endovenosa lenta);
· Nei rari casi in cui non si osserva miglioramento con questa strategia, si può tentare l'uso di neurolettici.
L'iniezione intramuscolare di un derivato dei butirrofenoni come il droperidolo (Sintodian®) 10 mg, si mostra generalmente efficace. I derivati delle fenotiazine, come la metopimazina (non disponibile in Italia) o la sulpiride (Dobren®), rivestono un certo interesse terapeutico, per la loro potente azione antiemetica. Alcuni Autori consigliano la somministrazione di un agente osmotico Il principio è identico a quello dei test osmotici. Il mannitolo trova così indicazione (500 ml al 10%, infuso in 2 ore, due volte al giorno durante le crisi vertiginose). Tra i molti altri farmaci consigliati, va ricordata la lidocaina (Xilocaina®) per via endovenosa, 1 mg/kg di soluzione all'1%, a dosi di 6 mg/min, che avrebbe una grande efficacia nei disturbi neurovegetativi per il suo effetto corticale. Infine, test calorici calibrati «ripetuti» durante il periodo intercritico sono stati proposti come «psicoterapia comportamentale», per i pazienti in cui le crisi di vertigine scatenano reazioni di panico.
Tutti questi farmaci ostacolano la pratica dei test vestibolari. D'altronde, queste norme devono essere seguite, alla scomparsa della crisi, da una terapia di fondo.
Trattamento di fondo
Il trattamento di fondo, prescritto durante le fasi intercritiche, mira a impedire o a ritardare l'insorgenza di una nuova crisi, a preservare l'udito residuo e a impedire la comparsa di un acufene invalidante. Il susseguirsi di varie teorie patogenetiche della malattia di Ménière ha suscitato lo sviluppo di un gran numero di protocolli. La molteplicità delle terapie rende conto della difficoltà di dimostrare l'efficacia di questa o quella strategia farmacologica.
LA DIETA NELLA MALATTIA DI’ MÉNIÈRE
S. GALLETTI
DA DIAGNOSI E TERAPIA DEI DISTURBI DELL’EQUILIBRIO,GIORGIO GUIDETTI ED. MARRAPESE 1997.
La malattia di Ménière costituisce una condizione patologica ad andamento cronico caratterizzata da ipoacusia. inizialmente fluttuante, acufeni, crisi vertiginose oggettive, con lunghi periodi di remissione della sintomatologia a seguito di cure mediche o anche spontaneamente.
Tale capriccioso decorso richiede di necessità una terapia medica continua per cercare di stabilizzare il periodo silente della malattia, ed evitare il lipetersi delle crisi vertiginose. Frequentemente però i pazienti vengono curati soltanto durante gli attacchi acuti della malattia
Tutti i dati istopatologici. semiologici e clinici permettono di concludere per l’esistenza di un idrope endolinfatico. anche se la patogenesi è tutt’oggi discussa .
L importanza dei fattori generali è indubbia, anche se difficilmente dimostrabile, per esempio
— il rapporto della malattia con turbe del ricambio idrosalino e dell’equilibrio acido-basico;
— il miglioramento della sintomatologia del paziente menierico sottoposto a dieta iposodica;
— il peggioramento delle crisi vertiginose in seguito all’assunzione di contraccettivi che determinano modificazione del
ricambio idrosalino.
La terapia medica di base consisterà nell’attuare la “deplezione” farmacologica del labirinto idropico mediante farmaci diuretici o vasoattivi (es:, glicerolo cv., urea) anche se tutti gli Autori concordano che sul piano pratico sono importanti non solo i provvedimenti farmacologici ma anche quelli dietetici finalizzati a correggere e prevenire l’alterazione idrosalina e a modificare sensibilmente l’intensità e la frequenza delle crisi .
È molto importante fornire al paziente all’atto della dimissione uno schema alimentare iposodico di riferimento, in quanto la generica raccomandazione di assumere pochi liquidi e di ridurre l’assunzione del sale si traduce praticamente in una grossolana semplificazione: la sola soppressione del sale aggiunto agli alimenti determina infatti un apporto medio giornaliero di sale pari a circa 2.1 g che è maggiore o equivalente a quello consentito dal regime iposodico “largo” (1 ,5 / 2
In Italia mediamente si consuma troppo sale:lO-15 g/die equivalenti a 4/6 g di sodio.
Ciò è molto più del necessario in quanto secondo i dettami della moderna scienza dell’alimentazione i ricercatori stimano che 4/6 g di sale al giorno siano il valore massimo accettabile (1.6/2.5 di sodio)(13).
Da dove proviene l’eccesso di sodio che ingeriamo?
Si possono individuare quattro fonti di assunzione di sodio:
— una modesta quota di sodio è assunta per mezzo di cibi che naturalmente lo contengono; il sodio è maggiormente concentrato nei cibi animali che non nei cibi vegetali (Prosciutto crudo 1.2 g/hg - Prosciutto cotto 0.5 g/hg - Formagni 2-3 mg/hg - Latte 1.25 mg/Lt);
— una rilevante quota di sodio è assunta con il sale aggiunto agli alimenti nel corso delle trasformazioni industriali (per ragioni di conservazione di gusto, e tecnologiche sottoforma di sali diversi da cloruro di sodio):
— in cucina, durante la cottura si aggiunge ai cibi una considerevole dose di sale;
— a tavola si aggiunge una ulteriore quota di sale
Esistono inoltre apporti di sodio “dissimulati”: occorre ricordare che nei cibi preconfezionati oltre al sale vengono utilizzati molti composti ricchi di sodio in particolare bicarbonato, propionato e arginato di sodio presenti nel cioccolato, nei gelati, in alcune bibite a base di latte. nei biscotti e sodio nitrato e monosodio glutammato (contenuti nei dadi per brodo).
Un’attenzione particolare è rivolta all’acqua e a determinati farmaci:
— il contenuto di sodio in quella potabile è molto variabile quella trattata con agenti anticalcarei per renderla meno “dura” è spesso ricca di sodio perché due atomi di Na+ rimpiazzano ciascun atomo di e Mg durante lo scambio;
— alcuni farmaci, come per esempio i salicilati. bicarbonati e sostanze alcalinizzanti in genere. sulfamidici e benzoati. possono contenere una notevole quantità di sodio.
Da quanto brevemente discusso risulta l’opportunità di attuare un controllo del sodio introdotto con la dieta:
1) scegliendo cibi più ricchi in K (cibi di origine vegetale) che hanno un rapporto NaIK ottimale. cioè < I (Nella nostra alimentazione il rapporto globale Na/K volge a favore del Na).
Il rapporto Na/K si inverte drasticarnente negli alimenti che hanno subito trasformazioni (pane, formaggi, insaccati,
tonno sott’olio);
2) riducendo l’uso di cibi preconfezionati;
3) abolendo l’uso del sale da cucina (usando sale iposodico);
4) aumentando il rapporto P/S (l’acido linoleico. un AGE e precursore delle prostaglandine ad azione vaso-dilatatoria e/o natriuretica;
5) aumentando l’assunzione della fibra alimentare oltre ad avere un effetto sul transito intestinale viene regolato attraverso l’attività degli ormoni gastro-intestinali il tasso di insulina sierica, cui può essere attribuita un’azione natriuretica.
Esistono tre tipi di regime iposodico:
— largo (1000-2000 mg)
— relativo (400-1000 mg)
— stretto (250-400 mg).
Per consentire al malato di attuare un regime alimentare realmente iposodico ed efficace. sono state calcolate 3 diete riferite al regime iposodico relativo, raggiungendo una razione media giornaliera pari a circa 600 mg Na.
Le diete sono state concepite prendendo come riferimento le esigenze metaboliche di un soggetto tipo di sesso maschile e femminile. di media età. in condizione di normopeso e svolgenti una modesta attività fisica (2500-2000 Kcal rispettivamente).
La dieta di 1700 Kcal è stata concepita invece per pazienti anziani o in sovrappeso corporeo. Tale schematismo dovuto, dovuto ad una necessaria generalizzazione dei modelli di riferimento rimane comunque adattabile ai singoli soggetti conformemente alle diverse necessità metaboliche. tenendo conto, nel calcolo del fabbisogno energetico giornaliero. dell’età, del peso. dell’altezza e dell’attività fisica,
Tab. 11- Menù a regime iposodico relativo,
COMPOSIZIONE BROMATOLOGICA
|
2500 Kcal |
2000 Kcal |
1700 Kcal |
|
P=14.4% |
P=15,8% |
P=17% |
|
COLAZIONE |
|
|
COLAZIONE
|
Calorie |
|
2500 |
2000 |
1700 |
|
1) Latte fresco (3v./sett.) |
gr |
200 |
200 |
200 |
|
The |
gr |
200 |
200 |
200 |
|
Yogurt magro |
gr |
180 |
180 |
180 |
|
2) Fette biscottate integr |
gr |
40 |
40 |
40 |
|
Burro non salato |
gr |
10 |
10 |
10 |
|
Marmellata (casalinga) |
gr |
10 |
10 |
10 |
|
o Biscotti secchi |
gr |
50 |
50 |
50 |
|
o Fiocchi cereali |
gr |
40 |
40 |
40 |
|
o Miscela di cereali e frutta secca |
gr |
30 |
30 |
30 |
|
SPUNTINO |
|
|
|
|
|
Frutta fresca di stagione |
gr |
200 |
|
|
PRANZO
|
|
|
2500 |
2000 |
17000 |
|
1) Pane toscano o pane specifico iposodico |
|
80 |
60 |
50 |
|
2) Minestra asciutta pomod./basilico o con ragù di carne o con verdure o legumi (es. Pasta e fagioli. Riso e Piselli ecc,) scegliendo tra Pasta semola grano duro (Spaghetti. Maccheroni, ecc.). |
gr |
100 |
80 |
70 |
|
Riso |
gr |
100 |
80 |
70 |
|
Gnocchi di patate( max 1 v./sett). |
gr |
250 |
220 |
180 |
|
Farina di mais (Polenta) è concesso salare l’acqua di bollitura con sale iposodico (sale dietetico: davasal, ecc.) |
gr |
100 |
80 |
70 |
|
Minestrone di verdura senza dado né grassi con pasta o riso |
gr |
30 |
30 |
30 |
|
3) Legumi lessi o in umido con pomod. o con altre verdure scegliendo tra: Fagioli freschi o surg. |
gr |
200 |
200 |
200 |
|
Fagioli secchi |
gr |
70 |
70 |
70 |
|
Piselli freschi o surg |
gr |
200 |
200 |
200 |
|
Piselli secchi |
gr |
70 |
70 |
70 |
|
Lenticchie |
gr |
70 |
70 |
70 |
|
Ceci |
gr |
70 |
70 |
70 |
|
4) Verdura cruda o cotta (pesata cruda al netto degli scarti) scegliendo tra: bietole, broccoli, cavolo, carciofi, carote, cavolfiore, porri,cetriolo, cipolle, fagiolini, finocchio, funghi freschi, lattuga, melanzane, pomodori, peperoni, radicchio, scarola, sedano, spinaci, zucca, zucchini, cicoria, rapanelli, indivia, rape. |
gr |
200 |
200 |
200 |
|
5) Condimenti: Olio di oliva |
gr |
25 |
20 |
15 |
|
Formaggio grana gratt. |
gr |
5 |
5 |
5 |
|
6) Frutta fresca di stagione scegliendo tra: albicocche, ananas, fragole, ciliege, mandarini, pere, pesche, pompelmo, prugne, lamponi, amarene, |
gr |
150 |
150 |
150 |
|
Oppure scegliendo tra: uva, banane, cachi, fichi. |
gr |
100 |
100 |
100 |
|
7) Condimenti: Olio di oliva. |
gr |
25 |
20 |
15 |
|
Formaggio grana gratt. |
gr |
5 |
5 |
5 |
|
8) Bevande: acqua minerale |
gr |
200 |
200 |
200 |
|
Vino NB.: Un bicchiere da tavola =200 gr |
gr |
200 |
100 |
70 |
CENA
|
1) Antipasto di verdure (ved. pranzo) |
gr |
200 |
200 |
200 |
|
2) Carne magra privata della parte glassa visibile Scegliendo tra: Maiale. manzo. pollo. coniglio, tacchino, agnello. vitellone) (Non più di 3 v/sett,) Oppure |
gr |
140 |
140 |
140 |
|
Pesce fresco surg. garantito (cioè non sbiancato in acqua salata, imparare a leggere l’etichetta di composizione degli alimenti!) Scegliendo tra: Sogliola, nasello, spigola, rombo, Oppure |
gr |
240 |
240 |
240 |
|
Formaggio (1 v/sett) Scegliendo tra: ricotta, mozzarella, stracchino, emmenthal, Bel Paese, certosino |
gr |
100 |
100 |
100 |
|
Oppure 1 Uovo (1 v/sett) |
gr |
70 |
70 |
70 |
|
3) Pane toscano o pane specifico iposodico |
gr |
120 |
90 |
70 |
|
4) Frutta fresca (vedi pranzo) |
|
|
|
|
|
5) Olio |
gr |
25 |
20 |
15 |
|
6) Vino |
gr |
200 |
200 |
200 |
|
7) Acqua |
gr |
200 |
200 |
200 |
|
CIBI CONSENTITI
|
CIBI VIETATI
|
|
Per il mantenimento di un regime iposodico relativo vengono consentiti gli alimenti con un contenuto in sodio inferiore a 10 mg/hg di alimento - pane senza sale - pane azimo - biscotti senza sale - latte e yogurt senza sale - farina e fecola - riso, pasta di semola. semolino e tapioca - dolce al latte iposodico senza lievito - succhi di frutta ftti in casa - frutta fresca - castagne - olio, burro e maionese con moderazione - aceto - sale senza NaCI - aglio, cipolla - aromi e spezie
|
Per il mantenimento di un regime iposodico relativo, è necessario scartare gli alimenti con un contenuto in sodio maggiore o uguale a 70 mg/hg di alimento - sale da cucina e da tavola - dadi per brodo - carne e pesci affumicati o essiccati - insaccati e salumi - frutti di mare - caviale - frattaglie - purè di patate istantaneo - formaggi - patatine fritte - pane bianco - latte in polvere - surgelati sbiancati in acqua salata - olive e capperi. ecc, - cacao e cioccolata al latte
|
Bibliografia
1) Angelborg C.. Klockhoff I.. Stahle J. Serum osmolarity in patient with Ménière’s disease, Acta otolaryngol. 76. 450. 1973
2) Celestino D.. lannetti G. Ménière’s disease and plasmatic hyperosmolarity J. Laryngol. Otol. 87 229, 1973.
3) Celestino D . Cerulli N . lannetti G.. Sagliaschi G, Acid-Base equilibrium in Ménière disease J. Laryngol. Otol. 90. 263, 1976.
4) Celestino D . Ralli G.. Plasmatic osmolaritv in Ménière’s disease, 95. 273. 1981
5) Creff A.F. Manual de diétetique Masson 1987
6) De Vincentiis I. Bozi L. Pizzichetta V. Sulla terapia medica di alcune gravi ipoacusie. Il Valsava. 40. 69. 79. 1964.
7) De Vincentiis I.. Ralli G,: Nuovi orientamenti sulla patogenesi e terapia della malattia di Ménière Attualità in otorinolaringoiatria. Edizioni Scientifiche Valeas. 105. 1980
8) De Vincentiis I . Ralli G,: Trattamento medico Tavola rotonda “Revisione critica della malattia di Ménière” Acta Otorhinol. Ital.. 5,317. 1985.
9) Fustenberg A. C., Lashmet F.H., lathrop F. : Ménière’s symptom complex: medical treatment. Ann. Otol., 43. 1035. 1934.
10) Griffith H. W. Guida completa alle vitamine, minerali e integratori alimentari. EDRA. 1993
11) Jackson C.G . Celestino D.. Meli. Studio dell’equilibrio acido-base nella malattia di Ménière Acta Otorhinol. Ital., 2. 19. 1982,
12) Ralli G.. Celestino D . Fabbricatore M.. Gabini S.. Taverniti L.: Effetto dell’acetazolamide sulla malattia di Ménière Acta Otorhinol. Ital.. 9. 503. 1989
13) Rapelli S.: Principi per una corretta alimentazione. SOHN. 1990
14) Weille F.L. , Microcirculation and fluid physiology of the inner ear correlated with Ménière’s disease.
Laryngoscope. 77. 2063. 1967.
Regole dietetiche e trattamenti farmacologici
I programmi dietetici, inclusa la restrizione dell'apporto di sale, acqua, alcol, nicotina, caffeina sono poco efficaci così come l'esercizio fisico, la pratica di evitare le basse temperature, la permanenza in camere ipobariche. L'anestesia del ganglio stellato, i diuretici, i farmaci vasoattivi sono stati raccomandati in base all'ipotesi secondo cui era possibile diminuire l'IE modulando il flusso sanguigno nell'orecchio interno. La terapia farmacologica dell'ansia è consigliata da numerosi Autori; in questo caso il panorama terapeutico è ampiamente dominato dalle benzodiazepine (Valium®, Transene®, Frisium®, ecc.), ma buoni risultati possono essere ottenuti anche con i barbiturici a basse dosi che, in assenza di controindicazioni respiratorie o epatiche sono utili per il loro effetto moderatamente sedativo. L'idrossizina (Atarax®), alla posologia di 300-400 mg, è molto ben tollerata ed efficace nel corso della crisi vertiginosa. I betabloccanti (Sectral® o Inderal®) hanno una notevole azione ansiolitica e sono indicati se il malato riferisce cefalea o emicrania. La somministrazione di antidepressivi sedativi trova in questo caso un'eccellente indicazione. L'amitriptilina (Laroxyl®), la mianserina (Lantanon®) possono essere prescritte alla sera, con posologia ridotta. Infine, si può anche impiegare un neurolettico o il litio. Tutti gli schemi terapeutici hanno subito l'andamento delle mode, ma tranne che per i diuretici e la betaistina, la loro efficacia non è mai stata dimostrata.
Nel 1977, Torok studiò 834 articoli medici pubblicati nel corso di 25 anni; egli concluse che l'efficacia della terapia medica sulla malattia di Ménière andava dal 60 all'80%. Nel 1991, Ruckenstein et al andarono più lontano, concludendo che tutti questi pazienti avevano in realtà beneficiato per la maggior parte del tempo di un effetto placebo.
Secondo una recente revisione della letteratura (Claes J, 1997) solo i diuretici (Petermann W, 1982) e la betaistina hanno dimostrato con studi in doppio cieco la loro efficacia sul controllo della vertigine. Ciononostante, nessun trattamento si è dimostrato veramente efficace sull'ipoacusia e sull'evoluzione a lungo termine della malattia:
· I diuretici a dosi scalari, idroclorotiazide (Esidrex®), associati alla dieta iposodica, sono stati raccomandati per il trattamento a lungo termine della malattia di Ménière. Una tale associazione terapeutica agirebbe attraverso una deplezione sistemica d'acqua o direttamente sulla omeostasi dei liquidi labirintici;
· La betaistina dicloridato (Microser®) è stata raccomandata come trattamento di prima scelta della sindrome di Ménière (Chüden HG , 1978 ; Le Père DM, 1967)poiché, supponendo che l'idrope risulti da uno spasmo degli sfinteri precapillari della stria vascolare, questo spasmo potrebbe essere risolto dall'istamina prodotta in loco mediante una decarbossilazione dell'istidina. Uno studio prospettico in doppio cieco ha concluso che questo trattamento era preferibile ad ogni altro farmaco e al placebo (Oosterveld WJ ,1984) efficacia riscontrata anche nello studio di Meyer(1985). Per prevenire le crisi, la betaistina deve essere somministrata per 6-12 mesi. Al contrario, gli antistaminici anti-H1, come il dimenidrato (Xamamina®) o la difenidramina (Difenidramina cloridridrato®), attenuerebbero gli stimoli labirintici.
· Di recente La Laser Terapia a basso livello energetico è stata impiegata con successo nel trattamento di patologie di tipo infettivo, ischemico (da difetto di irrorazione sanguigna), ipossico (da difetto di ossigenazione) ed infiammatorio-autoimmunitario , quindi non solo nella cura dell’acufene cronico ma anche nella riduzione di intensità e frequenza delle vertigini in pazienti affetti da sindromi vertiginose e da Malattia di Meniere.
· La protesizzazione acustica è indicata se permane un deficit uditivo. Se il paziente lamenta disequilibrio o oscillopsia a causa del deficit labirintico è molto importante eseguire dei cicli di riabilitazione vestibolare che è l’unica terapia in grado di ricompensare tale deficit.
terapie intratimpaniche conservative (steroidi) e ablative (gentamicina);
Labirintectomia chimica
La «labirintectomia funzionale» con l'impiego di aminoglicosidi (gentamicina o streptomicina), è stata proposta da Schuknecht fin dal 1957 Essa era basata sugli effetti ototossici degli aminoglicosidi e sull'affinità preferenziale di alcuni di essi per il vestibolo. Schuknecht trattò otto pazienti con streptomicina. Cinque di essi presentarono la scomparsa delle crisi vertiginose, ma tutti persero la funzione uditiva. Silverstein pers guì questo metodo successivamente, la streptomicina non è più stata utilizzata. Dalla fine degli anni Settanta, numerosi Autori hanno utilizzato instillatori locali di gentamicina per via transtimpanica secondo vari protocolli. La gentamicina è risultata più aggressiva nei confronti delle cellule ciliate vestibolari piuttosto che nei confronti delle cellule ciliate cocleari Inoltre, numerosi studi su animali hanno mostrato un'elettiva tossicità degli aminoglicosidi sulle cellule scure della stria vascolare, presunti produttori di endolinfa, cosa che potrebbe indurre una diminuzione del volume endolinfatico e quindi dell'idrope Secondo alcuni Autori il riscontro di un miglioramento delle vertigini, persino dell'udito, prima della scomparsa della funzione vestibolare alle prove caloriche, ha fatto evocare la possibilità di un interessamento primario delle cellule secernenti endolinfa, che precede la distruzione delle cellule sensoriali. Così, l'idrope verrebbe alleviata prima della comparsa di danni a carico della funzione sensitiva vestibolare e dell'instaurarsi, in compenso della scomparsa delle vertigini, di atassia e oscillopsie particolarmente invalidanti. Giocando sulle dosi e le modalità di somministrazione, si può quindi teoricamente trasformare un trattamento potenzialmente degenerativo in una terapia eziopatogenetica.
In pratica, la letteratura raccomanda la gentamicina per uso locale. Essa venne inizialmente impiegata in Europa come solfato di gentamicina (Gentalyn®), instillato quotidianamente per mezzo di un tubo di plastica inserito dietro l'anulus fibroso, attraverso un accesso transmeatale [108]
Le instillazioni venivano sospese quando l'audiometria o il nistagmo indicavano un inizio di deafferentazione cocleovestibolare. In seguito, le indicazioni e le tecniche del trattamento locale con gentamicina sono cambiate, specialmente da quando si è osservato che l'ototossicità, rispetto all'instillazione del farmaco, compariva in ritardo di alcuni giorni fino a una settimana dopo Le instillazioni transtimpaniche di aminoglicosidi permettono il trattamento isolato di un solo orecchio, senza effetti sistemici. Il farmaco raggiunge l'orecchio interno attraverso la finestra cocleare e, inoltre, secondariamente, attraverso il legamento anulare, per via ematica, linfatica o attraverso lacune ossee
L'ipotesi di una tossicità a step della gentamicina è stata confermata dalla constatazione che il deficit vestibolare era reversibile a uno stadio precoce, mentre diventava irreversibile a uno stadio tardivo
La somministrazione di gentamicina in quantità eccessive può quindi causare effetti indesiderati e non necessari a livello dei recettori dell'orecchio interno, in particolare delle cellule ciliate cocleari. La somministrazione di basse dosi, che possono anche non attenuare le risposte caloriche dell'orecchio trattato, si è rivelata efficace ed è pertanto attualmente raccomandata da alcuni come procedura standard
Le indicazioni alla somministrazione di gentamicina per via transtimpanica sono le seguenti:
· Evoluzione resistente al trattamento medico, con frequenti crisi vertiginose o cadute improvvise che continuano da oltre 6 mesi;
· Persistenza delle crisi nonostante la neurotomia vestibolare (che può essere dovuta ad anomalie anatomiche)
Con questa tecnica si corre il rischio di alterare la funzione uditiva, per questo, alcuni la riservano solo a casi in cui la perdita uditiva media è superiore ai 60 dB. Tuttavia, alcuni Autori la somministrano anche in pazienti con ipoacusia moderata, a condizione che la funzione uditiva dell'orecchio controlaterale sia normale [126]
Le manifestazioni bilaterali della sindrome di Ménière sono una controindicazione relativa al trattamento ototossico.
Non esiste consenso unanime sulla concentrazione ottimale, il dosaggio per seduta, il numero di instillazioni, la frequenza delle sedute e il dosaggio totale da somministrare. Concentrazioni di gentamicina non superiori a 30 mg/ml sono state usate nella maggior parte delle casistiche
Due o tre instillazioni consecutive si sono mostrate efficaci e con meno effetti collaterali, come la sordità, rispetto a quattro instillazioni o più Un'iniezione settimanale è raccomandata per gestire al meglio gli effetti ototossici tardivi; da 1 a 2 ml, di una concentrazione inferiore a 30 mg/ml sono così instillati attraverso il timpano per paracentesi, con una seconda incisione utile a richiamare aria.
Circa il 15% dei pazienti portatori di una deafferentazione vestibolare unilaterale presentano sintomi di insufficienza vestibolare cronica come oscillopsie durante i movimenti del capo e instabilità negli spostamenti. Ciò può essere attribuito a un'alterata funzione vestibolare nel labirinto ritenuto sano o a una compensazione centrale imprecisa durante i movimenti rapidi della testa
![]()
Farmaci comunemente utilizzati per un attacco acuto sono i seguenti:
· Meclizine (Antivert), chewable (Bonine). Meclizine (Antivert), masticabili (Bonine). Dose ranges from 12.5 twice/day to 50 mg three times/day. Dose varia da 12,5 due volte al di, a 50 mg tre volte al di.
· Lorazepam (Ativan) 0.5 mg. Lorazepam (Ativan) 0,5 mg. Usual dose is twice/day or both at the same time at onset.This medication is effective even if it is not swallowed (ie you can just suck on it). Dose abituale è di due volte al di o di 2 compresse contemporaneamente.questo farmaco è efficace anche se non è ingerito (cioè si può scioglere in bocca). Tiredness is expected. Può determinare stanchezza .
· Phenergan, orally (12.5) or rectal suppository (25 mg). Phenergan, per via orale (12,5) o con supposta per via rettale (25 mg). Usual dose is once every 12 hours as needed for vomiting. Viene utilizzato contro il vomito, la dose abituale è di una volta ogni 12 ore.
· Compazine (orally or suppository). Compazine (per via orale o rettale). Usual dose is 5-10 mg every 12 hours as needed for vomiting. La dose abituale è di 5-10 mg ogni 12 ore sempre per il vomito.
· Ondansetron (orally or sublingual). Ondansetron (per via orale o sublinguale). Usual dose is 8mg q 12 hrs for vomiting. Dose abituale è di 8 mg ogni 12 ore per il vomito. (this medication, sold by Glaxo, is ). (Questo farmaco, venduto dalla Glaxo, è molto costoso). Although Ondansetron isn't very strong, and doesn't always work, it also doesn't have much side effects either. Anche se Ondansetron non è molto forte, e non sempre funziona, non ha molti effetti collaterali. One can certainly work and drive after taking nearly any dose of ondansetron. Si può sicuramente lavorare e guidare dopo aver preso questo farmaco(Ondansetron). The same cannot always be said for meclizine, lorazepam and klonazepam. Lo stesso non si può sempre dire per glia altri farmaci(meclizina, lorazepam e klonazepam).
· Decadron (dexamethasone) 4 mg orally for 4-7 days. Decadron (desametasone) 4 mg per os per 4-7 giorni. Or a "medrol dose pack" This convenient, rapid, but not very effective treatment is gradually being replaced by steroid injections through the ear drum. O un "pacco dose di Medrol" Questo trattamento comodo, rapido, ma non molto efficace viene progressivamente sostituito da iniezioni di steroidi attraverso il timpano. It is usually an "add-on" at the time of a physicians visit for persistent symptoms (see flow chart above). Di solito è un farmaco "add-on" ,che viene somministrato al momento di una visita medica quando i sintomi sono persistenti (vedi diagramma sopra).
Additional information about is found here. Ulteriori indicazioni sulla prevenzione del vomito si trova qui.
During an acute attack, lay down on a firm surface.Durante un attacco acuto, bisogna sdraiarsi su una superficie solida. Stay as motionless as possible, with your eyes open and fixed on a stationary object. Stare immobile il più possibile, con gli occhi aperti e fissi su un oggetto fisso. Do not try to drink or sip water immediately, as you'd be very likely to vomit. Non cercare di bere acqua o sorseggiare immediatamente, come sarà molto probabilmente che si vomiti. Stay like this until the severe vertigo (spinning) passes, then get up SLOWLY. Bisogna rimanere così fino a quando le vertigine gravi (spinning) scompaiono, poi bisogna alzarsi lentamente. After the attack subsides, you'll probably feel very tired and need to sleep for several hours. Dopo che l'attacco è passato, probabilmente ci si sentirà molto stanchi e sarà necessario dormire per diverse ore.
If vomiting persists and you are unable to take fluids for longer than 24 hours (12 hours for children), contact your doctor.Se il vomito persiste e non si riesce ad assumere liquidi per più di 24 ore (12 ore per i bambini), contattare il medico. He can prescribe nausea medication, and/or vestibular suppressant medication. Egli può prescrivere farmaci contro la nausea e / o farmaci inibitori dell'attività vestibolare . He/she may wish to see you or even admit you to the hospital if you are dehydrated. Lui / lei può desiderare di vederti o persino farti ricoverare in ospedale se si è disidratati . Sono comunemente usati farmaci inibenti l'attività vestibolare(vestibular suppressant medications) come:Meclizine (Antivert), Lorazepam and Clonazepam are commonly used s and Compazine, Phenergan or Ondansetron are commonly used . Meclizine (Antivert), Lorazepam e per la nausea sono comunemente usati:In our practice in Chicago, we commonly provide an "emergency kit", consisting of a small prescription of lorazepam and ondansetron, to be taken sublingually for an acute attack..Clonazepam e Compazine, Phenergan o Ondansetron Nella pratica , si può comunemente fornire un "kit di emergenza", costituito da una piccola ricetta di lorazepam e ondansetron, da prendere per via sublinguale per un attacco acuto.
Diuretici - tutti quelli di uso comune tendono ad essere gli inibitori dell'anidrasi carbonica, o combinazioni, per ragioni che non sono del tutto chiare. Questi farmaci hanno il vantaggio che essi non possono esigere supplementazione di potassio.
In the United States, Dyazide (triamterine/HCTZ) is prescribed almost universally.Negli Stati Uniti,il Dyazide (triamterine / idroclorotiazide) è prescritto quasi universalmente. Maxide is used when a smaller dose than found in Dyazide is needed (it is scored). Maxide viene utilizzato quando è necessario (è prescritta)Van Deelen and Huizing studied the use of diuretics in Meniere's disease in a double-blind, placebo controlled trial, and reported that it reduces vestibular complaints, but has no significant effect on hearing (1986). una dose inferiore alla Dyazide. Van Deelen e Huizing hanno studiato l'uso di diuretici nella malattia di Meniere in uno studio in doppio cieco, controllato con placebo, ed hanno riferito che riduce i disturbi vestibolari, ma non ha alcun effetto significativo sulla funzionalità uditiva (1986). Thirlwall and S. Kundu (2006) were unable to come to a conclusion as to efficacy as no papers published up to 2006 were adequate for meta-analysis. Thirlwall e S. Kundu (2006) non sono stati in grado di arrivare ad una conclusione in merito alla efficacia in quanto i documenti pubblicati fino al 2006 erano inadeguati per la metanalisi. Our observations are that about 1/3 of Meniere's patients report a good response, and the remaining aren't sure whether it is doing them any good at all. Le nostre osservazioni sono che: circa 1 / 3 dei pazienti con Meniere segnalare una buona risposta, e per i rimanenti non si è sicuri che il diuretico sia utile per tutti.
Notes: as triamterine is a folate antagonist, pregnant women should take folate supplements if not otherwise contraindicated.Note: siccome il triamterine è un antagonista dei folati, le donne incinta dovrebbero assumere integratori di acido folico, se non altrimenti controindicata. Occasionally persons on long-term acetazolamide develop kidney stones. Ogni tanto le persone che utilizzano a lungo termine acetazolamide possono sviluppare calcoli renali. All of the above have sulfa in them, which persons with sulfa allergies may be unable to tolerate. Tutti i farmaci sopra riportati hanno sulfamidici , che i pazienti con allergie ai sulfamidici non sono in grado di tollerare.
Tutto ciò ha sulfamidici in loro, che le persone con allergie sulfamidici possono non essere in grado di tollerare. In questa situazione, si può provare a amiloride di per sé, o furosemide (Lasix). Laxix deve essere somministrato a basse dosi e con cautela, perché è leggermente ototossici stessa.
Diuretics that do not contain sulfa (Ponka, 2006): Diuretici che non contengono sulfamidici(Ponka, 2006):
When there is sulfa allergy, one may try amiloride by itself, or ethacrinic acid (edecrin). Quando c'è allergia ai sulfamidici, si può tentare di utilizzare da solo l’amiloride, o l’acido etacrinico (edecrin). Loop diuretics such as Edecrin should be used in low doses and with caution because they are ototoxic. I diuretici dell'ansa comel’ Edecrin deve essere usato in basse dosi e con cautela, perché sono ototossici. Note that the diuretics listed are mainly ones that increase serum potassium. Si noti che i diuretici elencati sono principalmente quelle che aumentano il potassio sierico. (Ponka, 2006). (Ponka, 2006).
Vestibular Suppressants ( ) Soppressori vestibolari ( clicca qui per maggiori dettagli su trattamenti farmacologici )
Steroids (commonly for severe bouts) Steroidi (comunemente per gli attacchi gravi)
Immune suppressants (rarely, see ) Gli immunosoppressori (raramente, vedere AIED )
farmaci che sono controversi secondo gli americani
Questo è il modo in cui si cerca di prevenire gli attacchi di Meniere al Chicago Dizziness and Hearing:
The purpose of treatment between attacks is to prevent or reduce the number of episodes, and to decrease the chances of further hearing loss and damage to the vestibular system. Lo scopo di trattamento tra gli attacchi è quello di prevenire o ridurre il numero di episodi, e per diminuire le probabilità di perdita dell'udito ulteriori e danni al sistema vestibolare. A permanent (ringing in the ears), constant imbalance, or a progressive hearing loss may be the consequence of long-term Meniere's disease. may be necessary. Un acufene permanente (fischi nelle orecchie), squilibrio costante o una perdita dell'udito progressiva può essere la conseguenza di una lunga malattia a termine di Meniere. Protesi acustiche)possono essere necessarie.
Standard medical treatments: cure mediche standard :
Trattamenti non standard :
Verapamil (typical dose: 120 SR) sometimes reduces the frequency of attacks. Verapamil (tipico dosi: 120 SR) riduce a volte la frequenza degli attacchi. Nimodipine and Flunarizine have also been used.Not so standard treatments Nimodipina e flunarizina sono stati utilizzati. These medications are all calcium channel blockers. Questi farmaci sono tutti calcio antagonisti. The evidence is not as good that these medications work. Non vi è una chiara evidenza di questi farmaci funzionino.Because Menieres and Migraine are very often combined, this medication's main role may be to treat the that can be confused with or accompany Menieres disease.
Poiché la malattia di Ménière e l’emicrania sono spesso combinati, il ruolo principale di questo farmaco potrebbe essere quella di trattare le vertigini associate all'emicrania Vertigine emicranica, che può essere confusa o accompagnare la malattia di Ménière. Utilizzare This medication is especially logical if the dizzy attacks are associated with headaches. questo farmaco è particolarmente logico se gli attacchi vertigini sono associate a mal di testa.
Some physicians prescribe Histamine injections.Alcuni medici prescrivono iniezioni di istamina. Most physicians in the US, however, consider this treatment to be ineffective. La maggior parte dei medici negli Stati Uniti, tuttavia, considera questo trattamento inefficace
Prednisone o altri steroidi (Decadron per esempio) sono a volte utili con somministrazioni brevi Potrebbero essere utilizzate più spesso se si vuole effettuare un un trattamento distruttivo. We would most often use these when considering a destructive treatment.
![]()
· There are a number of that do not have much of a track record that can be tried under the supervision of your doctor.
· Ci sono una serie di nuovi farmaci ,)che possono essere provato sotto la supervisione del medico. There also some which are either considered "alternative" or which are available only outside the US which might be worth considering. Ci sono anche alcuni farmaci insoliti che possono essere considerati "alternativi" (o che sono disponibili solo al di fuori degli Stati Uniti e potrebbe essere opportuno prenderli in considerazione.
Ciò che l' autore Dr. Timothy Hain suggerisce nella sua pratica per la prevenzione medica di Meniere. Questi farmaci vengono somministrati per la maggior parte dei suoi pazienti, in genere nel seguente ordine:
These are combined with symptomatic drugs such as meclizine, benzodiazepines, and antiemetics, to be taken during attacks.Questi farmaci sono combinati con farmaci sintomatici come la meclizina, benzodiazepine ed antiemetici, da assumere durante gli attacchi.
In persons with severe progressive bilateral disease, the author will generally recommend a trial of high dose steroids. Nelle persone con grave progressione della malattia bilaterale, l'autore consiglia generalmente un processo di steroidi ad alto dosaggio. If there is a significant improvement in hearing, then there is an attempt to switch to Enbrel, with the thought that in this situation an is more probable. Se vi è un significativo miglioramento dell'udito, poi c'è un tentativo di passare all’ Enbrel, con lil presupposto che in questa situazione è più probabile un disordine autoimmune . Of course this strategy should rationally be adjusted to the variability in hearing, as in any undertaking, one's confidence that a particular result has been obtained depends both on the size of the effect as well as the underlying variability in the effect. Naturalmente questa strategia dovrebbe essere regolata razionalmente per la variabilità della funzione uditiva, come in ogni impresa, la fiducia che un determinato risultato è stato ottenuto dipende sia dalla dimensione degli effetti così come la variabilità degli effetti che ne derivano. Much room for improvement in these algorithms is needed -perhaps involving daily hearing monitoring using an internet protocol. Molto spazio di miglioramento in questi algoritmi è necessario, magari coinvolgendo il monitoraggio quotidiano dell’udito utilizzando un protocollo internet.
In persons who do not respond to medical management, we move on to (see flowchart and ), and then definitive destructive treatment. Nelle persone che non rispondono alla terapia medica, si passa a basse dosi di gentamicina (vedi diagramma di flusso e "come ultima istanza" ), ed alla fine il trattamento distruttivo.
An emerging treatment that may eventually end up as a standard treatment is multiple injections of steroids into the middle ear. Un trattamento emergente che può diventare a sua volta un trattamento standard è l’iniezione multipla di steroidi nell'orecchio medio. We have encountered individuals who have had as many as 40 of these injections. Abbiamo incontrato persone che hanno avuto ben 40 di queste iniezioni. There is intrinsic risk of TM perforation and infection. Vi è il rischio intrinseco di perforazione della TM e infezioni
Riferimenti:
· Adunka, O., Moustaklis E., et al. (2003). "Anestesia Labirinto - un'opzione di trattamento dimenticato ma pratico nella malattia di Meniere." ORL J Otorhinolaryngol Relat Spec 65 (2): 84-90.
· Bretlau P, J Thomsen, Tos M e NJ Johnsen (1982). "L'effetto placebo in chirurgia per la malattia di Meniere. Un doppio cieco controllato con placebo sulla chirurgia shunt sacco endolinfatico." Adv Otorhinolaryngol 28: 139-46.
· Bretlau P, J Thomsen, Tos M e NJ Johnsen (1984). "L'effetto placebo in chirurgia per la malattia di Meniere:. Tre anni di follow-up dei pazienti in uno studio in doppio cieco controllati verso placebo sulla chirurgia shunt sacco endolinfatico" Am J Otol 5 (6): 558-61.
· Bretlau P, J Thomsen, Tos M e NJ Johnsen (1989). "L'effetto placebo in chirurgia per la malattia di Meniere: nove anni di follow-up." Am J Otol 10 (4): 259-61.
· Doyle, KJ, C. Bauch, R. Battista, et al. (2004). "Trattamento Intratympanic steroidi: una rassegna". Otol Neurotol 25 (6): 1034-9.
· Blakely, Am J Otol, 18:04, 1997
· Gates GA e altri. Gli effetti del trattamento micropressure transtympanic nelle persone con malattia di Meniere unilaterale. Arch. Otol HNS 2004:130; 718-725
· Hargunani e altri. Iniezione Intratympanic di dexamethoasone: durata di distrubuzione dell'orecchio interno e la conversione nella sua forma attiva. Otol Neurotol 27:564-569, 2006
· Kim HH, Wiet RJ, Battista RA. Tendenze nella diagnosi e nella gestione della malattia di Meniere: risultati di un'indagine Otolaryngol Testa Collo Surg 2005 maggio, 132 (5) :722-6...
· Rask-Andersen et al. Effetti di iniezione intratympanic di latanoprost nella malattia di Meniere: uno studio randomizzato controllato con placebo, in doppio cieco, studio pilota. Otol HNS 2005, 133, 441-443
· Ruckenstein MJ, Rutka JA e Hawke M (1991). "Il trattamento della malattia di Meniere: Torok rivisitato". Laringoscopio 101 (2): 211-8.
· Thomsen J, P Bretlau, Tos M e NJ Johnsen (1983). "Malattia di Meniere:. A 3 anni di follow-up dei pazienti in doppio cieco controllato con placebo sulla chirurgia shunt endolinfatico sac" Adv Otorhinolaryngol 30: 350-4.
· Thomsen, J., K. Sass, et al. (2005). "Trattamento sovrapressione locale riduce i sintomi vestibolari nei pazienti con malattia di Meniere:. Uno studio clinico, randomizzato, multicentrico, in doppio cieco, controllato con placebo" Otol Neurotol 26 (1): 68-73.
· Silverstein H, Isaacson JE, Olds MJ, Rowan PT, Rosenberg S, Am J Otol 19:2:1998, 196-201
· N Torok (1977). "Vecchio e nuovo nella malattia di Meniere." Laringoscopio 87 (11): 1870-7.
TERAPIE INTRATIMPANICHE ABLATIVE (GENTAMICINA);ABLATIVE E CONSERVATIVE (STEROIDI):
LABIRINTECTOMIA CHIMICA (GENTAMICINA);
Definizione
La Labirintectomia chimica è l'ablazione chimica del neuroepitelio vestibolare, per rimuovere gli eccessivi segnali vestibolari, con farmaci vestibolo tossici e con conservazione dell'udito.
Introduzione (fig. 5.29A)
l’Ablazione chimica del neuroepitelio vestibolare è comunemente realizzato con la somministrazione di aminoglicosidi (AG5) (Fig. 5.29A).
Tabella 1-7
|
AMMINOGLICOSIDI |
TOSSICITA’ |
MECCANISMO |
|
Gentamicina a |
Vestibulotossico |
Danneggiamento delle cellule acustiche esterne b. perdita delle cellule ciliate cocleari b . perdita delle cellule acustiche di i tipo c |
|
streptpmicina |
Vestibulotossica 2,3 Cocleotossica 3
|
|
|
kanamicina |
Cocleotossica |
perdita delle cellule ciliate cocleari b |
|
Amicacina |
Cocleotossica |
perdita delle cellule ciliate cocleari b |
|
1 effetto primario |
|
a Aminoglicoside più comunemente utilizzato |
|
2 basse dosi |
|
b meccanismo di Cocleotossicità |
|
3 alte dosi |
|
c meccanismo di Vestibulotossità |
A. Aminoglicosidi utilizzati per la labirintectomia chimica
La labirintectomia chimica è spesso considerata una tecnica in cui l'udito è preservato ed è generalmente effettuata prima di utilizzare procedure chirurgiche più invasive. La labirintectomia chimica ha un alto tasso di controllo dei sintomi (vengono riportati risultati positivi fino al 90%) e una conservazione utile dell'udito (SNHL riferisce il livello più basso del 3%)SensoriNeural hearing loss (SNHL) nella grande maggioranza l’ ipoacusia neurosensoriale è causata da anomalie nelle cellule ciliate dell’ organo del Corti nella coclea. Inoltre, questa procedura può essere eseguita in uno studio medico . Quando bisogna praticare la terapia deve essere stabilito prima dell'intervento e questo può essere ad esempio rappresentato da una mancanza completa di risposte , nistagmo, o SNHL (SensoriNeural Hearing Loss) alle stimolazioni caloriche. Il dosaggio può essere aumentato gradualmente in effetti, l'ablazione totale dell’ epitelio vestibolare è associato ad un rischio più elevato di SNHL( (SensoriNeural Hearing Loss ) che non è generalmente necessario per il controllo dei sintomi. Gli aminoglicosidi possono essere dati per via sistemica o con iniezione intratimpanica , quest'ultimo è il metodo più utilizzato . Questo permette di somministrare il farmaco nell'orecchio che non funziona risparmiando dell'orecchio controlaterale. La terapia sistemica AG può essere utilizzata per i pazienti con malattia di Ménière bilaterale. C'è una varietà di tecniche di somministrazione nell'orecchio medio AG (Fig.1.39 a/b) per via intra o trans timpanica
|
|
|
|
Fig. 1.39 a |
Fig. 1.39 b |
Indicazioni
Le indicazioni comprendono una grave compromissione funzionale a causa di sintomi vertiginosi intrattabile con gli apparecchi utilizzabili
Tecnica di Somministrazione (tab 1-8 )
Numerosi sono i protocolli utilizzati per la somministrazione di gentamicina intratimpanica:
— somministrazione continua attraverso una minipompa posizionata chirurgicamente in prossimità della finestra rotonda;
— dosi multiple giornaliere (es. 3 al giorno per 4 giorni consecutivi) (shotgun protocol);
— dosi settimanali attraverso l’iniezione diretta o un tubo di ventilazione per 3 o 4 settimane consecutive;
— dosi somministrate ad intervalli regolari fino alla comparsa di segni cImici di ipofunzione vestibolare unilaterale (titration protocol);
— singola dose da ripetere solo se persistono o ricompaiono le crisi di vertigine (low dose protocol).
Il grande vantaggio dell’ablazione labirintica con gentamicina si basa sul carattere minimamente invasivo della procedura e sulla dimostrazione che non è necessario raggiungere una totale distruzione delle strutture neurosensoriali del vestibolo per ottenere l’effetto terapeutico desiderato (Mino,; 1999). In effetti, l’attenuazione della funzione labirintica ottenuta con la gentarnicina è indubbiamente minore rispetto a quella conseguente a labirintectomia o neurectomia vestibolare (Care’ 2010). Specie se vengono utilizzati bassi dosaggi, la gentamicina mostra una tossicità selettiva per le cellule ciliate di I tipo; la conservazione dell’attività sinaptica delle cellule di tipo Il può mantenere una residua attività afferente del nervo vestibolare che potrebbe rivelarsi utile per favorire i meccanismi di compenso centrale (Carey, 2010).
viene riportato un esempio di protocollo pubblicato (tab n). Dopo l'intervento, i pazienti possono avere vertigini, disequilibrio, nausea / vomito e / o cadute verso il lato trattato , questi sintomi si risolvono spontaneamente in 6-8 settimane, il paziente viene sottoposto ad una serie di audiometria posto operatoria ed un’ulteriore trattamento può essere praticato se il controllo dei sintomi non è soddisfacente.
Vari protocolli sono stati proposti in letteratura con diversi gradi di controllo dei sintomi e delle complicanze. Di recente. due meta-analisi sono stati pubblicati affrontare l'efficacia complessiva della labirintectomia chimica e della efficacia di ciascuna modalità di somministrazione per il trattamento della malattia di Ménière intrattabile, rispettivamente.
Cohen-Kerem et al (2004) ha studiato la labirintectomia chimica con successo su un totale di 627 pazienti provenienti da 15 studi pubblicati con diagnosi di malattia di Ménière intrattabile in base alla commissione per udito e di equilibrio con il criteri (sia del 1985 e/o 1995) della AAO-HNS e cui esiti sono stati riportati in accordo alle linee guida del’ AAO-HNS linee guida. Le tecniche di somministrazione includono le iniezioni interventi o l'infusione con un micro catetere e la dose di somministrazione era fissata o nuovamente rititolata per il controllo dei sintomi Questa analisi ha riportato i tassi di successo globale del 74,7% (95% CI:67,8% -81,5%) e 92,7% (95% CL 89,5% -96,0%)per la classe A e classe A + B risultati, rispettivamente. La soglia di PTA è leggermente aumentata (1,5 dB SR [IC 95%: -12,0 a 9 1]) ed il punteggio di riconoscimento delle parole è leggermente diminuita (2,0% [95% CI: -16,5% al 20,4%]) nessuno di questi dati sono risultati statisticamente o clinicamente importanti. Questi risultati indicano che la gentamicina intratimpanica è un'opzione efficace nel trattamento delle malattie di Ménière intrattabile.
Chia et al, (2004) hanno studiato l'effetto delle tecniche di somministrazione di gentamicina sul controllo generale delle vertigine e sulla frequenza di ipoacusia , compreso una completa ablazione vestibolare che ha portato a livelli superiori di controllo dei sintomi per la malattia di Meniere intrattabile da 980 pazienti provenienti da 27 studi pubblicati, sono stati utilizzati criteri di inclusione simili a quelle sopra citate. Le tecniche di somministrazione includevano somministrazioni giornaliere multiple (3 dosi al giorno per 4 giorni), il dosaggio settimanale (1 dose / settimana per 4 settimane), tecniche a basse dosi (1-2 dosi totali, ripetute se si presentavano episodi ricorrenti di vertigine ), infusione continua con microcatetere, e la tecnica di titolazione (dose giornaliera o settimanale fino alla scomparsa dei disturbi dell'orecchio interno o al miglioramento dei sintomi) le percentuali di successo complessivo per le tecniche erano del 73,6% e 90 2% rispettivamente per le classi A e A-B,. Il protocollo con la titolazione è stata significativamente più efficace nel controllo della sintomatologia vertiginosa rispetto agli altri metodi:
81,7% (P <0001) per la classe A e del 96,3% (P <005)per la classe A-B, inoltre, non c'è riscontrato che una completa ablazione vestibolare migliori statisticamente il controllo dei sintomi.
Nel complesso la frequenza di perdita uditiva era rispettivamente della 6,6% e 251% rispettivamente per gravi o parzialmente gravi ipoacusie percettive.
Il programma di più somministrazione giornaliera ha determinato un più elevata incidenza di parziale profonda ipoacusia percettiva cocleare (SNHL) rispetto alle altre tecniche (34.7%, p <002). questi risultati indicano che il metodo di titolazione può offrire un maggiore livello di controllo dei sintomi con un tasso accettabili di ipoacusia percettiva (SNHL) rispetto alla somministrazione con altre tecniche. Inoltre, una completa ablazione vestibolare non ha aumentato i tassi di controllo dei sintomi.
Le due recenti metanalisi (Chia et al., 2004; Cohem-Kerem et al., 2004)soprariportate ci permettono di valutare i risultati del trattamento della ividivi con gentamicina intratimpanica (Tabella VI) evidenziando globalmente un controllo completo o sostanziale della vertigine in più del 90% dei pazienti in un periodo tra 2 e 5 anni di follow-up con una perdita uditiva, per lo più di modesta entità, nel 25% dei casi.
TABELLA 1-9 -Tabella riassuntiva dei risultati ottenuti con i diversi protocolli di somministrazione della gentamicina intratimpanica
|
|
Controllo completo della vertigine |
Controllo completo e sostanziale della |
Incidenza del danno uditivo |
|
Dosi multiple giornaliere |
76% |
91% |
35% |
|
Dosi multiple settimanali |
75% |
89% |
13% |
|
Titration |
81% |
96% |
24% |
|
Basso dosaggio |
67% |
87% |
24% |
|
Infusione continua |
71% |
89% |
24% |
|
Valore Globale |
76% |
90% |
25% |
Confrontando le diverse metodiche, il protocollo titration sembra quello che permette di ottenere un ottimo risultato in termini di riduzione delle crisi vertiginose in associazione con una bassa incidenza di danno uditivo, che è risultato più comune nei pazienti trattati con dosi multiple giornaliere. Tuttavia un recente report sembra indicare che anche il protocollo low-dose permette un controllo della vertigine in più del 90°c dei pazienti con una percentuale molto ridotta (l2,5%) di danno uditivo (Casani et al., 2012). L’incremento a più di 2 settimane dell’intervallo tra le due iniezioni ridLice la possibilità che l’accumulo del farmaco nell’organo del Corti aumenti l’effetto lesivo sulle cellule ciliare (Zhai et al., 2010); inoltre a bassi dosaggi l’azione tossica della enraniicina si esplica prevalentemente sulle dark ce/is risparmiando parzialmente le cellule sensoriali ( Pender 1985).
Complicazioni
Complicanze con iniezioni intratimpaniche comprendono SNHL, disequilibrio, oscillopsia(con concomitante deficit vestibolare controlaterale), e l'incapacità di ottenere il controllo dei sintomi
infiltrazione nell’orecchio medio
miringotomia
drenaggio trans timpanico
microwick
micro catetere
parenterale vestibulectomia selettiva1
1 Il canale semicircolare orizzontale viene infiltrato con una soluzione di amminoglicosidi.E’ necessaria una mastoidectomia per l’accesso chirurgico al canale semicircolare orizzontale
B Vie di somministrazione degli aminoglucosidi
Tab n°
(1) dose di gentamicina: 0.4 ml di 26.7 mg / ml (circa 10.7 mg; ph 5.4) utilizzando aghi di diametro (gauge) 25 - o 27-. Il pH può essere regolata a 6.4 in caso di necessità per un migliore comfort.
(2) Il paziente assume la posizione per l’esame neurotologico (testa girata in direzione opposta all’ orecchio target)
(3) il condotto uditivo esterno e la membrana timpanica sono anestetizzati (fenolo),
(4) nell’orecchio medio viene iniettata una soluzione di gentamicina
(5) La soluzione viene lasciato nell’orecchio medio per 30 minuti (il paziente non deve deglutire per evitare che il farmaco fuoriesca dall’orecchio medio attraverso la tuba),
(6) La soluzione viene aspirata dall'orecchio medio
(7) Il paziente viene sottoposto a controlli audiometrici settimanali per monitorare gli effetti cocleotossici e per tenere sotto controllo i sintomi.
(8) Può essere necessario ripetere la somministrazione se non è raggiunto il controllo dei sintomi e non sono presenti o soggettivamente ed oggettivamente effetti cocleotossici
C. Esempio di un protocollo di labirintectomia chimica modificato dal Minor et al. (1999)
Trattamento Intratimpanico/Transtimpanico Con Gentamicin Per La Malattia Di MénièreAPPROFONDIMENTODA Timothy C. Hain, MD La situazione è cambiata notevolmente con il trattamento di gentamicina negli ultimi anni - questo documento è stato recentemente aggiornato per riflettere gli ottimi risultati che sono stati ottenuti con un protocollo più recente, che utilizza la la gentamicina a basse dosi . Gentamicina Intratimpanica (ITG IntraTympanic Gentamicin) e Gentamicina Transtimpanica (TTG TransTympanic Gentamicin)
Nei casi di vertigine episodica grave, come ad esempio quella dovuto alla malattia di Ménière ,possono essere presi in considerazione trattamenti farmacologici, per distruggere l'orecchio interno , mediante iniezioni di gentamicina. Si tratta in genere del’ ultimo trattamento per i pazienti che hanno gravi attacchi vertiginosi le iniezioni di gentamicina vengono effettuate attraverso il timpano, utilizzando un ago sottile . Questa tecnica viene denominata: "trattamento intratimpanico con gentamicina ". Alcuni autori chiamano lo stesso processo " trattamento transtimpanico con gentamicina " (ad esempio Casani, Nuti et al 2005), ma il termine "intratimpanico" sembra essere molto più utilizzato. Questa procedura permette di trattare l’orecchio di un lato, senza influenzare l'altro lato . Per molti anni che sono stati utilizzati dosi multiple di gentamicina - in genere 4-6 iniezioni in un periodo poche fa più mesi. Se da un lato questo protocollo di gentamicina a "dose elevate" era molto efficace , dall'altro era accompagnato da mercati effetti collaterali - un notevole rischio di riduzione dell'udito e spesso un periodo prolungato di vertigini e vertigini provocate dallo stesso trattamento . Questa procedura non è consigliabile. Recentemente , sta rapidamente guadagnando favore, il protocollo "a bassa dose " in cui viene utilizzata in totale solo una o due iniezioni, distanziate di 1 mese, . La procedura non è (molto) dolorosa - un anestetico locale viene utilizzato per addormentare il timpano. Un altro metodo è quello di utilizzare una goccia di fenolo sul timpano. Un’altro ancora è l’applizazione di un anestetico topico come la crema "emla". Il farmaco viene iniettato, nell'orecchio medio sinistro per 30 minuti, mentre la persona sta tranquillamente sdraiata, e poi viene effettuato un tentativo di eliminarlo dall'orecchio medio attraverso il tubo ET (facendo delle deglutizioni). Questo ultimo passaggio è probabilmente importante per ottenere risultati riproducibili.
Dopo il trattamento con TTG (Trans Tympanic gentamicin ) nei pazienti con malattie di Meniere la disabilità è diminuita (Pfleiderer, 1998; Perez et al., 1999) ma la qualità soggettiva della vita è rimasta invariata (Soderman et al,) 2001. Le Le vertigini si possono ripresentare un anno più tardi, allora è necessario effettuare un'altra serie di iniezioni. Diversi autori hanno riportato che l'acufene o il senso di un trattamento auricolare possono migliorare sostanzialmente dopo TTG (ad es. Sala, 1997). L'effetto a lungo termine sulla funzionalità uditiva al punto al momento attuale non è chiaro. Un vantaggio sostanziale del trattamento con TTG è il basso costo, rispetto ai trattamenti alternativi e distruttivi A"[sezione del nervo vestibolare o la labirintectomia ]. La maggior parte degli autori hanno riscontrato che il controllo sulle vertigine è paragonabile alla sezione del nervo vestibolare (circa il 90%). Il trattamento con TTG ha, anche , un rischio intrinseco molto basso, soprattutto rispetto alla sezione del nervo vestibolare. Il trattamento TTG , ,rispetto alla labirintectomia ,ha anche un rischio inferiore perché non c'è alcuna necessità di anestesia generale.
La ITG/TTG è stato sostenuto per altri disturbi vestibolari oltre che alla malattia di Meniere (ad esempio Brantberg et al., 1996). a nostro parere l'utilizzo di questa tecnica deve essere utilizzata come "ultima risorsa".
Le due principali varianti di ITG/TTG: Sono qui indicati di seguito i dettagli tecnici per iniettare gentamicina.
A bassa dose -la nostra preferita Il metodo a basse dose comporta l'uso di 1-2 iniezioni di gentamicina, con l’ attesa di un mese tra le due iniezioni. Questa variante blocca le vertigine nel 66-80% del tempo, senza significativi effetti collaterali . La variante a basso dosaggio è relativamente nuova e non ci sono molti dati riguardanti il risultato come invece per la variante di alte dosi. La seconda iniezione viene effettuato solamente se vi sono state intense vertigini nelle due settimane precedenti . In altre parole, invece di determinare l'insorgenza di danni al sistema vestibolare (come avviene per le alte dosi ITG/TTG), questo criterio ha un buon effetto sulla malattia. Questa semplice idea sembra si traduca con risultati di gran lunga superiori . Occasionalmente viene somministrata una terza dose . Di solito questa determina una completa perdita della funzione vestibolare (cioè, vedi sotto Fig.1.41).
Risultati della variante a basso dosaggio Nella nostra pratica, abbiamo avuto ottimi risultati con la variante a basso dosaggio, con eccellente controllo sulle vertigini (100% finora) con nessun danno in tutti sulla funzionalità uditiva . Qui vengono riportati i risultati di altri autori : Presso la Mayo clinic è stato segnalato che Un trattamento monodose da, un tasso di risposta di riduzione delle vertigini nella 84% e nessun variazione della funzionalità uditiva. (Driscoll et al, 1997; Harner et al., 2001) questi risultati sono attribuiti al fatto che la gentamicina distrugga le cellule scure secernenti l’endolinfa prima di distruggere l'epitelio sensoriale vestibolare (Beck, 1978). Contro questa ipotesi è l'assenza di un cambiamento patologico nelle cellule scure dopo il trattamento con gli aminoglicosidi per via endovenosa (Cureoglu et al 2003). La principale alternativa al meccanismo di distruzione delle cellule scure è l'ipotesi che esista un danno parziale per le cellule ciliate vestibolare. Recenti studi sugli animali suggeriscono che il tipo I-delle cellule ciliate siano più sensibili, e le cellule ciliate di II tipo siano più resistenti .
Una recente meta-analisi (Chia, Gamst et al 2004) riporta che la tecnica a bassa dose abbia un controllo significativamente più basso sulle vertigini (66,7% complessivo). Tuttavia, nella nostra esperienza non abbiamo avuto questo risultato. Sembra anche molto probabile , che i metodi a basso dosaggio, avranno un ricorrenza maggiore dopo 1-2 anni . Ancora, la nostra opinione è che è molto più facile effettuare un altro "ritocco" iniezione dopo 1-2 anni, ma che è invece impossibile riottenere una funzionalità uditiva dopo che questa è stata danneggiata dal protocollo ad alte dosi. I risultati a lungo termine sulla funzionalità uditiva non sono chiari in questo articolo.Se il basso dosaggio infatti riduce la pressione nell'orecchio interno, può essere che la funzionalità uditiva si deteriorerà in misura minore.
Dose molto bassa - per le persone anziane una variante alla procedure dove la gentamicina viene somministrata anche meno frequentemente di una volta al mese, o in una soluzione più diluita rispetto alle dosi convenzionali deve essere presa in considerazione . Si raccomanda routinariamente l’uso di gentamicina a metà dosaggio nei pazienti con questi disturbi vestibolari che abbiano più di 70 anni. Contro questa ipotesi vi è la congettura che la gentamicina transtimpanica "saturi" rapidamente i siti di legame nell'orecchio interno, e quindi non non c'è alcuna reale differenza nel dare una dose molto bassa o una dose bassa , ma piuttosto è il numero di applicazioni di gentamicina che conta, più che la concentrazione. Si pensa che questa ipotesi non sia corretta, ma sarebbe un interessante progetto da far effettuare ad un ricercatore . Le basse dosi di gentamicina,somministrate per un tempo prolungato rischiano di avere un effetto più uniforme sull'orecchio rispetto a quella somministrate per breve tempo; è probabile che, le somministrazioni concentrate (Pender, 2003), rappresentino un rischio molto inferiore per la funzionalità uditiva .
Alte dosi:Nella variante a dosi elevate, viene somministrata più gentamicina per un periodo di tempo più breve. Con questa variante si hanno risultati migliori, riduzione delle vertigini nel (90% del tempo), ma è anche accompagnata da rischi di gran lunga superiori. Le iniezioni vengono generalmente somministrate ogni settimana, fino a un totale di 4-6. Il trattamento viene interrotto quando si producono vertigini questo indica che la gentamicina ha agito sull'orecchio interno . In altre parole, il trattamento è continuato fino a quando non ci sono prove , che si sono instaurati danni, all'orecchio interno. Raramente, anche dopo 6 iniezioni, le vertigini non possono essere indotte e la la funzione vestibolare rimane normale. A questo punto, il trattamento viene interrotto e viene utilizzato un altro metodo per eliminare la funzione vestibolare (ad esempio labirintectomia ). La vertigine peggiora per un pò dopo che il trattamento viene interrotto, la vertigine di solito dura da 7-10 giorni, ma può richiedere fino a un mese per risolversi . I sintomi sono controllati con farmaci per la nausea e con i soppressori vestibolari. A questo punto è necessario un buon supporto familiare o ricovero in ospedale. L’ìnstabilità di solito si risolve dopo diversi mesi, ma nei soggetti più anziani, qualche instabilità può rimanere in maniera permanente (anche se le vertigini vengono eliminate ). La funzionalità uditiva può peggiorare . Nei piccoli mammiferi, come le cavie, l'applicazione di gentamicina nell'area della finestra rotonda può comportare quasi una perdita totale dell'udito (Imamura et al 2003). Si dovrebbe però notare tuttavia, che i piccoli mammiferi , come le cavie, hanno le membrane finestra rotonda molto più sottile rispetto agli umani e quindi si può somministrare una maggiore quantità di gentamicina nello stesso periodo di tempo. La funzionalità uditiva non è così sensibile come negli esseri umani, ma su questo motivo si sta ancora lavorando. Siccome i protocolli farmacologici evolvono, la percentuale di trattamenti associati , ad una riduzione della funzionalità uditiva continua gradualmente a ridursi (vedi tabella sotto), ma c'è ancora qualche reale rischio di perdita dell'udito. Un rischio del 30%, per una lieve riduzione sembra essere normale, anche se di recente, i sono stati segnalati risultati migliori (Wu e minore, 2003). Si crede, considerazioni basate sulla farmacocinetica, che dove la gentamicina è somministrata molto lentamente, i protocolli siano meno rischiosi, per la funzionalità uditiva, rispetto a protocolli dove viene somministrata una grande quantità di farmaco in in una settimana o meno. Se un paziente ha già perso l'udito utilizzabile sul lato "cattivo" ovvero dove è presente la Meniere , il rischio è eliminato, e pertanto può essere utilizzato sia un protocollo lento o veloce.
La figura 1.42 qui sopra mostra il risultato previsto per alte dosi di gentamicina - nistagmo spontaneo e vertigini. Questo è il risultato auspicato per un paziente che ha avuto somministrato un alto dosaggio di gentamicina . Si è anche notato che tutti i pazienti che hanno avuto successi con con successi con alti dosaggi di gentamicina hanno un intenso nistagmo indotto da vibrazioni C'è anche un film con qualcosa di simile in un paziente con un protocollo a basso dosaggio: ivg.avi(8 meg)
Il Nistagmo qui è osservato 2 settimane dopo una singola dose di gentamicina intratimpanica. Questo non è comune ed è stato un effetto negativo del protocollo monodose.
Risultati della variante a dose elevata TABELLA 1-9 I risultati, in termini di eliminazione dei disturbi vertiginosi , sono in genere molto buoni (vedi tabella). La funzionalità uditiva è generalmente inalterata o peggiorata e potrebbe continuare a peggiorare, anche dopo che la vertigine viene eliminata . L’acufene rimane generalmente inalterato, ma alcuni recenti studi riferiscono una riduzione del tinnito. Alcuni pazienti ottengono sollievo dai sintomi di Meniere a dispetto di un subtotale ablazione della funzione vestibolare. Questo è attribuito al danno selettiva di gentamicina sulle cellule scure del labirinto (Atlas, 1999; Pender, 1985). A sostegno di questa ipotesi ipotesi è l'osservazione che TTG riduce la dimensione del potenziale di sommazione della ECochG, ELETTROCOCLEOGRAFIA PERITIMPANICA NON INVASIVA (ECochG) che è un test diagnostico per la malattia di Meniere (Adamonis et al, 2000). Contro questa ipotesi è la mancanza di un cambiamento nelle cellule scure dopo il trattamento (Cureoglu et al, 2003) con aminoglicosidi.
Risultati della varianti a dosi elevate TABELLA 1-9
Altre varianti nelle procedure di somministrazione di gentamicina intratympanic - generalmente non sembra che sia il miglior approcio.Prima di iniziare, si deve rilevare che in passato, la maggior parte dei praticanti ha utilizzato il protocollo semplice di circa 4 iniezioni di gentamicina, effettuate settimanalmente, fermandosi quando erano presenti segni di danni (questo tipo di somministrazione viene chiamata titolazione Titration). Questo ha dato senso ad una meta-analisi che è stato recentemente effettuata da Chia e altri (Chia, Gamst et al 2004), il metodo di somministrazione (titolazione )settimanale ha avuto i migliori risultati con un maggiore controllo delle vertigini e una tendenza ad avere complessivamente una minore perdita uditiva . Tuttavia, in questo momento, nella nostra pratica , così come in altri centri altamente specializzati, il protocollo a basso dosaggio è diventata routine, si pensa che sia ancora meno rischioso e che i risultati siano molto buoni. Perché questa procedura funziona così bene, gli esperimenti del passato che vengono riportati dettagliatamente più sotto sono diventati tutti piuttosto irrilevanti. Streptomicina: sono state segnalate molte altre varianti del protocollo ITG/TTG I risultati delle iniezione con streptomicina (la forma diidro) sono stati esaminati in due studi pubblicati ( Schuknecht, 1951), con risultati sensibilmente peggiori per la funzionalità uditiva rispetto a quelli ottenuti con gentamicina. Questo può essere causato dalla relativa selettività della gentamicina per la cellule acustiche vestibolari, rispetto alla diidro-streptomicina. Sembrerebbe, tuttavia, che la streptomicina solfato potrebbero essere altrettanto efficace quanto la gentamicina. Sembra essere poco vantaggioso sperimentare la streptomicina , in quanto già la gentamicina funziona molto bene senza rischi significativi per l'udito quando viene somministrata a lunghi intervalli. Streptomicina-desometasone: Questa particolare metodologia è favorita nella "Shea clinic", un centro di otologia situato a Memphis nel Tennessee. Sembrerebbe un trattamento illogico , che sarebbe meglio evitare. La streptomicina funziona meno della gentamicina per questo scopo (vedi sopra). Non si vede nessuna ragione logica per associare il desametasone (uno steroide intratimpanico ) con la streptomicina (un antibiotico ototossico). Sembra molto più logico utilizzare questi farmaci uno alla volta, piuttosto che mescolandoli insieme . Il problema degli steroidi intratimpanici viene affrontato in queste pagine.
Titolazione (Titration): un problema è anche quando smettere il trattamento, soprattutto per il protocollo ad alte dosi, con iniezioni settimanali. Una sospensione eccessivamente tardiva potrebbe essere più grave (tossica) per la funzionalità uditiva. Sarebbe meglio non trovarsi in questa situazione, in primo luogo e utilizzare una iniezione una volta di mese. Tuttavia, a volte ci sono situazioni in cui si vuole somministrare più velocemente i farmaci accettando il rischio per la funzione della uditiva. . Minor (1999) suggerisce di fermare il trattamento quando compare un nistagmo spontaneo , un nistagmo con “head-shaking test” o segni al "head-thrust test”. Perez et al (2003) utilizzano un metodo simile. Mentre questo protocollo appare ragionevole è complesso e fermarsi semplicemente su un cambiamento significativo nella direzione e di intensità del nistagmo spontaneo, o dopo che un totale di 6 trattamenti è stato effettuato potrebbe essere una alternativa adeguata . Abou-Halawa e Poe smettono il trattamento o rallentano il trattamento quando compare una perdita dell'udito alle alte frequenze . Sembrerebbe che utilizzare questa tecnica sia tardiva in quanto la funzionalità uditiva( l'udito) è insensibile alle gentamicina. Come è stato detto già - dare una superiorità a piccole dose di gentamicina rispetto ad un protocollo di più dosi, non sembra esserci alcuna ragione per fare di più di 1-2 iniezioni, così come la titolazione non sembra sia davvero un problema. Provvisoriamente, pensiamo che sia una buona idea effettuare un VEMP prima della di ITG e un altro,fig n, se sembra ci sia un fallimento con il trattamento. La letteratura supporta l’ipotesi che il VEMP sia ridotto o abolito in seguito alla ITG. Nella pratica , si è avuto un buon successo osservando il nistagmo prodotto da vibrazioni per decidere o meno se la gentamicina abbia avuto o meno un effetto. È un metodo semplice e veloce che appare molto sensibile alla gentamicina. Questo uso del VIN è non accompagnato da pubblicazionI una variante di questo metodo potrebbe essere di continuare la somministrazione per via parenterale, fino a quando il VEMP è notevolmente ridotto . Un altro problema con questa ipotesi è che l'iniezione stessa può provocare una sordità che interferisce con il VEMP. Modalità di somministrazione: numerosi metodi sono stati utilizzati per iniettare la gentamicina quale l'iniezione diretta, la somministrazione tramite un tubo per timpanostomia, cateteri chirurgici(Round window m-cath, Durect Corp; Silverstein MicroWick). Il metodo dell'arco (basso dosaggio) o metodo del tubo per timpanostomia (alte dosi quando non c'è più la funzionalità uditiva) sembra abbastanza ragionevole. Le procedure che richiedono il posizionamento chirurgico di un catetere, sembra irragionevole in quanto aggiunge il rischio (chirurgico) senza prova di risultati migliori
Le procedure che coinvolgono il posizionamento di uno stoppino"" nel tubo per timpanostomia (cioè il "Silverstein MicroWick(tm)"), non sembrano molto diverse dal semplice uso del tubo per sola timpanostomia . Non si dubita che funzioni, ma non si è convinti che lo sforzo supplementare e il costo necessario per inserire il tubo per timpanostomia speciale e lo stoppino, così come è successiva rimozione, è giustificata. È molto difficile competere con la procedura di basse dosi in termini di risultati. È anche difficile capire la logica di mettere una flebo costantemente , quando è ben noto che negli animali la gentamicina si accumula nell'orecchio per molti mesi. In questo gruppo di pazienti, i risultati migliori per le vertigini sono correlati con risultati di un peggioramento della funzionalità uditiva (Light et al, 2003) faceva un lavoro di essere la vostra rete viene Chirurgia supplementare: alcuni gruppi richiedono una esplorazione endoscopica dell'orecchio medio e "l'eliminazione delle aderenze" dalla nicchia della finestra rotonda. E a tutti noto che le aderenze sono presenti in circa il 20% delle finestre rotonde. Si ha il dubbio che in questa procedura si possono avere ulteriori danni alla alla membrana timpanica (da endoscopio). Questa procedura aggiunge anche un costo aggiunto, attrezzature specializzate e l'abilità per una procedura , che altrimenti sarebbe, piuttosto semplice Tempistica (Timing):: rispetto alla tempistica, protocolli che coinvolgono le amministrazioni rapide di grandi quantitativi di farmaco (qui definiamo rapida quella effettuata non oltre una settimana), sembrano essere incline a produrre risultati peggiori per la funzionalità uditiva , forse perché gentamicina ha un effetto ritardato e prolungato, che si estendono per settimane o mesi, ed è difficile sapere se si è già somministrato abbastanza o troppo, in una settimana. (Chia, Gamst et al 2004) Tuttavia, se la funzionalità uditiva è già inutilizzabile sul lato da trattare, i protocolli più breve sembrano essere abbastanza ragionevoli. Intratympanic Gentamicin (fig. 1.44)
Approccio chirurgico dell'autore favorisce l'esplorazione dell'orecchio medio utilizzando un otoscopico ottico rigido molto piccolo ottico di solo 2 mm di diametro per visualizzare la membrana della finestra rotonda per rimuovere qualsiasi tessuto cicatriziale o strati di muco sulla membrana della finestra rotonda che possono ostacolare l'accesso del farmaco alla membrana.
Dopo che è stato eliminato dalla membrana timpanica seconda ria (membrana di Scarpa) qualsiasi ostruzione, un tubo di Silverstein con lo stoppino vengono inseriti nel timpano. La Gentamicina viene quindi versata nell'orecchio medio. Lo stoppino Silverstein consente al paziente di continuare a inserire le gocce di gentamicina nell'orecchio a casa per continuare il trattamento. Nella maggior parte dei casi le gocce non vengono più somministrate dopo 5-7 giorni di utilizzo a casa . Lo stoppino è solitamente rimossi a questo punto, ma il tubo può essere lasciato sul posto per ulteriori trattamenti gentamicina, se necessario.
Dopo che il farmaco viene assorbito, molti pazienti presentano un periodo di lieve a moderato disequilibrio che inizia di solito 3-4 giorni dopo l'inizio del trattamento. Il disequilibrio si risolverà nella maggior parte dei pazienti, dopo un periodo di alcune settimane dopo che il trattamento con gentamicina viene interrotto. In molti casi, solo un breve trattamento di 5-7 giorni di gentamicina è necessario. Il temporaneo disequilibrio è descritto in genere come la sensazione, che la maggior parte delle persone prova quando è su una piccola barca. Il paziente si regolerà automaticamente con un'andatura con la base di appoggio allargata (a piedi con le gambe aperte). È importante per il paziente che rimanghi attivo in modo che l'orecchio interno regolerà più rapidamente i nuovi segnali che ora sta ricevendo dall'orecchio trattato. I movimenti attivo accelerano i centri del cervello per riequilibrare il nuovo modello segnale proveniente dall’ orecchio interno.
La perfusione con gentamicina è un trattamento ottimo per il paziente con problemi di udito in cui la funzionalità uditiva nell'orecchio coinvolto è significativamente ridotta , vertigini incontrollata e funzionalità uditiva normale o quasi normale nell'orecchio opposto. In questi pazienti l'obiettivo principale è quello di rendere nulli gli attacchi di vertigini fermare e la perfusione gentamicina bloccherà gli attacchi in oltre il 90% dei casi. Tuttavia, un dilemma per il trattamento può verificarsi nel paziente con attacchi di vertigini aggressivo, grave che non possono essere controllati con terapia medica, che ha anche un normale o quasi un udito normale nell'orecchio interessato dalla malattia di Meniere.
Purtroppo, non è possibile prevedere con precisione quali pazienti avranno una perdita uditiva a causa del di trattamento con gentamicina. Gli Studi negli ultimi 10 anni riportano una ulteriore ipoacusia dovuta al trattamento Gentamyicin tra 10 ed il 20% dei pazienti trattati. Se una ulteriore perdita dell'udito si verifica con la perfusione gentamicina la perdita solitamente non è grave, tuttavia ipoacusia grave o addirittura profonda nell'orecchio trattatato si possono verificare anche dopo nessun trattamento con gentamicina.
Continua ricerca è in corso per determinare il dosaggio ottimale di gentamicina che conserva l'audizione, ma controlla le vertigini. Qualche paziente, 12-18 mesi dopo il trattamento iniziale di gentamicina, può avere ulteriore di episodi di vertigini e a questo punto può richiedere ulteriori trattamenti. Infine, alcuni gruppi suggeriscono il trattamento intratimpanico di desametasone. Il desametasone è uno steroide e non è imparentato con la gentamicina. Il beneficio di questa procedura non è stato dimostrato chiaramente - potrebbe valere la pena di provare in quelle situazioni dove tutto il resto è stato processato e c'è poco da perdere. Silverstein et al hanno riscontrato che non è meglio del placebo (1998), ad esempio, potrebbe essere considerato il suo uso , quando l'orecchio rimasto colpito da Meniere è il solo orecchio l'orecchio in cui è rimasta la funzione uditiva..
Gentamicina vs steroidi vs sezione del nervo vestibolare TABELLA 1-10Ci sono alcuni giudizi complessi che insorgono quando si ha la necessità di " “aver fatto qualcosa " per la malattia di Meniere. In sostanza, si scende a costo vs beneficio. Essenzialmente, si tratta dei costi rispetto ai vantaggi
TABELLA 1-10
A nostro parere, la gentamicina a basso dosaggio è attualmente "il punto ottimale (sweet spot)" in questa tabella. Vediamo una scarsa motivazione perché dovrebbe essere sostenuta qualsiasi altra procedura, a meno che la gentamicina a basso dosaggio abbia già fallito. Gentamicina autogestita - di solito non è una buona idea La procedura più semplice (e meno costoso) finora segnalato è quella di Rutka e colleghi (Rutka, 2002). Essi avevano avuto semplicemente un paziente che si ha autosomministrava localmente della gentamicina attraverso un tubo di ventilazione. Un tubo di ventilazione viene posto nel quadrante posterio-inferiore del TM(membrana timpanica ). I pazienti sono istruiti a collocarsi su di un fianco e istillare 5-6 gocce nell'orecchio interessato 3 volte al giorno. Viene utilizzata una bassa concentrazione di gentamicina - 3 mg/ml combinato con 1 mg/ml di betametasone. La concentrazione totale giornaliera è di 3mg (dose/giorno) ed è circa 10 volte più debole di quelle utilizzate con iniezioni settimanali, con ago (30 mg). A questi pazienti è stato detto di somministrarsi le gocce fino a che le vertigini diventano costanti per 2 giorni e poi fermarsi. La maggior parte dei pazienti ha sperimentato ototossicità dopo 12 giorni di questo trattamento.
Circa il 50% dei pazienti ha riscontrato un peggioramento dell'udito e circa il 40% dei pazienti ha sviluppato delle perforazioni permanenti della loro membrana timpanica i. Questi risultati sono peggiori di quelli associati a gentamicina monodose. Si pensa che la complicanza delle perforazioni sia dovuta alla componente steroidea (Rutka, 2003). A nostro avviso, questa procedura è meno precisa rispetto alla maggior parte delle altre procedure sopra indicate, e la mancanza di precisione è probabilmente associata con un rischio maggiore di perdita uditiva . Tuttavia, sembra ragionevole in situazioni dove la funzionalità uditiva non è più inutilizzabile, come alternativa a un labirintectomia chirurgica dell'udito. Come accennato, potrebbe essere preferibile utilizzare gocce senza steroidi a causa del pericolo di una perforazione permanente. Inoltre, utilizzando meno gocce al giorno, si potrebbero avere risultati migliori sulla funzionalità uditiva, sebbene ci sia una latenza più lunga prima che inizi la tossicità. Non sembra che l'uso di steroidi, in questi casi sia una buona idea, poiché sembra che determini altre complicanze. Aggiungere altri agenti farmacologici alla gentamicina - anche questa non è una buona idea Alcuni gruppi hanno sperimentato l'aggiunta di altri farmaci alla gentamicina, apparentemente nel tentativo di rendere la soluzione più viscosa e meno propensa a correre giù attraverso la tromba di Eustachio, non appena il paziente si siede. Ad esempio, una a colla di fibrina (!?) è stata utilizzata per questo scopo (Casani, Nuti et al 2005). Non si consiglia questa procedura. Siccome in passato il problema principale è stato la tossicità per la funzionalità uditiva , procedure finalizzate ad aumentare la dose introdotta nell'orecchio all'orecchio sembrerebbe irrazionale a meno che l'orecchio sia già sordo. Non si è entusiasti per quanto concerne l'aggiunta di steroidi alla gentamicina, o steroidi alla streptomicina (come discusso in precedenza).
Perché la TTG potrebbe fallire?
Ci sono una serie di ragioni perché la ITG/TTG potrebbe avere avuto esito negativo. In primo luogo, la diagnosi potrebbe essere sbagliata. Il paziente potrebbe avere un disturbo centrale come l’emicrania) associata vertigini, patologia che è almeno 25 volte più comune rispetto alla malattia di Meniere), il paziente potrebbe avere una malattia nervosa (ad esempio una compressione microvascolare ,o potrebbe avere una Meniere bilaterale. Non ci si dovrebbe aspetterebbe che i disturbi del nervo vestibolare rispondino alla TTG.
Un secondo gruppo di motivi dipende dal fatto che il farmaco non è efficace. In teoria, potrebbe essere inefficace perché non raggiunge l'orecchio interno (forse a causa di aderenze sulla finestra rotonda o perché il farmaco fuoriesce dall'orecchio medio attraverso la tromba di Eustachio), il paziente in trattamento potrebbe avere una resistenza idiosincratica alla gentamicina (è stata documentata una suscettibilità idiosincratica,, forse c'è anche resistenza, o ci potrebbe essere un recupero delle cellule ciliate che sono state danneggiate in maniera incompleta. A questo proposito, inizialmente, la gentamicina può arrecare danni reversibili per le cellule ciliate. È comune che gli attacchi di Meniere ricompaiono 1 o 2 anni dopo il primo trattamento TTG (Waele et al, 2002). Uno otoneurologo può essere più certo che la TTG abbia ucciso una parte significativa dell'orecchio interno facendo dei test vestibolari, soprattutto le prove caloriche. A causa della possibilità di danni reversibili, potrebbe essere necessario fare un test calorico dopo circa 3 mesi dalla fine del trattamento (per vedere la risposta di picco), e fare un altro test se le vertigini si ripetono uno o due anni più tardi.
Nella nostra pratica abbiamo trovato, occasionalmente, individui che sembrano avere sistemi vestibolari "duri", che recuperano la funzione dopo le procedure ablative, che normalmente sono altamente efficace in molti altri pazienti. Presumiamo che questi individui hanno una migliore capacità di adattarsi alle lesioni vestibolare o recuperare da loro. Queste persone sono molto rare e si rimane sempre dell’opinione generale sopra riportata riguardante l'efficacia molto elevato di TTG/ITG. Si potrebbe pensare che, i pazienti con con crisi otolithic di Tumarkin otolithic crises of Tumarkin [AKA cadute improvvise (drop attacks), a volte una variante della malattia di Meniere] potrebbero avere un probabile esito negativo, in quanto questo è un disturbo di origine otolitica e si pensa che la gentamicina , negli esseri umani , sia meno tossica per gli otoliti rispetto per i canali semicircolari. A nostro parere, questo non è corretto, come evidenziato da dati recenti (Picciotti et al., 2005; Helling et al., 2007) viene suggerito che la gentamicina prima colpisce il sacculo (uno dei due organi Otolitici); Abou-Halawa e Poe (2002) riferiscono che su 4 pazienti con crisi Tumarkin, 2 non aveva ulteriori attacchi, 1 non ha risposto, e 1 aveva una ricorrenza di attacchi che ha richiesto la somministrazione di ulteriore gentamicina. La nostra esperienza è stata che la TTG/ITG funziona bene per gli attacchi di caduta improvvisa . Quando la TTG fallisce, bisognerebbe effettuare un esame accurato per escludere errori del primo gruppo (diagnosi sbagliata). Se la diagnosi risulta ancora essere sostenibile, uno potrebbe desiderare di prendere in considerazione le procedure più radicali come la sezione del nervo vestibolare la labirintectomia. Provvisoriamente, pensiamo che sia una buona idea effettuare un un VEMP fig n prima della ITG/TTG e un altro, se ci sembra ci sia un fallimento del trattamento.
Dove praticare il trattamento intratimpanico di gentamicina Questa è una procedura ambulatoriale. Quasi tutti i più grossi centri medici offrono ora il trattamento intratimpanico di gentamicina attraverso il loro servizio di Otorinolaringoiatria. Prima di iniziare il trattamento intratimpanico di gentamicina, pensiamo che sia prudente provare tutti i principali trattamenti medici Non riteniamo che bisogna provare i numerosi trattamenti per la malattia di Meniere , che sono probabilmente placebo ,come questi rifiuti tempo e denaro, e basso dosaggio gentamicina è molto efficacia. Esempi di procedure che sono probabilmente placebo o almeno solo leggermente efficace, sono il dispositivo Menniett, gli steroidi intratympanici e la chirurgia dello shunt indolinfatico .
Bibliografia riferita al trattamento intratimpanico con gentamicina:· Abou-Halawa AS, Poe DS. Efficacy of increased gentamicin concentraion for intratympanic injection therapy in Meniere's disease. Otol Neurotol 23:494-503, 2002 · Adamonis J and others. Electrocochleography and gentamicin therapy for meniere's disease: a preliminary report. Am. J. Otol 21:534-542, 2000
Informazioni Supplementari Concernente la Iniezione Intra/Transtimpanica di GentamicinaTimothyC.Hain,MD
anestesia Locale per TTG (or myringotomy) Fig. 1- 46 · Una goccia di fenolo sul timpano è il metodo più comunemente usato di anni per anestetizzare localmente il timpano. Brucia per pochi minuti, ma lascia un'area insensibile della membrana timpanica che è insensibile per diverse settimane. · Un'anestesia meno duratura può essere ottenuta con tetracaina o lidocaina, con o senza ionoforesi. · Può anche essere utilizzato la crema EMLA (lidocaina con prilocaina). Sistemi di Somministrazione per la Gentamicina · Iniezione di ago attraverso il timpano (vedi sopra) · Catetere a farfalla di tipo T-tube · Micro Wick inserito attraverso un tubo per timpanostomia · Microcatheter a pompa attraverso un tubo per timpanostomia
L'approccio più economico sembra essere il metodo dell'iniezione con 'ago semplice. Ci non sembra essere molto più vantaggioso un catetere a farfalla L'idea che sta dietro il Micro-Wick e Microcatheter è quella di fornire un livello più basso di farmaco ed un somministrazione costante di gentamicina. Mentre la logica è ragionevole, praticamente alla scrittura attuale, non sembra importante quale sistema di distribuzione viene utilizzato per amministrare. Il "Micro-Wick" Silverstein richiede un tubo per timpanostomia. La pompa Microcatheter richiede un approccio anche più invasivo. Preparazione del farmaco Una piccola quantità di soluzione di gentamicina è acquistata in farmacia, in concentrazioni di 20-40 mg/ml, tamponato con bicarbonato. Lo scopo del buffer è per evitare l'irritazione dell'orecchio medio a causa di pH. Una piccola quantità di lidocaina può anche essere aggiunta alla miscela, per rendere meno doloroso il processo. Metodologie per la iniezione Una siringa per tubercolina viene utilizzata, con un piccolo ago per iniezioni spinali, contiene 1 cc e la soluzione viene iniettato in modo da riempire l'orecchio medio. L'ago spinale è piegato in modo che il medico possa inserire l'ago senza che la siringa, oscuri il campo visivo . La soluzione è lasciata nell'orecchio medio per 30 minuti, mentre il paziente viene lasciato sdraiato . Dopo che sono passati 30 minuti , viene effettuato un tentativo di eliminare il liquido dall'orecchio medio attraverso le trombe di Eustachio, posizionando che il soggetto seduto in posizione verticale faccia delle manovre di compensazione . A volte viene effettuato un tentativo di fornire una ventilazione con un piccolo foro sulla membrana timpanica L'idea è di garantire che il farmaco lascia l'orecchio medio dopo 30 minuti. Questa sembra essere una procedura ragionevole , almeno per le persone che sono in grado di eliminare il farmaco dopo 30 minuti. Questo può essere accertato cercando di vedere se il farmaco è nell'orecchio medio (forse sarebbe una buona idea usare una soluzione colorata?). Regime di dosaggio - mensile (a basso dosaggio) Questo è attualmente il regime preferenziale di dosaggio. Un'iniezione viene somministrata ed il paziente viene ricontrollato dopo un mese (o 2 mesi). Se i sintomi sono invariati nella seconda metà del mese precedente, e non ci sono segni che il farmaco abbia agito sulla funzione vestibolare ed uditiva viene somministrata una una seconda iniezione.
Dosaggio di regime - settimanale Per le iniezioni settimanale, sono amministrate da 1 a 6 iniezioni, in genere una volta / settimana. Gentamicina Intratimpanica per la malattia di MeniereStorie Con il Contributo dei Pazienti
Solo per i tuoi commenti, io sono un paziente di 43 anni che avuto per un lungo anno la malattia di Meniere con attacchi di vertigine e trattato con gentamicina base dose che hanno eliminato completamente tutti i miei attacchi. La qualità della mia vita prima erano completamente differenti. E ' stato un miracolo assoluto. Solo dovuto dire a qualcuno che dà molto consigli. Leggere PA Trattamento Steroideo Intratimpanico per la Malattia di MeniereTimothy C. Hain, MD MODIFICATA DA A TANZARIELLO : June 25, 2011
· Metodologia Methodology · Risultati Results · Variante nelle procedure Variant procedures
CORTICOSTEROIDI INTRATIMPANICII principali effetti degli steroidi nell’Ol sono riconducibili all’azione antiinfiammatoria immuno-soppressiva ed all’interferenza sull’omeostasiionica. Gli effetti sono indubbiamente maggiori a seguito di somministrazione intratimpanica in virtù delle elevate concentrazioni localmente raggiunte, di gran lunga superiori rispetto a quelle ottenute attraverso la somministrazione per via sistemica (Bird et al.,2011), in assenza peraltro di effetti collaterali spesso presenti in quest’ultimo caso.Nei vari studi effettuati sulla terapia steroidea intratimpanica della MdM è stato utilizzato prevalentemente il metilprednisolone (MPS), la cui scelta si basava sull’evidenza che in studi su animali da laboratorio la concentrazione del suddetto farmaco a livello endolinfatico era molto elevata (Parnes et al., 1999). Una reinterpretazione dei risultati ha tuttavia evidenziato che è il desametazone (DMZ) il farmaco di scelta in virtù di un più rapido raggiungimento di elevate concentrazioni a livello della stria vascolare e dei tessuti circostanti. E noto che gli steroidi agiscono a livello intracellulare. Pertanto trovare alti livelli di MPS nell’endolinfa indica un basso livello intracellulare, per cui l’efficacia del DMZ è sicuramente maggiore. Inoltre il DMZ sembra incrementare il livello di acquaporina nell’orecchio interno, in particolare nel SE e nelle aree circostanti gli spazi endolinfatici, favorendo la capacità dell’acqua di attraversare le membrane. Un ulteriore effetto del DMZ, pare riconducibile ad un’azione vasodilatatoria, che comporterebbe effetti favorevoli sul flusso ematico cocleare, aspetto già osservato nella cavia a seguito dell’applicazione diretta del farmaco sulla finestra rotonda (Shìrwany et al., 1999). Definizione degli steroidi itratimpanici ( Intratympanic steroid ITS)
In casi estremamente gravi di vertigine episodica, come ad esempio quella dovuta alla malattia di Meniere, possono essere presi in considerazione somministrazione di farmaci nell'orecchio medio . Questa è l'ultima risorsa di trattamento per i pazienti che hanno attacchi gravi di vertigine. L'obiettivo di questi trattamenti è di influenzare l'orecchio interno utilizzando farmaci che entrano nell'orecchio interno attraverso la finestra rotonda. La presunzione è che la malattia sia immunologicamente mediata. I corticosteroidi diminuiscono l'infiammazione dell'orecchio e possono migliorare la circolazione labirintica. E’ stata inoltre avanzata l’ipotesi che gli steroidi influenzano il metabolismo dei sali dell'orecchio interno. Questa ipotesi sembra strana in quanto farmaco di solito utilizzato, il desametasone, ha molto poco o nessun effetto sui mineralcorticoidi. Qualche autore suggerisce che i corticosteroidi sono antiossidanti (Chi et al, 2011 Gli steroidi possono essere somministrati per via orale, e questo metodo è discusso qui’ . Indicazioni per ITG con steroidi. TABELLA 1-10L'autore di questo articolo non è molto entusiasta degli steroidi ITG per la malattia di Meniere. Il motivo è che il farmaco viene eliminato in pochi giorni e anche se funziona, deve essere ripetuto ogni 3 mesi. Sembra un metodo di gran lunga inferiore all'uso di gentamicina IT, che fornisce una soluzione molto più durevole. Le iniezioni di steroidi possono essere ragionevole quando uno sta tentando di diagnosticare malattie autoimmuni dell’ orecchio interno. Può anche essere giustificabile per la perdita improvvisa dell'udito Iniezioni di steroidi (come shunt chirurgico endolinfatico per malattia di Meniere) sono una procedura che sembra essere molto popolare come un intervento chirurgico, anche se un po' carente di una chiara logica. Tipo di trattamento Tuttavia, le iniezioni steroidee stanno rapidamente crescendo in popolarità. Al momento attuale (2008) nella pratica dell'autore a Chicago, ha occasionalmente raccomando a un paziente che sta avendo un chiara malattia di Meniere ben definita, o una perdita improvvisa dell'udito(. Le ragioni per la mancanza di entusiasmo sono indicate nell'articolo dell'autore sulla stessa malattia di Meniere, ma in sostanza, non sembra funzionare, a meno che non viene somministrata per un lungo periodo, e ci sono alternative (cioè la gentamicina a basse dosi che sono molto più durevoli, e si è scettici che sia una buona idea dare più iniezioni di steroidi nell'orecchio medio per un lungo periodo di tempo. Ancora, le cose stanno cambiando con questo tipo di trattamento. Metodologia: Le iniezioni di steroide possono essere effettuate attraverso il timpano, per mezzo di di un piccolo ago (Figura 1-35B), o somministrate con delle gocce attraverso un tubo di ventilazione (figura 1-35A). Gli steroidi IT permettono di trattare un solo lato, senza influenzare l’altro . Inoltre evita le complicazioni degli steroidi sistemici, può evitare l'intervento chirurgico e può funzionare quando gli altri trattamenti non funzionano . La soluzione di desametasone deve essere una preparazione fresca (i conservanti causano dolore intenso). Una miscela dura circa 1 settimana. Bisogna fare due piccole incisioni, un per l'iniezione e la seconda per la ventilazione. Conservare il desametasone a caldo a temperatura ambiente (per evitare le vertigini). Iniettare il desametasone attraverso l'incisione posteriore (Minor , 2008). Il protocollo consigliato per la maggior parte dei pazienti si inizia con una sola iniezione intratympanic di desametasone (12 mg/ml). Follow-up in 2-3 settimane. Ripetere l'iniezione a 6-8 settimane se si ripete la vertigine. (Minor, 2008)
Risultati TABELLA 1-11
Varianti nella procedura degli steroidi intratimpaniciLa maggior parte dei professionisti utilizzano un semplice protocollo per le iniezioni con gli steroidi, iniettati a intervalli più lunghi o settimanali. Tuttavia, i metodi di maggior successo riportati fino ad oggi, come gli studi di Sennaroglu e Boleas, implicano periodi più lunghi di somministrazione.Il Desametasone ha l'emivita più lunga: 36-54 ore. Ci si aspetterebbe che gli steroidi nell'orecchio interno dovrebbero persistere per un periodo più breve rispetto al corpo umano, perché nell'orecchio interno, gli steroidi in generale non sono in equilibrio con il corpo. Così, si potrebbe pensare che tutti i protocolli con un dovrebbero con una sola iniezione dovrebbero probabilmente fallire.Alcuni degli steroidi sembrano causare più dolore rispetto ad altri. Il Desametasone sembra di essere il più tollerato, alla una dose di 12-24 mg / ml. E’ stato segnalato da Parnes che il Solumedrol sia il più doloroso (1999).
Steroidi autogestiti (Self-administered steroids )La più semplice procedura (e meno costoso) segnalato finora è quella di Sennaroglu et al (2001). Essi avevano avuto un paziente che si somministrava desametasone semplicemente attraverso un tubo di ventilazione. Un tubo viene posto nel quadrante posterio-inferiore del TM. I pazienti sono istruiti a stare sul fianco interessato mentire e ad istillare 5 gocce nell'orecchio interessato una volta ogni due giorni. Dopo l'instillazione, sono a giacere con l'orecchio dritto per 15 minuti. Viene utilizzata una bassa concentrazione di desametasone - 1 mg/ml. Questo è molto inferiore alla quantità (24 mg/ml) che viene utilizzata quando il farmaco viene iniettato.Complicanze della ITS.Mentre generalmente si pensa che la ITS sia una tecnica sicura, ci sono molte possibili complicazioni (probabilmente minori) (vedi Doyle et al., 2004). I rischi comuni sono il dolore, vertigini di breve durata, episodi di otite media e perforazioni della membrana timpanica. Il dolore durante l'inserimento del farmaco è comune. Questo non è un fenomeno inaspettato in quanto la puntura in qualsiasi parte del corpo con aghi è solito doloroso. Il dolore dovuto alle gocce stesse è raro, soprattutto se viene utilizzato il desametasone, ma i conservanti presenti nelle gocce possono essere dolorosi. L'otite media (Otitis media) è stato segnalata in solo 1 su 24 pazienti, utilizzando il metodo di Sennaroglu et al (gocce attraverso tubo). Sembra che sia ancora più raro, in quei pazienti, in cui vengono somministrate direttamente le iniezioni. Quando si verifica di otite media di un paziente in cui è presente un drenaggio , è possibile utilizzare gocce di antibiotico nell'orecchio , come ad esempio gocce di Floxin (antibiotico fluorochinolonico). La perforazione del timpano è una complicanza possibile. Gli steroidi compromettono la guarigione della ferita e ci si potrebbe aspettare un chiusura della perforazione più lenta. Il rischio di perforazione è aumentata dalla presenza delle fibre radiali della membrana timpanica . Questa complicazione in generale può essere gestita facilmente da un otolo e la perforazione può essere chiuso Vertigini. Un vertigini temporanea può verificarsi quando le fiale utilizzate non hanno la stessa temperatura del corpo, o se le soluzioni contengano lidocaina. Molti pazienti sono in grado di camminare senza aiuto dopo 20-30 minuti dalla somministrazione delle iniezioni. Non sono stati segnalati disturbi dell'equilibrio e vertigini permanenti. Perdita dell'udito: la maggior parte dei medici che utilizza steroidi intratimpanici riferiscono che non c'è poco o quasi nessun rischio di perdita dell'udito (Doyle et al, 2005). Costo: Questo può essere un metodo molto costoso per trattare la malattia di Meniere. I chirurghi otologi statunitensi effettuano una fattura di $3000 per questa procedura di 30 minuti, possibilmente ripetuta 4 volte all'anno. Altri simili metodi di trattamento Menieres, come invece ad esempio l'utilizzo di gentamicina, a lo stesso costo per iniezione ma generalmente non è necessario fare più iniezioni . Così, il costo , per il sistema sanitario, di trattamento con la gentamicina è molto più basso rispetto al trattamento steroideo. Errori: La ITS può fallire per vari motivi :
o Compressione microvascolare (microvascular compression ) o Sindrome vertiginosa scarsamente definita o Meccanismo di Meniere che non risponde di steroidi
Dove praticare il trattamento steroideo intratimpanico L’ITS è un trattamento emergente. Generalmente viene fornito dai medici dell'orecchio (Otologi - una sotto specialità della otorinolaringoiatria). Le varianti sono comuni, e molti delle varianti sembrano che non siano meglio del placebo. Consigliamo un'attenta indagine del protocollo offerto dai vostri professionisti locali. Siamo favorevoli alla durata più lunga metodi sopra descritti. Siamo sicuri che qualche otologo può monitorare da vicino il trattamento.
RISULTATI (CASANI) Riguardo all’efficacia del cortisone intratimpanico nella MdM, i risultati della letteratura sono discordanti e non facilmente comparabili tra loro vista la notevole diversità in termini di tipo e dosaggio di steroide usato, protocollo di applicazione, tempi di follow-up ecc). Un trial prospettico ha riportato una buona percentuale di controllo delle crisi vertiginose utilizzando DMZ (12 mglml) con ripetute serie di trattamento, tanto che gli Autori propongono una sorta di titration protocol ipotizzando che lo steroide intratimpanico induca t.ma temporanea remissione della sintomatologia (Boleas-Aguirre et al., 2007); al ripresentarsi delle crisi il paziente può quindi essere sottoposto nuovamente al trattamento allo scopo di accelerare la naturale spontanea remissione della malattia. All’opposto un recente studio comparativo tra DMZ e gentamicina a basso dosaggio nel trattamento della malattia di Mènière porta a conclusioni opposte: pur in assenza di effetti collaterali di rilievo, lo steroide ha evidenziato una scarsa efficacia nel controllo della vertigine (Casani et al., 2012),
Bibliografia riferita al trattamento intratimpanico con steroidi:
Steroidi per perdita dell’udito o vertigini (Steroids for Hearing loss or Vertigo)Timothy C. Hain, MD:July 26, 2009 Gli steroidi sono comunemente prescritti per la perdita improvvisa dell'udito, (sudden hearing loss),così come per malattie autoimmuni orecchio interno (autoimmune inner ear disease) e per la neurite vestibolare( vestibular neuritis). Lo scopo di questa pagina è quello di descrivere la metodologia abituale. Non discutiamo sulla efficacia o la validità delle loro indicazioni.
I farmaci più comunemente utilizzati sono: TABELLA 1-12
C'è una differenza molto piccola rispetto al risultato finale con questi farmaci e per gli effetti collaterali, ma differiscono per potenza e durata di azione, e per questo motivo, la dose deve essere regolata. Nella maggior parte dei casi, l'obiettivo sarà di iniziare con un equivalente di 1 mg/kg di prednisone (cioè circa 60 mg/giorno). IL decadron orale sembrerebbe una cattiva scelta in quelle condizione in cui sono desiderabili effetti rapidi come nella perdita improvvisa della funzionalità uditiva o nella neurite vestibolare, in quanto per la sua lunga emivita, ci vogliono 20 giorni per raggiungere dello stato stazionario. Naturalmente, si può regolare il protocollo per dare all'inizio più farmaco , come è il caso con il "medrol dose pack". Il più comune metodo di somministrazione è quello orale. Non verrà affrontato il problema della somministrazione di endovenosa (più veloce e più forte, utilizzato qualche volta in quel situazioni in cui i sintomi sono molto gravi, come la sordità bilaterale associate a malattie autoimmuni orecchio interno). La somministrazione attraverso il timpano è stata discussa altrove Questo metodo ha il vantaggio di molto meno effetti collaterali, ma gli svantaggi di un costo molto più elevato e la necessità di un visita con degli otoneurologi per le iniezione intra timpaniche. Per il metodo orale, ci sono quattro protocolli comuni che si usano: Ad impulso breve e debole - ad esempio - confezione dose di Medrol (circa 1 / 2 mg / kg equivalenti)
Il metodo più sicuro, più facile e più conveniente di utilizzare gli steroidi è quello di utilizzare una confezione di medrol (metilprednisolone) medrol (methylprednisolone) dose pack. Questa è una scheda che contiene 6 giorni di steroidi, che vengono ridotti ogni giorno . La graduale diminuzione della quantità di steroidi ogni giorno viene chiamata "cono". La ragione per fare questo è di consentire che le ghiandole surrenali del paziente, che solitamente il eliminano gli steroidi, tornare gradualmente a fornire in proprio gli steroidi al paziente. Il Medrol è leggermente più forte del prednisone, così per convertire questo in "prednisone", quando si utilizza la dose di 4 mg-pack, uno ha appena al multiplo di 5. In altre parole, il medrol dose pack è l'equivalente di 30 mg di prednisone, si assottiglia fino a 0, in una settimana. Perché il dose pack di medrol non contiene di solito 1 mg/kg di steroidi per la maggior parte dei pazienti, può essere semplicemente un intervento troppo "debole" per ottenere una buona indicazione se è presente una condizione di reattività agli steroidi. Per le persone in cui è indicata una maggiore quantità di steroidi viene selezionato un protocollo più lungo e più intenso . In generale, si inizia con l'equivalente di 1 mg/kg di prednisone, si mantiene con un "impulso" di diverse settimane o qualche mese e poi si riduce verso il basso (in 21 giorni o 30 giorni). Gli impulsi richiedono coni più lunghi. Controllare la pressione sanguigna per assicurarsi che non diventi troppo basso e spesso sono richieste visite di follow-up visite durante il periodo di somministrazione . Alcuni pazienti sono "steroide dipendenti". Ad esempio, ogni volta che la dose di steroidi è ridotta al di sotto di una soglia, la funzionalità uditiva comincia a deteriorarsi nuovamente. In questo tipo di pazienti , viene effettuato un tentativo di trovare un farmaco steroide con risparmio di sostituzione di steroidi (ad esempio metotrexato o Enbrel), ma nel frattempo, gli steroidi sono ridotti ad un livello più basso. Questo è comunemente circa 5-10 mg/die di predisone. Gli steroidi hanno molti effetti collaterali, che sono più comuni con le somministrazioni più lunghe .Quelli comuni nel breve periodo (cioè 7 giorni) includono:
· Aumento della pressione sanguigna · Ritenzione di liquidi · Sensazione di benessere (perdita di dolori articolari, per esempio). · Deterioramento o induzione temporanea del diabete, glicemia alta · Insonnia, sbalzi d'umore
Problemi che possono verificarsi dopo somministrazione più lunga , oltre a quelli sopra riportati, possono essere :
· Aumento di peso con gonfiore alle caviglie e accumulo di grasso attorno al centro del corpo, con faccia di luna. · Debolezza alle gambe (miopatia da steroidi) · Cataratta · Aumento del rischio di infezioni · Soppressione delle ghiandole surrenali, bassa pressione sanguigna e altri problemi durante la somministrazione . · Ecchimosi, pelle sottile · Perdita di calcio dalle ossa · Necrosi asettica dell'anca References
21)Terapia chirurgica Chirurgia del Sacco Endolinfatico Questo intervento, introdotto da Portmann nel 1927 prima ancora della scoperta dell’origine idropica della MdM, successivamente modificata da Shambaugh negli anni Sessanta [1966].rappresenta forse la modalità di trattamento più controversa tanto che Schuknecht (1992) lo considera uno dei “miti della otochirurgia”. La sacculotomia mira a ridurre la pressione endolinfatica attraverso la creazione di una fistola tra il sacculo e la cassa del timpano o gli spazi perilinfatici Le indicazioni e le modalità tecniche delle molte varianti proposte nel tempo si basano schematicamente su quattro ipotesi patogenetiche:
Qualunque sia la tecnica utilizzata, i risultati riportano un miglioramento dei sintomi nel 50-80% dei casi (Glasscock ME, et al1984;Paparella MM, Hanson DG 1975;Portmann G.,1927); anche a lungo termine [ Telischi FF, Luxford WM 1993 ). Questo miglioramento, tuttavia, sembra sfumare nel corso del tempo (Cody DT, McDonald TJ ,1983/1983; Maddox HE 1977) presumibilmente perché la breccia chirurgica evolve ineluttabilmente verso una fibrosi che tende a occludere secondariamente lo shunt. La funzione uditiva, teoricamente rispettata, per alcuni sembra deteriorarsi nel postoperatorio nel 35% dei casi (Cody DT, McDonald TJ ,1983) I sostenitori della chirurgia del sacco endolinfatico raccomandano di intervenire il prima possibile nel corso della malattia di Ménière, meglio prima che compaia un'iporeflessia vestibolare definitiva. Tuttavia, non è dimostrato che il drenaggio del sacco possa ripercuotersi sul sistema endolinfatico a monte e, in tal modo, eliminare l'idrope. L'analisi della letteratura non permette di trarre conclusioni sulla reale efficacia di questa tecnica chirurgica. Così, è stato dimostrato che la chirurgia del sacco endolinfatico non era più efficace rispetto a un intervento placebo (mastoidectomia semplice) Ruckenstein MJ, et al 1991;Schuknecht HF1992 ; Thomsen J,et al 1981 ), anche a lungo termine ( Bretlau P, et al,1984/1989 ). Sacculotomie
§ il posizionamento di un chiodo transplatinare può, secondo alcuni Autori Cody DT, McDonald TJ ,1983;assicurare la pervietà permanente della fistola sacculare, decomprimendo automaticamente il sacculo che viene a forarsi sul chiodo ogni volta che si distende. L'efficacia di questa tecnica non è stata ancora provata (Thomsen J 1986 ) . § la cocleo-sacculotomia è stata proposta da Schuknecht nel 1982, considerando che una fistola endoperilinfatica è solo in grado di prevenire le dilatazioni e le rotture recidivanti del labirinto membranoso, giacché le fistole del canale cocleare sono permanenti, a differenza di quelle del vestibolo membranoso (Kimura RS 1984);Praticata a uno stadio precoce, la fistola del canale cocleare sarebbe compatibile con un udito normale per le frequenze non corrispondenti alla zona lesa. Tecnicamente, l'Autore introduce un uncino attraverso la finestra cocleare in direzione della finestra vestibolare, attraversando in un secondo tempo la lamina spirale, il canale cocleare e il sacculo dilatati.
Diverse sono le tecniche di chirurgia del sacco: incisione, shunt subaracnoideo, decompressione e shunt mastoideo (più utilizzato). Tuttavia la dimostrazione anatomopatologica che l’ostruzione delle vie endolinfatiche è presente a livello prossimale rispetto al sacco e la quasi certa ostruzione da parte di tessuto fibroso di ogni elemento drenante, rende poco verosimile l’efficacia delle procedure di shunt, tanto che, uno studio con follow-up a 9 anni ha evidenziato come questa chirurgia non si mostrava superiore al placebo nel controllo delle crisi vertiginose (Bretlau et al., 1989). All’opposto altri studi sembrano riportare una discreta efficacia delle procedure di shunt endolinfatico nel controllo dei sintomi della MdM (Derebery et al., 2010), nonostante l’evidenza istopatologica di persistenza dell’idrope nelle ossa temporali di soggetti menierici sottoposti a questo tipo di chirurgia (Chung et al., 2011),
Labirintectomia
Neurectomia Vestibolare Rispetto alla labirintectomia, la neurectomia vestibolare consente un ottimale controllo della vertigine con il vantaggio di preservare l’udito nei casi in cui la residua funzione cocleare sia sufficiente per una buona discriminazione vocale. Presenta tuttavia lo svantaggio di essere gravata da un maggior numero di complicanze. Diverse sono le tecniche utilizzate: — approccio attraverso la fossa cranica media (Gavilan e Gavilanl, 1984), estremamente efficace nel controllo della vertigine ma complesso ed associato ad un elevato rischio di danni al labirinto, al nervo faciale ed al SNC; — approccio retrolabirintico per via transmastoidea (Silverstein e Norrell, 1980) che presenta un minor rischio di complicanze (eccetto un 1000 di rischio di hstola liquorale) ma meno efficace nel controllo della vei tiiine. forse perché la sezione (leI nervo av\ iene nel condotte) uditivo interno prima della sua divisione dal ramo cocleare; — approccio per via retromastoidea (suboccipitale) (AlcKenna et al., 1996): permette una ottimale visualizzazione del nervo vestibolare da cui deriva un controllo sostanziale o completo della vertigine nel 85-95% dei pazienti con complicanze piuttosto rare. Una variante di questa tecnica da cui deriva un minor tasso di complicanze endocraniche, permette di sezionare il nervo vestibolare nel suo decorso dentro il condotto uditivo interno attraverso una sua apertura (Silverstein et al., 1987). Le complicanze sono quelle proprie di tutte le vie d'accesso dalla fossa posteriore: emorragia, otoliquorrea, meningite, ecc. La scelta tra queste differenti vie di accesso si basa sull'età del paziente, sullo stato del suo udito e sull'esperienza del chirurgo. I risultati, tutti simili [23, 27, 52], testimoniano una scomparsa delle crisi vertiginose rotatorie in oltre il 95% dei casi. Grazie alla sezione delle anastomosi acustico-facciali l'udito è teoricamente conservato, perfino migliorato. Non è raro tuttavia osservare un deterioramento inspiegabile dell'udito nelle fasi postoperatorie immediate o tardive. In particolare, può persistere uno stato d'instabilità, il cui grado e durata sembrano in funzione delle capacità di compensazione centrale dell'individuo e di un'efficace pratica di rieducazione vestibolare postoperatoria [174]. Nel postoperatorio, si nota spesso il verificarsi di crisi prive della loro componente vertiginosa. Ciò dimostra che la neurectomia vestibolare rimane un intervento meramente sintomatico, che non incide sul meccanismo patogenetico dell'idrope e, quindi, sull'evoluzione naturale della malattia e che non impedisce, pertanto, la comparsa dell'ipoacusia fluttuante. Le sue indicazioni sono, inoltre, le vertigini invalidanti che si ripercuotono in modo grave sulla vita sociale e professionale, resistenti alle terapie sistemiche, con una buona funzione uditiva residua. Alcuni propongono questo intervento da subito, mentre altri ricorrono ad esso solo in caso di fallimento della labirintectomia chimica. Dall’analisi dei dati suesposti è possibile concludere che nei pazienti con MdM in cui la terapia medica si è mostrata del tutto inefficace il trattamento con gentamicina intratimpanica, utilizzando la metodica di “titration” o con basso dosaggio, rappresenta la metodica di prima scelta nella IvldM “intrattabile”, dal momento che offre un controllo della vertigine in più deIl’85% dei casi con minimi rischi di danno uditivo. I pazienti che non rispondono positivamente alla gentamicina intratimpanica potrebbero essere sottoposti ad una esplorazione chirurgica endoscopica dell’orecchio medio allo scopo di verificare ed eliminare eventuali ostruzioni anatomiche che impediscano l’accesso del farmaco alla finestra rotonda e da qui all’QI. In quella piccola percentuale di pazienti nei quali le crisi vertiginose ricorrono precocemente nonostante ripetuti cicli di gentamicina intratimpanica, si pone l’indicazione ad una ablazione chirurgica attraverso la neurectomia vestibolare specie in presenza di residui uditivi utilizzabili ad esempio a fini protesici. La labirintectomia, comportando un minor rischio di complicanze (fistola liquorale, cefalea, paralisi facciale, ecc) è da preferire nei pazienti con perdita uditiva totale o subtotale; peraltro questa metodica lascia intatta la possibilità di ricorrere in un secondo tempo all’applicazione di un impianto cocleare. Nonostante il basso rischio di complicanze il cortisone intratirnpanico e la chirurgia del SE consentono una percentuale di controllo della vertigine non superiore al placebo per cui il loro utilizzo può essere riservato ai casi di MdM bilaterale o laddove il paziente rifiuti il trattamento ablativo farmacologico o chirurgico.
22) Evoluzione EVOLUZIONE • Possibile bilateralizzazione Kitahara M (1991) . • Catastrofe otolitica di Tumarkin (1936) Odkvist , Bergenius (1988): improvvisa caduta non associata a vertigine nè a perdita di coscienza, a volte caratterizzata da lateropulsione, determinata da brusca alterazione degli input maculari (variazione della pressione endolintatica?) con conseguente alterazione dei riferimenti gravito-inerziali e inappropriati aggiustamenti posturali.
EPIDEMIOLOGIA DELLE MALATTIE DI MÉNIÈRE: II°APPROFONDIMENTO Vi è un notevole disaccordo nella letteratura mondiale circa l'incidenza (nuovi casi / anno) e la prevalenza (tutti i casi della popolazione) della malattia di Meniere. Per riassumere, sembra che tale malattia Menieres ha una prevalenza di circa 200 casi/100 000 persone negli Stati Uniti, o in altre parole, circa 0,2% della popolazione ha la malattia di Meniere. La prevalenza può variare a livello internazionale, possibilmente essendo inferiore di quanto un fattore 10 in alcune popolazioni. La prevalenza aumenta con l'età, piuttosto linearmente, fino all'età di 60 anni.
l'autore, Dr. Timothy Hain , che ha una grande esperienza con Meniere. Semplicemente guardando l'età in soggetti con diagnosi di Meniere, in base al sesso (blu sono donne), produce il grafico qui sopra riportato. Naturalmente questo grafico è tratto dalla popolazione clinica, ma si può ragionevolmente riflettere la prevalenza di Meniere a Chicago nell’Illinois. Si dimostra ancora una volta prevalenza crescente con l'età fino a 60 anni di età. Per l'Inghilterra, Cawthorne e Hewlett (1954) riportarono 157 casi/100 000 casi sulla base dei registri di 8 pratiche generali in Inghilterra durante l'anno che termina a marzo 1952. Non è chiaro nella loro relazione se tali cifre riflettono l'incidenza o la prevalenza, anche se Arenberg et al suggeriscono che è l’incidenza (1980). Se fosse la prevalenza, questa cifra sarebbe molto simile a una cifra riportata per gli Stati Uniti da Wadislowvsky e soci, in seguito). Se incidenza, questa figura suggerisce una prevalenza molto più alta (circa .16 * 25%, o circa il 4% della popolazione). Pensiamo che questo è altamente improbabile. Mentre altri hanno anche suggerito un tasso di prevalenza più alto 1% (ad es Morrison, 1995; Harrison e Naftalin, 1968), sembra che ci sia poco di buono nella prova di questa affermazione. Goodman (1957) ha presentato dati che suggeriscono una prevalenza del 0,056%, che è simile alla figura trovano negli Stati Uniti da Wadislowvsky e soci. In Giappone ci sono stati diversi grandi studi epidemiologici. Secondo Watanabe (1988), la malattia di Meniere era raro fino al 1950.Dalla fine della seconda guerra mondiale, c'è stato un rapido aumento del numero di pazienti osservati con malattia di Meniere. In questi studi hanno definito Menieres come la combinazione di ripetuti attacchi di vertigine, fluttuante sintomi cocleari con le vertigini, e l'esclusione di altre malattie (Watanabe et al, 1995). Hanno riferito età media di insorgenza di 41-42 anni di età, con un picco di incidenza a 30-39 anni. La prevalenza era 16-17 per 100.000. Questa figura appare basso. Uno studio più recente di Shojaku e Watanabe (1997) ha trovato una prevalenza compresa tra 21,4 e 36.6/100, 000, che può essere ancora una stima bassa. Ci sono stati diversi studi di popolazione degli Stati Uniti. Nello studio Framingham, (Framingham, Mass, USA) 1,48% della popolazione ha affermato di avere una storia di malattia di Meniere (Moscicki et al, 1985). Questa grande figura prevalenza probabile deriva da una tendenza di molti medici accomunare tutti i casi di vertigini ricorrenti nella categoria della malattia di Meniere (Slater, 1988). Wladislavosky e soci, presso la Mayo Clinic hanno riportato una prevalenza nel 1980 nella popolazione di Rochester Minnesota di 218,2 casi/100, 000, e un tasso di incidenza di nuovi casi di 15.3/100, 000/anno. Essi hanno inoltre riferito un tasso di diagnosi fondamentalmente proporzionale alla età fino a 60 anni di età, con un successivo declino. Bilateralità è stata trovata nel 34% del loro gruppo. Essi hanno osservato che i tassi a Rochester MN appaiono inferiori a quelli segnalati in Inghilterra e in Svezia. In Finlandia, la prevalenza è stato segnalato per essere 43/100, 000 e incidenza era 4.3/100, 000 (Kotimaki et al, 1999). Questa cifra sembra bassa rispetto agli Stati Uniti e in Inghilterra. In Svezia, Stahle et al ha riportato l'incidenza per il 1973 di Menieres a Uppsala a 45/100, 000 population.This studio ha utilizzato anche criteri più rigorosi per la diagnosi di altri hanno avuto, ed è generalmente pensato per essere una sottostima. La malattia di Meniere, per i loro criteri, è di circa 4 volte più comune come l’otosclerosi . In Italia, Celestino e Ralli riportato un tasso di incidenza di 8/100, 000, e la stima che la prevalenza era di circa lo 0,4% della popolazione. Ciò fa supporre che la maggior parte delle persone con la Meniere vivono con la malattia, in media, per 50 anni. La loro distribuzione , non normalizzato per l'età della popolazione, viene alzata a 41-50. L'impressione generale è che entrambi i sessi sono ugualmente colpiti. Tuttavia ci può essere una differenza nella distribuzione dei pazienti gravemente disabili. Stahle (1976) ha osservato che il numero di maschi superano le femmine (206:150) in questo gruppo. Pochi dati disponibili sulla predisposizione razziale alla malattia di Meniere. Nel 1972 Nsamba ha riferito che la malattia di Meniere era rara in Uganda. Caparaosa (1963) ha riferito che la malattia di Meniere era prevalentemente una malattia della razza bianca e si è verificata solo raramente nei neri. D'altra parte, Kitahara e Futaki (1974) hanno trovato che l'incidenza della malattia di Meniere è quasi identico tra bianchi e neri americani i. La malattia di Meniere è rara nel sud-America (Wiet, 1979). Per riassumere, al momento non è chiaro se ci sono predisposizioni razziali alla malattia di Meniere. REFERENCES •Arenberg IK, Balkany TJ, Goldman G, Pillsbury RC 3rd. The incidence and prevalence of Meniere's disease -- a statistical analysis of limits. Otolaryngol Clin NA 13:5:697-601, 1980 •Caparosa RJ. Medical treatment of Meniere's disease, Laryngoscope 73, 66-72, 1963 •Cawthorne T, Hewlett A. Meniere’s Disease. Proc R. Soc Med, 47:663-670, 1954 •Celistino D, Ralli G. Incidence of Meniere’s disease in Italy. Am J Otology 12(2); 135-8, 1991 •Goodman WS. Aural vertigo: its diagnosis and treatment -- A survey of 268 cases. J. Larng and Otol, 71, 339-55, 1957 •Harrison MS, Naftalin L. Meniere’s disease. Mechanism and management. Springfield IL:CC Thomas, 1968 •Kitahara M, Futaki T. ethnic aspects of Meniere's disease. Equilib Res Suppl 1. 1971 •Kotimaki J, Sorri M, Aantaa E, Nuutinen J. Prevalence of Meniere disease in finland. Laryngoscope 109:748-753, 1999 •Morrison AW. Anticipation in Menieres disease. J. Laryngology and Otology, 109(6): 499-502, 1995 •Mosicki EK, Elkins EF, Baum HM, McNamara PM. Hearing loss in the elderly: an epidemiologic study of the Framingham Heart Study Cohort. Ear and Hearing 6(4):184-90, 1985 •Nsamba C (1972) A comparative study of the aetiology of vertigo in the African. J Laryng and Otol 86, 17-25 •Shojaku H, Watanabe Y.The prevalence of definate cases of Meniere's disease ... Acta Oto-laryngologica 528:94-6, 1997 •Slater. Vertigo. How serious are recurrent and single attacks ? Postgraduate medicine, 54, #5, 58-67, 1988 •Stahle J. Advanced Meniere's disease. Acta Otol 81: 113-119, 1976 •Stahle J, Stahle C, Arenberg IK. Incidence of Menieres disease. Arch Otol 104(2):99-102, 1978 •Watanabe I. Incidence of Meniere's disease including some other epidemiological data. In: Meniere's Disease: A comprehensive Appraisal. Edited by W. J. Oosterveld, 1983 (Wiley). •Watanabe Y, Mizokoshi K, Shojaku H, Watanabi I, Hinoki M, Kitahara M. Epidemiological and clinical characteristics of Menieres disease in Japan. Acta Otol (Supp) 519:206-10, 1995 •Wiet RJ. Patterns of ear disease in the south-western American Indian. Arch Otolaryng, 105, 381-5, 1979 •Wladislavosky-Waserman P, Facer G, et al. Meniere's disease: a 30-year epidemiologic and clinical study in Rochester, MN, 1951-1980. Laryngoscope 94:1098-1102, 1984
23) BIBLIOGRAFIA GENERALE GENERAL REFERENCES Adams J. Clinical implications of inflammatory cytokines in the cochlea: a technical note. Otol Neurotol 23:316-322, 2002 Abuzeid WM, Ruckenstein MJ.Spirochetes in otology: are we testing for the right pathogens? Otolaryngol Head Neck Surg. 2008 Jan;138(1):107-9. . Agrawal Y1, Minor LB. Physiologic effects on the vestibular system in Meniere's disease. Otolaryngol Clin North Am. 2010 Oct;43(5):985-93 Albers FW, Veldman JE, Huizing EH Early hair cell loss in experimental hydrops. Ann Otol Rhinol Laryngol 1987 ; 96 : 282-285 Alleman AM, Dornhoffer JL, Kaufman Arenberg I, Walker PD Demonstration of autoantibodies to the endolymphatic sac in Meniere's disease. Laryngoscope 1997 ; 107 : 211-215 [crossref] Altman F, Kornfeld M Histological studies of Meniere's disease. Ann Otol Rhinol Laryngol 1965 ; 78 : 915-943 Altman F, Fowler E Histological findings of Meniere's syndrome complex. Ann Otol Rhinol Laryngol 1943 ; 52 : 52-80 Anderson JP, Harris JP. Impact of Meniere's disease on quality of life. Otol Neurotol 22:888- 894,2001 Andersson G, Hagnebo C, Yardley L Stress and symptoms of Meniere's disease: a time-series analysis. J Psychosom Res 1997 ; 43 : 595-603 [crossref]Andrews JC, Honrubia V Vestibular function in experimental endolymphatic hydrops. Laryngoscope 1988 ; 98 : 479-485 Angelborg C, Klockhoff I, Stahle J The caloric response in Meniere's disease during spontaneous and glycerin-induced changes of the hearing loss. Acta Otolaryngol 1971 ; 71 : 462-468 [crossref] Antoli-Candela F The histopathology of Meniere's disease. Acta Otolaryngol [suppl] 1976 ; 340 : 1-42 Arenberg IK, Balkany TJ, Goldman G, Pillsbury RC 3rd. The incidence and prevalence of Meniere's disease -- a statistical analysis of limits. Otolaryngol Clin NA 13:5:697-601, 1980 Arenberg IK, Stroud MH, Spector GJ, Carver WF The salt loading provocative glycerol test for the early diagnosis of auditory endolymphatic hydrops (Meniere's disease). Rev Laryngol Otol Rhinol 1974 ; 95 : 709-719 Arenberg IK, Marovitz WF, Shambaugh GE The role of the endolymphatic sac in the pathogenesis of endolymphatic hydrops in man. Acta Otolaryngol [suppl] 1970 ; 275 : 1-49 Arnold W, Niedermeyer HP. Herpes simplex virus antibodies in the perilymph of patients with Meniere's disease. Arch Otol HNS 123(1):53-6, 1997 Arslan M Ultrasonic selective irradiation of the inner ear windows as a new treatment of vertigo and tinnitus. Acta Otolaryngol 1968 ; 65 : 224-235 [crossref] Arweiler DJ, Jahnke K, Grosse-Wilde H (1995) Menière disease as an autosome dominant hereditary disease [in German]. Laryngorhinootologie. 74: 512-515. Aw ST, Halmagyi GM, Curthoys IS, Todd MJ, Yavor RA Unilateral vestibular deafferentation causes permanent impairment of the human vertical vestibulo-ocular reflex in the pitch plane. Exp Brain Res 1994 ; 102 : 121-130 Ayache D, Nengsu Tchuente A, Plouin-Gaudon I, Vasseur J, Elbaz P Assessment of perilymphatic pressure using the MMS-10 tympanic membrane displacement analyser (Marchbank's test) in patients with Meniere's disease: preliminary report. Ann Otolaryngol Chirurgie Cervicofac 2000 ; 117 : 183-188 Bagger-Sjobak D Effects of streptomycin and gentamycin on the inner ear. Am NY Acad Sci 1997 ; 830 : 120-129 Baloh RW, Jacobson K, Winder T Drop attacks with Meniere's syndrome. Ann Neurol 1990 ; 28 : 384-387 [crossref] Bance M, Mai M, Tomlinson D, Rutka J The changing direction of nystagmus in acute Meniere's disease: pathophysiological implications. Laryngoscope 1991 ; 101 : 197-201 Barbara M, Monini S, Chiappini I, Ronchetti F, Raffa S, Tonisi MR (2007) Perisaccular Vascular Obstruction During an Acute Attack of Meniere’s Disease. The Mediterranean Journal of Otology Vol 3 Number 1 January. Beck C, Schmidt CL Ten-year experience with intratympanically applied streptomycin (gentamicin) in the therapy of Morbus Meniere. Arch Otorhinolaryngol 1978 ; 221 : 149-152 [crossref] Bernstein J Occurrence of episodic vertigo and hearing loss in families. Ann Otol Rhinol Laryngol 1965 ; 74 : 101-111 Birgerson L, Gustavson KH, Stahle J Familial Meniere's disease: a genetic investigation. Am J Otol 1987 ; 8 : 323-326 Black F.O., Effron M.Z., Burns D.S. Diagnosis and management of drop attacks of vestibular origin: Tumarkin's otolithic crisis. Otolaryngol Head Neck Surg 1982 ; 90 : 256-262 Bonflls, P.,Uziel,A.,& Pujol,R.; Evoked otoacoustic emissions from adults and infants: clinical applications Acta Otolaryngologica, 1988b 105, 445—449 Brandt T Drug and vertigo. In: T Brandt (Ed.) Vertigo. Its multisensory syndrome. London : Springer-Verlag: 1991; 213-228. Brandt T Meniere's disease. In: T Brandt (Ed.) Vertigo. Its multisensory syndrome. London : Springer-Verlag: 2000; 83-98 Braun, M lmpediment of basilar membrane motion reduces overload protection but not threshold sensitivity: evidence from clinical an experimental hydrops Hearing Research, 1996, 97, 1—10 Bremond G, Magnan J, Milliet JR La neurotomie vestibulaire par voie postérieure rétro-sigmoïde. Ann Otolaryngol Chir Cervicofac 1984 ; 101 : 103-107. Brenner M, Hoistad D, Hain TC. Prevalence of thyroid dysfunction in Meniere's Disease. Archives of Oto HNS, 130/2 226-228 (2004) Bretlau P, Thomsen J, Tos M, Johnsen NJ Placebo effect for surgery in Meniere's disease : nine-year follow-up. Am J Otol 1989 ; 10 : 259-261 [crossref] Bretlau P, Thomsen J, Tos M, Johnsen NJ Placebo effect in surgery for Meniere's disease: a three-year follow-up study of patients in a double blind placebo controlled study on endolymphatic sac shunt surgery. Am J Otol 1984 ; 5 : 558-561 Brown DH, McClure JA, Dowar-Zapolski Z The membrane rupture theory of Meniere's disease - is it valid? Laryngoscope 1988 ; 98 : 599-601 Caparosa RJ. Medical treatment of Meniere's disease, Laryngoscope 73, 66-72, 1963 Canonni M, Pech A, Zanaret M, Thomassin JM, Scavennec C, Morlec M , e al. La neurectomie vestibulaire dans le traitement de la maladie de Ménière. Résultats et commentaires à propos de 77 cas. Ann Otolaryngol Chir Cervicofac 1985 ; 102 : 551-560 Carey JP. Menière’s disease, In: Eggers SDZ, Zee DS, editors. Verrigo and Imbalance: Clinical Neurophysiology of the Vestibular System. Handbook of Clinical Neurophysioiogy, Vol. 9. Amsterdam: Elsevier; 2010.p 371-81 Carlborg BI, Farmer JC Jr Effects of hyperosmolar solutions on the labyrinthine fluid pressures. I. Effects of glycerol and urea tests. Ann Otol Rhinol Laryngol [suppl] 1983 ; 104 : 1-16 Casani AP; Fattori B; Berrettini S; De Ciccio M; Vannucci G; Ghilardi P L. Delayed Endolynphatic Hydrops : an analysis of 12 cases . Acta Otorhinolaryngol Ital. 1993 Lug-Ago; 13 (4): 297-303. Casani A, Nuti D, Sellari Franceschini S e. al, Transtyinpanic gentamicin and fibrin tissue adhesive for treatment of unilateral Ménière’s disease: effects on vestibular function. Otoiaryngol Head Neck Surg 2005;133:929-35. Casani AP, Piaggi P, Cerchiai N, Seccia V, Seilari Franceschini S, Dailan I(2011) Intratyinpanic Treatment of Intractable Unilateral Maniere’s Disease: Gentamicin or Dexamethasone? ARandomized Controlled Trial. Otoiaryngol Head Neck Surg. (Nov 18). Cawthorne T, Hewlett A. Meniere’s Disease. Proc R. Soc Med, 47:663-670, 1954 Celestino D, Ralli G. Incidence of Meniere’s disease in Italy. Am J Otology 12(2); 135-8, 1991 Cianfrone, O., Ralli. O, Fabbricatore M. e al. Distontion pnoduct otoacoustic emissions in Meniene’s disease. Scandinavian Audiology, 2000;29,111-119 Chouard CH Le rôle des anastomoses acoustico-faciales dans la pathogénie de la maladie de Ménière. Ann Otolaryngol Chir Cervicofac 1972 ; 89 : 681-696 Chüden HG Erfahrungsbericht über Betahistin - Anwendung bei Morbus Meniere. Laryngol Rhinol 1978 ; 57 : 997-1007 Chung JW, Fayad J, Linthicum F, Ishiyama A, Merchant SN. Histopathology after endolymphatic sac surgery for Ménière's syndrome. Otol Neurotol. 2011 Jun; 32 (4): 660-4. Chung, W. H., Cho, D. Y., Choi, J. Y., & Hong, 5. H. (). clinical usefulness of extratympanic electrocochleography in the diagnosis of Ménière’s disease. Otology & Neurotology, 2004;25, 144—149. Claes J, van de Heyning PH Medical treatment of Meniere's disease: a review of literature. Acta Otolaryngol [suppl] 1997 ; 526 : 37-42 Clemis JD Allergy of the inner ear. Ann Allergy 1967 ; 25 : 370-376 Clemis JD, Valvassori G Recent radiographic and clinical observations on the vestibular aqueduct. A preliminary report. Otolaryngol Clin North Am 1968 ; 1 : 339-346 Cody DT, McDonald TJ Endolymphatic subarachnoid shunt operation for idiopathic endolymphatic hydrops. Laryngoscope 1983 ; 93 : 1018-1020 Cody DT, McDonald TJ Tack operation for idiopathic endolymphatic hydrops: an update. Laryngoscope 1983 ; 93 : 1416-1418 Coelho DH, Lalwani AK Medical management of Ménière’s disease. Laryngoscope. 2008;1 18:1099-108 Colman BH, Friedmann I, Wright JL Meniere's disease: electron microscopy of the vestibular ganglion and the end organs after ultrasound. Acta Otolaryngol 1975 ; 79 : 189-196 [crossref] Committee on hearing and equilibrium. Guidelines for the diagnosis and evaluation of therapy in Meniere's disease. Otolaryngol Head Neck Surg 1995 ; 113 : 181-185 Conraux C, Collard M L'électronystagmographie. Paris : Sandoz, 1982 Dauman R, Aran JM, Portmann M Summating potential and water balance in Meniere's disease. Ann Otol Rhinol Laryngol 1986 ; 95 : 389-395 Dauphin D, Laffont J, Garand G, Reynaud J Meniere's disease: petrous bone tomography, a new sign? Neuroradiology 1981 ; 22 : 15-18 [crossref] de Kleine. E. Mateijesen, D.J.i, Wit, H. P., & Albers, FW () Evoked otoacoustic emissions in patients with Menieres disease Otology and Neuro-Otology 2002; 23, 510-516. Densert B Effects of overpressure on hearing function in Meniere's disease. Acta Otolaryngol 1987 ; 103 : 32-42 [crossref] Densert B, Arlinger S, Ödkvist LM. New technology to control symptoms in Menière’s disease. Derebery MJ. Allergic and immunologic aspects of Meniere's disease. Otolaryngology HNS 114(3): 360-5, 1996 Derebery MJ, Rao S, Siglock TJ, Linthicum FH, Nelson RA Meniere's disease: an immune complex-mediated illness? Laryngoscope 1991 ; 101 : 225-229 Devaiah, A.K., Dawson, K. L, Ferraro, J. A., & Ator, G. A. . Utilìty of area curve ratio electrocochleography in early Meniere’s disease. Archives of OtolarYngology- Head&Neck Surgery, 2003;129, 547—551. Dickins JR, Graham SS Meniere's disease 1983-1989. Am J Otol 1990 ; 11 : 51-65 Dibiase P, Arriaga MA. Post-traumatic hydrops. Meniere's disease. Otolaryngologic clinics of North America. 30:6: Dec 1997. Dohlman GF The mechanism of secretion and absorption of endolymph in the vestibular apparatus. Acta Otolaryngol 1965 ; 59 : 275-288 [crossref] Driscoll CL, Kasperbauer JL, Facer GW, Harner SG, Beatty CW Low-dose intratympanic gentamicin and the treatment of Meniere's disease: preliminary results. Laryngoscope 1997 ; 107 : 83-89 [crossref] Eggermont JJ Summating potentials in Meniere's disease. Arch Otorhinolaryngol 1979 ; 222 : 65-75 Eggermont JJ, Schmidt PH Meniere's disease: a long-term follow-up study of hearing loss. Ann Otol Rhinol Laryngol 1985 ; 94 : 1-9 Enander A, Stahle J Hearing in Meniere's disease. Acta Otolaryngol 1967 ; 64 : 543-556 [crossref] Feldman AM, Brusilow SM Effects of cholera toxin on cohlear endolymph production. Model for endolymph hydrops. Proc Natl Acad Sci USA 1976 ; 73 : 1761-1764 [crossref] Fetoni AR, Piacentini R, Fiorita A, Paludetti G, Troiani D (2009) Water-soluble Coenzyme Q10 formulation (Q-ter) promotes outer hair celi survival in a guinea pig model of noise induced hearing loss (NITIL). Brain Res. 1257: 108-116. Fetterman, B L () Distortion product otoacoustic emissions and cochlear microphonics: relationships in patients with and without endolymphatic hydrops Laryngoscope, 2001;III, 946—954 Fick IA Decompression of the labyrinth. Arch Otolaryngol 1964 ; 79 : 447-458 Fisch U Vestibular nerve section for Meniere's disease. Am J Otol 1984 ; 5 : 1265-1271 Flourens P Recherches expérimentales sur les propriétés du système nerveux. Paris : Masson, 1842 Fraysse B, Alonso A, House W Meniere's disease and endolymphatic hydrops : clinical and histopathological correlations. Ann Otol Rhinol Laryngol [suppl] 1980 ; 76 : 1-22 Franz P, Hamzavi JS, Schneider B, Ehrenberger K.Do middle ear muscles trigger attacks of Meniere's disease? Acta Otolaryngol 2003 Jan;123(2):133-7 Friberg U, Stahle J, Svedberg A The natural course of Meniere's disease. Acta Otolaryngol [suppl] 1984 ; 406 : 72-77 Furman JM, Durrant JD, Hyre R, Kamerer DB Vestibular recruitment in Meniere's disease. Ann Otol Rhinol Laryngol 1990 ; 99 : 805-809 Futaki T, Kitahara M, Morimoto P A comparison of the furosemid and glycerol tests for Meniere's disease. Acta Otolaryngol 1977 ; 83 : 272-278 [crossref] Futaki T, Kitahara M, Morimoto P The furosemid test for Meniere's disease. Acta Otolaryngol 1975 ; 79 : 419-424 [crossref] Gacek RR, Gacek MR. Meniere's disease as a manifestation of vestibular ganglionitis. Am J Otolaryngol 2001 Jul-Aug;22(4):241-50 Gacek RR. Evidence for a viral neuropathy in recurrent vertigo. ORL J Otorhinolaryngol Relat Spec 2008;70(1) 6-14, 14-5 Gail Ishiyama, MD; Akira Ishiyama, MD; Robert W. Baloh, MD. Drop Attacks and Vertigo Secondary to a Non-Meniere Otologic Cause. Arch Neurol, 2003 Glasscock ME, Gulya AJ, Pensak ML, Black JN Medical and surgical treatment of Meniere's disease. Am J Otol 1984 ; 5 : 536-542 Glasscock ME, Miller GW, Drake FD, Kanok MM Surgical management of Meniere's disease with the endolymphatic subarachnoid shunt: a five-year study. Laryngoscope 1977 ; 87 : 1668-1675 Glasscock ME, Thedinger BA, Cueva RA, Jackson CG An analysis of the retrolabyrinthine vs the retrosigmoid vestibular nerve section. Otolaryngol Head Neck Surg 1991 ; 104 : 88-95 Godlowski Z Hyperosmosis of endolymph as primary pathogenic mechanism of Meniere's disease and its clinical management. Acta Otolaryngol [suppl] 1972 ; 229 : 1-36 Goodman WS. Aural vertigo: its diagnosis and treatment -- A survey of 268 cases. J. Larng and Otol, 71, 339-55, 1957 Guild S The circulation of the endolymph. Am J Anat 1927 ; 39 : 57-81 [crossref] Gussen R Meniere's disease: new temporal bone findings in two cases. Laryngoscope 1971 ; 81 : 1695-1707 Gussen R Saccule otoconia displacement into cochlea in cochleosaccular degeneration. Arch Otolaryngol 1980 ; 106 : 161-166 Gussen R Vascular mechanisms in Meniere's disease. Arch Otolaryngol 1982 ; 108 : 544-549 Hallpike C, Cairns H Observations on the pathology of Meniere's syndrome. J Laryngol Otol 1938 ; 53 : 625-655 Halmagyi GM Vestibular insufficiency following unilateral vestibular deafferentation. Aust J Otolaryngol 1994 ; 1 : 510-512 Halmagyi GM, Fattore CM, Curthoys IS, Wade S Gentamicin vestibulotoxicity. Otolaryngol Head Neck Surg 1994 ; 111 : 571-574 [crossref] Hallpike C, Cairns H Observations on the pathology of Meniere's syndrome. J Laryngol Otol 1938 ; 53 : 625-655. Hamann KF, Arnold W Meniere's disease. Adv Otorhinolaryngol 1999 ; 55 : 137-168 Harker LA, Rassekh CH Episodic vertigo in basilar artery migraine. Otolaryngol Head Neck Surg 1987 ; 96 : 239-250 Harris, F.P.. & Probst, R. ) Transiently evoked otoacoustic emissions in patients with Ménières disease Acta Otolaryngologica 1992, ;112, 36—44 Harris JP, Aframian D: Role of autoimmunity in contralateral delayed endolymphatic hydrops. Am J Otol 15:710-716, 1994 Harrison MS, Naftalin L. Meniere’s disease. Mechanism and management. Springfield IL:CC Thomas, 1968 Hausler R, Toupet M, Guidetti G, Basseres F, Montandon P Meniere's disease in children. Am J Otol 1987 ; 8 : 187-193 [crossref] Havia M, Kentala E. Progression of symptoms of dizziness in Ménière's disease. Arch Otolaryngol Head Neck Surg 2004;130:431-5. Heermann J Predominance of left ear in Ménière's disease, sudden deafness, inner ear damage, tinnitus and abnormally patent eustachian tube. Ear Nose Throat J 1993 ; 72 : 205-208 Henriksson NG, Gleissner L Vestibular activity on experimental variation of the labyrinthine pressure. Acta Otolaryngol 1966 ; 61 : 380-386 [crossref] Henriksson NG, Gleissner L, Johansson G Experimental pressure variation in the membranous labyrinth of the frog. Acta Otolaryngol 1966 ; 61 : 281-291 Hilding DA, House WF An evaluation of the ultrastructural findings in the utricule in Meniere's disease. Laryngoscope 1964 ; 74 : 1135-1148 Hinchcliffe R Personality profile in Meniere's disease. J Laryngol Otol 1967 ; 81 : 477-481 House WF Subarachnoid shunt for drainage of hydrops. A report of 146 cases. Laryngoscope 1965 ; 75 : 1547-1551 Honrubia V. Pathophysiology of Meniere's disease. Ménière's Disease (Ed. Harris JP) 231-260, 1999, Pub: Kugler (The Hague) Horner, K. C., C. Aurousseau, et al. (1989). "Long-term treatment with chlorthalidone reduces experimental hydrops but does not prevent the hearing loss." Acta Otolaryngol 108(3-4): 175-83. Huang TS, Lin CC Endolymphatic sac ballooning surgery for Meniere's disease. Ann Otol Rhinol Laryngol 1994 ; 103 : 389-394 [crossref] Hulshof JH, Baarsma EA Follow-up vestibular examination in Meniere's disease. Acta Otolaryngol 1981 ; 91 : 397-401 [crossref] Ikeda M, Sando I Vascularity of the endolymphatic sac in Meniere's disease. A histopathologic study. Ann Otol Rhinol Laryngol [suppl] 1985 ; 118 : 11-16 Ishiyama G 1 , López IA , Ishiyama A . Aquaporins and Meniere's disease. Curr Opin Otolaryngol Head Neck Surg. 2006 Oct;14(5):332-6 Itard JM. Traité des maladies de l'oreille et de l'audition. Paris : 1821 Jackler RK, Brackman DE Endolymphatic hydrops and Meniere's disease. In: Neurotology. Chicago : Mosby-Year book: 1994; 633-639. Jahnke K Fur Pathogenes des akuten Symptome des Morbus Meniere. Laryngol Rhinol Otol 1981 ; 56 : 402-406 Jansen VD, Russel RD Conservative management of Tumarkin's otolithic crisis. J Otolaryngol 1988 ; 17 : 359-361 Johnson LG Reissner's membrane in the human cochlea. Ann Otol Rhinol Laryngol 1971 ; 80 : 425-438 [crossref] Johnstone BN, Robertson D The physiology and biophysics of hydrops. In: KH Vosteen (Ed.) Meniere's disease, Pathogenesis, diagnostic and treatment. New York : Georg Thieme Verlag: 1981; 44-46. Jongkees LB Medical treatment of Meniere's disease. Acta Otolaryngol [suppl] 1964 ; 192 : 109-112 [crossref] Juhn SK 1 , Ikeda K , Morizono T , M Murphy . Pathophysiology of inner ear fluid imbalance. Acta Otolaryngol Suppl. 1991; 485: 9-14 Katsarkas A Hearing and vestibular dysfunction in Meniere's disease. Acta Otolaryngol 1996 ; 116 : 185-188 [crossref] Kaufman RS, Tonndorf J, Khanna S Short-term changes in cochlear microphones after perforation of the saccule in the cat. Laryngoscope 1966 ; 76 : 719-732 Kaufmann-Arenberg I, Gibson WP, Bohlen HK Improvements in audiometric and electrophysiologic parameters following non-destructive inner ear surgery utilising a valved shunt for hydrops and Meniere's disease. In: JB Jr Nadol (Ed.) Second international symposium in Meniere's disease. Amsterdam : Kugler and Ghedini: 1985; 545-561 Kayan A, Hood JD Neuro-otological manifestations of migraine. Brain 1984 ; 107 : 1123-1142 K.han M, Gross J, Haupt H, Jainz A, Nikiowitz P, Scherer H, Schinidt FP, K.lapp BF, Reisshauer A, Mazurek B (2007) A pilot clinical trial of the effects of coenzyme Q1O on chronic tinnitus aurium. Otolaryngol. Head Neck Surg 136: 72-77. 44. Kimura RS An update of our experiences on endolymphatic hydrops. In: Meniere's disease update. Hague : Kugler Publication: 1999; 31-36. Kimura RS Animal models of endolymphatic hydrops. Am J Otol 1982 ; 3 : 447-451 [crossref] Kimura RS Fistulae in the membranous labyrinth. Ann Otol Rhinol Laryngol 1984 ; 93 : 36-43 Kimura RS, Schuknecht HF Membranous hydrops in the inner ear of the guinea pig after obliteration of the endolymphatic sac. Pract Otorhinolaryngol 1965 ; 27 : 343-354 [crossref] Kimura RS, Trehey JA, Hutta J Vein of the vestibular aqueduct in the gerbil. Acta Otolaryngol 1996 ; 116 : 44-51 [crossref] Kinney SE, Sandridge SA, Newman CW. Long-term effects of Meniere's disease on hearing and quality of life. Am J Otol 1997 Jan;18(1):67-73. Kitahara M, Kodama A, Ozawa H, Izukura H Pressure test for the diagnosis of Meniere's disease. Acta Otolaryngol [suppl] 1994 ; 510 : 107-110 [crossref] Kitahara M Bilateral aspects of Meniere's disease. Acta Otolaryngol [suppl] 1991 ; 485 : 74-77 [crossref] Kitahara M, Futaki T. ethnic aspects of Meniere's disease. Equilib Res Suppl 1. 1971 Kitahara M (1991) Bilateral aspects of Menière’s disease: Menière’s disease with bilateral fluctuant hearing loss. Acta Otolaryngol (Stockh). Suppl. 485: 74-77. Kitahara T, Doi K, Maekawa C, Kizawa K, Horii A, Kubo T, Kiyama H. Meniere's attacks occur in the inner ear with excessive vasopressin type-2 receptors. J Neuroendocrinol. 2008 Dec;20(12):1295-300. Kitamura K, Kaminga C, Ishida T, Silverstein H. Ultrastructural analysis of the vestibular nerve in Meniere's disease. Auris Nasus Larynx 1997;24(1):27-30. Klockhoff I, Lindblom U Glycerol test in Meniere's disease. Acta Otolaryngol [suppl] 1967 ; 224 : 449-457 Kobayashi M, Fukaya T, Noda M The endolymphatic sac in patients with Meniere's disease: correlation between the MRI and the surgical findings. Acta Otolaryngol 2000 ; 120 : 955-959 [crossref] Kodama A, Sando I Dimensional anatomy of the vestibular aqueduct and the endolymphatic sac (rugose portion) in human temporal bones. Statistical analysis of 79 bones. Ann Otol Rhinol Laryngol [suppl] 1982 ; 96 : 13-20 Konradsson KS, Carlborg B, Grenner J, Tjernstrom O Electrocochleographic and audiometric evaluation of hypobaric effect in Meniere's disease. Laryngoscope 1999 ; 109 : 59-64 [crossref] Konradsson KS, Nielsen LH, Carlborg BI, Borgkvist B Pressure transfer between intracranial and cochlear fluids in patients with Meniere's disease. Laryngoscope 2000 ; 110 : 264-268 Kotimaki J, Sorri M, Aantaa E, Nuutinen J. Prevalence of Meniere disease in finland. Laryngoscope 109:748-753, 1999 Kristensen HK Meniere's disease. Pathology and pathogenesis. Acta Otolaryngol [suppl] 1962 ; 188 : 149-154 Kubo T, Doi K, Koizuka I, Takeda N, Sugiyama N, Yamada K , e al. Assessment of auditory and vestibular functions after vestibular neurectomy for Meniere's disease. Acta Otolaryngol 1995 ; 115 : 149-153 [crossref] Jablonka, A., Pospiech, L. & Orendorz-Fraczkowska,K. (Evaluation of glycerol test in Meniere’s disease with pure tone audiometry and distortion product otoacoustic emission. Otolaryngologia Polska, 2003;57, 731-737 Honrubia V. Pathophysiology of Meniere's disease. Meniere's Disease (Ed. Harris JP) 231-260, 1999, Pub: Kugler (The Hague) Lacour M, Barthelemy J, Borel L, Magnan J, Xerri C, Chays A, Ouaknine M. Sensory strategies in human postural control before and after unilateral vestibular neurotomy. Experimental Brain Research (2) 300-10, 1997. Lacour M, van de Heyning PH, Novotny M, Tighilet B (2007) Betabistine ia the treatment ofMénière’s disease. Neuropsychiatr Dis Treat. August; 3 (4): 429-440. Kusuki, M Sakashita, T., Kubo, T, et al. Changes in distortion product otoacoustic emissions from ears with Meniere’s disease. Acta Otolaryngologica Supplement, 1998;538, 78-89 Lange G Die intratympanale Behandlung des Morbus Meniere mit ototxischen Antibiotika. Laryngol Rhinol 1977 ; 56 : 409-414 Larsen HC, Angelborg C, Hultcranz E The effect of glycerol on the cochlear blood flow. ORL J Otorhinolaryngol Relat Spec 1982 ; 44 : 101-107 Lawrence M, McCabe BF Inner ear mechanics and deafness, special considerations of Meniere's syndrome. JAMA 1959 ; 171 : 1927-1932 Lee H, Cho YW. Auditory disturbance as a prodrome of anterior inferior cerebellar artery infarction. J. Neurol Neurosurg Psych 2003:74:1644-1648 Le Père DM Evaluation of a new symptomatic treatment for Meniere's disease. Clin Med 1967 ; 74 : 63-64 Lemis JD, Valvassori G Recent radiographic and clinical observations on the vestibular aqueduct. A preliminary report. Otolaryngol Clin North Am 1968 ; 1 : 339-346 Lermoyez M Le vertige qui fait entendre. Presse Méd 1919 ; 27 : 1-3 Li, Q., & Zhong, N. Diagnostic significance of transiently evoked otoacoustic emissions in Meniere’s disease Lin Chuang Er Bi Yan Hon i Ke Za Zhi, 1999;13,435-437 Lezius F, Adrion C, Mansmann U, Jahn K, Strupp M.High-dosage betahistine dihydrochloride between 288 and 480 mg/day in patients with severe Menière's disease: a case series. Eur Arch Otorhinolaryngol. 2011 Aug;268(8):1237-40 Lin M, Timmer FCA,Oriel BS. et al.Vestibular Evoked Myogenic Potentials (VEMP) Can Detect Asymptomatic Saccular Hydrops The Laryngoscope Volume 116, Issue 6, pages 987–992, June 2006 Linthicum F. Herpes simplex virus DNA in endolymphatic sacs in patients with Meniere's disease. The National Temporal Bone Registry Newletter, Winter 2001/2002, Vol 9, #2. Lonsbury-Martin. B.L., & Martin. G.K.. The clinical utility of distortion-product otoacoustic emissions. Ear and Hearing, 1990;11, 144—154 Lundquist PG Aspects of endolymphatic sac morphology and function. Arch Otorhinolaryngol 1976 ; 212 : 231-240 [crossref] Maddox HE Endolymphatic sac surgery. Laryngoscope 1977 ; 87 : 1676-1679 Magliulo, G. , Cianfrone. G.. Di Cello, P. & Tersigni, A. Early diagnosis of endolymphatic hydrops with distortion product otoacoustic emission Anales Otorrinolaringologicos lberoamericanus, 2004;31, 173—189 Maier and others. Middle ear pressure and dysfunction of the labyrinth: is there a relationship ? Annals of ORL 106(6): 478-82, 1997 Mamikoglu B, Wiet RJ, Hain T, Check IJ. Increased CD4+ T cells during acute attack of Meniere's disease.Acta Otolaryngol 2002 Dec;122(8):857-60 Marchbanks R Why monitoring perilymphatic pressure in Meniere's disease? Acta Otolaryngol [suppl] 1997 ; 526 : 27-29 [crossref] Martin, G K., Ohlms. L.A. Franklin, D.J. , et al. Distortion product emissions in humans: III. Influence of sensorineural hearing loss. Annals of Otology, Rhinology, and Laryngology, 1990;Suppl 147, 30—42 Mateijsen DJ, van Hengel PW, Krikke AP, van Huffelen WM, Wit HP, Albers FW Three-dimensional magnetic resonance imaging of the inner ear in patients with uni- and bilateral Meniere's disease. In: Meniere's disease update. The Hague : Kugler Publications: 1999; 571-580. McClure JA, Copp JC, Down-Zapolski Z Recovery nystagmus in Meniere's disease. Laryngoscope 1981 ; 91 : 1727-1737 Ménière P Mémoire sur des lésions de l'oreille interne donnant lieu à des symptômes de congestion cérébrale apoplectiforme. Gaz Méd Paris 1861 ; 38 : 597-601 Meyer ED Treatment of Meniere disease with betahistine dimesilate (Aequamen) - double-blind study versus placebo (crossover). Laryngol Rhinol Otol 1985 ; 64 : 269-272 [crossref] Mira E.Betahistine in the treatment of vertigo. History and clinical implications of recent pharmacological researches.Acta Otorhinolaryngol Ital. 2001 Jun;21(3 Suppl 66):1-7. Monsell EM, Brackmann DE, Linthicum FH Jr Why do vestibular destructive procedures sometimes fail? Otolaryngol Head Neck Surg 1988 ; 99 : 472-479 Morales-Luckie, E; Cornejo-Suarez, A; Zaragoza-Contreras, Ml A; Gonzalez-Perez, O..Oral Administration of Prednisone to Control Refractory Vertigo in Ménière's Disease: A Pilot Study Otology & Neurotology:September 2005 - Volume 26 - Issue 5 - pp 1022-1026 Moretz WH, Shea JJ, Orchik DJ, Emmett JR, Shea JJ Streptomycin treatment in Meniere's disease. Otolaryngol Head Neck Surg 1987 ; 96 : 256-259 Morgenstern C, Miyamoto HD Potential and cancer activity in experimental endolymphatic hydrops. Arch Otorhinolaryngol 1979 ; 222 : 273-274 [crossref] Morrison AW. Anticipation in Menieres disease. J. Laryngology and Otology, 109(6): 499-502, 1995 Morrison AW Predictive tests for Meniere's disease. Am J Otol 1986 ; 7 : 5-10 Mosicki EK, Elkins EF, Baum HM, McNamara PM. Hearing loss in the elderly: an epidemiologic study of the Framingham Heart Study Cohort. Ear and Hearing 6(4):184-90, 1985 Morrison AW, Johnson KJ (2002) Genetics (molecular biology) and Ménière’s disease Otolaryngol Clin North Am. 35:497-516. Murofushi T, Halmagyi GM, Yavor RA Intratympanic gentamicin in Meniere's disease: results of therapy. Am J Otol 1997 ; 18 : 52-57 Naganawa S, Komada T, Fukatsu H, et al (2006) Observationa of contrast enhancemeat in the cochlear fluid space of healthy subjects using a 3D-FLAIR{ sequence at 3 Tesla. Eur Radiol; 16: 733-737. Naganawa S, Sugiura M, Kawamura M, Fukatsu H, Sone M, Nakashima T (2008) Imaging ofEndolymphatic and Perilymphatic Fluid at 3T After Intratympanic Administration of Gadohnium-DiethyleneTriamine Pentaacetic Acid. AJNR An J Neuroradiol. Apr; 29(4): 724-6. Naito T Experimental studies on Meniere's disease. Jpn J Otol 1950 ; 53 : 19-20 Naito T. Clinical and pathological studies on Meniere's disease. Proceeding of the 60th annual meeting japan ORL society, 1959 : 1-65 Nsamba C (1972) A comparative study of the aetiology of vertigo in the African. J Laryng and Otol 86, 17-25 Oh A, Ishiyama A, Baloh RB. Vertigo and the enlarged vestibular aqueduct syndrome. J. Neurol 248:971-974, 2001 Ohlms, LA., Lonsbury-Martin, B.L. & Martin, G.K.,). Acoustic-distortion products: separation of sensory from neural dysfunction in sensorineural hearing loss in human beings and rabbits. Otolaryngology-Head and Neck Surgery. 1991;104,159-174 Oliveira CA, Bezerra RL, Araùjo MF, Almeida VF, Messias CI Meniere's syndrome and migraine incidence in one family. Ann Otol Rhinol Laryngol 1997 ; 106 : 823-829 Oosterveld WJ Betahistine dihydrochloride in the treatment of vertigo of peripheral vestibular origin. A double-blind placebo-controlled study. J Laryngol Otol 1984 ; 98 : 37-41 Paparella MM Pathology of Meniere's disease. Ann Otol Rhinol Laryngol 1984 ; 93 : 31-35 Paparella MM, Griebie MS Bilaterality of Meniere's disease. Acta Otolaryngol 1984 ; 97 : 333-337 Paparella MM, Hanson DG Endolymphatic sac drainage for intractable vertigo (method and experience). Laryngoscope 1975 ; 85 : 697-703 Park JC, Cohen GM Vestibular ototoxicity in the chick: effects of streptomycin on equilibrium and on ampullary dark cells. Am J Otol 1982 ; 3 : 117-127 [crossref] Parker W Meniere's disease. Etiologic considerations. Arch Otolaryngol Head Neck Surg 1995 ; 121 : 377-382 Pender D Gentamicin tympanoclysis: effects on the vestibular secretory cells. Am J Otol 1985 ; 6 : 358-367 [crossref] Perez R 1 , Chen JM , Nedzelski JM . The Status of the Contralateral Ear in Established Unilateral Menière's Disease,† The Laryngoscope ,Volume 114, Issue 8, pages 1373–1376, August 2004 Petermann W, Mulch G Long-term therapy of Meniere's disease. Comparison of the effects of betahistine dihydrochloride and hydrochlorothiazide. Fortschr Med 1982 ; 11 : 431-435 Peron DL, Kitamura K, Carniol PJ, Schuknecht HF Clinical and experimental results with focused ultrasons. Laryngoscope 1983 ; 93 : 1217-1221 Philiips JS, Westerberg B (2011) Intratympanic steroids for Ménière’s disease or syndrome. Cochrane Database Syst Rev. Jul 6; (7): CD008514. Pyykkö I , Zou J , Poe D , Nakashima T , Naganawa S.Magnetic resonance imaging of the inner ear in Meniere's disease.Otolaryngol Clin Nord Am. ottobre 2010, 43 (5): 1059-1080. Piquet JJ, Decroix G, Vanecloo FM Le test au mannitol dans la maladie de Ménière. J Fr ORL 1975 ; 24 : 511-517 Ponka, D Approach to managing patients with sulfa allergy. Use of antibiotic and nonantibiotic sulfonamides. Can Fam Physician. 2006 November 10; 52(11): 1434–1438. Portmann G Recherches sur la physiologie du sac et du canal endolymphatiques des Sélaciens. C R Soc Biol 1921 ; 85 : 1070-1080 Portmann G Vertigo surgical treatment by opening of the endolymphatic sac. Arch Otolaryngol 1927 ; 6 : 309-319 Pulec JL. Meniere's disease of syphilitic etiology. ENT journal 76(8) 508-10, 1997 Rahman MU, Poe DS, Choi HK. Etanercept therapy for immune-mediated cochleovestibular disorders: preliminary results in a pilot study. Otol Neurotol 22:619-624, 2001 Rahman MU, Poe DS, Choi HK. Autoimmune vestibulo-cochlear disorders. Curr Opin Rheumatol 2001 May;13(3):184-9 Rauch S Biochemical aspects of pathogenesis of Meniere's disease. Otolaryngol Clin North Am 1968 ; 1 : 369-374 Rauch SD, Merchant SN, Thediner BA. Meniere's syndrome and endolymphatic hydrops: double blind temporal bone study. Ann ORL 98(11):873-883, 1989 Rauch SD Clinical hints and precipitating factors in patients suffering from Meniere's disease. Otolaryngol Clin North Am. 2010 Oct;43(5):1011-7. Rivzi SS Investigations into the cause of canal paresis in Meniere's disease. Laryngoscope 1986 ; 96 : 1258-1271 Rosingh HJ, Wit HP, Sulter AM, Albers FW Longitudinal non-invasive perilymphatic pressure measurement in patients with Meniere's disease. ORL J Otorhinolaryngol Relat Spec 1997 ; 59 : 135-140 [crossref] Ruckenstein MJ and others. Immunologic and serologic testing in patients with Meniere's disease. Otol Neurotl 23:517-521, 2002 Ruckenstein MJ, Rutka JA, Hawke M The treatment of Meniere's disease: Torok revisited. Laryngoscope 1991 ; 101 : 211-218 Rudnick MD, Ginsberg IA, Huber PS Aminoglycoside ototoxicity following middle ear injection. Ann Otol Rhinol Laryngol [suppl] 1980 ; 89 (6 Pt 4) : 1-28 Sakashita, T., Kubo, T., Kusuki, M., et al. Patterns of change in growth function of distortion product otoacoustic emissions in Meniere’s disease Acta Otolaryngologica Supplement, 1998;538, 70-77 Sakashita, T., Kubo, T., Kyunai, K., et al. (). Changes in otoacoustic emission during the glycerol test in the ears of patients with Meniere’s disease Nippon Jibiinkoka Gakkai Kaiho, 2001;104, 682—693 Sando I, Ikeda M Pneumatisation and thickness of the petrous bone in patients with Meniere's disease. Ann Otol Rhinol Laryngol [suppl] 1985 ; 118 : 2-5 Sando I, Ikeda M The vestibular aqueduct in patients with Meniere's disease. A temporal bone histopathological investigation. Acta Otolaryngol 1984 ; 97 : 558-570 [crossref] Santos, P. M., R. A. Hall, et al. (1993). "Diuretic and diet effect on Meniere's disease evaluated by the 1985 Committee on Hearing and Equilibrium guidelines." Otolaryngol Head Neck Surg 109(4): 680-9. Sass, K. . Sensitivity and specificity of transtympanic electrocochleography in Meniere’s disease. Acta Oto-Laryngologica, 1998;118, 150—156. Savastino M, Marioni G, Aita M. Psychological characteristics of patients with Meniere's disease compared with patients with vertigo, tinnitus or hearing loss. ENT journal, 148-156, 2007 Savastano M, Maron MB, Mangialaio M, Longhi P, Rizzardo R. Illness behavior, personality traits, anxiety and depression in patients with Meniere's disease. J Otolaryngol 1996 Oct;25(5):329-333. Schaaf H, Seling B, Rienhoff NK, Laubert A, Nelting M, Hesse G. [Is recurrent loss of low frequency tone perception--without vertigo--a precursor of Meniere disease?] HNO 2001; 49: 543-7. Schessel DA, Nedzelski JM. Presentation of large vestibular aqueduct syndrome to a dizziness unit. J. Otolaryngol 21:265-269, 1992 Schindler RA, Horn KL, Jones PL, Maglio M The ultrastructure of endolymphatic sac in Meniere's disease. Laryngoscope 1979 ; 89 : 95-107 Schmalbrock P, Dailiana T, Chakeres DW, Oehler MC, Welling DB, Williams PM , e al. Submillimeter-resolution MR of the endolymphatic sac in healthy subjects and patients with Meniere's disease. AJNR Am J Neuroradiol 1996 ; 17 : 1707-1716 Segal, S., E. Eviatar, et al. (2003). "Is there a relation between acoustic trauma or noise-induced hearing loss and a subsequent appearance of Meniere's Disease? An epidemiologic study of 17245 cases and a review of the literature." Otol Neurotol 24(3): 387-91. Selivanova, O. A., H. Gouveris, A. Victor, et al. (2005). "Intratympanic dexamethasone and hyaluronic acid in patients with low-frequency and Meniere's-associated sudden sensorineural hearing loss." Otol Neurotol 26(5): 890-5. Selmani et al. Use of electrocochleography for assessing endolymphatic hydrops with Lyme Disease and Meniere's disease. Acta Otolaryngol 122(2) 173-8, 2002 Shen J Ruckenstein M Medical Treatment of Meniere's Disease, Menieres Disease: Evidence Outcomes: Evidence and Outcomes by Michael J. Ruckenstein Author, Publisher: Plural Publishing Inc; 1 edition (30 April 2010) , Shinkawa, H. and R. S. Kimura (1986). "Effect of diuretics on endolymphatic hydrops." Acta Otolaryngol 101(1-2): 43-52. Shojaku H, Watanabe Y.The prevalence of definate cases of Meniere's disease ... Acta Oto-laryngologica 528:94-6, 1997 Schuknecht HF Ablation therapy in the management of Meniere's disease. Acta Otolaryngol [suppl] 1957; 32 : 1 Schuknecht HF, Northrop C, Igarashi M Cochlear pathology after destruction of the endolymphatic sac in the cat. Acta Otolaryngol 1968 ; 65 : 479-487 [crossref] Schuknecht HF, Belal AA The utriculo-endolymphatic valve : its functional significance. J Laryngol Otol 1975 ; 89 : 985-996 Schuknecht HF Pathophysiology of endolymphatic hydrops. Arch Otorhinolaryngol 1976 ; 212 : 253-262 [crossref] Schuknecht HF Delayed endolymphatic hydrops. Ann Otol Rhinol Laryngol 1978 ; 87 : 743-748 Schuknecht HF Mondini dysplasia. A clinical and pathological study. Ann Otol Rhinol Laryngol [suppl] 1980 ; 89 (1 Pt 2) : 1-23 Schuknecht HF Cochleo-sacculotomy for Meniere's disease: theory, technique and results. Laryngoscope 1982 ; 92 : 853-858 Schuknecht 1W, Gulya AJ (1983) Endolymphatic hydrops. An overview and classifìcation. The Annals ofOtology, Rhinology & Laryngology. Suppl. 106: 1-20. Schuknecht HF Myths in neurootology. Am J Otol 1992 ; 13 : 124-126 Schuknecht HF Pathology of the ear. Philadelphia : Lea and Febiger, 1993 Schuknecht HF, Belal AA The utriculo-endolymphatic valve : its functional significance. J Laryngol Otol 1975 ; 89 : 985-996 Schuknecht HF, Gulya AJ Endolymphatic hydrops. An overview and classification. Ann Otol Rhinol Laryngol [suppl] 1983 ; 106 : 1-20 Shambaugh GE Surgery of the endolymphatic sac. Arch Otolaryngol 1966 ; 83 : 305-315 Shea JJ Teflon film drainage of the endolymphatic sac. Arch Otolaryngol 1966 ; 83 : 316-319 Shen J. Ruckenstein M.J .medical treatment of meniere disease Meniere's Disease: Evidence and Outcomes Hardcover – April 15, 2010 by Michael Ruckenstein (Author),Plural Publishing 2010,p. 97-104. Shinozaki N, Kimura RS Scanning electron microscopic observations on the distended Reissner's membrane in the guinea pig. Acta Otolaryngol 1980 ; 90 : 370-384 [crossref] Shojaku H, Watanabe Y The prevalence of definite cases of Meniere's disease in the Hida and Nishibubiki districts of central Japan: a survey of relatively isolated areas of medical care. Acta Otolaryngol [suppl] 1997 ; 528 : 94-96 Silverstein H, Hyman SM, Feldbaum J, Silverstein D Use of streptomycin sulfate in the treatment of Meniere's disease. Otolaryngol Head Neck Surg 1984 ; 92 : 229-232 Silverstein H, Norrel H, Rosenberg S The resurrection of vestibular neurectomy: a 10-year experience with 115 cases. J Neurosurg 1990 ; 72 : 533-539 [crossref] Sjöberg A, Stahle J Treatment of Meniere's disease with ultrasound. Arch Otolaryngol 1965 ; 82 : 498-502 Slater. Vertigo. How serious are recurrent and single attacks ? Postgraduate medicine, 54, #5, 58-67, 1988 Smith CA, Lowry OH, Wu MI The electrolytes of the labyrinthine fluids. Laryngoscope 1954 ; 64 : 141-153 Spector GJ, Smith PG Endolymphatic sac surgery for Meniere's disease. Ann Otol rhinol Laryngol 1983 ; 92 : 113-118 Spoendlin H, Balle V, Bock G, Bredberg G, Felix H, Gleeson M , e al. Multicenter evaluation of the temporal bones obtained from a patient with suspected Meniere's disease. Acta Otolaryngol [suppl] 1992 ; 499 : 1-21 Stahle J, Friberg U, Svedberg A. Long-term progression of Meniere's disease. Acta Otolaryngol (Stockh) 1991:Suppl 485:75-83 Stahle J, Stahle C, Arenberg IK. Incidence of Menieres disease. Arch Otol 104(2):99-102, 1978 Stahle J. Advanced Meniere's disease. A study of 356 severely disabled patients.Acta Otol 81: 113-119, 1976 Sterkers JM, Maton P, Briault F Efficacité du mannitol dans certaines surdités de perception. Ann Otolaryngol Chir Cervicofac 1980 ; 97 : 621-631 Sterkers JM, Vialat P La décomposition vestibulaire (étude à long terme des neurectomies vestibulaires unilatérales). J Fr ORL 1987 ; 36 : 5-8 Strupp M, Hupert D, Frenzel C, Wagner J, Hahn A, Jahn K, Zingler VC, Mansmann U, Brandt T.Long-term prophylactic treatment of attacks of vertigo in Menière's disease--comparison of a high with a low dosage of betahistine in an open trial.Acta Otolaryngol. 2008 May;128(5):520-4. Tabor JR, Best L, Donohoe RW Results in labyrinthine cryosurgery monitored by evoked response. Laryngoscope 1972 ; 82 : 1431-1439 Takeda T, Sawada S, Kakigi A, Saito H Computed radiographic measurement of the dimensions of the vestibular aqueduct in Meniere's disease. Acta Otolaryngol [suppl] 1997 ; 528 : 80-84 Tanioka H, Kaga H, Zusho H, Araki T, Sasaki Y MR of the endolymphatic duct and sac: findings in Meniere's disease. AJNR Am J Neuroradiol 1997 ; 18 : 45-51 Tasaki I, Fernandez C Modifications of the cochlear microphonics and action potentials by KCL solution and by direct current. J Neurophysiol 1952 ; 15 : 497-512 Telischi FF, Luxford WM Long-term efficacy of endolymphatic sac surgery for vertigo in Meniere's disease. Otolaryngol Head Neck Surg 1993 ; 109 : 83-87 Thirlwall, A. S. and S. Kundu (2006). "Diuretics for Meniere's disease or syndrome." Cochrane Database Syst Rev 3: CD003599. Tighilet B, Trottier S, Lacour M (2005) Dose- and duration-dependent effects of betahistine dihydrochloride treatrnent on histarnine turnover in the cat. Eur I Pharmacoi. Oct 31; 523 (1-3): 54-63. Thomsen J Defining valid approaches to therapy for Meniere's disease. Ear Nose Throat J 1986 ; 65 : 10-18 Thomsen J, Bretlau P, Tos M, Johnson NJ Placebo effect in surgery for Meniere's disease. Arch Otolaryngol 1981 ; 107 : 271-277 Thomsen J, Sass K, Odkvist L, Arlinger S.Local overpressure treatment reduces vestibular symptoms in patients with Meniere's disease: a clinical, randomized, multicenter, double-blind, placebo-controlled study. Otol Neurotol. 2005 Jan;26(1):68-73. Tumarkin A (1936) The otolithib catastrophe: a new syndrome. Br. Med J. 1:175-177. Tonndorf J Endolymphatic hydrops: mechanical causes of hearing loss. Arch Otorhinolaryngol 1976 ; 212 : 293-299 [crossref] Tonndorf J Vestibular signs and symptoms in Meniere's disorder: mechanical considerations. Acta Otolaryngol 1983 ; 95 : 421-430 [crossref] Torok N Old and new in Meniere's disease. Laryngoscope 1977 ; 87 : 1870-1877 Toshiaki Y, Yoshio O, Kayo S, Eriko K, Takayuki K 3D analysis of nystagmus in peripheral vertigo. Acta Otolaryngol 1997 ; 117 : 135-138 [crossref] Tran Ba Huy P Electrophysiological and biomedical findings in four cases of Meniere's disease. Acta Otolaryngol 1984 ; 97 : 571-579 Tran Ba Huy P, Brette MD, Chic M Maladie de Ménière. Encycl Méd Chir (Éditions Scientifiques et Médicales Elsevier SAS, Paris), Oto-rhino-laryngologie, 20-205-A-10: 1989; 1-18. [interref] Tran Ba Huy P, Hassan JM, Wassef M, Mikol J, Thurel C Acoustic schwannoma presenting as a tumor of the external auditory canal. Ann Otol Rhinol Laryngol 1987 ; 96 : 415-418 Tumarkin A Otolithic catastrophe, a new syndrome. Br Med J 1936 ; 2 : 175-177 [crossref] van Deelen, G. W. and E. H. Huizing (1986). "Use of a diuretic (Dyazide) in the treatment of Meniere's disease. A double-blind cross-over placebo-controlled study." ORL J Otorhinolaryngol Relat Spec 48(5): 287-92. Vrabec JT.Herpes simplex virus and Meniere's disease. Laryngoscope. 2003 Sep;113(9):1431-8. Yazawa Y and others. Detection of Viral DNA in the Endolymphatic Sac in Meniere's Disease by in situ Hybridization. ORL 2003;65:162-168 Wackym PA, Friberg U, Linthicum FH Jr, Bagger-Sjoback D, Bui HT, Hofman F , e al. Human endolymphatic sac: morphologic evidence of immunologic function. Ann Otol Rhinol Laryngol 1987 ; 96 : 276-281 Watanabe I, Mizukoshi K, Nakae K, Okubo J (1981) Epidemiologic studies on Meniere’s disease in Japan. In: Vosteen KH, Schuknecht H, Pfaltz R, Wersäll J, Kimura RS, Morgenstern C, Juhn K (eds) Meniere’s disease: Pathogenesis, Diagnosis and Treatment, pp. 194-199. Georg Thieme Verlag, Stuttgart/New York. Watanabe I. Incidence of Meniere's disease including some other epidemiological data. In: Meniere's Disease: A comprehensive Appraisal. Edited by W. J. Oosterveld, 1983 (Wiley). Watanabe Y, Mizokoshi K, Shojaku H, Watanabi I, Hinoki M, Kitahara M. Epidemiological and clinical characteristics of Menieres disease in Japan. Acta Otol (Supp) 519:206-10, 1995 Wiet RJ. Patterns of ear disease in the south-western American Indian. Arch Otolaryng, 105, 381-5, 1979 Welling DB, Miles BA, Western L, Prior TW. Detection of viral DNA in vestibular ganglia tissue from patients with Meniere's disease. Am J. Otol 18(6) 734-7, 1997 Welling DB, Clarkson MW, Miles BA, Schmalbrock P, Williams PM, Chakeres DW , e al. Submillimeter magnetic resonance imaging of the temporal bone in Meniere's disease. Laryngoscope 1996 ; 106 : 1359-1364 [crossref] Williamson DG, Gifford F Psychosomatic aspects of Meniere's disease. Acta Otolaryngol 1971 ; 72 : 118-120 [crossref] Wladislavosky-Waserman P, Facer GW, Moleri B, Kurland LT Meniere's disease: a 30-year epidemiologic and clinical study in Rochester. Laryngoscope 1984 ; 94 : 1098-1102 Wladislavosky Y, Kitahara M Computerized tomography of the petrous bone in Meniere's disease. Acta Otolaryngol [suppl] 1994 ; 510 : 67-72 [crossref] Wu IC, Minor LB (2003) Long-Terrn Hearing Outcome in Patients Receiving Intratympanic Gentainicin for Meniere’s Disease. Laryngoscope. May; 113 (5): 815-820. 26. Xia AP’, Kikuchi T, Minowa O, et aI (2002) Late-onset hearing loss in a mouse model of DFN3 non syndromic deafness: morphologic and inununohistochemical analyses. Hear Res. 166: 150-158. Yilmazer -Waserman P, Facer GW, Moleri B, Kurland LT Meniere's disease: a 36-year epidemiologic and clinical study in Rochester. Laryngoscope 1984 ; 94 : 1098-1102 Yazawa C. Relationship of the cochlear aqueduct and inner ear pressure in Meniere's disease and in a normal population. Otol Neurotol 22: 534-538, 2001 Yoo TJ, Stuart JM, Kang AH, Townes AS, Komoda K, Dixit S Type II collagen autoimmunity in otosclerosis and Meniere's disease. Science 1982 ; 217 : 1153-1154 Zucca G, Botta L, Mira E, Manfrin M, Poletti A, Buizza A , e al. Effects of hydrostatic pressure on sensory discharge in frog semicircular canals. Acta Otolaryngol 1991 ; 111 : 820-826 [crossref
Books on Meniere's Disease: Meniere's Disease : What you need to know by P.J. Haybach, Jerry Underwood (This book was written under the auspices of VEDA (Vestibular Disorder Association) for patients). Meniere's Disease, An Issue of Otolaryngologic Clinics (The Clinics: Surgery) by Jeffrey Harris MD Dr. and Quyen T. Nguyen MD Dr. (Hardcover - 8 Nov 2010) |
Per vedere il PDF clicca qui
IPOACUSE FLUTTUANTE Parole chiave : Sordità fluttuante, Fistola perilinfatica, Dilatazione dell'acquedotto del vestibolo, Dilatazione dell'acquedotto cocleare, Sordità autoimmune
L’ipoacusia fluttuante è un’entità nosologica tuttora non ben definita. Si tratta di una patologia in cui la soglia uditiva di un orecchio (o di entrambi) è soggetta a variazioni nel tempo. Non esiste una definizione precisa della sordità fluttuante, come, per esempio, per le sordità improvvise. Essa può essere clinica : episodi di sordità ravvicinati, più o meno regressivi, che possono lasciare delle sequele (Sauvage JP,e Al 2004.1. Essa può essere audiometrica, definita per alcuni come una variazione superiore a 10 dB tra due audiogrammi successivi (Marlin S., e Al,2006); oppure come una fluttuazione di 30 dB almeno su due ottave (Kakigi A. e Al,2003) .. Il quadro di sordità fluttuante raggruppa numerose entità differenti e complesse che è difficile sistematizzare. Le si può considerare secondo la loro evoluzione e si contrappongono, allora, le sordità fluttuanti con restitutio ad integrum uditiva, alle sordità fluttuanti con deterioramento progressivo dell'udito. Le si può considerare in funzione dell'età di comparsa, schematicamente, con le sordità del bambino che orientano verso le cause genetiche, le sindromi malformative o, anche, le cause infettive neonatali; le sordità dell'adulto devono far sospettare, in primo luogo, una sordità autoimmune o una malattia sistemica, quando sono bilaterali, oppure una fistola perilinfatica, quando sono monolaterali ed esiste un contesto traumatico associato.

Fig.1
Spesso si tratta di ipoacusie neurosensoriali che, pur avendo una modalità d’insorgenza simile all’ipoacusia improvvisa, recuperano spontaneamente i valori audiologici precrisi. Proprio il ripetersi nel tempo di queste poussèes di ipoacusia, non necessariamente accompagnate da risentimento vestibolare, giustifica il termine “fluttuanti”. Alcune evolvono verso una rilevante sordità, a volte bilaterale. La causa più frequente è la malattia di Ménière (Fig.1) con vertigini parossistiche presenti sin dall'inizio, oppure che si manifestano in un secondo momento dopo un intervallo di 6 mesi. Quando sono bilaterali, si deve pensare alla sifilide, alle malformazioni cocleari, alle malattie autoimmuni. Spesso la causa rimane sconosciuta. Il loro trattamento è tuttora dubbio.
Le sordità improvvise e fluttuanti sono due entità cliniche caratterizzate da una sordità di percezione senza causa individuabile che si sviluppano rapidamente: in pochi secondi, alcuni minuti o in qualche ora, al massimo 72 ore. [Tran Ba Huy P, 2002 ] La sordità improvvisa comporta un solo episodio irreversibile o più o meno regressivo. La sordità fluttuante comporta diversi episodi ravvicinati più o meno regressivi che possono lasciare delle sequele. Quando la sordità improvvisa si verifica nel quadro di una malattia conosciuta, oppure è rivelatrice di questa malattia, in Francia viene abitualmente indicata col termine di «sordità improvvisa». [Martin C, 2000 ]
Queste due entità non hanno altri criteri obbligatori dell'audiometria tonale con curve audiometriche in grado di assumere tutte le forme, posto che esse restino sordità di percezione pure con una perdita uditiva di almeno 30 dB [Tran Ba Huy P, 2002 ] su tre frequenze audiometriche contigue. Per quanto riguarda i sintomi associati, si ammette che una sordità improvvisa possa accompagnarsi ad acufeni e vertigini. Al contrario, quando una sordità fluttuante predomina sulle frequenze basse, si associa a vertigini parossistiche ed è di eziologia sconosciuta, per definizione, prende il nome di malattia di Ménière. [Ménière’s disease,1995 ] Rimane la difficoltà di trattare una patologia di cui si ignora la causa. Questa sfida potrebbe essere vinta da indagini cliniche prospettiche metodologicamente rigorose. Nel caso delle sordità improvvise, è difficile ottenere dimostrazioni dell'efficacia di un trattamento per il fatto che quasi due terzi dei pazienti recuperano in meno di 15 giorni. [Mattox DE, 1989 ] Quanto alle sordità fluttuanti, la loro nosologia deve ancora essere precisata prima di intraprendere studi simili.
In alcuni casi però, il ripetersi di tali episodi può indurre un progressivo deterioramento delle strutture neurosensoriali cocleari. e determinare quindi l’insorgenza di un’ipoacusia neurosensoriale di entità medio-grave.
L'iter diagnostico inizialmente è quindi di ricercare e riconoscere una causa poiché il sintomo «sordità improvvisa o sordità fluttuante» diventa un'entità clinica solo nel momento in cui non si è trovata alcuna eziologia. Questa delimitazione del soggetto è frustrante, ma non deve portare alla rinuncia. In effetti, si è concordi nel ritenere che vi siano molteplici eziopatogenesi sottostanti.
Il bilancio eziologico è negativo perché manca di esplorazioni dirette dell'orecchio interno. Il meccanismo eziologico ditale affezione rimane oscuro, La maggior parte degli Autori concorda per una sofferenza cocleare su base idropica come nella malattia di Ménière. Raggruppa probabilmente varie patologie: infezioni virali, blocchi microcircolatori, processi autoimmuni, rotture membranose(v. ipoacusia improvvisa). Le diagnosi differenziali principali sono con il neurinoma dell'acustico e le dissecazioni arteriose vertebrobasilari che possono manifestarsi con una sordità improvvisa. Per sperare un giorno di chiarire la loro diagnosi, bisogna conoscere le patologie in grado di interessare l'orecchio interno e le vie uditive. Bisogna anche seguire i numerosi lavori che tentano di conoscerne la fisiopatologia.
Soprattutto in caso di bilateralità è necessario escludere le malformazioni cocleari (es. EVA), le patologie autoimmuni, la sifilide.
Clinicamente l’ipoacusia fluttuante si caratterizza per un deficit uditivo che tende a manifestarsi improvvisamente per poi risolversi, completamente o parzialmente, nel giro di alcune ore o giorni. L’ipoacusia tende a ripresentarsi altre volte nel tempo con la stessa modalità, con frequenza imprevedibile e senza chiari fattori scatenanti. Possono concomitare acufeni.
In alcuni casi l’ipoacusia fluttuante può rappresentare il sintomo d’esordio di una malattia di Ménière, in cui la sintomatologia vertiginosa si manifesta in un secondo momento dopo un intervallo di alcuni mesi.
La diagnosi (strumentale) si avvale dell’esame audiometrico, che eseguito in fase acuta, dimostra la presenza di un deficit neurosensoriale. per lo più. localizzato inizialmente alle basse e medie frequenze, di lieve-media entità.
I principali elementi prognostici sono: la gravità della sordità, il tipo di curva audiometrica (ascendente, piatta o discendente) e la presenza di vertigini. È difficile dimostrare l'efficacia dei trattamenti per la frequenza di regressioni spontanee precoci
Il trattamento dell’ipoacusia fluttuante è tuttora dubbio e reso difficile dal fatto che la causa è per lo più sconosciuta. E inoltre difficile dimostrare l’efficacia dei vari trattamenti anche per la frequente regressione spontanea.
E stato proposta la combinazione di corticosteroidi e farmaci vasoattivi, Sono stati proposti anche altri trattamenti: carbogeno, antivirali, ecc.
Epidemiologia
La dilatazione dell'acquedotto del vestibolo (Fig.2)
|
|
Non esistono stime a proposito delle sordità fluttuanti al di fuori della malattia di Ménière. Sono probabilmente molto basse. La dilatazione dell'acquedotto del vestibolo[endolymphatic duct (ED on figure above)] è la malformazione più frequente dell'orecchio interno. La sua incidenza è valutata tra lo 0,64% Levenson M.J., 1989 ; 9 e il 4% Koesling S.ed Al., 2006 ; secondo i criteri radiologici scelti. La sua prima descrizione è stata pubblicata nel 1978 da Valvassori, che constatava che questa anomalia colpiva due femmine per un maschio e che era associata ad altre malformazioni dell'orecchio interno nel 60% dei casi Clemis J., Valvassori G. 1978 ; 11. Questa malformazione può essere associata a vari gradi di sordità, che può essere progressiva, fluttuante o brusca [Phelps P.D. ed Al., 1997 ; Ramirez-Camacho R. ed Al., 2003], Fig.2 |
Eziopatogenesi
La causa di sordità improvvise e di sordità fluttuanti senza vertigini rimane misteriosa nonostante gli sforzi di ricercatori e clinici e malgrado i progressi nelle conoscenze sulla fisiologia cocleare. La maggior parte degli studi sono stati indirizzati soprattutto sulle sordità improvvise.
Eziologie genetiche e non genetiche sono coinvolte nelle sordità fluttuanti del bambino. In uno studio già vecchio Brookhouser P.E ed Al., 1998, basato su 229 bambini che presentavano una sordità progressiva o fluttuante, le eziologie supposte sono correlate nel 14% dei casi a una causa ereditaria, nel 14% dei casi a fattori di rischio neonatali, nell'8% dei casi a meningiti, nell'8% dei casi a idrope, nel 5% dei casi a fistole perilinfatiche e nel 4% dei casi a un trauma cranico, mentre, nel 47% dei casi, la causa presunta è incerta.
La possibilità di una causa virale o infettiva è una spiegazione comoda, spesso data al soggetto giovane. È noto in effetti che numerosi microrganismi possono provocare delle sordità improvvise: quelli della sifilide, della malattia di Lyme; e di virus: parotite, virus della varicella-zoster (VVZ), herpes simplex (VHS), virus para-influenzale, morbillo e rosolia. Il meccanismo alla base è sia una labirintite che una neurite. Il problema è di sapere se si può chiamare in causa un'infezione nella genesi di una sordità improvvisa al di fuori di qualsiasi contesto clinico evocatore di tale infezione.
Infezioni da spirochete
 La sifilide (Fig.3) è spesso asintomatica ed è una causa nota di sordità improvvisa o fluttuante che può essere trattata con penicillina G con qualche speranza di successo. È quindi sempre utile prescrivere i test fluorescent treponemal antibody absorption (FTA-Abs) e microhemagglutination- Treponema pallidum (MHA-TP). Tuttavia, bisogna ricordare la possibilità di avere reazioni crociate con il virus Epstein-Barr (EBV), il bacillo della lebbra e altre treponematosi. Vi è anche il fatto che tre quarti dei casi sono falsi-positivi in rapporto a un semplice cicatrice sierologica.
La sifilide (Fig.3) è spesso asintomatica ed è una causa nota di sordità improvvisa o fluttuante che può essere trattata con penicillina G con qualche speranza di successo. È quindi sempre utile prescrivere i test fluorescent treponemal antibody absorption (FTA-Abs) e microhemagglutination- Treponema pallidum (MHA-TP). Tuttavia, bisogna ricordare la possibilità di avere reazioni crociate con il virus Epstein-Barr (EBV), il bacillo della lebbra e altre treponematosi. Vi è anche il fatto che tre quarti dei casi sono falsi-positivi in rapporto a un semplice cicatrice sierologica.
 Nella malattia di Lyme, (Fig.4) è stato riportato il 10-15% dei casi con una sordità improvvisa, vertigini o una paralisi facciale. Questi effetti compaiono nel quadro di una neuroborelliosi tardiva. In Sud America, alcuni Autori ritengono che la malattia decorre più frequentemente in modo silente [21] e consigliano lo studio sistematico della sierologia nel siero e nel liquido cefalorachideo in caso di sordità improvvisa. Tuttavia, la tecnica enzyme-linked immunoassorbent assay (Elisa) fornisce molti falsi-positivi a causa di reazioni crociate con sifilide, mononucleosi, meningite tubercolare, leptospirosi e artrite reumatoide. Il tasso di immunoglobuline Ig M è elevato solo per pochi giorni dopo l'infezione. Quanto ai livelli di IgG, l'aumento è spesso tardivo ed è soprattutto utilizzato per confermare retrospettivamente la diagnosi. Il test sierologico immunoblot è più specifico del test Elisa. In realtà, nelle sordità improvvise, se si tiene conto solo di una sierologia per la diagnosi della malattia di Lyme, non c'è alcuna differenza clinica ed evolutiva tra i pazienti sieropositivi e quelli sieronegativi. In particolare, l'utilizzo di un'antibioticoterapia con ceftriaxone o amoxicillina non aumenta il tasso di recupero uditivo. [Lorenzi MC, ed Al. 2003]
Nella malattia di Lyme, (Fig.4) è stato riportato il 10-15% dei casi con una sordità improvvisa, vertigini o una paralisi facciale. Questi effetti compaiono nel quadro di una neuroborelliosi tardiva. In Sud America, alcuni Autori ritengono che la malattia decorre più frequentemente in modo silente [21] e consigliano lo studio sistematico della sierologia nel siero e nel liquido cefalorachideo in caso di sordità improvvisa. Tuttavia, la tecnica enzyme-linked immunoassorbent assay (Elisa) fornisce molti falsi-positivi a causa di reazioni crociate con sifilide, mononucleosi, meningite tubercolare, leptospirosi e artrite reumatoide. Il tasso di immunoglobuline Ig M è elevato solo per pochi giorni dopo l'infezione. Quanto ai livelli di IgG, l'aumento è spesso tardivo ed è soprattutto utilizzato per confermare retrospettivamente la diagnosi. Il test sierologico immunoblot è più specifico del test Elisa. In realtà, nelle sordità improvvise, se si tiene conto solo di una sierologia per la diagnosi della malattia di Lyme, non c'è alcuna differenza clinica ed evolutiva tra i pazienti sieropositivi e quelli sieronegativi. In particolare, l'utilizzo di un'antibioticoterapia con ceftriaxone o amoxicillina non aumenta il tasso di recupero uditivo. [Lorenzi MC, ed Al. 2003]
Ipotesi virale
Il primo a prenderla in seria considerazione è stato van Dishoeck nel 1957. Si Vedrà più avanti il dettaglio degli aspetti clinici e di laboratorio a favore e quelli contrari. Mentre è fuori di dubbio che l’agente virale riveste un ruolo causale diretto nelle sordità improvvise che si manifestano in corso di mononucleosi, herpes zooster oticus, parotite epidemica, rosolia e morbillo, il nesso causale è molto più sfumato per le assai più frequenti virosi delle vie aerodigestive.
Secondo Jaffe(1975) e Miyake(1988) i virus possono modificare la microcircolazione cocleare. Uno dei meccanismi potrebbe essere l’ipercoagulabilità, l’emoagglutinazione, l’edema endoteliale, tutti fenomeni secondari all’infezione virale. Nel dettaglio gli autori suggeriscono una diminuzione della deformabilità dei globuli rossi (lesione diretta della membrana cito-plasmatica dell’emazia) ed un effetto “sludge”. Si creerebbe quindi una perturbazione del microcircolo cocleare che ridurrebbe l’ossigenazione ed altererebbe la composizione ionica dell’endolinfa, con evidente sofferenza dell’organo del Corti.
|
Viremia |
Aumento della permeabilità vascolare |
|
Contaminazione dell’orecchio interno
|
Iperviscosità ematica |
|
|
Diminuzione del flusso ematico cocleare |
|
Alterazione del funzionamento enzimatico e degenerazione cellulare della coclea |
Ipossia |
|
Carenza di ATP+ Accumulo di radicali liberi dell’ O2
|
Diminuzione della glicolisi aerobia e aumento della glicolisi anaerobia |
|
|
Acidosi |
Tabella 1: Perturbazione del microcircolo cocleare secondario ad un’infezione virale (possibile interferenza sulla perfusione cocleare)
Ipotesi immunologica
Si comincia a parlare razionalmente di meccanismo immuno-mediato con Veldman nel 1986 e Mac Cabe nel 1991.
In analogia a quanto accade in altre condizioni patologiche come nel lupus eritematosus sistemico, la poliarterite nodosa, o la sindrome di Cogan, si dovrebbero rilevare autoanticorpi specifici per l’orecchio interno, nonché la formazione di immunocomplessi nella stria vascolare, nel sacco e nel dotto endolinfatico . Ed
infatti Therrocha(2002) dimostra anticorpi specifici e non, contro epitopi antigenici dell’orecchio interno in corso di ipoacusia improvvisa (collagene, cardiolipidi, fosfolipidi) ma, attenzione, anche contro le cellule endoteliali, come nelle varie vasculiti autoimmuni sistemiche.
Anche in questo caso ritorna dunque in primo piano l’effetto perturbante della patologia immunomediata sulla microcircolazione cocleare.
Se poi si pensa al fatto che questi anticorpi possono essere scatenati da agenti virali, sembra dimostrarsi come ciascuna delle ipotesi illustrate non debba necessariamente escludere le altre.
Ipotesi metabolica
Recenti lavori (Tiede, 2009)postulano come l’evento finale di tre importanti noxae patogene (rumore, ototossicità, invecchiamento)sia l’apoptosi, la morte delle cellule ciliate. La novità sta nell’avere individuato nell’eccesso di radicali liberi la causa scatenante(Tiede, 2009; Cotanche, 2008) (tavola2).
Si ricorda come i radicali liberi provengono dall’attività enzimatica mitocondriale, che appare molto elevata in condizione di stress funzionale (rumore, ototossicità, invecchiamento).
Orientamenti eziologici
Malformazioni dell'orecchio interno
Nell'adulto, diversi meccanismi o patologie appaiono essere responsabili di variazioni pressorie dei liquidi dell'orecchio interno, il che provoca una sintomatologia fluttuante. Si riscontrano le malformazioni descritte nel bambino e, in particolare, le dilatazioni dell'acquedotto del vestibolo (Figura 3, Figura 4, Figura 5 ) e della coclea. Queste anomalie devono essere sospettate sistematicamente in caso di sordità improvvisa che compare dopo una puntura lombare, una rachianestesia e un barotrauma dell'orecchio interno.
Malattia di Ménière Fig.5
Si riscontra anche la malattia di Ménière Herman P, ed Al.2003. . Benché il termine di Ménière non si debba applicare alle forme puramente cocleari o semplicemente vestibolari ,, la malattia può iniziare con una sordità fluttuante isolata. L'elemento semeiologico che orienta verso una patologia pressoria in genere, e, quindi, verso un'idrope, è una sordità fluttuante sulle 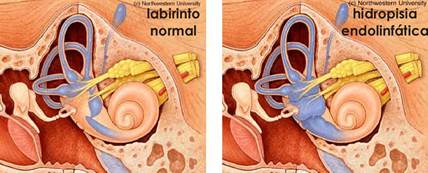 frequenze gravi in audiometria. Il test al glicerolo è positivo in circa il 60% dei casi: i criteri più comunemente riconosciuti sono un miglioramento di 10 dB almeno su due delle tre frequenze 500, 1 000 e 2 000 Hz 32.
frequenze gravi in audiometria. Il test al glicerolo è positivo in circa il 60% dei casi: i criteri più comunemente riconosciuti sono un miglioramento di 10 dB almeno su due delle tre frequenze 500, 1 000 e 2 000 Hz 32.
 Le circostanze dell'ipotensione endocranica sono o ricondotte a un gesto, puntura lombare , Michel O., Brusis T.,1992 rachianestesia Wang L.P., ed Al., 1993 , chirurgia della fossa posteriore o rachidea Walsted A., Walsted A., ed Al., 1994 o spontanee Christoforidis G.A., ed Al.,1998. . L'ipopressione si definisce quando il valore pressorio scende sotto i 60 cmH2O. La deplezione di LCS provoca una deplezione di liquido perilinfatico attraverso un acquedotto cocleare troppo pervio, responsabile di un'idrope. La terapia si basa sul riposo, poiché la sintomatologia si attenua con la nuova produzione di liquor. Sono state proposte la somministrazione di caffeina, di glucocorticoidi o di mineralcorticoidi, così come delle infusioni intradurali di soluzione fisiologica (5 ml/h) fino alla scomparsa dei segni uditivi 5. In caso di perdita documentata e localizzata al momento della realizzazione di una rachianestesia, un blood patch con iniezione di 30 ml di sangue autologo nello spazio peridurale permette di realizzare un coagulo di riempimento.
Le circostanze dell'ipotensione endocranica sono o ricondotte a un gesto, puntura lombare , Michel O., Brusis T.,1992 rachianestesia Wang L.P., ed Al., 1993 , chirurgia della fossa posteriore o rachidea Walsted A., Walsted A., ed Al., 1994 o spontanee Christoforidis G.A., ed Al.,1998. . L'ipopressione si definisce quando il valore pressorio scende sotto i 60 cmH2O. La deplezione di LCS provoca una deplezione di liquido perilinfatico attraverso un acquedotto cocleare troppo pervio, responsabile di un'idrope. La terapia si basa sul riposo, poiché la sintomatologia si attenua con la nuova produzione di liquor. Sono state proposte la somministrazione di caffeina, di glucocorticoidi o di mineralcorticoidi, così come delle infusioni intradurali di soluzione fisiologica (5 ml/h) fino alla scomparsa dei segni uditivi 5. In caso di perdita documentata e localizzata al momento della realizzazione di una rachianestesia, un blood patch con iniezione di 30 ml di sangue autologo nello spazio peridurale permette di realizzare un coagulo di riempimento.
Idrope post-traumatica Shea J.J., ed Al., 1995.
Shea suggerisce tre meccanismi che possono portare a un'idrope post-traumatica. La fistola perilinfatica è stata descritta sopra. Il secondo meccanismo ipotizzato è il trauma diretto del labirinto membranoso che può provocare, a causa della reazione infiammatoria locale, un'ipersecrezione di liquido endolinfatico responsabile di un'idrope transitoria. Il terzo meccanismo è un ostacolo meccanico alla circolazione dei liquidi del labirinto per lesione anatomica del labirinto osseo: blocco del canale endolinfatico per rimaneggiamenti fibroinfiammatori locali.
Idrope e otosclerosi Fig.7 Shea J.J., ed Al.,1994
La sordità fluttuante può essere secondaria alla chirurgia, facendo sospettare una fistola perilinfatica. Essa può essere primitiva: può trattarsi di un'associazione fortuita, ma l'otosclerosi può produrre un'idrope e Shea descrive tre meccanismi:
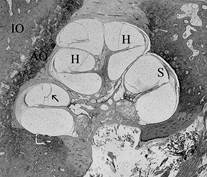 • per difetto di riassorbimento di liquido, a causa di un focolaio che avvolge il canale o il sacco endolinfatico;
• per difetto di riassorbimento di liquido, a causa di un focolaio che avvolge il canale o il sacco endolinfatico;
• per alterazione del liquido endolinfatico nella sua composizione e nella sua densità;
• per alterazione del microcircolo locale: questa alterazione è stata dimostrata a livello del legamento spirale e non si può escludere una lesione vascolare lungo il canale e il sacco che altera il bilancio produzione/riassorbimento.
Istologia del diritto dell'orecchio interno ( Fig.7 ) mostra una coclea circondato da otospongiosis attivo (AO) all'interno di un focolaio otosclerotico inattiva (IO). Normale stria vascolare, idrope endolinfatica (H), estroflessione della membrana di Reissner (freccia), (S)
Sordità fluttuanti
Il paziente ricorre al medico per episodi di sordità unilaterali fluttuante in alcune ore, alcuni giorni o alcune settimane. Acufeni e sensazione di orecchio pieno sono quasi sempre segnalati da parte del paziente che si lamenta di avere l'orecchio tappato a intermittenza. Gli acufeni sono soprattutto a bassa frequenza a tipo di ronzio. Spesso, il paziente tenta senza successo di disostruire l'orecchio con manovre di Valsalva.
Anamnesi: Deve essere accurata alla ricerca di argomenti a favore (Tabella 2) :
§ di una malattia di Mènière: vertigini parossistiche;
§ di una fistola perilinfatica: sordità che si aggrava per gradi, storia di traumi pregressi, di rumori d'acqua, presenza di vertigini scatenate da cambiamenti di posizione, dai rumori forti (fenomeno di Tullio), dal soffiarsi il naso, dal sollevare un grosso peso oppure da sforzo violento alla defecazione;
§ di una malattia autoimmune : cheratite interstiziale, episodi di infiammazione della cartilagine del padiglione auricolare, lesioni renali ecc.
Nella maggior parte dei casi, la sordità è isolata senza altro segno associato.
|
Tabella 2 - Malattie rivelate da una sordità fluttuante. [ Martin C 1998] |
|||||||||
|
Audiogramma preliminare tonale: fatto al momento dell'episodio di sordità, mostra una sordità di percezione che predomina il più delle volte sulle basse frequenze, ma sono possibili tutte le forme di curve. [ Martin C., 1998 ]
Studio cocleovestibolare: completano l'audiometria tonale la ricerca di un segno di fistola, un test di Frazer. Il test di Metz, i PEA sono di solito in favore di una sordità di tipo endococleare. Si devono provare i test osmotici.
VNG con prova del calore: ricerca un interessamento vestibolare di tipo distruttivo sviluppato senza gravi disturbi in favore di un neurinoma se monolaterale o in favore di una patologia immunologica se è bilaterale.
Bilancio biologico: sierologia per la sifilide, VES, fondo dell'occhio, radiografia polmonare sono gli esami richiesti soprattutto in caso di sordità fluttuante bilaterale (Tabella 3).
|
Tabella 3 - Esami ematochimici ed immunitari «massimalisti». [ Tran Ba Huy P, Manach Y 2002 ] |
||||||||
|
||||||||
|
PCR: proteina C reattiva ; VES: velocità di eritrosedimentazione; ALT: alanina aminotrasferasi; AST: aspartato aminotransferasi; LDH: latticodeidrogenasi; CMV: citomegalovirus; HIV: virus dell'immunodeficienza umana; HBV: virus epatite B; HSV: virus herpes simplex; HVZ: virus herpes zoster; ANCA: autoanticorpi citoplasmatici antineutrofili. |
Studio per immagini: una sordità fluttuante predominante sulle frequenze acute, dei PEA precoci di tipo retrococleare impongono una RMN con gadolinio alla ricerca di una lesione della fossa posteriore, in particolare un neurinoma dell'acustico. Se esiste un'anomalia dell'orecchio esterno, l'esame tomografico delle rocche è necessario per ricercare una malformazione cocleare responsabile di idrope labirintica: sindrome di Mondini (Fig. 8) , sindrome dell'acquedotto largo.
Figura 8 :
Malformazione cocleare bilaterale tipo Mondini. Paziente di 51 anni che si era presentato con sordità di percezione fluttuante destra. Rare vertigini mal sistematizzate. Sordità di percezione bilaterale predominante sul lato destro con curva audiometrica piatta. Anomalie del padiglione auricolare. Precedenti di intervento per palatoschisi. A. Scansione assiale della rocca destra. Dilatazione del vestibolo. B. Scansione assiale della rocca sinistra. Dilatazione del vestibolo. C. Difetto di angolatura del padiglione auricolare.
Vi sono solo pochi dati della letteratura sull'evoluzione delle sordità fluttuanti. Nel 1976, su 52 pazienti colpiti da sordità fluttuante di cui 16 bilaterali, Martin [ Martin H, Martin C ,1997 ] dimostra che in 26 casi, vertigini e acufeni erano associati evocando sia dall'inizio che successivamente una malattia di Menière in 24 casi e una vertigine di Lermoyez in due. In quasi tutti questi pazienti, la curva audiometrica era di tipo A. Nei restanti 26 casi, le successioni di caduta uditiva, spesso notevole e improvvisa, erano seguite da recuperi il cui ritmo era molto variabile, talvolta accompagnati da acufeni a timbro acuto. La curva audiometrica era molto spesso di tipo C ma anche di tipo A. Il recupero uditivo poteva essere spontaneo o apparentemente indotto dal trattamento medico. L'evoluzione a lungo termine non è stata sempre peggiorativa. In molti pazienti, per un lungo periodo di tempo, è stata osservata sordità di percezione fluttuante per le frequenze basse, poi tardivamente una flessione verso le frequenze acute.
Così, la maggior parte delle sordità fluttuanti si integrano in una malattia di Menière sin dall'inizio o secondariamente. La malattia rimane puramente cocleare prima che appaiano le vertigini e che si possa essere quindi autorizzati a parlare di malattia di Menière. Un intervallo di 6 mesi è classico, ma può essere molto più lungo. Per definizione, la malattia di Menière comporta vertigini e in nessun caso si è autorizzati a parlare di forma cocleare della malattia di Menière perché nessun elemento permette di predire questo tipo di evoluzione. La fase più o meno lunga senza vertigini si spiegherebbe con il fatto che l'idrope esordisce all'apice della coclea. Il carattere fluttuante della sordità si spiega con la teoria delle rotture membranose di Schuknecht con contaminazione potassica della perilinfa seguita da cicatrizzazioni che spiegano il recupero uditivo. Nella teoria di Tonndorf, la dilatazione del canale cocleare provoca una rigidità della membrana basilare all'apice e quindi una sordità predominante per le basse frequenze. Le variazioni di sordità sarebbero soltanto il riflesso delle variazioni di distensione del canale cocleare. Le lunghe fasi senza vertigini si spiegherebbero anche con il fatto che la valvola otricoloendolinfatica(detta di Bast) resterebbe a lungo continente.
Se non si trovano altre cause, non esistono altre ipotesi patogenetiche al di fuori della malattia di Mènière. Sono stati a volte ipotizzati un conflitto arterovenoso o degli equivalenti emicranici. [ Baloh RW 1997 ]
Nel bambino, [ Dinces EA, ed Al.,2001 ] la diagnosi di fluttuazione è particolarmente difficile. L'origine immunologica potrebbe essere più frequente con test di trasformazione immunoblastica positivo. Spesso, la sordità fluttuante è bilaterale. Bisogna ricercare in particolare una storia clinica evocatrice di fistola perilinfatica. Essa deve essere quindi confermata con l'esplorazione chirurgica. La terapia cortisonica può essere proposta soltanto nei casi in cui la presunzione di eziologia autoimmune è forte. A questa età i risultati sembrano poco probanti e gli effetti collaterali troppo importanti.
Sordità fluttuanti monolaterali
Fistole perilinfatiche Fig.9
 Il termine di fistola perilinfatica indica una comunicazione tra le cavità dell'orecchio interno e dell'orecchio medio, o a livello della finestra cocleare o a livello della finestra vestibolare o attraverso una deiscenza traumatica o erosiva, soprattutto a livello del rilievo del canale semicircolare orizzontale o del promontorio. Questa entità è soggetta a numerosi dibattiti. Mentre non vi sono dubbi quando sono visualizzati dei segni diretti (pneumolabirinto, rima di frattura translabirintica, lisi del canale semicircolare laterale, che complicano un'otite cronica colesteatomatosa), essa è soggetta a controversie di fronte a qualsiasi patologia cocleovestibolare fluttuante monolaterale e post-traumatica.
Il termine di fistola perilinfatica indica una comunicazione tra le cavità dell'orecchio interno e dell'orecchio medio, o a livello della finestra cocleare o a livello della finestra vestibolare o attraverso una deiscenza traumatica o erosiva, soprattutto a livello del rilievo del canale semicircolare orizzontale o del promontorio. Questa entità è soggetta a numerosi dibattiti. Mentre non vi sono dubbi quando sono visualizzati dei segni diretti (pneumolabirinto, rima di frattura translabirintica, lisi del canale semicircolare laterale, che complicano un'otite cronica colesteatomatosa), essa è soggetta a controversie di fronte a qualsiasi patologia cocleovestibolare fluttuante monolaterale e post-traumatica.
I meccanismi traumatici lesivi che portano a lesioni della finestra cocleare sono rappresentati dal «colpo di pistone», che corrisponde a un brutale affondamento della staffa nella finestra, per una brutale compressione (blast timpanico e ricompressione rapida in discesa in immersione, per esempio). I meccanismi traumatici lesionali che provocano delle lesioni della finestra cocleare sono stati sistematizzati da Goodhill [Goodhill V. 1971/2]: via implosiva con rottura della finestra cocleare verso la scala tympani per una brutale iperpressione nella cassa del timpano (manovra di Valsalva intempestiva, breve e violenta) e via esplosiva con rottura della finestra per brutale iperpressione dei liquidi perilinfatici, secondaria a un'iperpressione del LCS, che può essere indotta da una manovra di Valsalva forzata e che richiede una pervietà aumentata del canale cocleare. Tuttavia, una sintomatologia fluttuante regressiva in un contesto traumatico può anche essere dovuta a un'idrope traumatica [Klingmann C., ed Al ,2004; Shea J.J., ed Al 1995].
Clinica
Il segno clinico è un’ipoacusia fluttuante, provocata dagli sforzi (tosse, defecazione, ecc.) o dal rumore (fenomeno di Tullio). Gli acufeni sono spesso presenti e variabili nella loro intensità. Infine, esistono spesso delle vertigini associate. Portmann propone l'uso di una scala diagnostica per valutare la probabilità di fistola Portmann D., ed Al., 2005 ; . Un punteggio superiore o uguale a 7 è fortemente suggestivo di fistola (Tabella 4 ).
Tabella 4 - Punteggio per sospetto di una fistola perilinfatica (secondo [Portmann D., ed Al., 2005 ].
Bilancio funzionale strumentale
L'audiometria oggettiva una sordità di percezione. Una sordità mista, in questo contesto, deve far sospettare in prima intenzione una lesione stapedia.
L'audiometria posizionale è interessante solo quando è positiva, cioè con un guadagno di 10 dB su più di tre frequenze in audiometria tonale, tenendo l'orecchio malato verso l'alto per 30 minuti (rispetto alle soglie audiometriche con il capo eretto e il paziente seduto) Hazell J.W., ed Al.,1992 , oppure con una perdita di 10 dB su più di tre frequenze, con l'orecchio malato rivolto verso il basso.
La timpanometria presenta un interesse diagnostico quando l'esame scatena un nistagmo realizzando il segno della fistola.
La prova calorica calibrata, in assenza di una perforazione timpanica e dopo la regressione dell'eventuale emotimpano, evidenzia spesso un'ipovalenza sul lato leso.
Diagnostica per immagini
La diagnostica per immagini di riferimento nella diagnosi delle fistole perilinfatiche è la TC dell'orecchio medio. Il segno diretto della fistola è la presenza di aria nel vestibolo: ciò esce dal contesto delle sordità fluttuanti ed è identificato su immagini precoci dopo il trauma. I segni indiretti si basano sullo studio delle densità delle finestre, sulla presenza di un'eventuale rima di frattura in prossimità, sull'esistenza di una lussazione stapedia e sulla presenza di un versamento liquido minimo nella cassa.
Quando gli elementi di sospetto di fistola sono notevoli, può essere proposta un'esplorazione chirurgica per l'esplorazione delle finestre e il riempimento.
Lesioni pressorie dell'orecchio interno: idrope
L'elemento clinico che orienta prioritariamente verso un'idrope è la comparsa di una sordità fluttuante sulle frequenze gravi, per le ragioni descritte in precedenza, vale a dire la dilatazione più facile a livello della porzione apicale del canale cocleare.
La timpanometria esclude un'alterazione della pervietà tubarica.
Sul piano audiometrico, si tratta di una sordità di percezione. I test osmotici hanno un interesse fondamentale: l'ingestione di una sostanza altamente osmotica crea un gradiente di osmolarità tra il settore vascolare e il settore labirintico, che induce uno spostamento di liquidi verso il settore vascolare e riduce la pressione labirintica. Questo effetto ha come conseguenza un miglioramento o un ripristino delle prestazioni uditive. Si utilizza tradizionalmente il glicerolo alla dose di 1,5 g/kg, in un soggetto a digiuno. Si può usare del mannitolo per via endovenosa.
Si realizza un'audiometria tonale prima della somministrazione della soluzione osmotica e 3-4 ore dopo. Classicamente, il test è considerato positivo se si ha un guadagno di 10 dB su almeno due delle tre frequenze seguenti: 500, 1 000 e 2 000 Hz. Herman P, ed Al.,2003. .
L'elettrococleografia registra tre tipi di potenziali:
• il potenziale microfonico, di origine sensoriale, poco utilizzato, che può essere eliminato con una stimolazione alternata;
• il potenziale di sommazione (PS), di origine sensoriale: in caso di idrope, questo potenziale è elevato e diminuisce al momento dei test osmotici;
• il potenziale d'azione composito (PA) di origine neurale: esso aumenta dopo la somministrazione di sostanze osmotiche.
Con un rapporto PS/PA superiore a 0,35, può essere affermata l'idrope Eggermont J.J.1979. In caso di idrope, questo rapporto PS/PA diminuisce dopo la somministrazione di una sostanza osmotica.
Marchbanks Measurement System-10 Tympanic Displacement Analyser (MMS-10)
Il principio di questo apparecchio è di determinare deboli variazioni di volume nel meato acustico esterno, indotte dai movimenti della membrana timpanica al momento della contrazione del muscolo della staffa. Questo spostamento dipende dalla posizione di riposo della platina della staffa, che è essa stessa in funzione della pressione del liquido perilinfatico Reid A., ed Al.,1989. In caso di iperpressione del liquido perilinfatico, la staffa a riposo è sospinta verso la cassa del timpano e la contrazione del muscolo della staffa induce uno spostamento all'interno e, quindi, un minimo spostamento timpanico all'interno. Dieci stimoli sonori a 20 dB al di sopra della soglia del riflesso stapedio su 1 000 Hz sono presentati sull'orecchio controlaterale all'orecchio testato. Lo stimolo dura 0,5 secondi e l'intervallo tra i due stimoli è di 5 secondi. Lo spostamento della membrana timpanica è calcolato come media sulle dieci stimolazioni e sono considerati due parametri: Vi (in nanolitri) è definito come lo spostamento massimo all'interno e Vm (in nanolitri) come lo spostamento medio a partire dal momento in cui è raggiunto Vi, fino all'interruzione della stimolazione. Dei valori negativi di Vi e Vm sono correlati ad alte pressioni perilinfatiche, mentre dei valori vicini a 0 oppure positivi indicano una bassa pressione Rosingh H.J., ed Al.,1996. Questo test non è praticabile in caso di perforazione timpanica e in caso di abolizione del riflesso stapedio, di lesione ossiculare e di patologia tubarica.
Test di valutazione funzionale del legamento anulare della staffa e di studio della conduttanza acustica G (TEFLAG)
Questo test permetterebbe di valutare la compliance del legamento anulare, misurata attraverso la frequenza di risonanza che si trova intorno ai 1 000 Hz, la suscettanza caratterizzata dall'autore come l'allungamento del sistema vibrante e la conduttanza, che è l'inverso delle forze resistive del legamento anulare. La frequenza di risonanza è direttamente legata alla pressione o alla tensione che si esercita sul legamento anulare. In caso di idrope, questa tensione aumenta e l'autore descrive un aumento della frequenza di risonanza (1 300 Hz) Camicas-Van Gout M., ed Al.,1999. .
In caso di sordità fluttuante bilaterale, sono, ovviamente, da ricercare le eziologie descritte precedentemente. A volte si deve, tuttavia, anche orientare l'iter diagnostico verso la ricerca di malattie sistemiche o autoimmuni. Sono raccomandati tre esami di base: il laboratorio con ricerca di proteinuria o di ematuria (lesione renale), un esame oftalmologico con lampada a fessura e fondo dell'occhio e degli esami di laboratorio specifici e non specifici. Il bilancio non specifico ricerca dei marcatori dell'infiammazione (fibrinogeno, proteina C reattiva [PCR]), un emocromo con conta piastrinica, uno ionogramma, una creatininemia, un dosaggio delle frazioni C3 e C4 del complemento, il fattore reumatoide, gli anticorpi antinucleari, gli anticorpi anticitoplasma dei polimorfonucleati neutrofili (ANCA) (e i loro sottotipi P [perinucleare] e C [citoplasmatico]) e i complessi immuni circolanti. Il bilancio specifico permette la diagnosi di lesione autoimmune dell'orecchio interno:
• autoimmunità cellulare mediante studio della reattività dei linfociti del paziente (inibizione della migrazione linfocitaria, trasformazione linfoblastica) testata contro estratti di orecchio interno;
• autoimmunità umorale mediante ricerca di autoanticorpi nel siero del paziente, con immunofluorescenza (su sezione di osso temporale) oppure con western blot (individuazione di proteine di estratti di orecchio interno che reagiscono con gli anticorpi del paziente) oppure con metodo enzyme-linked immunosorbent assay [Elisa] (che quantifica gli autoanticorpi).
Malattie sistemiche
La lesione dell'orecchio è associata ad altre lesioni viscerali.
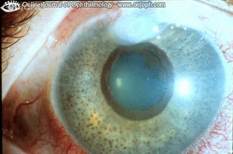 Questa sindrome associa una cheratite interstiziale, bilaterale, una sordità di percezione che evolve per puntate, aggravandosi progressivamente, una sindrome vestibolare spesso improvvisa e, in un terzo dei casi, una lesione multiviscerale: segni generali (febbre, dimagrimento), segni digestivi (diarree, rettorragie), segni neurologici (comizialità, neuropatia periferica, disturbi della coscienza), segni cardiovascolari (trombosi, stenosi arteriose) e disturbi locomotori (artralgie, mialgie). Si possono osservare un'epatosplenomegalia, delle adenopatie e delle pleuropneumopatie. Sul piano laboratoristico, si possono riscontrare dei complessi immuni circolanti, una caduta del complemento e un'iperleucocitosi. La malattia evolve per puntate e la terapia corticosteroidea, utile al momento delle puntate, sembra avere pochi risultati sull'evoluzione uditiva.
Questa sindrome associa una cheratite interstiziale, bilaterale, una sordità di percezione che evolve per puntate, aggravandosi progressivamente, una sindrome vestibolare spesso improvvisa e, in un terzo dei casi, una lesione multiviscerale: segni generali (febbre, dimagrimento), segni digestivi (diarree, rettorragie), segni neurologici (comizialità, neuropatia periferica, disturbi della coscienza), segni cardiovascolari (trombosi, stenosi arteriose) e disturbi locomotori (artralgie, mialgie). Si possono osservare un'epatosplenomegalia, delle adenopatie e delle pleuropneumopatie. Sul piano laboratoristico, si possono riscontrare dei complessi immuni circolanti, una caduta del complemento e un'iperleucocitosi. La malattia evolve per puntate e la terapia corticosteroidea, utile al momento delle puntate, sembra avere pochi risultati sull'evoluzione uditiva.
Policondrite atrofizzante Fig.11 Yetiser S., ed Al.,2001.
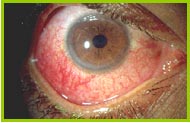 È una connettivite che si caratterizza per un'infiammazione delle cartilagini che evolve per puntate. La sordità può essere fluttuante, brusca o progressiva. La lesione della cartilagine tubarica, all'origine di un'alterazione della pervietà tubarica, può essere responsabile di un fattore trasmissivo associato. Le cartilagini interessate sono quelle dell'orecchio, del naso e della laringe. Alle artralgie delle grosse articolazioni si possono associare delle lesioni oculari (congiuntivite, cheratite, uveite, sclerite), cardiovascolari (valvulopatie, aneurismi arteriosi), renali (glomerulonefrite necrotizzante a depositi di immunoglobuline) e cutanee. Sul piano laboratoristico, la presenza di anticorpi anticollagene di tipo II è evocatrice. Il trattamento si basa sui trattamenti immunosoppressori e sulla terapia corticosteroidea.
È una connettivite che si caratterizza per un'infiammazione delle cartilagini che evolve per puntate. La sordità può essere fluttuante, brusca o progressiva. La lesione della cartilagine tubarica, all'origine di un'alterazione della pervietà tubarica, può essere responsabile di un fattore trasmissivo associato. Le cartilagini interessate sono quelle dell'orecchio, del naso e della laringe. Alle artralgie delle grosse articolazioni si possono associare delle lesioni oculari (congiuntivite, cheratite, uveite, sclerite), cardiovascolari (valvulopatie, aneurismi arteriosi), renali (glomerulonefrite necrotizzante a depositi di immunoglobuline) e cutanee. Sul piano laboratoristico, la presenza di anticorpi anticollagene di tipo II è evocatrice. Il trattamento si basa sui trattamenti immunosoppressori e sulla terapia corticosteroidea.
Periarterite nodosa Fig.12 Tsunoda K., ed Al.,2001.
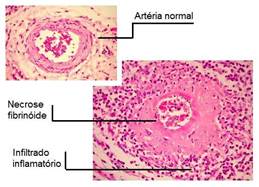 È una vasculite necrotizzante che colpisce le arterie di calibro medio. La sordità è raramente fluttuante, ma più spesso brutale o progressiva. Le lesioni associate sono renali (insufficienza renale cronica, ipertensione arteriosa), digestive (infarto mesenterico), neurologiche (mononeuriti, polinevriti e accidenti vascolari cerebrali). Si riscontra la presenza di ANCA di tipo P. Il trattamento si basa sulla terapia corticosteroidea e sugli immunosoppressori.
È una vasculite necrotizzante che colpisce le arterie di calibro medio. La sordità è raramente fluttuante, ma più spesso brutale o progressiva. Le lesioni associate sono renali (insufficienza renale cronica, ipertensione arteriosa), digestive (infarto mesenterico), neurologiche (mononeuriti, polinevriti e accidenti vascolari cerebrali). Si riscontra la presenza di ANCA di tipo P. Il trattamento si basa sulla terapia corticosteroidea e sugli immunosoppressori.
Poliartrite reumatoide Fig.13
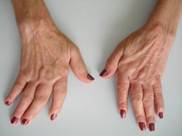 La lesione otologica è, in questo caso, neurogena (alterazione dei potenziali evocati uditivi). È, il più delle volte, presente il fattore reumatoide, poco specifico; gli anticorpi antipeptide ciclico citrullinato (CCP), molto specifici, lo sono più raramente. Il trattamento di fondo si basa sul metotrexate, sugli anti-tumor necrosis factor (TNF), sugli anti-CD20 oppure sugli immunosoppressori.
La lesione otologica è, in questo caso, neurogena (alterazione dei potenziali evocati uditivi). È, il più delle volte, presente il fattore reumatoide, poco specifico; gli anticorpi antipeptide ciclico citrullinato (CCP), molto specifici, lo sono più raramente. Il trattamento di fondo si basa sul metotrexate, sugli anti-tumor necrosis factor (TNF), sugli anti-CD20 oppure sugli immunosoppressori.
Sindrome degli antifosfolipidi Fig.14
 È una malattia che si caratterizza per delle trombosi vascolari a ripetizione, con una possibile lesione dell'orecchio interno, e per la presenza di anticorpi antifosfolipidi (antiprotrombinasi e anticardiolipina).
È una malattia che si caratterizza per delle trombosi vascolari a ripetizione, con una possibile lesione dell'orecchio interno, e per la presenza di anticorpi antifosfolipidi (antiprotrombinasi e anticardiolipina).
Lupus eritematoso disseminato Fig.15
 È una connettivite caratterizzata dalla presenza di anticorpi antinucleari. La presenza di anticorpi antifosfolipidi sarebbe un fattore peggiorativo Compadretti G.C., ed Al.,2005.
È una connettivite caratterizzata dalla presenza di anticorpi antinucleari. La presenza di anticorpi antifosfolipidi sarebbe un fattore peggiorativo Compadretti G.C., ed Al.,2005.
Sindrome di Susac Fig.16 [Ayache D., ed Al.,2000 ; Clement P., ed Al.,2003 ; Grover N. ed Al.,2011 ]
 È una microangiopatia dell'orecchio interno, cerebrale e retinica, da cui il suo acronimo SICRET syndrome (small infarction of cochlear, retinal and encephalic tissue). Questa patologia interessa la donna giovane (20-40 anni). Essa deve essere ipotizzata davanti ad ogni sordità fluttuante associata a segni neurologici (disturbi della memoria, confusione, atassia, cefalee e disturbi visivi). La diagnosi si basa sul fondo dell'occhio (ostruzione dei rami dell'arteria centrale della retina) e sulla RM (lesione diffusa della sostanza bianca di origine ischemica). La terapia si basa sulla terapia corticosteroidea, sugli immunosoppressori, sulla plasmaferesi e sugli anticoagulanti.
È una microangiopatia dell'orecchio interno, cerebrale e retinica, da cui il suo acronimo SICRET syndrome (small infarction of cochlear, retinal and encephalic tissue). Questa patologia interessa la donna giovane (20-40 anni). Essa deve essere ipotizzata davanti ad ogni sordità fluttuante associata a segni neurologici (disturbi della memoria, confusione, atassia, cefalee e disturbi visivi). La diagnosi si basa sul fondo dell'occhio (ostruzione dei rami dell'arteria centrale della retina) e sulla RM (lesione diffusa della sostanza bianca di origine ischemica). La terapia si basa sulla terapia corticosteroidea, sugli immunosoppressori, sulla plasmaferesi e sugli anticoagulanti.
Si tratta di una sordità neurosensoriale fluttuante, progressiva e asimmetrica che progredisce per diversi anni e che è potenzialmente rapidamente reversibile sotto immunosoppressori 49. Essa coesiste, nel 15-30% dei casi, con una malattia autoimmune di tipo sistemico (cfr. supra). Gli autoanticorpi sembrano svolgere un ruolo fondamentale e se ne riscontra una grande varietà, contro i principali antigeni dell'orecchio interno che sono:
• il collagene di tipo II, che si esprime sulla membrana tectoria e sul legamento spirale. La presenza di anticorpi anticollagene II è, quindi, un indicatore, probabilmente non specifico (presenza in altre patologie) e legato a una buona corticosensibilità;
• la proteina P0, associata al nervo acustico (proteina della mielina). È possibile la ricerca degli anticorpi anti-P0;
• la proteina Raf-1; essa è presente nel labirinto membranoso; la presenza di anticorpi antiproteina Raf-1 non è, peraltro, specifica;
• la beta-actina, presente in tutte le cellule non muscolari e nelle cellule ciliate dell'organo di Corti. La presenza di anticorpi potrebbe compromettere il loro funzionamento;
• l'alfatubulina, presente nelle cellule di sostegno dell'organo di Corti, e le cellule neurosensoriali;
• la proteina colina COCH (o coclina), presente esclusivamente nell'orecchio interno dell'uomo, che è un precursore della colina fortemente espressa nella coclea e nel vestibolo.
 Nella sua forma omozigote, sono state descritte delle sordità fluttuanti improvvise. Esse sarebbero associate a un fenomeno vascolare e ostruttivo, a causa della rigidità e della deformazione delle emazie, scatenate in particolare dall'ipossia. Occorre, quindi, pensarvi in un soggetto di razza nera.
Nella sua forma omozigote, sono state descritte delle sordità fluttuanti improvvise. Esse sarebbero associate a un fenomeno vascolare e ostruttivo, a causa della rigidità e della deformazione delle emazie, scatenate in particolare dall'ipossia. Occorre, quindi, pensarvi in un soggetto di razza nera.
Arterite temporale a cellule giganti o malattia di Horton Fig.18
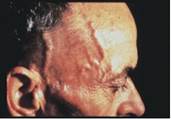 Arterite che interessa il più delle volte i rami dell'arteria carotide e, in particolare, l'arteria temporale (cefalee, disturbi visivi transitori, claudicatio dei masseteri), occorre pensarvi anche davanti a un quadro menieriforme con accelerazione della velocità di sedimentazione. La diagnosi si basa sulla biopsia dell'arteria temporale.
Arterite che interessa il più delle volte i rami dell'arteria carotide e, in particolare, l'arteria temporale (cefalee, disturbi visivi transitori, claudicatio dei masseteri), occorre pensarvi anche davanti a un quadro menieriforme con accelerazione della velocità di sedimentazione. La diagnosi si basa sulla biopsia dell'arteria temporale.
 Può essere presente una sordità fluttuante e le soglie sarebbero correlate alla stanchezza e al grado di gravità dell'ipotiroidismo Anand V.T., ed Al.,1989 .
Può essere presente una sordità fluttuante e le soglie sarebbero correlate alla stanchezza e al grado di gravità dell'ipotiroidismo Anand V.T., ed Al.,1989 .
Diagnosi differenziale (cause di sordità improvvise e fluttuanti)
Numerose malattie sono responsabili di sordità improvvise e di sordità fluttuanti. Uno studio esauriente è stato realizzato da J.-B. Booth nel 1997 .. (562 riferimenti bibliografici). La difficoltà è di trovare la relazione tra sordità e quadro eziologico. Talvolta, questa relazione è evidente. Talvolta, essa è dubbia. Per farsi un'opinione, è utile conoscere le patologie in grado di essere in causa, anche se molto rare. È anche interessante conoscere il risultato dei trattamenti in caso di causa accertata, in particolare virale, vascolare o immunologica. Si possono classificare queste malattie in funzione della sede anatomica della lesione(Tabella 5) . Uno dei problemi è che la stessa malattia può ledere la funzione uditiva a vari livelli anatomici. Peraltro, molte cause coesistono in uno stesso paziente
|
Tabella 5 - Cause di sordità di percezione improvvise e fluttuanti. [Tran Ba Huy P, ed Al.2002] |
|||||||||||||||||||||
|
DIAGNOSI DIFFERENZIALE
L’ipoacusia improvvisa è per definizione idiopatica, non riconoscendosi mai una causa certa. È dunque nell’ambito della diagnostica differenziale che si inserisce la problematica delle patologie rivelate da una sordità improvvisa.
Diagnosi differenziale (cause di sordità improvvise e fluttuanti)
Numerose malattie sono responsabili di sordità improvvise e di sordità fluttuanti. Uno studio esauriente è stato realizzato da J.-B. Booth nel 1997 . (562 riferimenti bibliografici). La difficoltà è di trovare la relazione tra sordità e quadro eziologico. Talvolta, questa relazione è evidente. Talvolta, essa è dubbia. Per farsi un'opinione, è utile conoscere le patologie in grado di essere in causa, anche se molto rare. È anche interessante conoscere il risultato dei trattamenti in caso di causa accertata, in particolare virale, vascolare o immunologica. Si possono classificare queste malattie in funzione della sede anatomica della lesione(Tabella 6) . Uno dei problemi è che la stessa malattia può ledere la funzione uditiva a vari livelli anatomici. Peraltro, molte cause coesistono in uno stesso paziente. Alcune di queste sono molto rare, ma è comunque impor-tante concepirne il sospetto (Tab. 6).
Cocleari
Infiammatorie: batteri, spirochete, virus
Traumatiche
Vascolari
Ematologiche (anemia, embolia, disturbi della coagulazione)
Malattie autoimmuni, vasculiti
Idrope endolinfatica compreso la malattia di Ménière
Malattie metaboliche
Malattie ossee della capsula otica
Ototossici
Varie: sclerodermia, colite ulcerativa, sarcoidosi
Retrococleari e sistema nervoso centrale
Meningite in tutte le sue forme
Sclerosi o placche
Atassia di Friedreich
Sclerosi laterale amiotrofica
Sindrome di Vogt-Koyanagi-Koyanagi
Xeroderma pigmentoso
Tumori della fossa cranica posteriore (schwannoma vestibolare)
Sordità centrale
Idiopatica
Febbre tifoide. Fig.20
 La sordità, a volte bilaterale, compare tra la 2a e la 3a settimana. Il recupero è incostante.
La sordità, a volte bilaterale, compare tra la 2a e la 3a settimana. Il recupero è incostante.
Brucellosi. Fig.21
 L'VIII paio è uno dei nervi cranici più spesso colpito dalla neurobrucellosi (5% delle brucellosi). La lesione può comparire tardivamente, diversi mesi dopo l'esordio dei sintomi, ed essere accertata con un'emocoltura positiva per Brucella melitensis. I pazienti che presentano una neurobrucellosi hanno un'alterazione dei PEA, anche in assenza di sordità improvvisa. [ Thomas R, ed Al 1993 ] La terapia antibiotica con tetraciclina e rifampicina è abitualmente inefficace.
L'VIII paio è uno dei nervi cranici più spesso colpito dalla neurobrucellosi (5% delle brucellosi). La lesione può comparire tardivamente, diversi mesi dopo l'esordio dei sintomi, ed essere accertata con un'emocoltura positiva per Brucella melitensis. I pazienti che presentano una neurobrucellosi hanno un'alterazione dei PEA, anche in assenza di sordità improvvisa. [ Thomas R, ed Al 1993 ] La terapia antibiotica con tetraciclina e rifampicina è abitualmente inefficace.
Micoplasmi. Fig.22
 mycoplasma pneumoniae è una causa comune di infezioni respiratorie. Una lesione neurologica si verifica nel 5% dei casi. Numerose pubblicazioni dimostrano la coesistenza di un'infezione polmonare, seguita da otite media e da sordità profonda che più o meno regredisce con la doxiciclina. Le miringiti bollose si associano a sordità di percezione nella quasi totalità dei casi. [ Hariri MA., 1990 ] La sordità è quasi sempre moderata ma alcuni postumi persistono nel 20% circa dei casi. Il ruolo del mycoplasma pneumoniae è stato dimostrato solo raramente, ma bisogna sottolineare la difficoltà di avere dei prelievi utili.
mycoplasma pneumoniae è una causa comune di infezioni respiratorie. Una lesione neurologica si verifica nel 5% dei casi. Numerose pubblicazioni dimostrano la coesistenza di un'infezione polmonare, seguita da otite media e da sordità profonda che più o meno regredisce con la doxiciclina. Le miringiti bollose si associano a sordità di percezione nella quasi totalità dei casi. [ Hariri MA., 1990 ] La sordità è quasi sempre moderata ma alcuni postumi persistono nel 20% circa dei casi. Il ruolo del mycoplasma pneumoniae è stato dimostrato solo raramente, ma bisogna sottolineare la difficoltà di avere dei prelievi utili.
Labirintiti batteriche di origine otitica.
Infezioni da clamidia Fig.23
 Chlamydia trachomatis e Chlamydiae psittaci possono essere causa di sordità fluttuante bilaterale con disturbi dell'equilibrio che evolvono verso una cofosi bilaterale. La combinazione a sintomi oculari, cheratite interstiziale e uveite, ha permesso di isolare Chlamydiae psittaci. Il trattamento con doxiciclina non ha permesso il recupero. [ Booth JB 1997]
Chlamydia trachomatis e Chlamydiae psittaci possono essere causa di sordità fluttuante bilaterale con disturbi dell'equilibrio che evolvono verso una cofosi bilaterale. La combinazione a sintomi oculari, cheratite interstiziale e uveite, ha permesso di isolare Chlamydiae psittaci. Il trattamento con doxiciclina non ha permesso il recupero. [ Booth JB 1997]
Nel tifo esantematico, causato dalla Rickettsia prowazekii, quando compare la sordità è precoce ed è sempre grave.
[ Friedman I, Frohlich A,1993]
Spirochetosi Fig.25
La sifilide e la malattia di Lyme (Borrelia burgdorferi) sono già state ricordate (vedi sopra).
Parotite. Era responsabile di sordità nello 0,1% dei casi. La sordità può apparire qualunque sia la gravità della parotite e anche in sua assenza. Nella maggior parte dei casi, è una cofosi o una sordità grave monolaterale quasi sempre definitiva che passa inosservata nel bambino. La sordità è solo eccezionalmente bilaterale e completa. Disturbi vestibolari esisterebbero nel 45% dei casi. La labirintite virale sarebbe di origine ematogena, colpirebbe la stria vascolare, creando gravi alterazioni nel sistema endolinfatico. Dal punto di vista anatomopatologico, si tratta di una labirintite. Il virus della parotite è stato messo in evidenza nella perilinfa di soggetti deceduti che hanno presentato negli anni precedenti una sordità improvvisa.
[ Westmore GA, Pickard BH,1979 ]
Morbillo e rosolia. Fig.26 [ Kobayashi H, ed Al.,1994 ]
 Sono malattie note da lungo tempo per essere causa di sordità. Questa si sviluppa di solito contemporaneamente all'eruzione. Tipicamente, è bilaterale e asimmetrica e predomina sui suoni acuti. I programmi mondiali di vaccinazione dovrebbero far scomparire queste tre malattie infantili. È stata riportata una sordità bilaterale dopo vaccinazione contro morbillo e parotite. [ Hulbert TV, ed Al.,1991 ]
Sono malattie note da lungo tempo per essere causa di sordità. Questa si sviluppa di solito contemporaneamente all'eruzione. Tipicamente, è bilaterale e asimmetrica e predomina sui suoni acuti. I programmi mondiali di vaccinazione dovrebbero far scomparire queste tre malattie infantili. È stata riportata una sordità bilaterale dopo vaccinazione contro morbillo e parotite. [ Hulbert TV, ed Al.,1991 ]
Varicella. Fig.27

Essa colpisce eccezionalmente il sistema nervoso centrale. Sono state descritte sordità bilaterali definitive.
Herpes zoster otico. Fig.28
 Comporta sordità improvvisa, vertigini, paralisi facciale ed eruzione nella zona di Ramsay-Hunt. La sordità è molto spesso totale. Generalmente, la diagnosi viene posta precocemente e si può intraprendere un trattamento con acyclovir a condizione che le funzioni renali siano normali. Le sequele sono tuttavia molto frequenti. La RMN in T1 con gadolinio dimostra, nell'herpes zoster otico, che si può avere un enhancement non soltanto del nervo facciale, ma anche dei nervi vestibolare e cocleare. Questo enhancement persisterebbe 6 settimane e talvolta fino a 6 mesi dopo l'esordio dei sintomi. [ Downie AC, ed Al.,1994] Al di fuori dello zoster otico caratteristico, si pone il problema di sapere se il HVZ può essere in causa nelle sordità improvvise o fluttuanti.
Comporta sordità improvvisa, vertigini, paralisi facciale ed eruzione nella zona di Ramsay-Hunt. La sordità è molto spesso totale. Generalmente, la diagnosi viene posta precocemente e si può intraprendere un trattamento con acyclovir a condizione che le funzioni renali siano normali. Le sequele sono tuttavia molto frequenti. La RMN in T1 con gadolinio dimostra, nell'herpes zoster otico, che si può avere un enhancement non soltanto del nervo facciale, ma anche dei nervi vestibolare e cocleare. Questo enhancement persisterebbe 6 settimane e talvolta fino a 6 mesi dopo l'esordio dei sintomi. [ Downie AC, ed Al.,1994] Al di fuori dello zoster otico caratteristico, si pone il problema di sapere se il HVZ può essere in causa nelle sordità improvvise o fluttuanti.
Mononucleosi infettiva. Fig.29
 Può raggiungere il sistema nervoso centrale nell'1% dei casi e in
Può raggiungere il sistema nervoso centrale nell'1% dei casi e in ![]() particolare essere responsabile di sordità improvvise di solito bilaterali e molto spesso transitorie. I casi descritti sono soggetti giovani e quasi tutti di sesso femminile. [ Booth JB .,1997]
particolare essere responsabile di sordità improvvise di solito bilaterali e molto spesso transitorie. I casi descritti sono soggetti giovani e quasi tutti di sesso femminile. [ Booth JB .,1997]
Febbre di Lassa. Fig.30
 Questo virus, il cui reservoir è rappresentato dal ratto, è responsabile di una febbre emorragica africana, fatale nel 30-70% dei casi. Circa il 30% dei pazienti colpiti presenta una sordità bilaterale nell'80% dei casi. Tra quelli che sopravvivono, il 15% conserva una sordità definitiva; possono recuperare, ma le terapie antivirali non sembrano ridurne la gravità. Il meccanismo sarebbe emorragico. Ciò rimette in discussione il fatto che il meccanismo lesivo dei virus potrebbe essere quello vascolare. Non ci sono dati disponibili sulla relazione tra sordità improvvisa e una forma inapparente di febbre di Lass a. [ Cummings D, ed Al.,1990 ]
Questo virus, il cui reservoir è rappresentato dal ratto, è responsabile di una febbre emorragica africana, fatale nel 30-70% dei casi. Circa il 30% dei pazienti colpiti presenta una sordità bilaterale nell'80% dei casi. Tra quelli che sopravvivono, il 15% conserva una sordità definitiva; possono recuperare, ma le terapie antivirali non sembrano ridurne la gravità. Il meccanismo sarebbe emorragico. Ciò rimette in discussione il fatto che il meccanismo lesivo dei virus potrebbe essere quello vascolare. Non ci sono dati disponibili sulla relazione tra sordità improvvisa e una forma inapparente di febbre di Lass a. [ Cummings D, ed Al.,1990 ]
AIDS. Fig.31
 L'HIV può raggiungere l'orecchio esterno, medio e interno.
L'HIV può raggiungere l'orecchio esterno, medio e interno.
[ Linstrom CJ, ed Al.,1993 ] Inoltre, agenti opportunistici quali Toxoplasma, Pneumocystis carinii o Aspergillus possono provocare una meningite con le proprie sequele uditive. L'HIV aumenta il rischio di manifestare una sifilide. Infine, un tumore del sistema nervoso centrale come un linfoma o, più raramente, una metastasi da sarcoma di Kaposi può ledere la funzione uditiva più o meno improvvisamente. Casi di sordità improvvise e di sordità fluttuanti sono stati descritti nel corso delle infezioni HIV al di fuori dei meccanismi descritti sopra. Sono spesso bilaterali.
Protozoarie Fig.32
 Per diffusione ematogena, il toxoplasma gondii può raggiungere il sistema nervoso centrale, ma molto raramente nel soggetto immunocompetente. Le lesioni dell'udito sono eccezionali nelle toxoplasmosi acquisite. La lesione talvolta bilaterale può presentare uno sfasamento di diversi mesi tra le due orecchie.
Per diffusione ematogena, il toxoplasma gondii può raggiungere il sistema nervoso centrale, ma molto raramente nel soggetto immunocompetente. Le lesioni dell'udito sono eccezionali nelle toxoplasmosi acquisite. La lesione talvolta bilaterale può presentare uno sfasamento di diversi mesi tra le due orecchie.
Benché non rientrino nel quadro delle sordità improvvise quando il trauma è evidente, si può porre talvolta il rapporto con un trauma o un intervento iatrogeno. I traumi della rocca e fistole perilinfatiche: realizzano una comunicazione anomala tra i compartimenti liquidi e perilinfatici dell’orecchio interno e l’orecchio medio. La perilinfa filtra attraverso una deiescenza della fine-stre rotonda od ovale o di uno dei canali semicircolari24-25. Questa perdita di liquidi altera la trasmissione meccanica dello stimolo sonoro. Il trauma può essere esterno con iper-pressione o ipo-pressione improvvisa trasmessa o dallo spazio cefalorachidiano all’orecchio medio (tipo esplosivo) o dall’interno attraverso la tuba di Eustachio in occasione di un starnuto violento o dall’esterno grazie ad una perforazione traumatica in occasione o di uno schiaffo (tipo implosivo). Secondo quest’ultimo meccanismo, è stato descritto un caso di sordità improvvisa dopo salto da una scogliera26. Questo stesso meccanismo è proposto per le sordità improvvise che sopraggiungono nel quadro di un incidente automobilistico con esplosione di “air bag”27. La fistola può essere diagnosticata dal test audiometrico di Frazer che paragona le curve raccolte in posizione seduta ed in decubito laterale sul lato sano. Questo test è positivo se si ottiene una variazione delle soglie di almeno 10 dB su due frequenze. È soprattutto l’associazione di manifestazioni vertiginose o di instabilità breve scatenate dai cambiamenti di posizione, dalle variazioni di pressione (immersione, starnuti, tosse, sforzi) o per suoni forti che depongono in favore di tale diagnosi. Il segno della fistola è particolarmente utile ma ritrovato raramente
Le diminuzioni di pressione intracranica
Una sordità improvvisa può osservarsi dopo una diminuzione della pressione intracranica secondaria ad una puntura lombare, ad una mielografia, o secondaria a chirurgia del rachide28. Il meccanismo supposto è quello di una perdita di liquido cefalorachidiano che abbassa la pressione intra-cranica sotto i 60 mm H2O. A causa della permeabilità dell’acque-dotto cocleare, questa diminuzione di pressione provoca una diminuzione di pressione perilinfatica che a sua volta induce una iperpressione endolinfatica relativa, realizzando un’idrope endolinfatica di origine peri-linfatica. Lo stesso meccanismo è alla base della fistola perilinfatica. La diagnosi si basa sulla misurazione diretta della pressione del liquido cefalorachidiano o sulle misurazioni indirette di spostamento timpanico (apparecchio di Marchbranks), sui segni radiologici nella RMN. Il tratta-mento terapeutico consiste empiricamente nel riposo a letto, nell’assun-zione di caffeina e di corticosteroidi e nella tecnica definita “blood-patch” che consiste nell’iniezione di sangue autologo nello spazio epidurale nelle vicinanze del sito della puntura lombare precedente realizzando così un coagulo che colma la breccia.
Quando i pazienti sono al telefono durante un temporale.
Può essere coinvolta dopo irradiazione della parotide o del rinofaringe. C'è una correlazione tra la dose ricevuta dall'orecchio interno e il grado della sordità di percezione. Il peggioramento avviene per fasi più o meno brusche e può essere ritardato rispetto alla fine dell'irradiazione. L'esame anatomopatologico delle ossa temporali mostra lesioni delle strutture membranose dell'orecchio interno. [ Smouha EE, Karmody YS 1995 ]
Casi di sordità improvvisa compaiono dopo un intervento chirurgico. Essi sono generalmente ascritti a un microembolismo nel territorio cocleare dell'arteria labirintica. Tuttavia, differenti studi non mostrano rischi particolari per interventi sulle coronarie, o che necessitano di ipotermia. [ Ness JA, ed Al.,1993 ]
 Sono stati descritti alcuni casi di sordità dopo anestesia per patologie non otologiche. [In-Hoo Kim,ed Al.2008] Molti di questi pazienti erano stati operati in precedenza di stapedotomia.
Sono stati descritti alcuni casi di sordità dopo anestesia per patologie non otologiche. [In-Hoo Kim,ed Al.2008] Molti di questi pazienti erano stati operati in precedenza di stapedotomia.
[ Hochermann M, Reimer A,1987 ] In questi casi, deve essere sospettata una fistola perilinfatica.
Mielografia, rachidea, chirurgia del rachide
A volte si riscontra una sordità transitoria, spesso associata a sintomi vestibolari. La sordità colpisce le basse frequenze. Di solito è bilaterale ed è associata a cefalea. In effetti, nelle rachianestesie, è stato portato in causa il diametro dell'ago perché favorente la perdita di liquido cefalorachideo negli spazi subaracnoidei provocando una ipopressione endocranica. In questi pazienti, se l'acquedotto cocleare è permeabile, [ Michel O, Brusis T 1992 ] avviene anche una fuga di perilinfa con ipopressione perilinfatica e idrope labirintica. È stata suggerita la tecnica del blood patch, che utilizza una iniezione di 10 mL di sangue autologo nello spazio epidurale nelle vicinanze del sito della puntura lombare precedente.
Sono state portate in causa nella sordità improvvisa anche le estrazioni dentarie. La sordità può insorgere qualche ora o qualche giorno dopo. [ Farrel RW, ed Al.,1991 ]
Mentre le cause vascolari sono spesso invocate per spiegare le sordità improvvise, è raro riscontrare casi in cui una tale causa sia certa.
Accidenti ischemici periferici
La sordità improvvisa associata a violente vertigini entra nel quadro di un accidente ischemico nel territorio vertebrobasilare, per esempio una trombosi dell'arteria cerebellare antero-inferiore . L'esecuzione sistematica di una RMN dovrebbe aumentare la frequenza della loro scoperta. In tal modo, in 37 pazienti colpiti da sordità improvvisa, la RMN sistematica con, quando necessaria, angiografia convenzionale dell'arteria vertebrale ha permesso di scoprire 11 accidenti vascolari costituiti e fra di essi tre dissecazioni vertebrobasilari. Queste dissecazioni, annunciate classicamente da violente rachialgie, ma non sempre, sono caratterizzate da un ematoma intramurale interessante l'origine dell'arteria cerebellare antero-inferiore [ Nagahata M, ed Al.,1997 ] visibile in T1 o da uno sdoppiamento del lume dell'arteria basilare nelle sequenze 3 D spoiled gradient-recalled acquisition in steady state (SPGR). L'angiografia può anche dimostrare una dilatazione aneurismatica di questa arteria, responsabile di sordità improvvise a ripetizione. [ Rinehart R, ed Al.,1992 ] In altri casi, la sordità improvvisa associata a paralisi facciale è compresa nel quadro clinico di un accidente ischemico del tronco cerebrale. Numerose osservazioni di sordità improvvise sono state riportate dopo manipolazioni vertebrali nei soggetti giovani. Una stenosi o una dissecazione di un'arteria vertebrale o del tronco basilare ha potuto quindi essere messa in evidenza.
Sono caratterizzate dalla comparsa di un quadro clinico con trombosi a ripetizione, comprese le embolie polmonari. Sono stati pubblicati casi di sordità improvvisa. [ Einer H, ed Al1994 ]
 Alcuni casi di sordità improvvise bilaterali sono stati pubblicati, associati ad anemia grave con livelli di emoglobina inferiori a 6,5 g/dl con deficit in ferro. Le trasfusioni non hanno dato alcun miglioramento. Dei casi di sordità improvvise sono stati descritti nelle anemie aplasiche e anche nella sindrome di Fanconi. C'era sempre una caduta improvvisa del numero delle piastrine subito prima della sordità. [ Ogawa K, Kanzaki J ,1994 ]
Alcuni casi di sordità improvvise bilaterali sono stati pubblicati, associati ad anemia grave con livelli di emoglobina inferiori a 6,5 g/dl con deficit in ferro. Le trasfusioni non hanno dato alcun miglioramento. Dei casi di sordità improvvise sono stati descritti nelle anemie aplasiche e anche nella sindrome di Fanconi. C'era sempre una caduta improvvisa del numero delle piastrine subito prima della sordità. [ Ogawa K, Kanzaki J ,1994 ]
 I n questa patologia, la viscosità del sangue può essere moltiplicata per 8, mentre la massa eritrocitaria circolante può essere moltiplicata per 3. Tuttavia, i casi di sordità improvvisa sono rari e non sembrano migliorare con il salasso. [ Booth JB ,1997 ]
I n questa patologia, la viscosità del sangue può essere moltiplicata per 8, mentre la massa eritrocitaria circolante può essere moltiplicata per 3. Tuttavia, i casi di sordità improvvisa sono rari e non sembrano migliorare con il salasso. [ Booth JB ,1997 ]
Drepanocitosi Fig.36
 Nella forma omozigote, le sordità di percezione progressive sono frequenti e sarebbero legate alla riduzione del FEC per ostruzione delle piccole arteriole e dei capillari da parte di globuli rossi deformati e rigidi. Si pensa che le prime perdite uditive improvvise possono iniziare fin dalla prima infanzia. Sordità improvvise possono insorgere a qualsiasi età. La sordità può anche essere di tipo fluttuante. Si deve ipotizzarla quando il paziente è di origine africana. [Odetoyinbo O, Adekile A .,2002 ]
Nella forma omozigote, le sordità di percezione progressive sono frequenti e sarebbero legate alla riduzione del FEC per ostruzione delle piccole arteriole e dei capillari da parte di globuli rossi deformati e rigidi. Si pensa che le prime perdite uditive improvvise possono iniziare fin dalla prima infanzia. Sordità improvvise possono insorgere a qualsiasi età. La sordità può anche essere di tipo fluttuante. Si deve ipotizzarla quando il paziente è di origine africana. [Odetoyinbo O, Adekile A .,2002 ]
 Le sordità di percezione in tale patologia sarebbero frequenti e legate a una iperviscosità ematica che rallenta il FEC. Sordità improvvise sono state descritte, talvolta bilaterali, a volte recidivanti. Esse potrebbero essere migliorate dalla plasmaferesi. Il meccanismo è differente dalle vertigini che sono legate a depositi di macroglobuline sulla cupola. Nel caso di sordità improvvise, si tratterebbe di emorragie labirintiche. [ Booth JB ,1997]
Le sordità di percezione in tale patologia sarebbero frequenti e legate a una iperviscosità ematica che rallenta il FEC. Sordità improvvise sono state descritte, talvolta bilaterali, a volte recidivanti. Esse potrebbero essere migliorate dalla plasmaferesi. Il meccanismo è differente dalle vertigini che sono legate a depositi di macroglobuline sulla cupola. Nel caso di sordità improvvise, si tratterebbe di emorragie labirintiche. [ Booth JB ,1997]
 Le sordità improvvise riscontrate nelle leucemie acute sono note da molto tempo. Sarebbero legate a tre meccanismi:
Le sordità improvvise riscontrate nelle leucemie acute sono note da molto tempo. Sarebbero legate a tre meccanismi:
[ Booth JB ,1997 ] infiltrazione leucocitaria, emorragie o labirintiti infettive. Una sordità improvvisa a bascula è stata rivelatrice di leucemia linfoide cronica. La chemioterapia può dare eccellenti risultati.
Malattie autoimmuni
L'insorgenza di sordità improvvise è descritta in un certo numero di malattie autoimmuni non organo-specifiche.
Lupus eritematoso sistemico Fig.39
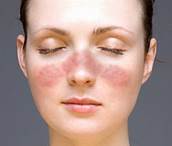 È un'affezione infiammatoria del tessuto connettivo di origine sconosciuta che si verifica nelle donne giovani e anche nei bambini. Il siero di questi pazienti contiene anticorpi antinucleo. Sordità improvvise bilaterali e deficit cocleovestibolari improvvisi sono stati riscontrati in questa patologia con livelli elevati di anticorpi anticardiolipina solitamente correlati a episodi di trombosi arteriosa o venosa. [ Vyse T, ed Al.,1994 ]
È un'affezione infiammatoria del tessuto connettivo di origine sconosciuta che si verifica nelle donne giovani e anche nei bambini. Il siero di questi pazienti contiene anticorpi antinucleo. Sordità improvvise bilaterali e deficit cocleovestibolari improvvisi sono stati riscontrati in questa patologia con livelli elevati di anticorpi anticardiolipina solitamente correlati a episodi di trombosi arteriosa o venosa. [ Vyse T, ed Al.,1994 ]
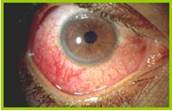 Policondrite atrofizzante Fig.40
Policondrite atrofizzante Fig.40
In questa patologia infiammatoria intermittente distruttiva della cartilagine e del tessuto connettivo dell'occhio, sono tipici la sordità mono o bilaterale a esordio improvviso e i disturbi vestibolari. [ Albers FW, ed Al.,1991 ]
Vasculiti sistemiche Fig.41
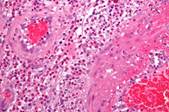 Esse sono attualmente in piena riclassificazione in funzione della grandezza dei vasi colpiti, dell'introduzione di test per gli autoanticorpi citoplasmatici antineutrofili (ANCA) e le loro sotto-classi in tipo c (citoplasmatica) e tipo p (perinucleare) e gli autoanticorpi cellulari anti-endoteliali circolanti (AECA).
Esse sono attualmente in piena riclassificazione in funzione della grandezza dei vasi colpiti, dell'introduzione di test per gli autoanticorpi citoplasmatici antineutrofili (ANCA) e le loro sotto-classi in tipo c (citoplasmatica) e tipo p (perinucleare) e gli autoanticorpi cellulari anti-endoteliali circolanti (AECA).
Periarterite nodosa (PAN) Fig.42
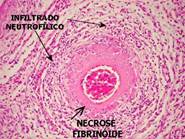 È una malattia caratterizzata da infiammazione e necrosi segmentaria di arterie muscolari di medio calibro con ischemia secondaria del tessuto irrorato dai vasi colpiti. Sordità improvvise e fluttuanti, a volte con interessamento vestibolare, sono descritte nel corso dell'evoluzione di questa malattia ma sono raramente inaugurali. Lo studio anatomopatologico dell'osso temporale mostra un'ostruzione dell'arteria cocleare comune. [ Schuknecht HF, Donovan ED 1986 ]
È una malattia caratterizzata da infiammazione e necrosi segmentaria di arterie muscolari di medio calibro con ischemia secondaria del tessuto irrorato dai vasi colpiti. Sordità improvvise e fluttuanti, a volte con interessamento vestibolare, sono descritte nel corso dell'evoluzione di questa malattia ma sono raramente inaugurali. Lo studio anatomopatologico dell'osso temporale mostra un'ostruzione dell'arteria cocleare comune. [ Schuknecht HF, Donovan ED 1986 ]
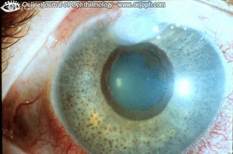 Diversa, ma simile alla periarterite nodosa tipica, associa una sordità a una cheratite con lacrimazione (crying deafness). Le sindromi deficitarie cocleovestibolari mono o bilaterali rapidamente progressive, perfino repentine, fanno parte del quadro clinico. La RMN [ Booth JB ,19976] e l'esame anatomopatologico [ Schuknecht HF, Nadol JB ,1994 ] suggeriscono che si tratti di una vasculite ostruttiva della stria vascolare.
Diversa, ma simile alla periarterite nodosa tipica, associa una sordità a una cheratite con lacrimazione (crying deafness). Le sindromi deficitarie cocleovestibolari mono o bilaterali rapidamente progressive, perfino repentine, fanno parte del quadro clinico. La RMN [ Booth JB ,19976] e l'esame anatomopatologico [ Schuknecht HF, Nadol JB ,1994 ] suggeriscono che si tratti di una vasculite ostruttiva della stria vascolare.
Sordità improvvise sono state descritte in corso di altre malattie autoimmuni con vasculite: [6] arterite di Takayasu con vasculite dell'aorta nella donna giovane orientale o malattia delle donne senza polso; malattia di Kawasaki che compare nel bambino con vasculite coronarica; malattia di Behçet, malattia infiammatoria polisistemica che inizia con ulcerazioni della bocca simili ad afte.
Arterite temporale a cellule giganti Fig.44
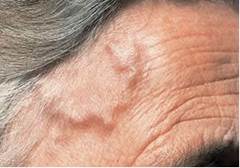 Si tratta di una malattia infiammatoria dei grandi vasi che colpisce più spesso i rami della carotide, in particolare l'arteria temporale (cefalea, disturbi visivi transitori, claudicatio del massetere e della lingua), caratterizzata da un forte aumento della VES che supera 100 mm alla prima ora. La diagnosi si effettua mediante biopsia dell'arteria temporale. Sono state riportate sordità improvvise e fluttuanti. Si deve prenderle in considerazione [ McKennan KX, ed Al.,1993 ] quando un soggetto anziano presenta una sindrome distruttiva cocleovestibolare improvvisa, mono o bilaterale, o una pseudomalattia di Menière con una VES elevata e quando il quadro si completa più o meno rapidamente con paralisi facciale, disturbi della visione, paralisi del decimo nervo cranico. La RMN mostra lesioni ischemiche multiple, recenti, soprattutto nel territorio vertebrobasilare, che corrispondono a un'occlusione dell'arteria vertebrale.
Si tratta di una malattia infiammatoria dei grandi vasi che colpisce più spesso i rami della carotide, in particolare l'arteria temporale (cefalea, disturbi visivi transitori, claudicatio del massetere e della lingua), caratterizzata da un forte aumento della VES che supera 100 mm alla prima ora. La diagnosi si effettua mediante biopsia dell'arteria temporale. Sono state riportate sordità improvvise e fluttuanti. Si deve prenderle in considerazione [ McKennan KX, ed Al.,1993 ] quando un soggetto anziano presenta una sindrome distruttiva cocleovestibolare improvvisa, mono o bilaterale, o una pseudomalattia di Menière con una VES elevata e quando il quadro si completa più o meno rapidamente con paralisi facciale, disturbi della visione, paralisi del decimo nervo cranico. La RMN mostra lesioni ischemiche multiple, recenti, soprattutto nel territorio vertebrobasilare, che corrispondono a un'occlusione dell'arteria vertebrale.
Granulomatosi di Wegener Fig.45
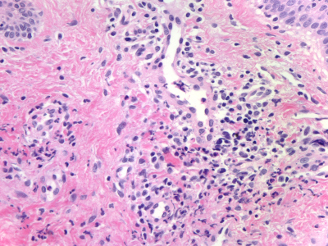 Caratterizzata all'inizio da lesioni infiammatorie granulomatose delle vie aeree superiori, è stata descritta una sordità improvvisa allo stadio di vasculite disseminata. Il trattamento comprende la ciclofosfamide associata ai corticosteroidi.
Caratterizzata all'inizio da lesioni infiammatorie granulomatose delle vie aeree superiori, è stata descritta una sordità improvvisa allo stadio di vasculite disseminata. Il trattamento comprende la ciclofosfamide associata ai corticosteroidi.
La sordità improvvisa è stata descritta come il sintomo rivelatore di una sarcoidosi29-30 o di una periartrite nodosa31.
Idrope endolinfatica e malattia di Menière Fig.46
 Nel 1985, il «Committe on Hearing and Equilibrium of the American Academy of Otolaryngology - Head and Neck Surgery» ha deciso che il termine Menière non doveva più essere applicato alle forme puramente cocleari o vestibolari della malattia. [ Committee on hearing and equilibrium Guidelines 1995 ] Si sa tuttavia che la malattia di Menière può esordire con sordità improvvisa predominante sulle frequenze basse o con una sordità fluttuante monolaterale che si completa secondariamente con vertigini parossistiche in circa il 10% dei casi. [ Yamasoba T, [ McKennan KX, ed Al.,1994 ] In questi pazienti, in più del 60% dei casi, il test al glicerolo era positivo e c'era un aumento significativo del rapporto potenziale di sommazione/potenziale d'azione (SP/AP) al PEA.
Nel 1985, il «Committe on Hearing and Equilibrium of the American Academy of Otolaryngology - Head and Neck Surgery» ha deciso che il termine Menière non doveva più essere applicato alle forme puramente cocleari o vestibolari della malattia. [ Committee on hearing and equilibrium Guidelines 1995 ] Si sa tuttavia che la malattia di Menière può esordire con sordità improvvisa predominante sulle frequenze basse o con una sordità fluttuante monolaterale che si completa secondariamente con vertigini parossistiche in circa il 10% dei casi. [ Yamasoba T, [ McKennan KX, ed Al.,1994 ] In questi pazienti, in più del 60% dei casi, il test al glicerolo era positivo e c'era un aumento significativo del rapporto potenziale di sommazione/potenziale d'azione (SP/AP) al PEA.
Insufficienza renale Fig.47[ Booth JB ,1997 ]
 Il danno uditivo non è legato all'insufficienza renale ma al trattamento stesso. Antibiotici aminoglicosidici e diuretici hanno una posologia difficile da adattare. Durante l'emodialisi, le variazioni osmotiche sono responsabili di sordità fluttuanti. Si tratta soprattutto di fluttuazioni sulle frequenze basse. Dopo trapianto, sono state osservate sordità improvvise di cui alcune sono inspiegabili mentre altre sono legate a uno stato d'ipercoagulabilità
Il danno uditivo non è legato all'insufficienza renale ma al trattamento stesso. Antibiotici aminoglicosidici e diuretici hanno una posologia difficile da adattare. Durante l'emodialisi, le variazioni osmotiche sono responsabili di sordità fluttuanti. Si tratta soprattutto di fluttuazioni sulle frequenze basse. Dopo trapianto, sono state osservate sordità improvvise di cui alcune sono inspiegabili mentre altre sono legate a uno stato d'ipercoagulabilità
Sindrome di Alport. Fig.48
 Si tratta di una nefrite ereditaria che provoca una sordità neurosensoriale progressiva e spesso simmetrica. Sono stati riportati alcuni casi di sordità improvvisa. L'esame della stria vascolare mostra una sua degenerazione.
Si tratta di una nefrite ereditaria che provoca una sordità neurosensoriale progressiva e spesso simmetrica. Sono stati riportati alcuni casi di sordità improvvisa. L'esame della stria vascolare mostra una sua degenerazione.
Nefropatia da Iga. Fig.49
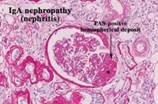 Sono stati riportati casi di sordità improvvisa reversibili conseguenti a terapia cortisonica endovenosa.
Sono stati riportati casi di sordità improvvisa reversibili conseguenti a terapia cortisonica endovenosa.
Diabete mellito Fig.50
 Un rapporto tra sordità e diabete è sospettato da tempo ma sembra difficile da dimostrare sul piano statistico. [Virtaniemi J, ed Al.,1994 ] Nel caso delle sordità improvvise, la causa potrebbe essere una neuropatia periferica, ma nei diabetici insulinodipendenti, i PEA non sono di tipo retrococleare. Inoltre, il tasso di recupero non differisce dal gruppo controllo, fatta eccezione forse per quel che riguarda le frequenze acute. L'esame dell'osso temporale dei soggetti diabetici mostra la presenza quasi costante di una microangiopatia della stria vascolare e dei microvasi del sacco endolinfatico.
Un rapporto tra sordità e diabete è sospettato da tempo ma sembra difficile da dimostrare sul piano statistico. [Virtaniemi J, ed Al.,1994 ] Nel caso delle sordità improvvise, la causa potrebbe essere una neuropatia periferica, ma nei diabetici insulinodipendenti, i PEA non sono di tipo retrococleare. Inoltre, il tasso di recupero non differisce dal gruppo controllo, fatta eccezione forse per quel che riguarda le frequenze acute. L'esame dell'osso temporale dei soggetti diabetici mostra la presenza quasi costante di una microangiopatia della stria vascolare e dei microvasi del sacco endolinfatico.
Iperlipidemia Fig.51
 Anche se l'ipercolesterolemia sembra aggravare le sordità professionali, l'iperlipidemia e i fattori di rischio vascolari non sono più frequenti nelle popolazioni con sordità improvvisa. [ Ullrich D, ed Al.,1992 ]
Anche se l'ipercolesterolemia sembra aggravare le sordità professionali, l'iperlipidemia e i fattori di rischio vascolari non sono più frequenti nelle popolazioni con sordità improvvisa. [ Ullrich D, ed Al.,1992 ]
Ipotiroidismo Fig.52
 La relazione tra ipotiroidismo e sordità è stato oggetto di molti studi da quando era stato constatato che tali pazienti presentavano una sordità fluttuante le cui soglie erano correlate alla fatica e alla gravità dell'ipotiroidismo. L'analisi dei PEA mostrerebbe una correlazione tra le latenze dei PEA e la compliance al trattamento sostitutivo dopo tiroidectomia totale. Queste correlazioni sono tuttora in discussione. [ Anand VT, ed Al.,1989 ]
La relazione tra ipotiroidismo e sordità è stato oggetto di molti studi da quando era stato constatato che tali pazienti presentavano una sordità fluttuante le cui soglie erano correlate alla fatica e alla gravità dell'ipotiroidismo. L'analisi dei PEA mostrerebbe una correlazione tra le latenze dei PEA e la compliance al trattamento sostitutivo dopo tiroidectomia totale. Queste correlazioni sono tuttora in discussione. [ Anand VT, ed Al.,1989 ]
Patologia dell'osso temporale Fig.53
 Le lesioni ossee dell'osso temporale possono essere causa di sordità improvvisa: metastasi, istiocitosi X (Fig.53) , mieloma. Lo studio dell'osso temporale ha potuto talvolta rivelare un'emorragia negli spazi perilinfatici. È stato anche descritto un osteoma del condotto uditivo interno. [ Clerico DM, ed Al.,1994 ]
Le lesioni ossee dell'osso temporale possono essere causa di sordità improvvisa: metastasi, istiocitosi X (Fig.53) , mieloma. Lo studio dell'osso temporale ha potuto talvolta rivelare un'emorragia negli spazi perilinfatici. È stato anche descritto un osteoma del condotto uditivo interno. [ Clerico DM, ed Al.,1994 ]
Ototossicità Fig.54
 Oltre ad aminoglicosidi e diuretici, sono stati incriminati numerosi farmaci e molecole chimiche. L'interferone è responsabile di sordità correlata alle dosi ricevute ma reversibile alla sospensione del trattamento. Gli anticoncezionali orali sono stati incriminati in molti casi di sordità improvvisa con un meccanismo di trombosi.
Oltre ad aminoglicosidi e diuretici, sono stati incriminati numerosi farmaci e molecole chimiche. L'interferone è responsabile di sordità correlata alle dosi ricevute ma reversibile alla sospensione del trattamento. Gli anticoncezionali orali sono stati incriminati in molti casi di sordità improvvisa con un meccanismo di trombosi.
[ Hanna GS ,1986 ] La sordità è di norma reversibile. La sieroterapia antitetanica è responsabile di neuropatie periferiche e sono stati descritti casi di sordità improvvisa che si manifesta 48 ore dopo l'iniezione. [ Booth JB ,1997 ] Si tratta probabilmente di una reazione da ipersensibilità. L'intossicazione da monossido di carbonio è una causa classica di sordità improvvisa. Il gas, combinato con l'emoglobina, forma carbossiemoglobina che causa un'anossia cocleare. In caso di intossicazione acuta, la sordità è bilaterale ed è spesso asimmetrica. Si possono avere dei recuperi. Sono stati descritti casi di sordità fluttuante.
Varie
§ Casi di sordità improvvisa sono stati descritti nella rettocolite ulceroemorragica. La causa è probabilmente una vasculite.
§ Le forme neurologiche della sarcoidosi rappresentano il 5% dei casi di malattia. L'VIII paio di nervi cranici è frequentemente interessato sotto forma di una sordità fluttuante o improvvisa, a volte bilaterale con uno sfasamento di diversi mesi tra i due lati. Talvolta sono associati sintomi vestibolari. La lesione, a volte inaugurale, si produce con l'intermediazione di una meningite granulomatosa. La diagnosi può essere stabilita solo in base al riscontro di lesioni polmonari tipiche, di lesioni granulose cutanee, congiuntivali o lacrimali. La biopsia di una di queste lesioni o di un'adenopatia sopra-claveare può condurre alla diagnosi mostrando i granulomi epitelioidi. I corticosteroidi sono efficaci.
Cause retrococleari
Meningiti Fig.55
 Esse possono tutte essere responsabili di sordità improvvise, ma soprattutto le meningiti batteriche, in particolare la meningite da pneumococco. Più raramente sono in causa lesioni meningee in corso di leptospirosi, di tubercolosi o di criptococcosi. Le sordità sono spesso totali e bilaterali. Anche quando sono parziali, l'audiometria vocale è più alterata di quanto non lascerebbe prevedere l'audiometria tonale.
Esse possono tutte essere responsabili di sordità improvvise, ma soprattutto le meningiti batteriche, in particolare la meningite da pneumococco. Più raramente sono in causa lesioni meningee in corso di leptospirosi, di tubercolosi o di criptococcosi. Le sordità sono spesso totali e bilaterali. Anche quando sono parziali, l'audiometria vocale è più alterata di quanto non lascerebbe prevedere l'audiometria tonale.
Sclerosi a placche Fig.56
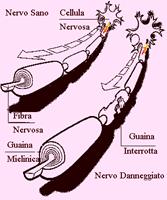 Raramente la sclerosi multipla si manifesta attraverso un’ipoacusia improvvisa Couturier L.,2001; Cummings D ed Al.,1990; - Dauman B, ed Al.,1985 ; Deguine O, Gardini B 2000 . La sordità in questa patologia è molto meno frequente delle vertigini. È la constatazione di anomalie neurologiche associate, anche minori, che devono orientare verso questa diagnosi. La RMN mostra tuttavia che il numero di sordità improvvise che precedono una sclerosi a placche è in aumento. [ Drulovic B, ed Al.,1993 ] Si deve sospettare alla scoperta di una placca di demielinizzazione localizzata sul sito di entrata della radice dell'VIII o sul tronco cerebrale con anomalie ai PEA.
Raramente la sclerosi multipla si manifesta attraverso un’ipoacusia improvvisa Couturier L.,2001; Cummings D ed Al.,1990; - Dauman B, ed Al.,1985 ; Deguine O, Gardini B 2000 . La sordità in questa patologia è molto meno frequente delle vertigini. È la constatazione di anomalie neurologiche associate, anche minori, che devono orientare verso questa diagnosi. La RMN mostra tuttavia che il numero di sordità improvvise che precedono una sclerosi a placche è in aumento. [ Drulovic B, ed Al.,1993 ] Si deve sospettare alla scoperta di una placca di demielinizzazione localizzata sul sito di entrata della radice dell'VIII o sul tronco cerebrale con anomalie ai PEA.
mori della fossa posteriore Fig.57
 Secondo le casistiche, si ritiene che il 10-15% dei neurinomi dell'acustico si presentano come una sordità improvvisa. Può trattarsi di una sordità improvvisa classica, con amputazione delle frequenze acute. In altri casi, si tratta di una sordità improvvisa che recupera dando l'impressione che il trattamento sia efficace. Qualunque sia il meccanismo patogenetico, ischemico o tumorale, due conclusioni meritano di essere sottolineate: 1- un recupero uditivo anche totale non esclude la possibilità di un neurinoma. Questo può essere con-fermato dai risultati recenti di Nageris e Popovtzer che hanno mostrato come il recupero completo dell’udito dopo un episodio di sordità improv-visa è identico sia in caso di neurinoma dell’acustico che di ipoacusia improvvisa idiopatica7; 2- la RMN con gadolinio deve essere un esame sistematico4-8.Il quadro più caratteristico è quello di una sordità improvvisa recidivante con segni premonitori omolaterali, vertigini o acufeni a testimonianza di un processo evolutivo. È possibile la confusione con la malattia di Menière, con la differenza che la sordità è predominante sulle frequenze acute invece di quella basse. Lo screening mediante lo studio dei PEA rimane valido benché siano stati riportati alcuni casi di neurinomi con PEA normali. È raro che questi ultimi non diventino di tipo retrococleare quando si ripetono a 6 mesi di intervallo. Altri tumori della fossa cranica posteriore possono essere chiamati in causa: un tumore primitivo o secondario del tronco cerebrale ,un meningioma o metastasi da cancro della mammella, della prostata, una sordità improvvisa è stata descritta anche come primo sintomo in una meningite carcinomatosa metastatica di un tumore polmonare primitivo10.. Sordità improvvise sono state descritte nel contesto di meningiti carcinomatose. [ Civantos F, Choi YS, 1992 ] In realtà, è ancora la risonanza magnetica nucleare che permette la diagnosi di questi tumori.
Secondo le casistiche, si ritiene che il 10-15% dei neurinomi dell'acustico si presentano come una sordità improvvisa. Può trattarsi di una sordità improvvisa classica, con amputazione delle frequenze acute. In altri casi, si tratta di una sordità improvvisa che recupera dando l'impressione che il trattamento sia efficace. Qualunque sia il meccanismo patogenetico, ischemico o tumorale, due conclusioni meritano di essere sottolineate: 1- un recupero uditivo anche totale non esclude la possibilità di un neurinoma. Questo può essere con-fermato dai risultati recenti di Nageris e Popovtzer che hanno mostrato come il recupero completo dell’udito dopo un episodio di sordità improv-visa è identico sia in caso di neurinoma dell’acustico che di ipoacusia improvvisa idiopatica7; 2- la RMN con gadolinio deve essere un esame sistematico4-8.Il quadro più caratteristico è quello di una sordità improvvisa recidivante con segni premonitori omolaterali, vertigini o acufeni a testimonianza di un processo evolutivo. È possibile la confusione con la malattia di Menière, con la differenza che la sordità è predominante sulle frequenze acute invece di quella basse. Lo screening mediante lo studio dei PEA rimane valido benché siano stati riportati alcuni casi di neurinomi con PEA normali. È raro che questi ultimi non diventino di tipo retrococleare quando si ripetono a 6 mesi di intervallo. Altri tumori della fossa cranica posteriore possono essere chiamati in causa: un tumore primitivo o secondario del tronco cerebrale ,un meningioma o metastasi da cancro della mammella, della prostata, una sordità improvvisa è stata descritta anche come primo sintomo in una meningite carcinomatosa metastatica di un tumore polmonare primitivo10.. Sordità improvvise sono state descritte nel contesto di meningiti carcinomatose. [ Civantos F, Choi YS, 1992 ] In realtà, è ancora la risonanza magnetica nucleare che permette la diagnosi di questi tumori.
Sordità centrali Fig.58
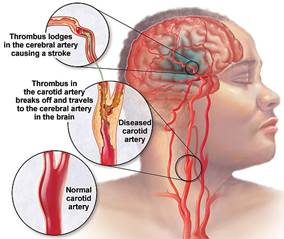 Sono stati riportati casi di infarto temporale bilaterale da occlusione dei rami terminali delle due arterie cerebrali medie, con una sordità centrale. Questi casi compaiono in generale in un contesto di embolismo in rapporto con la sostituzione di valvole mitraliche. Il recupero avviene in 2 -3 mesi, ma lascia spesso un'agnosia uditiva. Si può anche trattare di piccole lesioni ischemiche situate nella porzione posteriore del putamen che interrompono le fibre tra corpo genicolato mediale e lobi temporali. Nell'infarto del tronco cerebrale, l'audiometria può rimanere normale e sono alterati solo i PEA. L’insufficienza vertebro-basilare si manifesta con manifestazioni vertigi-nose. Possono tuttavia associarsi ad una sordità percettiva talvolta bila-terale17, spesso severa, ma con un calo peggiore nell’audiometria vocale che l’audiometria tonale non lascerebbe sospettare. Le otoemissioni acu-stiche sono in linea di massima negative18. Può trattarsi di un meccani-smo acuto, come la dissezione arteriosa dei vasi vertebro-basilari19 che può sopraggiungere dopo manipolazioni del rachide cervicale20. L’ipoacusia improvvisa può riscontrarsi anche nel quadro di patologie subacute: insufficienza vertebro-basilare emodinamica21, o di malformazioni congenite: “megadolico basilare”22. Nel ubbio di una tale eziologia l’esecuzione di un’angio-RMN e/o di un eco-doppler possono dirimere eventuali dubbi. Bisogna inoltre sottolineare il valore di una sordità improvvisa bilaterale come predittiva di un infarto dell’AICA1. Basandosi su dei dati necrosco-pici, Gussen ha proposto un meccanismo fisiopatogenetico secondo cui un’arteriosclerosi vertebro-basilaire prolungata potrebbe essere all’origine di una rottura prematura della membrana di Reissner23.
Sono stati riportati casi di infarto temporale bilaterale da occlusione dei rami terminali delle due arterie cerebrali medie, con una sordità centrale. Questi casi compaiono in generale in un contesto di embolismo in rapporto con la sostituzione di valvole mitraliche. Il recupero avviene in 2 -3 mesi, ma lascia spesso un'agnosia uditiva. Si può anche trattare di piccole lesioni ischemiche situate nella porzione posteriore del putamen che interrompono le fibre tra corpo genicolato mediale e lobi temporali. Nell'infarto del tronco cerebrale, l'audiometria può rimanere normale e sono alterati solo i PEA. L’insufficienza vertebro-basilare si manifesta con manifestazioni vertigi-nose. Possono tuttavia associarsi ad una sordità percettiva talvolta bila-terale17, spesso severa, ma con un calo peggiore nell’audiometria vocale che l’audiometria tonale non lascerebbe sospettare. Le otoemissioni acu-stiche sono in linea di massima negative18. Può trattarsi di un meccani-smo acuto, come la dissezione arteriosa dei vasi vertebro-basilari19 che può sopraggiungere dopo manipolazioni del rachide cervicale20. L’ipoacusia improvvisa può riscontrarsi anche nel quadro di patologie subacute: insufficienza vertebro-basilare emodinamica21, o di malformazioni congenite: “megadolico basilare”22. Nel ubbio di una tale eziologia l’esecuzione di un’angio-RMN e/o di un eco-doppler possono dirimere eventuali dubbi. Bisogna inoltre sottolineare il valore di una sordità improvvisa bilaterale come predittiva di un infarto dell’AICA1. Basandosi su dei dati necrosco-pici, Gussen ha proposto un meccanismo fisiopatogenetico secondo cui un’arteriosclerosi vertebro-basilaire prolungata potrebbe essere all’origine di una rottura prematura della membrana di Reissner23.
Malattia di Creutzfeldt-Jakob Fig.59
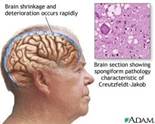 Vi si riscontrano casi di sordità improvvisa corticale.
Vi si riscontrano casi di sordità improvvisa corticale.
Encefaliti corticali Fig.60
 Nell'encefalite diffusa corticale può sopraggiungere una sordità centrale più o meno fluttuante con audiometria tonale normale. Il recupero è possibile, ma spesso tardivo, anche con terapia cortisonica. Casi di encefalite subacuta, in donne nel loro 3o o 4o decennio, caratterizzati da sordità improvvisa o fluttuante associata a occlusione delle arterie retiniche sono stati descritti senza altre manifestazioni sistemiche. La sordità unilaterale o bilaterale predomina sulle frequenze basse e medie. In alcuni di questi pazienti, con sintomi in progressione, una terapia con ciclofosfamide ha interrotto l'evoluzione.
Nell'encefalite diffusa corticale può sopraggiungere una sordità centrale più o meno fluttuante con audiometria tonale normale. Il recupero è possibile, ma spesso tardivo, anche con terapia cortisonica. Casi di encefalite subacuta, in donne nel loro 3o o 4o decennio, caratterizzati da sordità improvvisa o fluttuante associata a occlusione delle arterie retiniche sono stati descritti senza altre manifestazioni sistemiche. La sordità unilaterale o bilaterale predomina sulle frequenze basse e medie. In alcuni di questi pazienti, con sintomi in progressione, una terapia con ciclofosfamide ha interrotto l'evoluzione.
Trattamento
Aumentare il flusso ematico e l'ossigenazione cocleari
Vasodilatatori
Essi si propongono di aumentare la gittata sanguigna cocleare e di aumentare le pressioni parziali di O 2 nei liquidi endo e perilinfatici. Un vasodilatatore che agisce per via sistemica dovrebbe poter aumentare la gittata cocleare senza abbassare il flusso ematico cerebrale. Non si è mai potuto dimostrare nell'uomo un tale effetto collaterale. [ Kronenberg J, 1992]
Al contrario, gli esperimenti sugli animali mostrano che farmaci vasocostrittori come l'angiotensina causano paradossalmente un leggero aumento della PO2 nei liquidi perilinfatici. Al contrario, una vasodilatazione prodotta da questi farmaci è seguita da un'azione opposta. In realtà, le misure di PO2 negli spazi perilinfatici mostrano che esiste una correlazione diretta tra l'ossigenazione dell'orecchio interno e la pressione arteriosa. I farmaci vasodilatatori dovrebbero quindi essere abbandonati. [ Wilkins SA, 1987]
Soluzione a basso peso molecolare: destrano
Questo prodotto era usato contro la ipercoagulabilità. Tuttavia, questo farmaco ha provocato incidenti in caso di insufficienza cardiaca o di emorragia. Non è stato osservato alcun beneficio nel caso della sordità improvvisa. [ Kronenberg J, 1992]
Inalazioni di carbogeno
Si tratta di una miscela di 95% di ossigeno e di 5% di gas carbonico. Questa miscela gassosa è conosciuta come vasodilatatore cerebrale. Avrebbe la proprietà di aumentare la pressione parziale di ossigeno dei liquidi perilinfatici. Effetti benefici sono possibili ma non ancora chiaramente provati. [ Kallinen J, 2001] .
Emodiluizione
Essa consiste nel realizzare un salasso, centrifugare le emazie e reiniettare nel paziente il suo stesso plasma. In altri protocolli, il sangue prelevato è sostituito, volume per volume, con succedanei del plasma (gelatine, soluzioni per infusione endovenosa). Il monitoraggio dell'emodiluizione si fa pesando le sacche di sangue e misurando con regolarità l'ematocrito su tubo capillare. La riduzione dell'ematocrito comporta un abbassamento della viscosità e una riduzione della resistenza alla circolazione di ritorno e, dunque, un aumento della frequenza cardiaca. Nei microcircoli, il ridotto numero di globuli rossi provoca un'accelerazione della perfusione. Ciò permette di mitigare il rallentamento circolatorio nei territori patologici a bassa gittata. L'ossigenazione fornita dal plasma è aumentata. Se si analizza la curva del flusso in ossigeno in rapporto al valore dell'ematocrito, riducendo progressivamente l'ematocrito, si aumentano progressivamente le capacità di trasporto dell'ossigeno [ Dauman B,1985 ]. Questo si fa fino a un valore ottimale che si situa nell'uomo su un ematocrito tra 28 e 31%. Al di sotto, si verifica il contrario e la quantità di ossigeno trasportato si riduce. In pratica, l'emodiluizione dovrebbe ridurre il valore iniziale dell'ematocrito del 25% per raggiungere un valore ottimale del 30%. Il prelievo sarebbe in tal modo di 12 mL/kg di peso corporeo senza superare la soglia di 15 mL con un prelievo che può raggiungere 890 mL per un soggetto di 80 kg. La metà del prelievo deve essere raggiunta in 20 minuti, essendo la durata dell'emodiluizione compresa tra 40 e 60 minuti. In tali condizioni, i rischi sono coronarici per l'aumento della gittata e del lavoro cardiaco. Può comparire ipotensione 4 - 8 ore dopo l'inizio del prelievo. Ciò richiede quindi un monitoraggio della pressione e la conservazione delle vie venose. L'emodiluizione persiste per 21 giorni. È controindicata in gravidanza, nel postoperatorio immediato e nel bambino i cui compartimenti idrici sono differenti con rischio di shock, d'ipotensione arteriosa e anche di anuria.
Ossigeno iperbarico
Si tratta di ossigeno puro somministrato a una pressione superiore alla pressione atmosferica con aumento della quantità di O2 disponibile a livello cellulare e saturazione tissutale di questo gas. Si avrebbe un aumento della pressione parziale di O2 perilinfatica e una lieve riduzione del FEC. Il paziente è posizionato in una camera iperbarica e sottoposto a una pressione di 2,2 atmosfere per 90 minuti dopo essersi assicurati di una funzione tubarica normale. I protocolli variano da un centro all'altro: una seduta al giorno per 10 giorni consecutivi o due sedute al giorno per 5 giorni. Si deve notare che spesso compare un fattore trasmissionale a causa di catarro tubarico post-terapia. Il trattamento con ossigeno iperbarico è controverso. Si tratta di un trattamento astenizzante, non esente da rischi di fibrosi polmonare. Tuttavia, alle pressioni generalmente utilizzate, le complicanze sono rare. Alcuni centri vi trovano un interesse terapeutico, altri no. [ Couturier L, 2001 ;] 11
Defibrinogenazione (Batroxobin)
Una riduzione del fibrinogeno ematico diminuisce la viscosità ematica. [ Shiraishi T, 1993 ] .I fibrinolitici hanno l'effetto di abbassare il tasso del fibrinogeno ematico. L'obiettivo non è di sciogliere un trombo, ma di diminuire la viscosità sanguigna: è un modo di aumentare la gittata del microcircolo. Tali tecniche sono state testate in contrapposizione con i corticosteroidi in uno studio in doppio cieco, randomizzato. Esisterebbe una differenza significativa. Ma gli effetti collaterali dei fibrinolitici non sono banali: dolori toracici, vertigini, nausea ecc...
Terapie ipolipemizzanti
Dieta e terapia farmacologica sono state proposte anche 1 mese dopo l'esordio della sordità in pazienti in cui l'iperlipidemia era di 230 mg/dl o più.[ Kojima Y, 2001 .]
Prostaglandine
Esse sono sintetizzate dalla parete vascolare dei vasi della stria vascolare e del legamento spirale. In caso di sordità improvvisa, la somministrazione di prostaglandina E1 o di prostaciclina è stata tentata nella speranza di ottenere l'effetto antiaggregante delle piastrine e vasodilatatore che si è dimostrato efficace nella malattia di Raynaud grave. Sfortunatamente, i risultati restano dubbi e il trattamento difficile da gestire. Sono tuttora in corso altri studi sull'effetto delle prostaglandine sulla sordità fluttuante. L'uso di prostaglandina E2 migliora transitoriamente la sordità fluttuante di questi pazienti come farebbe la furosemide. [ Booth JB A Kerr Scott-Brown's otolaryngology. London: Butterworth-Heinemann: 1997]
Corticosteroidi
I corticosteroidi agiscono sui processi infiammatori e autoimmuni e più in generale sui processi risultanti da danni fisici, chimici, ischemici e ipossici. I protocolli utilizzati sono molto variabili. Generalmente 1 mg/kg per 10 giorni quindi dosi decrescenti. Il protocollo di Stennert utilizzato nella paralisi facciale è stato suggerito in caso di ricovero: [ Tran Ba Huy P, 2002 :81] metilprednisolone: g1 - g2: endovenosa lenta, se il peso è < 70 kg: 100 mg × 2/die e se peso > 70 kg: 120 mg × 2/die; g3 - g4: per via orale, 80 mg × 2/die; g5 - g6: 100 mg/die; g7 - g10: 75 mg/die. Il monitoraggio del trattamento comprende misurazioni regolari della pressione arteriosa, il bilancio idroelettrolitico e glucidico. In caso di controindicazioni, è stata proposta la via transtimpanica [ Gianoli GJ, 2001 ] .
Trattamento antipertensivo
mannitolo e diuretici sono utilizzati soprattutto nelle sordità fluttuanti per analogia con le sordità fluttuanti della malattia di Menière. Per quanto riguarda il mannitolo, è uno zucchero che potrebbe spostare l'acqua dei liquidi intralabirintici in direzione del plasma in caso di somministrazione breve, e spostare l'endolinfa verso la perilinfa in caso di perfusione prolungata. [ Tran Ba Huy P, 2002] Se ne possono prescrivere 500 ml al 10% in 6 ore associati a 2 g di KCl e una dieta senza sale.
Antivirali
Per il momento, soltanto uno studio sperimentale su modello animale di labirintite virale da HSV1 suggerisce che la somministrazione di acyclovir associato a corticosteroidi migliora la rapidità del recupero in confronto all'acyclovir o al cortisonico da soli [ Stokroos RJ, 1999 ].
Riposo a letto
È alla base del trattamento se si privilegia l'origine da rottura membranosa. Si ritiene che il riposo affretti la cicatrizzazione del labirinto membranoso. Si devono quindi evitare anche gli sforzi che provocano una pressione endocranica come sollevare grossi pesi, in caso di stipsi o durante gli sforzi sessuali.
Indicazioni, discussione
Il dogma dell'urgenza è stato recentemente rimesso in discussione. Nessuno studio ha potuto provare l'efficacia di un trattamento precoce. Tenuto conto del recupero spontaneo nei primi 15 giorni, il ritardo di trattamento seleziona i casi sfavorevoli e una terapia precoce seleziona quelli con prognosi buona.
La scelta della terapia non è unanime, ma in pratica, è inconcepibile non trattare (Tran Ba Huy P, ed Al.2002).Il ricovero ha almeno il merito di obbligare al riposo e di isolare ma non esistono valutazioni al riguardo e il suo valore è ancora da dimostrare).
L'impiego dei corticosteroidi è attualmente il trattamento meno discusso. Esistono studi versus placebo, ma i loro risultati sono contraddittori. Mattox DE, Lyles CA 1989 e Simmons 1968 hanno rilevato che 20 su 28 pazienti non trattati (71%) recuperano l'udito completamente o in buona parte rispetto a 63 su 88 trattati con corticosteroidi (72%). Wilson WR, ed Al.,1980 hanno isolato un gruppo di 67 pazienti con una sordità improvvisa che predomina sulle frequenze acute o sulle frequenze basse, escludendo i pazienti in cui la sordità è predominante sulle frequenze medie dato che questi recuperano quasi costantemente. In questo gruppo, senza trattamento, ha osservato il 32% di recuperi spontanei (11/34 pazienti) e con corticosteroidi: 61% (20/33 pazienti). [Moskowitz D, ed Al., 1984, hanno dimostrato che 24 pazienti su 27 (89%) trattati con corticosteroidi recuperava per lo meno il 50% dell'udito, rispetto a quattro su nove pazienti non trattati (44%). Veldman JE,ed Al, 1993 hanno osservato il 50% di miglioramento (6/12) nel gruppo con corticosteroidi e il 32% senza corticosteroidi (6/19). Tutti questi studi hanno imperfezioni metodologiche: troppo pochi pazienti, gruppi non omogenei ecc. La tendenza è tuttavia a dimostrare una certa efficacia, tranne per quanto riguarda il tipo audiometrico [ Kitajiri SK,ed Al. 2002]
Esistono dunque pochi elementi per sostenere un protocollo piuttosto che un altro. Il rapporto della Società francese di ORL 2002 (81)suggerisce il protocollo di Stennert utilizzato nella paralisi facciale, ma sottolinea che nessun trattamento ha dato prova della sua efficacia reale nell'uomo.
Metilprednisolone liofilizzato in soluzione iniettabile: g1 - g2, endovenosa lenta; se < 70 kg: 100 mg × 2/die; se > 70 kg: 120 mg × 2/die; g3 - g4: 80 mg × 2/die; g5 - g6: 100 mg/die; g7: 75 mg/die.
Pentossifillina 400: 2 fiale/die a g1 e g2; 3 fiale/die da g3 a g7.
Quindi in via ambulatoriale: metilprednisolone 16 mg o prednisolone 20 mg: 4 compresse/die a dosi decrescenti fino a g18 per stadi ogni 2 giorni; pentossifillina 400: 3 compresse/die.
Il rapporto non precisa le eventuali indicazioni all'emodiluizione, all'ossigeno iperbarico ecc.
Il protocollo personale degli Autori comporta una prescrizione di carbogeno per sei sedute quotidiane di 20 minuti ognuna con un flusso di 3-5 l/min. I presidi terapeutici possono essere utilizzati diversamente secondo le scuole: forti dosi di corticosteroidi (200 mg/die), ossigeno iperbarico [ Deguine O, 2000] emodiluizione [ Dauman B, 1985] in seconda intenzione. In genere viene stabilita una politerapia «shotgun regimen». Per gli Autori del rapporto, ci si trova, dunque, ancora nella necessità di realizzare studi prospettici.
Conclusione
Il meccanismo intimo delle sordità improvvise e fluttuanti è ancora da scoprire. Nelle sordità improvvise, alcuni quadri clinici di diversa eziologia possono essere sospettati sulla morfologia audiometrica, ma nessuna delle cause attualmente proposte possono essere comprovate su paziente vivente. Fatta eccezione per la malattia di Ménière, le sordità fluttuanti hanno dato luogo a molto rari studi. La speranza è ancora di scoprire l'esame complementare o l'esame radiografico che permetta di scoprire quel che succede nell'orecchio interno. Per il momento, l'approccio diagnostico consiste nel non sottovalutare patologie suscettibili di richiedere una cura specifica: neurinoma dell'acustico, accidente cerebrovascolare, sifilide, immunopatie. La valutazione dei trattamenti non è sempre stata realizzata perché il tasso di recuperi spontanei è elevato. Tuttavia, la maggior parte degli Autori propone una terapia. Riposo e cortisonici sono i meno discussi. Né i corticosteroidi, né i trattamenti a obiettivo vascolare hanno dimostrato la loro efficacia. Il ricovero stesso non ha dimostrato una qualche superiorità rispetto ai trattamenti ambulatoriali. L'utilità di una terapia precoce nemmeno. Nelle sordità improvvise, sarebbero necessari studi prospettici ma sono difficili da realizzare perché si tratta di una patologia rara e perché ogni singolo centro non può riunire grandi casistiche omogenee. Inoltre, esistono numerosi parametri in grado di influire sulla probabilità di recupero: il ritardo del trattamento studiato, l'età del paziente, la coesistenza di vertigini e il tipo di curva audiometrica. Altre molecole dovrebbero essere testate. Non si dispone di modelli sperimentali che permettano di scegliere tali molecole prima di proporle per una sperimentazione umana. Giocoforza è quindi, per il momento, gestire i pazienti con modestia e con il minimo di limiti e di rischi terapeutici.
Le sordità fluttuanti restano un'entità complessa, in quanto mal definita. La loro origine può essere legata a cause malformative o traumatiche e la diagnosi si basa, prima di tutto, sulla diagnostica per immagini; tuttavia, esse sono, a volte, la manifestazione di patologie genetiche, sindromiche o meno, e di patologie autoimmuni o infiammatorie che richiedono una consulenza multidisciplinare con il ricorso rispettivo ai pediatri, ai genetisti e agli internisti.
Riferimenti
Albers FW, Majoor MH, Van Der Gaag R Corneal autoimmunity in a patient with relapsing polychondritis. Eur Arch Otorhinolaryngol 1992 ; 249 : 296-299 [crossref]
Ayache D., Plouin-Gaudon I., Bakouche P., Elbaz P., Gout O. Microangiopathy of the inner ear, retina and brain (Susac syndrome). Report of a case Arch Otolaryngol Head and Neck Surg 2000 ; 126 : 82-84 [cross-ref]
Alexiou C, Arnold W, Fauser C, Schratzenstaller , Gloddek B, Fuhrman S , e al. Sudden sensorineural hearing loss. Does application of glucocorticoids make sense. Arch Otolaryngol Head Neck Surg 2001 ; 127 : 253-258
Anand VT, Mann SB, Dash RJ, Mehra YN Auditory investigations in hypothyroidism. Acta Otolaryngol 1989 ; 108 : 83-87 [crossref]
Asakura M., Kato I., Takahashi K., Okada T., Minami S., Takeyama I., e al. Increased platelet agregability in patients with vertigo, sudden deafness and facial palsy Acta Otolaryngol [suppl] 1995 ; 520 (Pt2) : 399-400 [cross-ref]
Baker SR, Lilly DJ Hearing loss from acute carbon monoxide intoxication. Ann Otol Rhinol Laryngol 1977 ; 86 : 323-328
Baloh RW Neurotology of migraine. Headache 1997 ; 37 : 615-621 [crossref]
Bichey B.G., Hoversland J.M., Wynne M.K., Miyamoto R.T. Changes in quality of life and the cost-utility with cochlear implantation in patients with large vestibular aqueduct syndrome Otol Neurotol 2002 ; 23 : 323-327 [cross-ref]
Booth JB Sudden and fluctuant sensorineural hearing loss. A Kerr Scott-Brown's otolaryngology. London: Butterworth-Heinemann: 1997; 1-82.
Cadoni G, Agostino S, Manna R, De Santis A, Fetoni AR, Vulpiani P , e al. Clinical associations of serum antiendothelial cell antibodies in patients with sudden sensorineural hearing loss. Laryngoscope 2003 ; 113 : 797-801 [crossref]
Cama E., Alemanno M.S., Bellacchio E., Santarelli R., Carella M., Zelante L., e al. Identification of a novel mutation in the SLC26A4 gene in an Italian with fluctuating sensorineural hearing loss Int J Pediatr Otorhinolaryngol 2009 ; 73 : 1458-1463 [cross-ref]
Camaro Da Silva D.P., Montovani J.C., Oliveira D.T., Fioravanti M.P., Tamashiro I.A. The large vestibular aqueduct syndrome: a cause of neurosensory dysacusia Pro Fono 2008 ; 20 : 133-135
Camicas-Van Gout M., Negrevergne M., Portmann D., Lahrizia R., Dauman R., Darrouzet V., e al. Impedancemétrie multifréquentielle et maladie de Ménière : analyse des résultats du Teflag Rev Laryngol Otol Rhinol 1999 ; 120 : 317-321
Clement P., Conessa C., Dot C., Kossowski M., Flocard F., Poncet J.L. Syndrome de Susac ou microangiopathie cochléo-encéphalo-rétinienne Ann Otolaryngol Chir Cervicofac 2003 ; 120 : 49-53
Clemis J., Valvassori G. The large vestibular aqueduct syndrome Laryngoscope 1978 ; 88 : 723-728
Brookhouser P.E. Fluctuating and progressive sensorineural hearing loss in children Pediatric Otology and Neurotology Philadelphia: Lippincott-Raven Publishers (1998). 617-626
Christoforidis G.A., Mehta B.A., Landi J.L., Czarnecki E.J., Piaskowski R.A. Spontaneous intracranial hypotension: report of four cases and review of the literature Neuroradiology 1998 ; 40 : 636-640 [cross-ref]
Civantos F, Choi YS, Applbaum EL Meningeal carcinomatosis producing bilateral sudden hearing loss: a case report. Am J Otol 1992 ; 13 : 369-371
Clerico DM, Jahn AF, Fontanella S Osteoma of the internal auditory canal: case report and literature review. Ann Otol Rhinol Laryngol 1994 ; 103 : 619-623
Committee on hearing and equilibrium Guidelines for the diagnosis and evaluation of therapy in Menière's disease. Otolaryngol Head Neck Surg 1995 ; 113 : 181-185
Compadretti G.C., Brandolini C., Tasca I. Sudden sensorineural hearing loss in lupus erythematous associated with antiphopholipid syndrome. Case report and review Ann Otol Rhinol Laryngol 2005 ; 114 : 214-218
Couturier L Surdité brutale : deux études divergent sur l'intérêt de l'oxygénothérapie hyperbare. Quot Méd 2001 ; 6988 : 21
Cummings D, McCormick JB, Bennett D, Samba JA, Farrar B, Machin SH , e al. Acute sensorineural deafness in Lassa fever. JAMA 1990 ; 264 : 2093-2096
Dauman B, Poisot D, Cross AM, Mehsen M Hémodilution, oxygénothérapie hyperbare et vasodilatateurs dans les surdités brusques. J Fr ORL 1985 ; 34 : 93-96
Deguine O, Gardini B Surdités d'apparition brutale. Rev Prat 2000 ; 50 : 1695-1700 Dinces EA, Yang S,
Balogun AO Pediatric fluctuating sensorineural hearing loss: problems in medical management. Laryngoscope 2001 ; 111 : 21-25 [crossref]
Downie AC, Howlett DC, Koefman RJ, Banerjee AK, Tonje KA Prolonged contrast enhancement of the inner ear on magnetic resonance imaging in Ramsay Hunt syndrome. Br J Radiol 1994 ; 67 : 819-821 [crossref]
Drulovic B, Ribaric-Jankes F, Kostic VS, Sternic N Sudden hearing loss as the initial mono-symptom of multiple sclerosis. Neurology 1993 ; 43 : 2703-2705 Eggermont J.J. Summating potentials in Ménière's disease Arch Otorhinolaryngol 1979 ; 222 : 65-75
Einer H, Tengborn L, Axelsson A, Edström S Sudden Sensorineural hearing loss and hemostatic mechanisms. Arch Otolaryngol Head Neck Surg 1994 ; 120 : 536-540
Farrel RW, Pemberton MN, Parker AJ, Buffin JT Sudden deafness after dental surgery. Br Med J 1991 ; 303 : 1034
Fetterman BL, Luxford WM, Saunders JE Sudden Bilateral sensorineural Hearing loss. Laryngoscope 1996 ; 106 : 1347-1350 [crossref]
Finizia C, Jönsson R, Hanner P Serum and cerebral fluid pathology in Patients with Sudden Hearing Los. Acta Otolaryngol 2001 ; 121 : 823-830
Fong R.S., Beste D.J., Murray K.J. Pediatric sensorineural hearing loss after temporal bone radiation Am J Otol 1995 ; 16 : 793-796
Fraser G.R. Association of congenital deafness with goitre (Pendred syndrome): a study of 207 familiesAnn Hum Genet 1965 ; 28 : 201-249
Fraser F.C., Sproule J.R., Halal F. Frequency of the branchio-oto-renal syndrome in children with profound hearing loss J Med Genet 1980 ; 7 : 341-349 [cross-ref]
Friedman I, Frohlich A, Wright A Epidemic typhus fever and hearing loss: a histological study. J Laryngol Otol 1993 ; 107 : 275-283
Fuse T, Hayashi T, Oota N, Fukase S, Asano S, Kato T , e al. Immunological responses in acute low-tone sensorineural hearing loss and Menière's disease. Acta Otolaryngol 2003 ; 123 : 26-31 [crossref]
Gagnebin J, Maire R Infection screening in sudden and progressive idiopathic sensorineural hearing loss. A retrospective study of 182 cases. Otol Neurotol 2002 ; 23 : 160-162 [crossref]
Gianoli GJ, Li JC Transtympanic steroids for treatment of sudden hearing loss. Otolaryngol Head Neck Surg 2001 ; 125 : 142-146 [crossref]
Goodhill V. Sudden deafness and round windows ruptures Laryngoscope 1971 ; 81 : 1462-1474 [cross-ref]
Goodhill V. Inner ear barotrauma Arch Otolaryngol 1972 ; 13 : 70-72
G Grover N., Whiteside O.J., Ramsden J.D. Susac syndrome: outcome of unilateral cochlear implantation J Laryngol Otol 2011 ; 125 : 856-858 [cross-ref]
ussen R Sudden hearing loss associated with cochlear membrane rupture. Arch Otolaryngol Head Neck Surg 1981 ; 107 : 598-600
Guyot JP, Thielen K Évolution des surdités brusques sans traitement. Schweiz Med Wochenschr [suppl] 2000 ; 116 : 93S-96S [crossref]
Hall SJ, McGuigan JA, Rocks MJ Red blood cell deformability in sudden sensorineural deafness: another aetiology. Clin Otolaryngol 1991 ; 16 : 3-7 [crossref]
Hanna GS Sudden deafness and the contraceptive pill. J Laryngol Otol 1986 ; 100 : 701-706
Hariri MA Sensorineural hearing loss in bullous myringitis. A prospective study in eighteen patients. Clin Otolaryngol 1990 ; 15 : 351-353 [crossref]
Hazell J.W., Fraser J.G., Robinson P.J. Positional audiometry in the diagnosis of perilymphatic fistula Am J Otol 1992 ; 113 : 21-25
Hegarty JL, Patel S, Fischbein N, Jackler RK, Lalwani AK The value of enhanced magnetic resonance imaging in the evaluation of endocochlear disease. Laryngoscope 2002 ; 112 : 8-17 [crossref]
Herman P, Hervé S, Portier F, Tronche S, De Waele C, Tran Ba Huy P. Maladie de Ménière. EMC (Elsevier Masson SAS, Paris), Oto-rhino-laryngologie, 20-205-A-10, 2003.
Hochermann M, Reimer A Hearing loss after general anesthesia. A case report and review of the literature. J Laryngol Otol 1987 ; 101 : 1079-1082
Honings J., Pennings R.J., Hoefsloot L.H., Joosten F.B., Cremers C.W. Head trauma as eliciting event in transient deterioration of sensorineural hearing loss and vertigo in Pendred/EVA syndrome Int J Pediatr Otorhinolaryngol Extra 2008 ; 3 : 177-181 [cross-ref]
Hulbert TV, Larsen RA, Davis CL, Holtom PD Bilateral hearing loss after measle and rubella vaccination in an adult. N Engl J Med 1991 ; 325 : 134
Hultcrantz E Sudden deafness-A critical Evaluation of Pathogenesis and cure. Otorhinolaryngol Nova 1999 ; 9 : 178-189 [crossref] In-Hoo Kim, Jin-Kyoung Kim, Si-Ra Bang, ,Woo-Seok Sim, . and Ik-Soo Chung, Sudden Sensorineural Hearing Loss after General Anesthesia - A case report - Korean Journal of Anesthesiology. 2008 Mar;54(3):359-362 http://dx.doi.org/10.4097/kjae.2008.54.3.359
Kakigi A., Sawada S., Takeda T., Takeuchi S., Higashiyama K., Azuma H., e al. Electrocochleographic findings in cases of auto immune disease with sensorineural deafness Auris, Nasus Larynx 2003 ; 30 : 349-354 [cross-ref]
Kallinen J, Laurikainen E, Bergroth L, Grenman R A follow-up study of patients suffering from sudden sensorineural hearing loss. Acta Otolaryngol 2001 ; 121 : 818-822
Katholm M, Johnsen NJ, Siim C, Willumsen L Bilateral sudden deafness and acute aquired toxoplasmosis. J Laryngol Otol 1991 ; 105 : 115-118
Khonishi K, Yamane H, Igushi H Local substances regulating cochlear blood flow. Acta Otolaryngol [suppl] 1998 ; 553 : 40-46
Kemperman M.H., Stinckens C., Kumar S., Huygen P.L., Joosten F.B., Cremers C.W. Progressive fluctuant hearing loss, enlarged vestibular aqueduct and cochlear hypoplasia in brancio-oto-renal syndrome Otol Neurol 2001 ; 22 : 637-643 [cross-ref]
Kemperman M.H., Koch S.M., Kumar S., Huygen P.L., Joosten F.B., Cremers C.W. Evidence of progression and fluctuation of hearing impairment in branchio-oto-renal syndrome Int J Audiol 2004 ; 43 : 523-532 [cross-ref]
Klingmann C., Benton P., Schellinger P., Knauth M. A safe treatment concept for divers with acute inner ear disorders Laryngoscope 2004 ; 114 : 2048-2050 [cross-ref]
Kobayashi H, Susuki A, Nomura Y Unilateral hearing loss following rubella infection in an adult. Acta Otolaryngol [suppl] 1994 ; 514 : 49-51 [crossref]
Koesling S., Rasinski C., Amaya B. Imaging and clinical findings in large endolymphatic duct and sac syndrome Eur J Radiol 2006 ; 57 : 54-62 [cross-ref]
Kojima Y, Ito S, Furuya N Hearing improvement after therapy for hyperlipidemia in patients with chronic-phase sudden deafness. Ann Otol Rhinol Laryngol 2001 ; 110 : 105-108
Kronenberg J, Almagor M, Bendet E, Kushnir D Vasoactive therapy versus placebo in the treatment of sudden hearing loss: a double blind clinical study. Laryngoscope 1992 ; 102 : 65-68
Levenson M.J., Pariser S.C., Jacobs M., Edelstein D.R. The large vestibular aqueduct syndrome in childrenArch Otolaryngol Head And Neck Surg 1989 ; 115 : 54-58
Linstrom CJ, Pincus RL, Leauitt EB, Urbina MC Otologic neurotologic manifestations of HIV-related diseases. Otolaryngol Head Neck Surg 1993 ; 108 : 680-687
Lorenzi MC, Bittar RS, Pedalini ME, Zerati F, Yoshinari NH, Bento RF Sudden Deafness and Lyme disease. Laryngoscope 2003 ; 113 : 312-315 [crossref]
Madden C., Wiley S., Schleiss M., Benton C., Meinzen-Derr J., Greinwald J., e al. Audiometric, clinical and educational outcomes in a pediatric symptomatic congenital cytomegalovirus population with sensorineural hearing loss Int J Pediatr Otorhinolaryngol 2005 ; 69 : 1191-1198 [cross-ref]
Marlin S., Feldmann D., Blons H., Loundon N., Rouillon I., Garabedian E.N., e al. GJB2 and GJB6 mutations: genotypic and phenotypic correlations in a large cohort of hearing impaired patients Arch OtoLaryngol Head Neck Surg 2005 ; 131 : 481-487 [cross-ref]
Martin H, Martin C Les surdités fluctuantes. Ann Otolaryngol Chir Cervicofac 1977 ; 94 : 679-699 Martin C Les surdités fluctuantes. OPA Prat 1998 ; 121 : 1-6 [crossref]
Martin C, Mosnier I, Robier A, Bertholon P, Dubreuil C, Chobaut JC , e al. La pathologie vasculaire en ORL. Part du vasculaire dans les manifestations cochléo-vestibulaires. Rapport de la société française d'ORL 2000 : 237-258 [crossref]
Mattox DE, Lyles CA Idiopathic sudden sensorineural hearing loss. Am J Otol 1989 ; 10 : 242-247
Maturo S., Horlbeck D. Enlarged vestibular aqueduct syndrome: a case of bilateral sudden sensorineural hearing loss in a child Int J Pediatr Otorhinolaryngol Extra 2006 ; 1 : 142-144 [cross-ref]
Mazzoni A Internal auditory artery supply to the petrous bone. Ann Otol Rhinol Laryngol 1972 ; 81 : 13-21
McKennan KX, Nielsen SL, Watson C, Wiesner K Meniere's syndrome: an atypical presentation of giant cell arteritis (temporal arteritis). Laryngoscope 1993 ; 103 : 1103-1107
Mercier E, Quere I, Chabert R, Lallemant JG, Daures JP, Berlan J , e al. The 20210A allele of the prothrombin gene is an independent risk factor for perception deafness in patients with venous thromboembolic antecedents [letter]. Blood 1999 ; 93 : 3150-3152
Michel O, Brusis T Hearing loss as a sequel of lumbar puncture. Ann Otol Rhinol Laryngol 1992 ; 101 : 390-394
Mom T, Avan P, Bonfils P, Gilain L Vulnerability of the gerbil cochlea to sound exposure during reversible ischemia. Hear Res 1999 ; 136 : 65-74 [crossref]
Mom T, Porret C, Carvahlo S, Laurent S, Velin JF, Crestani S , e al. Analyse des oto-émissions acoustiques en cas de surdité brusque. Communication à la société française d'ORL. Rev Off Soc Fr ORL 2003 ; 80 : 110
Moskowitz D, Lee KJ, Smith HW Steroid use in idiopathic sudden sensorineural hearing loss. Laryngoscope 1984 ; 94 : 664-666
Mosnier I, Bouccara D, Sterkers O Les surdités brusques en 1997 : hypothèses étiopathogéniques, conduite à tenir, facteurs pronostiques, traitements. Ann Otolaryngol Chir Cervicofac 1997 ; 114 : 251-266
Nagahata M, Hosoya T, Fuse T, Aoyagi M, Yamaguchi K Arterial dissection of the vertebrobasilar systems: a possible cause of acute sensorineural hearing loss. Am J Otol 1997 ; 18 : 32-38
Ness JA, Stankiewicz JA, Kaniff T, Pifarre R, Allegretti J Sensorineural hearing loss associated with aortocoronary bypass surgery: a prospective study. Laryngoscope 1993 ; 103 : 589-593
Nobutoki T., Sasaki M., Fukumizu M., Hanaoka S., Sugai K., Anzai Y., e al. Fluctuating hearing loss, episodic headache and stroke with platelet hyperaggregability: coexistence of auditory neuropathy and cochlear hearing loss Brain Dev 2006 ; 28 : 55-59 [cross-ref]
Nozawa I, Imamura S, Mizukoshi A, Honda H, Okamoto Y Clinical study of acute low-tone sensorineural hearing loss: survey and analysis of glycerol test and orthostatic test. Ann Otol Rhinol Laryngol 2002 ; 111 : 160-164
Odetoyinbo O, Adekile A Sensorineural hearing loss in children with sickle cell anemia. Ann Otol Rhinol Laryngol 1987 ; 96 : 258-260
Ogawa K, Kanzaki J Aplastic anemia and sudden sensorineural hearing loss. Acta Otolaryngol [suppl] 1994 ; 514 : 85-88 [crossref]
Ohinata Y, Makimoto K, Haginomori SI, Araki M, Takahashi H Blood viscosity and plasma viscosity in patients with sudden deafness. Acta Otolaryngol 1994 ; 114 : 601-607 [crossref]
Pelisse JM, Perles B, Jobert F, Charpy N, Fabiani F, Baril C À propos de 100 surdités brusques traitées en 10 ans : relations avec la maladie de Barlow. J Fr ORL 1988 ; 37 : 459-469 Phelps P.D.,
Mahoney C.F., Luxon L.M. Large endolymphatic sac: a congenital deformity of the inner ear shown by magnetic resonance imaging J Laryngol Otol 1997 ; 111 : 754-756
Pirodda A, Ferri GG, Modugno GC, Borghi C Systemic hypotension and the development of acute sensorineural haring loss in young healthy subjects. Arch Otolaryngol Head Neck Surg 2001 ; 127 : 1049-1052
Pitkäranta A, Vasama JP, Julkunen I Sudden deafness and viral infections. Otorhinolaryngol Nova 1999 ; 9 : 190-197 Portmann D., Souza Leao F., Bussières R., Noyon P. Validation de l'échelle clinique pour le diagnostic des fistules périlymphatiques Rev Otol Laryngol Rhinol 2005 ; 126 : 243-248
Psifidis A.D., Psillas G.K., Daniilidis J.C. Sudden sensorineural hearing loss: long-term follow-up resultsOtolaryngol Head Neck Surg 2006 ; 134 : 809-815 [cross-ref]
Ramirez-Camacho R., Ramon Garcia Berrocal J., Arellano B., Trinidad A. Familial isolated unilateral large vestibular aqueduct syndrome ORL J Otorhinolaryngol Relat Spec 2003 ; 65 : 45-48 [cross-ref]
Reid A., Marchbanks R.J., Bateman D.E., Martin A.M., Brighwell A.P., Pichard J.D. Mean intracranial pressure monitoring by a non-invasive audiological technique: a pilot study J Neurol Neurosurg Psychiatry 1989 ; 52 : 610-612 [cross-ref]
Ren T, Laurikainen E, Quirk WS, Miller JM, Nuttal AL Effects on stellate ganglion stimulation on bilateral cochlear blood flow during increases in blood presure in human. Ann Otol Rhinol Laryngol 1993 ; 102 : 378-384
Rinehart R, Harre RG, Roski RA, Dolan KD Anevrysm of the anterior inferior cerebellar artery producing hearing loss. Ann Otol Rhinol Laryngol 1992 ; 101 : 705-706
Roman S, Aladio P, Paris J, Nicolla R, Triglia JM Prognostic factors of sudden hearing loss in children. Int J Pediatr Otorhinolaryngol 2001 ; 61 : 17-21 [crossref] Rosingh H.J., Wit H.P., Albers F.W. Non-invasive perilymphatic pressure measurement in normal hearing subjects using MMS 10 tympanic Displacement analyser Acta Otolaryngol 1996 ; 116 : 382-387 [cross-ref]
Sauvage JP, Puyraud S, Khalifa N. Surdités brusques et fluctuantes. EMC (Elsevier Masson SAS, Paris), Oto-rhino-laryngologie, 20-183-A-10, 2004.
Shea J.J., Xianxi G., Orchik D.J. Endolymphatic hydrops associated with otosclerosis Am J Otol 1994 ; 16 : 348-357Schuknecht HF, Donovan ED The pathology of idiopathic sudden sensorineural hearing loss. Arch Otolaryngol Head Neck Surg 1986 ; 243 : 1-15 [crossref]
Schuknecht HF, Nadol JB Temporal bone pathology in a case of Cogan syndrome. Laryngoscope 1994 ; 104 : 1135-1142
Schultz P, Arbusow V, Strupp M, Dieterich M, Rauch E, Brandt T Highly variable distribution of HSV-1-specific DNA in human geniculate, vestibular and spiral ganglia. Neurosci Lett 1998 ; 252 : 139-142
Shaia FT, Sheehy JL Sudden sensorineural hearing impairment: a report of 1220 cases. Laryngoscope 1976 ; 86 : 389-398
Shea J.J., Ge X., Orchik D.J. Traumatic endolymphatic hydrops Am J Otol 1995 ; 16 : 235-240
Shiraishi T, Kubo T, Okumura S, Naramura H, Nishimura M, Okusa Hearing recovery in sudden deafness patients using a modified defibrinogenation therapy. Acta Otolaryngol [suppl] 1993 ; 501 : 46-50
Simmons FB Theory of membrane breaks in sudden hearing loss. Arch Otolaryngol Head Neck Surg 1968 ; 88 : 68-74
Smouha EE, Karmody YS Non-osteitic complications of therapeutic radiation to the temporal bone. Am J Otol 1995 ; 16 : 83-87
Soucek S, Michael L The ear in the acquired immunodeficiency syndrome: II. Clinical and audiologic investigation. Am J Otol 1996 ; 17 : 35-39
Stinckens C., Huygen P.L., Joosten F.B., Van Camp G., Otten B., Cremers C.W. Fluctuant progressive hearing loss associated with Ménière like vertigo in three patients with the Pendred syndrome Int J Pediatr Otorhinolaryngol 2001 ; 61 : 207-215 [cross-ref]
Stokroos RJ, Albers FW, Krikke AP, Casselman JW Magnetic resonance imaging of the inner ear in patients with idiopathic sudden sensorineural hearing loss. Eur Arch Otorhinolaryngol 1998 ; 255 : 433-436 [crossref]
Stokroos RJ, Albers FW, Schirm J Therapy of idiopathic sudden sensorineural hearing loss: antiviral treatment of experimental herpes simplex virus infection of the inner ear. Ann Otol Rhinol Laryngol 1999 ; 108 : 423-428
Takasaki T, Higashikawa M, Motoyama S, Sugita K, Kurane I Serum antibodies to human herpesvirus 7, human herpesvirus 6 and cytomegalovirus in patients with idiopathic facial nerve palsy and sudden deafness. J Laryngol Otol 1998 ; 112 : 617-621
Therrocha JR, Ramirez-Camacoj IR Sudden sensorineural hearing loss: supporting the immunologic theory. Ann Otol Rhinol Laryngol 2002 ; 111 : 989-997
Thomas R, Kameswaran M, Murugan V, Okafor BC Sensorineural hearing loss in neurobrucellosis. J Laryngol Otol 1993 ; 107 : 1034-1036
Tomasi J.P., Gersdorff M. Autoimmune inner ear disease: diagnostic and treatments Acta Otorhinolaryngol Belg 2002 ; 56 : 371-374
Tran Ba Huy P, Manach Y Les urgences en ORL. Conduite à tenir en urgence face à une surdité brusque. Rapport de la société française d'ORL 2002 : 207-225
Tran Ba Huy P., Sauvaget E. Les maladies pressionnelles de l'oreille interne Pathologie pressionnelle en ORL : Rapport de la SFORL (2005).
Tsunoda K., Akaogi J., Ohya N., Murofushi T. Sensorineural hearing loss as the initial manifestation of polyarteritis nodosa J Laryngol Otol 2001 ; 115 : 311-312
Ueda T, Murai T, Nario K, Fujita N, Miyahara H, Matsunaga T Inner ear blood flow in the rat after unilateral occlusion in the vertebrobasilar system. Acta Otolaryngol [suppl] 1998 ; 533 : 36-39 [crossref]
Ullrich D, Aurbach G, Drobik C A prospective study of hyperlipidemia as a pathogenic factor in sudden hearing loss. Eur Arch Otorhinolaryngol 1992 ; 249 : 273-276 [crossref]
Unal M, Katircioglu S, Karatay MC, Suoglu Y, Erdamar B, Aslan I Sudden total bilateral deafness due to asymptomatic mump infection. Int J Pediatr Otorhinolaryngol 1998 ; 45 : 167-169 [crossref]
Vasama JP, Linthicum FH Idiopathic sudden sensorineural hearing loss: temporal bone histopathologic study. Ann Otol Rhinol Laryngol 2000 ; 109 : 57-59
Vass Z, Shore SE, Nutall AL, Miller JM Direct evidence of trigeminal innervation of the cochlear blood vessels. Neuroscience 1998 ; 84 : 559-567 [crossref]
Veldman JE, Hanada T, Meeuwsen T Diagnostic and therapeutic dilemmas in rapidly progressive sensorineural hearing loss and sudden deafness. A reappraisal of immune reactivity in inner ear diseases. Acta Otolaryngol 1993 ; 113 : 303-306 [crossref]
Virtaniemi J, Laakso M, Nuutinen J, Karjalainen S, Vartiainen E Hearing thresholds in insulin-dependent diabetic patients. J Laryngol Otol 1994 ; 15 : 109-113 [crossref]
Vrabec JT, Payne DA Prevalence of herpesviruses in cranial Nerve Ganglia. Acta Otolaryngol 2001 ; 121 : 831-835
Vyse T, Luxon LM, Walport MJ Audiovestibular manifestations of the antiphospholipid syndrome. J Laryngol Otol 1994 ; 108 : 57-59
Wackym PA Molecular temporal bone pathology: II. Ramsay Hunt syndrome (herpes zoster oticus). Laryngoscope 1997 ; 107 : 1165-1175 [crossref]
Walsted A., Nielson O.A., Borum P. Hearing loss after neurosurgery. The influence of cerebrospinal fluid pressure J Laryngol Otol 1994 ; 108 : 637-641
Wang L.P., Lundberg L., Magnusson M., Törnebrandt K. Auditory function after spinal anesthesia Rev Anesth 1993 ; 18 : 162-165
Westmore GA, Pickard BH, Stern H Isolation of mumps virus from the inner ear after sudden deafness. Br Med J 1979 ; 1 : 14-15 [crossref]
Wilkins SA, Mattox DE, Lyles A Evaluation of a a shotgun regimen for sudden hearing loss. Otolaryngol Head Neck Surg 1987 ; 97 : 474-480
Wilson WR, Byl FM, Laird N The efficacity of steroids in the treatment of idiopathic sudden hearing loss. Arch Otolaryngol Head Neck Surg 1980 ; 106 : 772-776
Wilson WR The relationship of the herpesvirus family to sudden hearing loss: a prospective clinical study and literature review. Laryngoscope 1986 ; 96 : 870-877
Yamasoba T, Kikuchi S, Yagi M, Higo R, O'Uchi T, Tokumaru A Sudden sensorineural hearing loss associated with slow blood flow of the vertebral system. Ann Otol Rhinol Laryngol 1993 ; 102 : 873-877
Yamasoba T, Kikuchi S, Sugasawa M, Harada T Acute low-tone sensorineural hearing loss without vertigo. Arch Otolaryngol Head Neck Surg 1994 ; 120 : 532-535
Yeo SW, Park SN, Park YS, Suh BD, Hari H, Choi HB , e al. Different distribution of HLA Class II alleles according to response to corticosteroid therapy in sudden sensorineural hearing loss. Arch Otolaryngol Head Neck Surg 2001 ; 127 : 945-949
Yetiser S., Inal A., Taser M., Ozkaptan Y. Otolaryngological aspects of relapsing polychondritis: course and outcome Rev Laryngol Otol Rhinol 2001 ; 122 : 195-200
Yoon TH, Paparella MM, Schachern PA, Alleva M Histopathology of sudden hearing loss. Laryngoscope 1990 ; 100 : 707-715