NEURINOMA ACUSTICO-
NEURINOMA DEL NERVO VIII
SCHWANNOMA VESTIBOLARE
NEUROFIBROMATOSI TIPO
2(NF-2)
INDICE
Che cosa è la neurofibromatosi di tipo 2?
Quanto è diffusa la neurofibromatosi di tipo 2? Epidemiologia
Crescita e Cause del Neurinoma
Segni e Sintomi
Quali sono i sintomi di un neuroma acustico?
Perdita Uditiva Acufene Vertigine
Paralisi Facciale
Diagnosi del Neurinoma Acustico
Audiometria Convenzionale Esami Abr ENG
Immagini Cerebrali
Diagnosi Differenziale
Gestione dei Neuromi Acustici

|

|
Neurinoma del Nervo Acustico (gonfiore
del nervo 8°, appena al di sotto del nervo facciale)
|
Punti Principali:
·
1.
Il Neuroma del n.
acustico rappresenta, una rara causa,di perdita uditiva unilaterale, vertigini,
e raramente vi sono altri sintomi cerebrali.
·
2. Le prove migliori per fare diagnosi di neuroma del n.
acustico sono gli esami audiometrici e la RM della testa con mezzo di
contrasto (gadolinio).
·
3. Circa la metà, di tutti i neuromi acustici , sono trattati
con la chirurgia, circa un quarto con radioterapia ( in aumento), ed un quarto
controllati nel tempo .
·
4. Non
importa quale metodo di trattamento viene utilizzato, la conservazione
dell'udito è molto difficile.
CHE COSA È LA
NEUROFIBROMATOSI DI TIPO 2?
Ipoacusia genetica associata a
disturbi neurologici
Neurofibromatosi
tipo 2(NF-2).
- trasmissione autosomica
dominante
- elevata penetranza
- neoplasie del sistema
nervoso centrale
- neurofibromatosi cutanea
- dicromatismi cutanei
Ci sono due tipi principali di
neurofibromatosi:
•Neurofibromatosi di tipo 1 (NF1) è
il tipo più comune di neurofibromatosi, che colpisce circa uno su 3.000
persone.
• Neurofibromatosi di tipo 2
(NF2) è meno comune, che colpisce circa uno su 35.000 persone.
|

|

|
|
Neurofibromatosi
di tipo 1 (NF1)
|
Neurofibromatosi
di tipo 2 (NF2)
|
Nonostante che condividono lo stesso
nome, i due tipi di neurofibromatosi sono distinte condizioni che hanno diverse
cause e sintomi.
La Neurofibromatosi tipo 2 (NF-2) è
determinata da una mutazione nel gene “merlin”, un gene soppressore tumorale
localizzato nella regione 22ql2. Presenta modalità di trasmissione autosomica
dominante a penetranza elevata (123). Il 50% dei casi è rappresentato da nuove
mutazioni. Questa condizione patologica si ritrova in circa il 5% di soggetti
affetti da neurinoma dell’acustico (sordità neurosensoriale retrococleare) Il
quadro clinico è rappresentato dalla presenza di tumori del sistema nervoso
centrale e periferico (neurinomi, glomi, meningiomi), che a seconda della loro
sede danno luogo a sintomi diversi Le prime manifestazioni avvengono in età
giovanile, spesso è presente
La Neurofibromatosi di tipo II (o
"Sindrome MISME", per "Schwannomi Multipli
Ereditati, meningiomi , e Ependimomi ") o Neurofibromatosi
centrale, o neurofibromatosi tipo 2 (NF2),è una malattia ereditaria , genetica caratterizzata dalla predisposizione a sviluppare una
varietà di tumori del sistema nervoso centrale e periferico. La manifestazione
principale della malattia è lo sviluppo di tumori cerebrali non- maligni simmetrici, nella
regione del VIII nervo cranico , che è il "nervo cocleo -vestibolare" che
trasmette informazioni sensoriali dal orecchio interno al cervello. La maggior parte delle persone con questa condizione possono
avere problemi visivi. La NF2 è causata da mutazioni del gene [1] "Merlin" che sembra influenzare la forma e il movimento
delle cellule . I principali trattamenti consistono nella
rimozione neurochirurgica dei tumori e nel trattamento chirurgico delle lesioni
oculari. In contrasto con la neurofibromatosi di tipo 1 (NF1), la NF2
produce una scarsità di manifestazioni cutanee.
Quanto è diffusa la neurofibromatosi
di tipo 2? Epidemiologia
La prevalenza alla nascita della
Neurofibromatosi tipo ii è stata stimata di 1/40.500- 87.000; circa il 4% dei
soggetti con neurinoma dell’VIII nervo cranico presenta una NF’-Z (126, 127,
128). Nel 1920 Feiling e Ward (Evans D.G.R., et AL., 1999) descrissero una
famiglia con neurinoma dell’Vili nervo cranico bilaterale ed ipoacusia
neurosensoriale, tuttavia casi isolati erano già stati descritti un secolo
prima (Feiling A., Ward E., 1920).
L'incidenza stimata di
neurofibromatosi tipo 2 (NF2) è di 1 su 37.000 all'anno, con circa la metà
degli individui affetti rappresentano i primi casi in famiglia a seguito di
nuove mutazioni dominanti.
Sebbene il cambiamento genetico che
causa NF2 è presente al momento del concepimento, le manifestazioni cliniche si
verificano nel corso di molti anni. L'età tipica di esordio dei sintomi è nella
tarda adolescenza a 20 anni, ma la fascia d'età copre l'intero ciclo di vita
Goutagny S,.e 2013. Alcune evidenze indicano che l'età di insorgenza dei
sintomi clinici è più basso in NF2 maternamente trasmesso. Mentre NF2 è
abbastanza variabile in gravità da persona a persona, famiglia studi hanno
dimostrato una certa coerenza intrafamilial in età di insorgenza. Mosaicismo somatico
per la mutazione NF2 in casi sporadici può anche complicare il quadro clinico,
con conseguente sottostima o diagnosi tardiva.
Tuttavia, poiché circa la metà dei
casi derivano da nuove mutazioni, la storia familiare è spesso negativa.
Diversamente dal NF1, che
spesso è associato con un numero di indizi diagnostici cutanei, l’NF2 è
accompagnato da pochi segni esterni. I Sintomi con cui si presenta sono i
seguenti:
Nella maggior parte dei casi i
sintomi si manifestano nell’adolescenza o attorno ai 20 anni; raramente possono
comparire precocemente, durante i primi 10 anni di vita, o tardivamente, dopo i
70 anni. Circa il 70% dci soggetti manifesta un deficit della vista (Vishart
J.H.,1822). Dal 20 al 65% dei casi sviluppano pochi piccoli neurofibromi
cutanei, soprattutto a livello dello scalpo (Maccollin M., Maumer VF., 1998).
Circa il 40% degli affetti presenta poche piccole macchie cutanee color
‘caffelatte” (Kluwe I., Et Al., 2000). La perdita dell'udito, ronzio nelle
orecchie, e problemi di equilibrio associata a lesioni del nervo vestibolare
Sembra possibile identificare due Forme: il Tipo Wishart con neurinomi dei
nervi cocleo-vestibolari e di altri nervi ad insorgenza precoce e decorso
rapido (Feiling A., Ward E., 1920), e il Tipo Gardner con neurinomi dei nervi
cocleo-vestibolari solamente ad insorgenza tardiva e decorso lento (Kanter
W.R., EI AL.,1980; Gardner W.J., Frazier C.H., 1999).
Criteri diagnostici sono
considerati: neurinoma dell’Vili nervo cranico bilaterale, un familiare di
primo grado affetto da NF-2 e neurinoma dell’VIII nervo cranico monolaterale,
oppure nn familiare di primo grado affetto da NF-2 e due delle seguenti forme:
glioma, meningioma, neurofibroma, schwannoma, opacità lenticolare subcapsulare
posteriore giovanile ( Evans D.G.R., Et AL., 1992) Paralisi dei nervi
cranici
I
Neuromi acustici, noti anche come neurinomi vestibolari, non sono tumori
maligni dell'ottavo nervo cranico . Generalmente nel 98% dei casi prendono
origine dalle cellule del rivestimento (cellule
di Schwann) del nervo vestibolare inferiore (Komatsuzaki e Tsunoda, 2001; Kras,
2007). Possono anche insorgere nel labirinto (Neff et al, 2003). Insorge, nella maggioranza dei
casi,nel nervo vestibolare (superiore o inferiore), in corrispondenza del
passaggio tra il rivestimento mielinico centrale e quello periferico, nella
così detta ‘transition zone’, dove l’anatomia delle fibre, consistenza della
mielina e fine vascolarizzazione intraneurale, sono più fragili. Questa zona di
transizione è situata a livello del meato acustico interno. La definizione più
corretta sarebbe in effetti schwannoma vestibolare e così è oggi definito nella
letteratura internazionale, è chiamato neurinoma dell’acustico per la
sintomatologia clinica, che, in una prima fase almeno, è a carico del nervo
uditivo (nervo cocleare propriamente detto) per un evidente effetto compressivo
e, talora, persino destruente delle fibre uditive da parte delle cellule
tumorali. E’ questa sintomatologia che rende diagnosticabile il neurinoma in
fasi precoci.
|

|
|
Fig.2°2A-2B Distribuzione dei
casi di neurinoma del VIII secondo l’età ed il sesso. A maschi ,B donne (Dutton
ed al 1999)
|
Si possono anche produrre nel labirinto
(Neff et al, 2003). Essi comprendono circa il 6 per cento di tutti i tumori
intracranici,
dopo i gliomi e i meningiomi. (Anderson et al, 2000), circa il 30% dei tumori del tronco
cerebrale, e circa il 85% dei tumori nella regione ponto-cerebellare - altro
10% sono meningiomi. Il numero 6%
probabilmente è troppo alto come i meningiomi e tumori ipofisari sono
sottostimati. Solo circa 10 tumori acustici per milione di persone sono ultimamente
diagnosticati ogni anno (Evans et al, 2005), corrispondenti a 2000 e 3000
nuovi casi ogni anno negli Stati Uniti. Un altro modo di vedere questo è che
una persona media ha un rischio di circa 1/1000 di sviluppare un neuroma
acustico nel corso della loro vita (Evans et al, 2005). In Danimarca,
l'incidenza annuale è stato stimato a 7,8 pazienti operati / anno (Tos et al,
1992). Come la tecnologia è migliorata, i tumori più piccoli sono stati
diagnosticati, con conseguente analoga stima di circa 10 tumori / milioni /
anno. Si manifestano
prevalentemente nel sesso femminile tra i 35 e 60 anni
di età (Fig.2A-2B).
E’
stato descritto per la prima volta da Sandifort E. nel 1772.circa
il 30% dei tumori del tronco encefalico, e circa l'85% dei tumori nella regione
del ponto-cerebellare - un altro 10% sono rappresentati dai meningiomi. Sono
solo circa 10, i nuovi tumori , che vengono diagnosticati ogni anno per
milione di persone (Evans et al, 2005), corrispondente negli Stati Uniti a
2000/ 3000 nuovi casi il ogni anno. Un altro modo di considerare questi dati
è che una persona normale ha un rischio di circa 1 / 1000 di sviluppare un
neuroma acustico nel ciclo della propria vita (Evans et al, 2005).
Nei pazienti con
asimmetria uditiva , si ritiene che solo 1 su 1000 abbia una neuroma acustico
(fonte: NIH), sebbene alcuni autori riportano una prevalenza più alta 2,5%
elevati a (Baker et al.2003). Questa prevalenza più elevata non risulta dalla
nostra esperienza clinica. I neuromi acustici si
verificano soprattutto negli adulti - sono molto rari nei bambini. Solo
in 39 casi di neurinomi nei bambini è stato riportato riportati in letteratura,
come ad esempio nel 2001 (Pothula et al, 2001).
Quali geni sono legati alla neurofibromatosi di tipo 2?
Le mutazioni nel gene causa neurofibromatosi di tipo 2 NF2 .Il
gene NF2 fornisce istruzioni per fare una proteina chiamata Merlin smeriglio (noto anche come schwannomin).
Questa proteina viene prodotta nel sistema nervoso, in particolare nelle
cellule di Schwann, che circondano e isolano le cellule nervose (neuroni) nel
cervello e nel midollo spinale. Merlin agisce come un soppressore del tumore,
il che significa che permette alle cellule di crescere e dividendo troppo
rapidamente o in modo incontrollato. Anche se la sua funzione esatta non è
nota, questa proteina è probabile anche coinvolto nel controllo dei movimenti
delle cellule, forma delle cellule, e la comunicazione tra le cellule.
Mutazioni nel gene NF2 piombo per la produzione di una versione non funzionale
della proteina esmerejon che non può regolare la crescita e la divisione delle
cellule. La ricerca suggerisce che la perdita di merlin permette alle cellule,
in particolare le cellule di Schwann, per moltiplicare troppo frequentemente e
formare tumori caratteristici della neurofibromatosi di tipo 2.
Per saperne di più sul NF2 gene.
Come fanno i pazienti ad ereditare la neurofibromatosi di tipo 2?
|

|
NF-2 può
essere trasmessa come autosomica dominante moda, così come attraverso la
mutazione casuale.
|
La Neurofibromatosi di
tipo 2 è considerato abbia un modello di trasmissione autosomica dominante, anche se la metà degli individui affetti
hanno NF2 a seguito di una nuova mutazione del gene.. Le persone con
questa condizione sono nati con una copia mutata del gene NF2 in
ogni cellula. In circa la metà dei casi, il gene alterato è ereditato da
un genitore affetto. I casi rimanenti derivano da nuove mutazioni del
gene NF2 e si verificano in persone senza storia di malattia
nella loro famiglia. L'incidenza della
malattia è di circa 1 a 60.000 Evans DG (2009). Vi è un ampio spettro clinico
noto, ma tutti i pazienti controllati sono stati trovati per avere qualche
mutazione dello stesso gene sul cromosoma 22 . Attraverso le statistiche, si
sospetta che una metà dei casi siano ereditati, e la metà sono il risultato di
nuove mutazioni .
A differenza di molte
altre condizioni autosomiche dominanti, in cui per causare il disturbo è
sufficiente una copia alterata del gene in ogni cellula, due copie del gene NF2 devono
essere modificati per innescare la formazione di tumori nella neurofibromatosi
di tipo 2 Una mutazione nella seconda copia di il gene NF2 si
verifica in cellule di Schwann o altre cellule del sistema nervoso durante la
vita di una persona. Quasi tutti coloro che sono nati con una
mutazione NF2 acquista una seconda mutazione (noto come una
mutazione somatica) in queste cellule e sviluppa i tumori caratteristici della
neurofibromatosi di tipo 2.
Patogenesi, Biologia Molecolare e rapporti fisiopatologici
NF 2 è causata da un
difetto nel gene che produce normalmente un prodotto chiamato Merlin o Schwannomin, localizzato
sul cromosoma 22 banda q11-13.1. Si pensa che Questo peptide abbia una
funzione soppressiva sul tumore. In una cellula normale, le
concentrazioni di Merlin attivo (defosforilato) siano controllati mediante
processi quali l’adesione cellulare (il che indica la necessità di limitare la divisione
cellulare). E 'noto che la carenza di Merlin può provocare progressione
mediata attraverso il ciclo cellulare a causa della mancanza di soppressione tumorale contatto
mediata, sufficiente a causare tumori caratteristici della neurofibromatosi
tipo II. Mutazioni di NF II si presume provochino sia un fallimento per
la sintesi del Merlin o la produzione di un peptide difettoso che manca il
normale effetto soppressivo sul tumore. Il peptide Schwannomin è formato
da 595 aminoacidi . Il confronto dello Schwannomin con le altre proteine mostra somiglianze
alle proteine che collegano il citoscheletro alla membrana cellulare . Mutazioni nel gene-Schwannomin si pensa alterino
il movimento e la forma delle cellule colpite con perdita di inibizione da
contatto.
Patologia


Schwannoma del
N. Vestibolare


Meningioma in un
paziente con NFII
Il cosiddetto neuroma acustico NF II è in realtà uno Schwannoma del nervo,
vestibolare o Schwannoma vestibolare. Il termine improprio di neurinoma
del nervo acustico è ancora utilizzato spesso. Gli Schwannomi vestibolari crescono
lentamente all'ingresso interna del meato uditivo interno (meato acoustico
interno). Esse derivano dalle guaine nervose della parte superiore dei
nervi vestibulari nella regione tra la mielina centrale e periferica
(Obersteiner-Redlich-Zone) all'interno dell'area del poro acustico, ad 1 cm dal
tronco cerebrale.
Correlazione Genotipo-fenotipo
Molti pazienti con
NF II sono stati inclusi negli studi che sono stati progettati per confrontare
tipo di malattia e la progressione con la determinazione esatta della mutazione
associata. Lo scopo di tali confronti di genotipo e fenotipo è determinare
se mutazioni specifiche causano rispettive combinazioni di sintomi. Questo
sarebbe estremamente utile per la predizione della progressione della malattia
e la pianificazione di terapia partendo in giovane età. I risultati di
tali studi sono i seguenti:
·
Nella
maggior parte dei casi peptidi La mutazione nel gene cause NF II abbreviato.
·
Non
ci sono hot-spot mutazionali.
·
I
pazienti con mutazione
Frameshift - o mutazioni nonsenso soffrono prognosi infausta.
·
I
pazienti con mutazioni missense hanno una prognosi migliore.
·
Nei
casi con mutazioni nel splice accettore-regione , non c'è una
buona correlazione per determinare.
·
Le mutazioni puntiformi possono avere solo effetti minori.
·
I
casi sono pubblicati [ citazione necessaria ], in cui
esattamente la stessa mutazione è associata ad esito chiaramente diverso.
Questi risultati suggeriscono che
probabilmente altri fattori (ambientali ed altre mutazioni) determineranno
l'esito clinico.
Una mutazione
frameshift (chiamato anche un errore di frame o l'orientamento reading
frame) è una mutazione genetica
causata da indels ( inserzioni
o delezioni
) di un numero di nucleotidi in una sequenza di DNA che non è
divisibile per tre. Due to the triplet nature of gene expression by codons , the insertion or deletion can change the reading frame (the grouping of the codons), resulting
in a completely different translation from the original. A causa della natura tripletta di espressione genica
da codoni , l'inserimento o l'eliminazione
possono cambiare il reading frame
(il raggruppamento dei codoni), risultando in un completamente diversa Traduzione
dall'originale. The earlier in the sequence the
deletion or insertion occurs, the more altered the protein. [ 1 ] A frameshift mutation
is not the same as a single-nucleotide polymorphism in which a nucleotide
is replaced, rather than inserted or deleted.
In genetica , una mutazione non
senso è una mutazione puntiforme in una sequenza di DNA che si traduce in un
premature codone di stop che
provoca il troncamento delle proteine risultanti, o un codone dialogo
nel mRNA trascritta e in un tronco incompleto e di solito prodotta proteina non funzionale
In genetica , una mutazione missenso (un
tipo di sostituzione nonsynonymous
) è una mutazione puntiforme
in cui un singolo nucleotide risulti cambiamento in un codone che codifica per un diverso amminoacido . [1]
CRESCITA
E CAUSE DEL NEURINOMA
Le cause che determinano la crescita
di un neurinoma non sono attualmente note .
Circa
7 su 100 neuromi acustici sono causati da neurofibromatosi tipo 2 (NF2). NF2 è
una malattia genetica molto rara che provoca tumori benigni del sistema
nervoso. Essa colpisce circa 1 su 350.000 persone. Quasi tutti con NF2 sviluppa
un neuroma acustico su entrambi i nervi acustici (cioè, tumori bilaterali). Il neurinoma del nervo acustico
si presenta in due forme: una forma sporadica ed una forma associata con una
sindrome ereditaria chiamata neurofibromatosi di
tipo II (NF2). Circa il 93 per cento di tutti i casi sono sporadici.
Maggiori informazioni su NF2 si possono trovare alla http://ghr.nlm.nih.gov/gene=nf2
Attualmente
non vi è evidenza che le radiazioni emesse dai telefoni cellulari possono
causare neuroma acustico (Muscat et al, 2002).
Solo nei casi
di Neurofibromatosi tipo II si può attribuire una causa genetica. I tumori del
nervo acustico generalmente hanno una crescita lenta (circa 2 mm). Se il neurinoma, come avviene nella
maggior parte dei casi, si sviluppa nel segmento del nervo in prossimità
delineato acustico interno, e pertanto può espandersi (la sua crescita è di ca.
0,5 cm. all’anno) verso il meato acustico interno e attraverso questo,
diffondersi nella cavità endocranica .A tal punto il quadro clinico si
modifica. Il deficit uditivo peggiora. si aggravano la vertigine, i disturbi
dell’equilibrio e la sensazione di incertezza della marcia. Compare la cefalea
che e prevalentemente localizzata in sede occipitale o frontale Si rendono
manifesti i segni di sofferenza del n. faciale a causa della comparsa dell’asimmetria
della rima palpebrale e di quella buccale. Essi rimangono avvolti da una capsula e tendono a
erodere l'osso e a spostare i tessuti neurovascolari normali. Per la crescita
lenta esiste un adattamento graduale dell'organismo alternato a periodi di sintomi
più o meno evidenti dovuti alla compressione del nervo uditivo e/o del nervo
facciale, quindi il tumore esce dal canale osseo ed invade lo spazio
dell'angolo ponto-cerebellare. A questo stadio, alla risonanza magnetica
cerebrale, il tumore assume l'aspetto di una massa globosa peduncolata sul
C.U.I.. Nella sua ulteriore crescita, il tumore comprime il nervo trigemino ed
il tronco cerebrale rendendo il trattamento chirurgico non dilazionabile.
|

|
|
Figura
2: Neurinoma dell'acustico sinistro di circa 1,5 cm nell'angolo
ponto-cerebellare. Non compressioni sul tronco cerebrale. Il CUI non appare
deformato ed è appena lievemente allargato. Figura 3: Neurinoma
dell'acustico destro di dimensione superiore a 4 cm. Importante deformazione
del tronco cerebrale e del cervelletto. Notevole allargamento del CUI
|
|

|
|
Figura
3: Neurinoma dell'acustico destro di dimensione superiore a 4 cm. Importante
deformazione del tronco cerebrale e del cervelletto. Notevole allargamento
del CUI
|
Compare la cefalea che
e prevalentemente localizzata in sede occipitale o frontale Si rendono
manifesti i segni di sofferenza del n. faciale a causa della comparsa
dell’asimmetria della rima palpebrale e di quella buccale.
Si
osserva una riduzione del riflesso corneale e un’alterazione della lacrimazione
nell’occhio omolaterale alla sede della lesione. La presenza, nel 25-30% dei
casi, di una ipoestesia all’emifaccia indica una sofferenza del V. La comparsa
di un deficit a carico di altri nervi cranici (VI, IX, X, XII) dimostra che la
neoplasia si è ulteriormente diffusa. Si realizza in tal modo, un quadro
clinico neurologico con un corredo sintomatologico multiforme a causa non solo
della paralisi dei nn. cranici e dell’interessamento dei distretti bulbare,
cerebellare e pontino ma anche della comparsa di un’ipertensione endocranica
per l’ostacolo al deflusso del liquor.
SEGNI
E SINTOMI:
La diagnosi di una richiede di
solito un medico con esperienza otologica che possono integrare insieme
l'intera immagine, o una risonanza magnetica con gadolinio(Fig. 8d ).
Perché neuromi acustici sono molto rari, e la RM sono molto costose, a nostro
parere - tutti i pazienti con un rischio sostanziale di avere una chitarra acustica
devono essere valutati da un medico con esperienza otologica. In altre parole ,
tutti i pazienti , con una inspiegabile stabile perdita uditiva, asimmetrica ,
in generale dovrebbero essere valutati da un medico con esperienza otologica.
Il testo seguente descrive come questo processo di integrazione possa essere
effettuato .
Quali sono i
sintomi di un neuroma acustico?
I
sintomi iniziali sono costituiti da ipoacusia, che si verifica in 9 su 10 pazienti,
cioè diminuzione progressiva dell’udito dal lato della neoformazione che spesso
inizia con un’alterata comprensione del significato di parole e frasi nella
conversazione al telefono, da acufeni (ronzii e fischi all’orecchio). Gli acufeni,
che si presenta in 7 su 10 persone, rappresentano il motivo più frequente di
visita medica in questi pazienti. A questi due sintomi spesso si associa
un lieve disturbo dell’equilibrio,
quasi la metà delle
persone con un neuroma acustico hanno questo sintomo, ma meno di 1 su 10 lo hanno
come primo sintomo. Intorpidimento
del viso, formicolio o dolore . Questi sintomi sono dovuti alla pressione del
neuroma acustico su altri nervi. Il nervo comunemente colpite è chiamato il
nervo trigemino che controlla sensazione in faccia. Circa 1 persona su 4 con
neurinoma acustico ha qualche intorpidimento del viso - questo è un sintomo più
comune di quanto la debolezza dei muscoli facciali. Tuttavia, è spesso un
sintomo inosservato ; mentre
la perdita dell'udito è comune nel neuroma acustico (vale a dire che è
sensibile), ci sono miriadi di altre cause di perdita dell'udito (l’ipoacusia
cioè è molto aspecifica). A causa della elevata sensibilità, ma bassa
specificità, l'uso di routine di un test diagnostico molto costoso come un gad-RM(risonanza
magnetico con gadolinio) della IAC(condotto uditivo interno) in tutte le
persone con una perdita uditiva asimmetrica non è sempre giustificata. In altre
parole, gli errori sono possibili sulla base del rapporto costi / benefici
sociali. Mentre alcuni clinici effettuano una RM su tutti i pazienti con udito
asimmetrico, questo è un modo molto costoso per "trovare" una neurinoma
acustico.
La perdita dell'udito è il sintomo
più frequente del neuroma acustico, che si verificano in più del 95% dei pazienti.
L'ipoacusia è
generalmente associata ad un ronzio o rumore monolaterale nonchè a disturbi
dell'equilibrio con instabilità o, raramente, vere crisi vertiginose. Non è
raro che un neurinoma dell'acustico possa presentarsi con i sintomi di una
Malattia di Ménière (vertigini violente accompagnate da perdita di udito e
acufeni).. Circa il 90
per cento si presentano con una , perdita uditiva lentamente progressiva
monolaterale. Un esempio è riportato qui di seguito.
I medici spesso cercano di stimare il
rischio di un neuroma acustico guardando il modello di perdita dell'udito (vedi sotto per
audiogrammi più frequenti).
Il tipo più comune è un pattern neurosensoriale ad alta frequenza, si verifica in
circa in due terzi dei pazienti. Nel terzo rimanente l'osservazione più comune
è una perdita dell'udito a bassa frequenza (che sarebbe più tipico della Malattia di Ménière). Ancora meno frequentemente,
alcuni hanno il morso "cookie pattern " (indicativi di perdita dell'udito
congenita o di
una incisura da rumore noise notch).
Alcune volte il sintomo
rilevatore di un neurinoma dell'acustico può essere una sordità improvvisa,
talvolta con recupero uditivo dopo trattamento medico, oppure il paziente può
sperimentare una ipoacusia fluttuante o senso di orecchio pieno. Una
perdita uditiva improvvisa si verifica in
circa il 25 per cento dei pazienti con neuroma acustico. Tuttavia, poiché il
neuroma acustico è una condizione rara, la perdita uditiva improvvisa dovuta a
un tumore acustico si verifica solo nel 1-5 per cento dei pazienti con perdita
uditiva improvvisa in quanto ci sono molte cause più comuni (Daniels et al,
2000). Anche una perdita improvvisa dell'udito, con recupero completo può essere
causato da una chitarra acustica(Nageris e
Popovtzer, 2003).
Una ipoacusia asimmetrica è
sensibile ma non specifica di neuroma acustico. La mancanza di specificità e
rarità di neuromi acustici, rispetto alla miriade di altre cause di audizione
asimmetrica rende il "costo" della scansione di ogni persona con un
udito asimmetrico, per trovare una chitarra acustica in 1 / 1000 estremamente
elevato. La mancanza di specificità è stato commentato da Margolis e Saly
(2008). Questa conclusione deve essere temperata da altre informazioni cliniche
,qualcuno con una progressiva riduzione asimmetrica dell'udito neurosensoriale
avrà (a nostro parere) una probabilità di gran lunga maggiore, di avere una
chitarra acustica rispetto a qualcuno con una asimmetria statico o che migliora
nel tempo .
La specificità è un'altra
considerazione è. A questo proposito, alcuni riscontrano una funzionalità
uditiva del tutto normale in circa l'11% dei pazienti (Morrison e Sterkers,
1996). A parere, di Heine tale percentuale è alta, ma certamente il
neurinoma dell’acustico si può trovare in persone con udito simmetrico.
Acufene
L’Acufene è molto comune nel neuroma dell’acustico, è
solitamente unilaterale e limitato nell'orecchio colpito, se avete un acufene,
è molto molto improbabile che si abbia un neuroma acustico, perché questi
tumori sono molto più rari rispetto ad altri meccanismi di danno uditivo.
Vertigine
Nonostante l'origine
abituale del neurinoma acustico dal nervo vestibolare inferiore (Komatsuzaki e
Tsunoda, 2001; Kraj et al, 2007), le vertigini (spinning) prima di un
intervento chirurgico non sono comuni, si verificano solo in circa nel 20 per
cento delle persone con neuroma acustico. Quando
la neoplasia si espande nell’angolo ponto-cerebellare a ridosso delle strutture
nervose centrali, compare un nistagmo nello sguardo diretto verso il lato della
lesione (nistagmo di Bruns) E di tipo orizzontale, aritmico. con scosse di
piccola ampiezza. In questo stadio del neurinoma, si osservano quindi due tipi
di nistagmo di opposta direzione l’uno spontaneo di tipo “deficitario”,
presente fin dall’inizio della malattia dovuto all’asimmetria vestibolare
periferica, l’altro “da direzione dello sguardo”, di tipo “irritativo”,
omolaterale alla sede della lesione d’origine centrale, Questo nistagmo indica
che la neoplasia. dopo essersi estesa all’angolo ponto-cerebellare, comprime
parzialmente le aree nucleari vestibolari del bulbo e contemporaneamente le vie
di connessione vestibolo-cerebellari omolaterali alla sede della neoplasia (Fig.
4A).
Anche la motilità
oculare riflessa risulta compromessa. Si osserva, infatti, una anomalia dei
movimenti lenti di inseguimento (pursuit) diretti verso il lato del neurinoma.
Il NOC risulta facilitato, per l’interferenza del nistagmo spontaneo quand’è
diretto verso il lato opposto alla sede del tumore, mentre appare parzialmente
inibito e aritmico quand’ è diretto omolateralmente
A causa dell’ulteriore
estensione del tumore, l’interessamento delle strutture nervose del tronco
encefalico si fa più evidente. Il nistagmo da “direzione dello sguardo”
omolaterale alla sede del tumore subisce delle profonde modificazioni del ritmo
e della forma delle scosse. Se si invita il paziente a volgere lo sguardo verso
il lato malato. si nota infatti che le scosse nistagmiche appaiono, all’inizio,
assai frequenti ma. dopo qualche secondo, esse si riducono progressivamente di
ampiezza e di numero man mano che i bulbi oculari ritornano lentamente e in
modo del tutto involontario nella posizione primaria di sguardo.
|

|
Fig.
4A -
Z.S., a. 52 - Neurinoma dell’VIII° di destra.
Ipoacusia
neurosensoriale destra, nistagmo spont. “deficitario” diretto verso sinistra;
nistagmo di Bruns diretto verso destra;
iporeflettività
vest. destra allo stim. cal. (20°) del lab.; RMN Con mdc evidenzia una
formazione ovalare a Contorni netti, ancora parzialmente insinuata nel meato
ac. int. Che determina modesta impronta sul ponte e sull’emisfero
cerebellare. BABIGHIAN-OTONEURGIA-PICCIN-2008-
|
Si tratta del nistagmo “dello
sguardo paretico” che indica una soffe- renza più profonda delle connessioni
cerebellopontine e dei centri nervosi del tronco encefalico che regolano
l’attività oculomotoria, Una volta che i bulbi oculari hanno raggiunto la posizione
primaria dello sguardo. il nistagmo dello “sguardo paretico” cessa totalmente e
sul grafico ricompare il nistagmo “deficitario” diretto verso il lato opposto
alla sede della lesione (Fig. 4C-D). Il NOC evocato ipsilateralmente alla sede
della neoplasia appare, in questo caso, maggiormente alterato e, a volte,può
anche mancare. È lo stadio della malattia in cui, oltre alla cefalea occipitale
e frontale e agli altri sintomi neurologici (paralisi di nervi cranici,
atassia, disdiadococinesi), si osservano i primi segni dell’ipertensione
endocranica (papilla da stasi, vomito mattutino a stomaco vuoto, ecc.) mentre i
caratteri istochimici del liquor risultano normali. In qualche caso. si può
anche notare un nistagmo “alternante”
(Fig. 4B) di tipo orizzontale o diagonale che, come si è già detto, è
caratterizzato da gruppi di scosse di opposta direzione che si alternano tra
loro separati da brevi periodi di pausa Secondo la maggior parte degli Autori,
tale nistagmo dipenderebbe dalla mancanza dell’azione inibitrice che le aree
cerebellari svolgono sui neuroni dei nuclei vestibolari mentre per altri il
nistagmo “alternante” conseguirebbe all’interessamento di alcune strutture
nervose del tronco encefalico in particolare della reticolare paramediana del
tetto del ponte e anche dei mesencefalo.

Fig. 4B
nistagmo “alternante”
La diagnosi differenziale andrà
posta con alcun neoplasie della fossa cranica posteriore: meningioma, lipoma.
angioma, cisti aracnoidea, tumore del giorno giugulare, neurinoma di altri
nervi cranici, medulloblastoma o con altre lesioni quali l’aracnite della base.
anomalie vasali, etc. Anche le metastasi di neoplasie del polmone, del rene,
della prostata e della mammella che realizzano la cosiddetta “sindrome maligna
dell’angolo ponto-cerebellare” dovranno venir considerate per la diagnosi
differenziale.
|

|
Fig.
4C-
F.S, a. 22. Neurinoma dell’VIII° in sede di a. ponto-cerebellare destro con
paresi del VII. Grave deficit uditivo all’or, destro, nist. spont.
“deficitario” diretto verso sinistra; nistagmo dello “sguardo paretico” verso
destra (col ritorno involontario degli occhi nella posizione primaria compare
il nistagmo spontaneo), areflessia vest. destra. allo stim. cal. (20°) del
lab. (A); NOC oriz. alterato; RMN eseguita con mdc rivela una masserella
rotondeggiante a livello del meato. ac. mt. di destra che sporge nell’a.
pontocerebellare (B). BABIGHIAN-OTONEURGIA-PICCIN-2008-
|
Siccome il nervo vestibolare
inferiore innerva il canale semicircolare posteriore ed il sacculo, ci si
potrebbe aspettare che i VEMP’s , che sono un esame funzionale del sacculo ,
siano uniformemente anormali nel neurinoma dell’acustico ed in effetti questi
esami sono abbastanza sensibili. Allo stesso modo, ci si potrebbe aspettare che
una VPPB ipsilaterale sia rara. Tale questione non è stata affrontata. Si può
anche prevedere anomalie nelle OAE in quanto lei vie uditive efferenti entrano
nell'area cocleare tramite la divisione inferiore del nervo. Ancora una volta,
la questione non è stata affrontata.
|

|
Fig.
4D
Neurinoma dell’VIII° in sede di ang. ponto-cerebellare di sinistra. Anacusia
sin.; nist. “deficitario” verso destra, nist. dello ‘sguardo paretico” verso
sinistra; areflessia vest, sinistra alla stim. cal. (200) del lab;
alterazioni del NOC orizzontale in particolare di quello verso sinistra; RMN
con mdc: grossa formazione a livello dell’ang. ponto-cerebellare sinistro.
ABR
tracciato destrutturato a sinistra, non deficit di altri nervi cranici; non
segni di stasi al fundus. BABIGHIAN-OTONEURGIA-PICCIN-2008-
|
La vertigine è più comune nei
piccoli tumori .L’instabilità è molto più diffusa rispetto alle vertigini alle
vertigini e circa il 70 per cento dei pazienti con tumori di grandi dimensioni
hanno questo sintomo. I sintomi CerebellarI
(cioè scarso coordinamento delle armi) sono inusuali.
L’iperventilazione che
produce nistagmo
è un segno fisico poco conosciuto che può essere molto più specifici per il
neuroma acustico. Valutazione delle HVIN richiede delle attrezzature più
sofisticate di quanto non sia disponibile nella maggior parte degli uffici.
Richiede anche che l'esaminatore abbia ad avere familiarità con questo segno -.
Paralisi facciale
I Disturbi
Sensoriali Facciali
si verificano solo nei tumori di grandi dimensioni (circa nel 50 per cento di
quelli con dimensioni superiori a 2 centimetri di). Il disturbo sensoriale del
viso può rispondere alla carbamazepina o oxcarbamazine farmaco utilizzato per
le nevralgie. Una debolezza del facciale è rara. Contrazioni del viso, note
anche come synkinesis facciale o spasmo facciale, si verifica in circa il 10
per cento dei pazienti. Mal di testa prima di un intervento chirurgico si
verifica in circa il 40 per cento dei pazienti i con un tumore di grandi
dimensioni. . La
presenza, nel 25-30% dei casi, di una ipoestesia all’emifaccia indica una
sofferenza del V. La comparsa di un deficit a carico di altri nervi cranici
(VI, IX, X, XII) dimostra che la neoplasia si è ulteriormente diffusa.
DIAGNOSI DEL NEURINOMA
ACUSTICO :
Diagnosi
Prenatale
Neuromi acustici bilaterali sono
diagnostici di NF2. [2]
Postnatale
Ferner et al, 2011. danno tre serie
di criteri diagnostici per NF2:
1. Schwannoma vestibolare
bilaterale (VS) o storia familiare di NF2 più VS unilaterale o due
di: meningioma, glioma, schwannoma, neurofibroma, posteriore subcapsulare
opacità del cristallino
2. Schwannoma vestibolare
unilaterale VS più eventuali due di meningioma, glioma, schwannoma,
neurofibroma, posteriore subcapsulare opacità del cristallino
3. Due o più meningioma
più VS unilaterale o due di glioma, schwannoma e cataratta.
NF II può essere diagnosticata con il 65%
di precisione prenatale con villocentesi o amniocentesi . [4]
Un'altra serie di
criteri diagnostici è il seguente:
·
Rilevamento
di neuroma acustico bilaterale da parte di procedure di imaging
·
Parente
di primo grado con NF 2 ea comparsa di :
·
Neurofibroma , meningiomi , glioma o Schwannoma
·
Parente
di primo grado con NF 2 e l'insorgenza di cataratta sottocapsulare posteriore
giovanile.
La diagnosi di NF2
comporta quanto segue:
I test genetici
Studi di imaging
Esami uditivi, oftalmici, e istologiche
I test genetici
Una volta che la diagnosi clinica è stata stabilita
inequivocabilmente in un dato individuo, analisi molecolare diretta può essere
offerto
Tassi di rilevamento per i test molecolari basati su approcci 65%
Se viene trovata una mutazione, altri familiari asintomatici
possono beneficiare di test presintomatico
Test molecolare del tessuto tumorale può aumentare studi
molecolari tradizionali quando l'analisi del DNA ottenuto da linfociti di
sangue è non diagnostico
Per le famiglie in cui nessun mutazione può essere identificato in
una persona colpita nota, analisi di linkage o metodi di test genetici
indiretti possono essere utilizzati
Test presintomatico dei membri a rischio della famiglia richiede
un vigoroso processo di consenso informato e potrebbe essere meglio fatto
durante una sessione di consulenza genetica in un cancro, centro genetico, o
neurofibromatosi specializzata in tali questioni
Test prenatale per NF2 è la seguente:
Quando un genitore ha NF2, test prenatale può essere fatto su
amniociti o villi coriali, sia attraverso l'analisi diretta mutazione del gene
quando è stata identificata la modifica o mediante analisi di linkage
La diagnosi prenatale può non essere possibile se il genitore
affetto è la prima persona colpita in famiglia e una mutazione non può essere
trovato
Se un genitore prospettico ha una nota NF2 mutazione,
la diagnosi genetica preimpianto può essere possibile se la coppia è disposto a
sottoporsi a fecondazione in vitro con trasferimento di embrioni non affetti
La risonanza magnetica
MRI rimane il fondamento
per la diagnosi e lo screening del sistema nervoso centrale, nervi cranici e tumori
del midollo spinale
Soggetti a rischio
possono essere monitorati per i tumori del sistema nervoso centrale che
iniziano durante l'adolescenza, con scansioni MRI annuali della testa eseguita
attraverso i loro fine degli anni '50
MRI con 3 dimensioni (3D) volumetria è ora il metodo preferito per
seguire la crescita schwannoma vestibolare nel tempo Harris GJ, e 2008.
Routine MRI del midollo spinale probabilmente non è indicato nei
soggetti asintomatici affetti oa rischio
Risonanza magnetica della colonna vertebrale è indicata
diagnostico quando un individuo si presenta con motori o sensoriali modifiche
suggestivi di una lesione del midollo spinale o lesioni
Come accennato in precedenza - il
neurinoma acustico può essere diagnosticata o da un medico con esperienza
otologica, che possa integrare insieme l'intera immagine, o con una risonanza
magnetica con gadolinio del cervello. Siccome le MRI, sono molto costose , il
metodo più efficiente per contenere i costi della diagnosi (già scritto nella
2008), è che , tutti i pazienti con una inspiegabile perdita dell'udito
asimmetrica, siano valutati da un medico con esperienza otologica. Qualcosa
che finora è stato trascurato nella valutazione preoperatoria dei pazienti con
neurinoma dell’acustico è stato di stabilire preoperatoriamente, in tutti i
casi, i parametri della funzione facciale ricavati dalla elettroneuronografia e
dal blink test e i dati dell’udito preoperatorio da accertamenti più
approfonditi che comprendano:
• es audiometrico
tonale e vocale
• test sopraliminari
• audiometria automatica
• potenziali evocati
uditivi
• test audiometrici
vocali competitivi
• valutazione protesica
sia con protesi acustiche tradizionali che con protesi ad induzione magnetica
solo la combinazione di tutte queste
informazioni ottenute bilateralmente potrebbe darci la possibilità di offrire
informazioni più precise ai nostri pazienti cui va peraltro spiegato che ogni
intervento chirurgico è una realtà a sé e che le possibilità offerte sono solo
quelle su base statistica (se siamo in due e io mangio una mela per la
statistica ne abbiamo mangiato ciascuno il 50%!!!) è inoltre da considerare tra
le altre cose anche l’applicazione di un impianto BAHA nei casi di perdita
totale dell’udito e, in un futuro si spera non lontano, un impianto cocleare
più sofisticato di quelli attualmente disponibili per offrire la possibilità di
un ripristino seppur parziale di una funzione uditiva nel lato
|

|
|
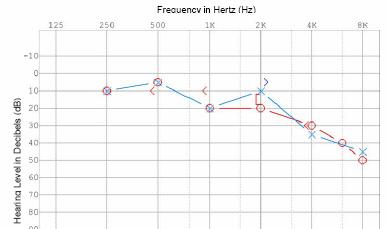
Fig.5 Audiogramma
tipico di paziente con un neuroma acustico.
|
Audiometria Convenzionale è il test più utile per diagnosticare un
neurinoma acustico. L'anomalia più comune è una perdita neurosensoriale
asimmetrica alle alte frequenze (vedi figura 5 sopra). Non più di 1 su 20
pazienti , con tumori di grandi dimensioni , hanno una asimmetria entro 15 dB
a 4000 Hz. Tuttavia, bisogna ricordarsi che solo 1 su 1000 pazienti con
asimmetria uditiva può avere neuroma del nervo acustico . È stato stimato che
il 5 per cento delle persone con ipoacusia neurosensoriale hanno un neurinoma
acustico (Daniels et al, 2000), ma questa stima è sospetta in quanto
comporterebbe una prevalenza molto più elevato di neuromi acustici di quanto
siano comunemente accertati. L'audiometria vocale (SRT) è normale in molti
pazienti con tumori di piccole dimensioni. La discriminazione vocale è
eccellente in circa il 50% dei pazienti con piccoli tumori, e un terzo dei
pazienti con tumori di grandi dimensioni hanno una discriminazione vocale
ancora quasi normale (> 80%), la discriminazione discorso. Perché
l’asimmetria uditiva è dovuta dovuto principalmente a condizioni diverse da
neuromi acustici, altri elementi di informazione devono essere integrati per
fare la diagnosi clinica di neuroma acustico. Di solito questo processo di
integrazione è fatto da un medico con esperienza otologica, e non dagli
audiometristi .
|

|
|
Fig.
6
Audiogramma del paziente con un grande neuroma acustico sul lato sinistro, ma
(quasi) la funzionalità uditiva è quasi simmetrica . Questo esempio dimostra
che i test con simmetria uditiva, non sempre escludono la diagnosi di un
neuroma acustico. Si veda il commento in testo.
|
Ipoacusie
simmetrica o anche normale funzionalità uditiva non escludere una chitarra
acustica, ma è molto raro .si sono trovati diversi pazienti con una
funzionalità uditiva simmetrica , ma con un grande neurinoma acustico da un
lato sopra è riportato un esempio di un uomo che aveva una grande neurinoma acustico
sul lato sinistro - per essere sicuri che si deve fare una risonanza magnetica,
è di essere il più sicuri possibile, si deve fare una risonanza magnetica ad alta
risoluzione del IAC (condotto uditivo interno )con gadolinio. Perché quest’esame
è terribilmente costoso (lo screening di tutti i pazienti con problemi d'udito
di qualsiasi tipo), tuttavia a volte sono stati fatti degli errori i. Mentre
questa è davvero una decisione che per gli economisti sanitari, ci sembra che
complessivamente sono ammissibili degli errori occasionali è ammissibile, se uno
considera ciò che è meglio per una grande popolazione .
Esami
ABR Fig. 6b
Quando
l’esame audiometrico è anormale con un peggioramento uditivo progressivo,
audiometria in genere vengono effettuati ulteriori test, come l’ABR (Auditory
Brainstem Response ) o risposte uditive del tronco cerebrale, e RM (risonanza
magnetica), con determina la diagnosi. L’esame ABR è meno sensibile di quello
RM (il tasso di falsi negativi è di circa il 33%), ma è molto meno costosa. Una
nuova tecnica chiamata "summated ABR", in sostanza, ABR diversi
registrati in tempi diversi , possono dare una migliore sensibilità. Nel nostro
contesto clinico, questa tecnica è non è poco indicata e comunemente il test
più sensibili per l'acustica (MRI) è così. Tuttavia, questo metodo potrebbe
avere utilità in contesti in cui le RM sono di difficile accesso.
Una
configurazione caratteristica ABR in una persona con un neuroma acustico è
un'onda i e dopo nulla assenza delle onde 3° o 5° (10-20% dei casi). Un
ritardo dell’intervallo onda I- III è comune, un ritardo dell’onda V si
verifica nel 40-60% dei casi. Con l’ ABR si hanno un elevato numero di falsi
positivi e falsi negativi. Fino a 1 / 3 dei pazienti con tumori di piccole
dimensioni (con MRI) hanno un ABR normale.
|

|
Fig
6b.
ABRs registrato da pazienti con tumori acustici chirurgicamente confermati.
La forma d'onda superiore in ogni pannello è da un orecchio normale. La forma
d'onda inferiore a (a) mostra l'intervallo I-V prolungato da un paziente con
un neuroma acustico. La forma d'onda inferiore a (b) mostra l'assenza dell’
onda V da un paziente con un meningioma dell'angolo ponto-cerebellare.
|
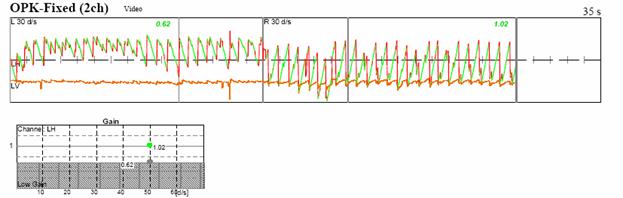
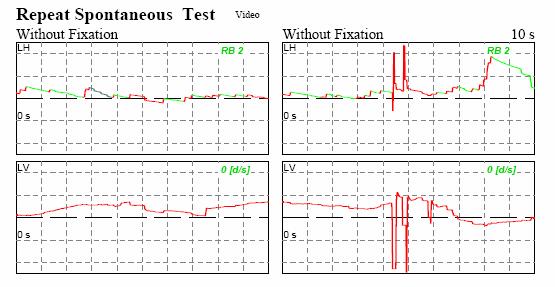
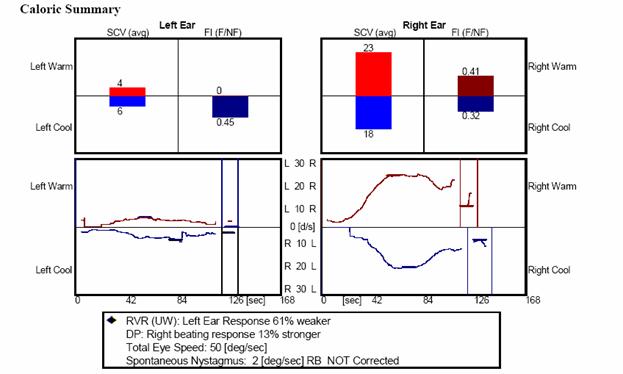
Esami Videonistagmografici(
ENG)
La
Videonistagmografia, (test ENG) è
spesso alterata e circa il 60 per cento di tutti i tumori , sono associati ad
una iporeflettività unilaterale alle prove
caloriche (Hulshof et al, 1989). Tuttavia, l’
ENG non è un test diagnostico specifico. Il Test
con la sedia rotatoria è meno sensibile del test calorico. La
posturografia è insensibile al neuroma acustico. Il
decay test,o test di
Anderson (decadimento del riflesso acustico) è anche poco sensibile (circa il
36%). Anche le Otoemissioni acustiche sono considerate un test poco sensibile
per il neurinoma acustico. Come accennato in
precedenza, ci si aspetterebbe che i VEMP’s
siano sensibili al neuroma acustico.
|

|

|
|
Fig.-7a
Risonanza magnetica del cervello (coronale) che mostra un neuroma acustico
(la macchia bianca sul lato sinistro della foto).
|
Fig.-7b
Risonanza
magnetica del cervello assiale (con contrasto) che mostra un gran neuroma
acustico intracanalicolare, sul lato destro del cervello (parte sinistra
della scansione).
|
|

|

|
|
Fig.-7c
Un altro neurinoma acustico intracanaliculare sul lato destro.
|
Fig.-7d
Grande
neurinoma acustico di tre centimetri con interessamento del tronco cerebrale
sul lato L.
|
Esame oftalmico
I controlli annuali sono raccomandate per i bambini e gli adulti
con NF2
Visite oculistiche dilatati per opacità del cristallino, amartomi
retinici, o membrane epiretiniche può essere molto utile anche in un bambino a
rischio di NF2
Cataratta giovanile possono essere visti molto prima che un
bambino mostra alcun segno di schwannoma vestibolare
IMMAGINI CEREBRALI
Anche se è relativamente costosa rispetto all’
audiometria o ABR, la prova ottimale per escludere il neuroma acustico è un RMI
T1 con gadolinio ( vedi foto sopra). Con la RM, i neuromi acustici sono spesso
ingrossati n modo uniforme , densi, e si espandono nel condotto uditivo
interno. A Una variante della RM(fast spin-echo T2 )è molto sensibile al
neuroma del nervo acustico, e in alcune situazioni cliniche, può essere
effettuato a buon mercato. Se una risonanza magnetica non può essere fatta,
come ad esempio nei pazienti con un pacemaker o di clips metalliche, -
dovrebbero essere effettuata nei soggetti ad alto rischio un CT aperta, in
particolare se l'ABR è indicativo di un neuroma acustico. La TAC con contrasto
non è un buon esame per la diagnosi di neuromi acustici, in quanto ha un alto
tasso di falsi negativi (circa il 37%).
Mentre la RM è la prova più sensibile per il neuroma
acustico, anche se si possono commettere errori. Falsi negativi (errori )si
verificano soprattutto nelle persone con tumori molto piccoli, o nelle
scansioni eseguite male (come ad esempio in una scansione fatto con una
bassa-unità di campo e senza contrasto). Errori di tipo falsi positivi sono
molto rari, ma anche possibili (House et al, 2008).
Un Neuroma acustico può raggiungere dimensioni anche di
a 4 cm. Il più piccolo, neuroma acustico intracanalicolare (vedi sopra a
destra), è misurata in millimetri. Un "piccolo" neuroma acustico è
inferiore a 1,5 cm (sopra a sinistra). Un neuroma acustico "moderato"
acustica è 1,5-3 cm, e un "grande" un neuroma acustico è di 3 cm o
superiore.
I tumori sono stadiati in base alla combinazione
della loro localizzazione ed alle dimensioni. Un tumore
"intracanalicolare" è piccolo ed è collocato nel IAC (condotto
uditivo interno). A tumore "cisternale" si estende al di fuori
della IAC. Un tumore "compressivo" l è quello a contatto con il
cervelletto ed il tronco encefalico, e un tumore "idrocefalico" è
quello che sta ostruendo le vie di drenaggio del CSF(liquido-cefalo-rachidiano)
nel IV° ventricolo .Il Neuroma acustico si può estendere dal nervo all'orecchio
interno,il che può rendere più difficile la loro rimozione (Falcioni et al,
2003). Gli schwannomi
Intralabirintici nonché gli schwannoma intracocleari esistono (Kennedy et al, 2004). Il neurinoma acustico
riportato al di sopra ,nella figura a destra ha una piccola estensione
intracocleare.
|

|
|
Fig.8a Immagine Assiale
di un paziente con NF2 mostra un neuroma acustico su entrambi i lati (Image
cortesemente fornita dal Dr. Richard Wiet ). Fig.8b Immagine a più
elevata definizione che mostra meningiomi multipli in uno stesso paziente
con NF2.
|
Raramente,
i neuromi acustici sono di origine ereditaria. Neuroma acustico causato da una
neurofibromatosi di II tipo ,dovrebbe essere sospettata nei giovani pazienti e
in quelli con una storia familiare di tumori neurali. La figura sopra mostra un
esempio di tale paziente. E 'comune in questa malattia diventare sordi a causa
di neuromi acustici bilaterali. Il test genetico per la NF1 e NF2 è disponibile
in commercio, per esempio, dalla diagnostica
Athena.
|

|
Fig.8c
Caratteristiche radiologiche di
neuroma acustico:
1. Ampliamento
del meato acustico interno "segno di Trumpet"
2. Estensione
extracanalicolare ponto-cerebellare (percorso di minor resistenza) può
portare a comparsa del "cono gelato”
|
|

|
|
Fig.8d
MRI petrous bone with gadolinium is the most diagnostic one.
|
Diagnosi
Differenziale
Ci sono diversi altri tumori che possono verificarsi
nella stessa regione del cervello, l'angolo cerebello-pontine o CPA, come i
neuromi acustici. Di tutte le lesioni del CPA, l'angolo ponto cerebellare i
neuromi acustici rappresentano rappresentano all’incirca il 70-90 per cento. I
meningiomi sono secondi per frequenza (10 per cento), seguita dai tumori
epidermoidi, e successivamente dai lipomi. Di tanto in tanto i tumori
collocati in altri organi, come il polmone, possono metastatizzare al CPA.
I tumori metastatici di solito crescono
rapidamente – La funzionalità uditiva peggiora velocemente, e spesso il nervo
facciale è coinvolto con una paralisi di Bell
(Bells palsy), , nel corso di poche settimane.
Neuromi
Acustici Scoperto per Caso Accidentalmente
Siccome la TC e la
risonanza magnetica sono più comunemente utilizzati, sempre più Neuromi
Acustici, sono scoperti casualmente . Per esempio, una persona che ha un mal
di testa o emicrania, può richiedere una risonanza magnetica, che rivela un
neuroma acustico. O qualcuno che ha avuto un incidente automobilistico,
potrebbe richiedere una risonanza magnetica, che rivela un neuroma acustico.
Questa situazione ha un
considerevole potenziale di guai. Non è molto probabile che un neuroma acustico
in precedenza in silenzio, all'improvviso si manifesta al tempo stesso come un
altro problema -, come un lieve infortunio testa o emicrania. Piuttosto, è comunemente il caso che la persona che
avrà una delle cause più comuni di vertigine, e appena capita di avere una
chitarra acustica in silenzio.
Se qualcuno in una
simile situazione procede con la chirurgia o radioterapia, n è certo che
l'intervento chirurgico o radiazioni creeranno uno squilibrio vestibolare e
sordità. Questo alla fine si verificano in ogni caso, ma il trattamento di un
tumore che non è in crescita accelererà il processo. Per questo motivo, estrema cautela è suggerita - a nostro parere, fatta
eccezione per i tumori di grandi dimensioni, è meglio avere una prova oggettiva
- ossia la progressione della perdita di udito o di un allargamento su MRI -
che il tumore è in crescita prima di imbarcarsi su un intervento chirurgico o
radioterapia. Vale la pena di chiedere un secondo parere .
DIMENSIONE
DEL TUMORE
I rischi e le complicanze della
chirurgia di un tumore del nervo acustico, variano a seconda delle dimensioni.
Più grande è il tumore, più seria e
maggiore è lo probabilità di avere delle complicanze. La rimozione di un tumore
del nervo acustico, sia grande che piccolo, è un procedimento chirurgico
importante , con la possibilità di gravi complicazioni, inclusa la morte.
Il rischio nella chirurgia di questi
tumori non deve mai essere minimizzato.
Classifichiamo i tumori come:
piccoli, medi, grandi, molto grandi.
I nostri accertamenti indicano che
il vostro tumore è:
A) INTRAMEATALE ( ancora
dentro l’osso)
B) PICCOLO( inferiore a 1 cm
nell’angolo ponto-cerebellare )
C) MEDIO( maggiore di 1 cm,
inferiore a 2 cm )
D) GRANDE( maggiore di 2 cm,
inferiore a 4 cm )
E) MOLTO GRANDE (
maggiore di 4 cm )
Gestione
Dei Neuromi Acustici
Nikolopoulos E O'Donoghue hanno recentemente rivisto 111
articoli sul trattamento del neuroma acustico e ha dichiarato che non
esistono metodi "ben programmati per poter effettuare un confronto tra
i diversi trattamenti, e quindi la pretesa di medici che sono favorevoli ad
un trattamento particolare, sono infondate" (2002). Noi non pensiamo che
la saggezza e l’esperienza clinica non debbano essere prese in considerazione ,
ma certamente al momento attuale ci sembra essere che il trattamento del
neuroma acustico sia uno un'arte.
Ci sono tre opzioni distinte:
• gestione medica o attesa vigile "wait and see" [aspetta ed osserva
(trattamento conservativo)]
• intervento chirurgico per rimuovere il tumore
• radioterapia con Gamma-Knife o radioterapia
stereotassica
Che linee
guida mettere in atto di fronte ad un neurinoma di pochi millimetri nel
condotto uditivo interno?
In questi casi ci sono due opzioni che vanno discusse con il paziente.
La prima è l’attesa vigile la seconda un intervento chirurgico volto alla
preservazione dell’udito. I fattori da considerare nella scelta sono: età e
condizioni generali del paziente, udito nell’orecchio interessato e funzione
del nervo facciale
E se si
tratta di una neoformazione di parecchi centimetri che occupa tutto l’angolo
ponto-cerebellare (fase otoneurologica), o peggio con effetto compressivo sul
ponte, escavazione del peduncolo cerebellare e del cervelletto (fase
francamente neurologica)?
Vanno
distinti i tumori in fase otoneurologica da quelli in fase neurologica;
quest’ultimi vanno rimossi in toto o in parte al più presto per salvare la vita
del paziente mentre per quelli senza segni neurologici esiste la doppia opzione
della chirurgia e della radioterapia stereotassica. L’orientamento terapeutico
si baserà essenzialmente sulla durata dei sintomi, sulla loro intensità e i
desideri del paziente una volta che gli siano stati spiegati i pro e i contro
delle due opzioni. Nella tabella che segue sono riportati vantaggi e svantaggi
delle due opzioni.
|
vantaggi
|
svantaggi
|
microchirurgia
|
asportazione completa
diagnosi certa bassissimo rischio per la vita
|
bassa percentuale di conservazione dell udito alta percentuale di paralisi facciale postoperatoria
|
radioterapia stereotassica
con raggi gamma
|
nessun rischio chirurgico
basso rischio di perdita uditiva
basso rischio di paralisi facciale
eseguibile in pazienti in cattive condizioni
di salute
|
permanenza del tumore
diagnosi non certa necessità di
continui controlli
|
Assistenza medica per i
pazienti con neurofibromatosi di tipo 2 è costituito da esami di routine
incentrati sulla diagnosi precoce di alcuni dei potenziali complicazioni legate
alla CNS o lesioni del midollo spinale. [2] Gestione da un
team di specialisti in una clinica multidisciplinare può fornire la più
completa e conveniente cura nel tempo. Quello che segue è uno schema di
linee guida ragionevoli nella cura del paziente con NF2:
Esame annuale neurologico cercando deficit sottili o cambiamenti
di stato neurologico che potrebbero suggerire la progressione della malattia
Screening uditivo annuale con BAER, con rinvio ad un audiologo per
le raccomandazioni di amplificazione, di aumento o di logopedia
MRI annuale per monitorare le lesioni esistenti o per cercare
lesioni presintomatica
Valutazioni oftalmologiche annuali per monitorare l'acuità visiva
Gestione Medica (attesa Vigile): Circa il 25% di
tutti i neuromi acustici sono trattati con il trattamento medico. L’attesa
vigile si attua nei pazienti con neurinoma dell’acustico piccolo nell’unico
orecchio udente, nei pazienti che hanno un alto rischio operatorio per altre
patologie concomitanti e nei pazienti che rifiutano le altre due modalità di
intervento Il trattamento medico consiste nel controllo periodico dello stato
neurologico del paziente, l'uso di apparecchi acustici da parte di questi
pazienti, se del caso, controlli periodici radiologici(come RM). Si tratta di
un appropriato metodo di trattamento per alcuni pazienti (Hoistad et al,
2001). Non
esistono farmaci noti che anno un effetto rilevante sulla crescita dei tumori
acustici. I tumori possono crescere molto
lentamente, a circa 1-1/2 mm per anno, e si può scegliere di seguire un tumore
con una serie di esami audiometrici e / o risonanza magnetica (Shin et al,
2000). Nei pazienti di età avanzata, una grave minaccia per la vita o la
funzione corporea di crescita tumorale può essere giudicata improbabile nel
resto della prospettiva o durata di vita prevista di un paziente e per questo
motivo, può essere preferita la gestione medica (Perry et al, 2001). Una volta
che un tumore è diagnosticato, la Ia RM viene effettuata dopo 6 mesi
e poi con cadenza annuale (Perry et al, 2001).
Questa procedura ha i suoi rischi. Anche quando non si riscontra una crescita
del tumore con la RM, vi è sempre il rischio che il paziente perda la
funzionalità uditiva utile, rendendo il paziente non più un candidato per la
chirurgia conservativa. All’incirca dal 10 al 43% dei pazienti ,seguiti per
circa 2 anni, perde quella percentuale di udito “utile” per sentire (Warrick et
al, 1999; Shin et al, 2000; Lin et al, 2005).
Trattamento medico
sistemico
In uno studio clinico del 2009
presso il Massachusetts General Hospital si è utilizzato
il farmaco antitumorale Bevacizumab (nome commerciale: Avastin ) per il
trattamento di 10 pazienti con neurofibromatosi di tipo II. Il risultato è
stato pubblicato nel New England Journal of Medicine . Dei dieci
pazienti trattati con bevacizumab, i tumori si è ridotto a 9 di loro, con il
miglior tasso di risposta medio del 26%. La funzione uditiva è migliorata
in alcuni dei pazienti, ma i miglioramenti non sono stati fortemente correlati
con restringimento del tumore. Bevacizumab agisce tagliando l'apporto di
sangue ai tumori e quindi privandoli del loro vettore di crescita. Gli
effetti collaterali durante lo studio incluso alanina aminotransferasi , proteinuria e ipertensione (pressione sanguigna elevata) tra gli altri. [8] Uno studio
separato, pubblicato in The Neuro-oncologia
Journal , mostrano riduzione del tumore del 40% nei due pazienti
con NF2, insieme con significativo miglioramento dell'udito Mautner VF, et
al. (January 2010).
Nel complesso, i ricercatori credono che
il bevacizumab ha mostrato effetti clinicamente significativi sui pazienti NF
II. Tuttavia, sono necessarie ulteriori ricerche prima che gli effetti del
bevacizumab possAno essere stabilite nei pazienti NF2.
La terapia farmacologica
per meningioma NF2 legati
Sunitinib è stato studiato
per il trattamento di meningioma che è associato
con Neurofibromatosi . [10]
Sono in corso studi per verificare mTORC1
inibitore rapamicina come un potenziale terapeutico in schwannomi NF2 e
meningiomi
La terapia farmacologica
per schwannoma vestibolare
Lapatinib è stato studiato
da Jeffrey Allen presso la NYU Langone Medical Center per il trattamento di
schwannoma vestibolare in Neurofibromatosi di tipo II. [11]
L'uso terapeutico di erlotinib ha
mostrato risultati promettenti nel trattamento di inoperabili, schwannoma
vestibolare progressivo, che comporta non solo una riduzione delle dimensioni
del tumore, ma anche nel miglioramento della funzione uditiva. Ulteriori studi
clinici sono in ordine prima con questo agente chemioterapico orale può essere
consigliato su una base di routine. [16] Una prova di bevacizumab, un fattore
di crescita endoteliale anticorpo monoclonale antivascolare, ha anche mostrato
una certa efficacia nel ritiro di schwannoma vestibolare; l'udienza farmaco
migliorato in alcuni pazienti con tumori non operabili. [Plotkin SR,e 2009]
D'altra parte, non importa
quale tipo di trattamento viene utilizzato, nel lungo tempo, è molto
improbabile che l'udito rimanga "utile". La cosiddetta "chirurgia conservativa dell’udito
" raramente mantiene una funzionalità uditiva utile, questa tende a
deteriorarsi abbastanza rapidamente con il tempo, anche se il tumore non è più
presente. In base a questi dati , alcuni chirurghi consigliano semplicemente di
eliminare tutto l’intero nervo 8°, in quanto questa soluzione rende molto
improbabile una recidiva del tumore. A nostro parere, questo è un giudizio
opportuno - ma non un'idea irragionevole. Una stima ragionevole è che dopo più
di un anno, circa il 75% dei tumori avrà un allargamento visibile, una media di
1,5 millimetri, e circa il 25% non lo avrà. Alcune varietà crescono molto più
rapidamente di altri.
Nei
pazienti con la neurofibromatosi, l'udito è destinato a rimanere stabile nel orecchio
operato per circa 1-2 anni (Masuda et al, 2004).
La
Radioterapia con raggi gamma ha la finalità di bloccare l’accrescimento
del tumore e ottiene questo in un’alta percentuale di casi con minori rischi e
complicanze della chirurgia. Naturalmente il tumore rimane e deve essere
controllato nel tempo.
Gamma Knife: quando il rischio di intervento chirurgico è
elevato a causa di altri problemi di salute, o se il paziente rifiuta la
chirurgia, può essere utilizzata la "gamma Knife " . Questo
è un metodo di irradiare il tumore, inventato da Lars Leksell nel 1971. Questa
procedura evita un intervento chirurgico con i rischi che ne possono derivare.
In passato, questa opzione è stata generalmente consigliata solo per i casi , a
più elevato rischio chirurgico, a causa della possibilità di complicazioni
tardive da radiazione, e la necessità di un monitoraggio continuo con RM dei
risultati della procedura.
Non si consiglia utilizzare la gamma knife ad alte dosi a causa della
possibilità di complicazioni da radiazione dopo e oltre i 2 anni. Tuttavia,
gamma knife a basso dosaggio è alla ricerca molto meglio e ci sono sicuramente
molte volte quando è l'opzione migliore. Basse dosi di radiazioni (ad esempio
13 Gy) sono attualmente consigliato a causa del rischio molto più basso di
debolezza e intorpidimento facciale (Wackym et al, 2004).
Una
conseguenza interessante del protocollo di radiazioni a basso dosaggio è che si è riscontrato che i pazienti, dopo le radiazioni,
non hanno una perdita completa dell'udito o della funzione vestibolare. In
alcuni casi questa ridotta funzionalità vestibolare può essere molto
fastidiosa in quanto può provocare sintomi di irritabilità nervosa, come ad
esempio l'iperventilazione che può indurre del nistagmo. Ciò è una probabile
conseguenza di utilizzare una metodologia di trattamento che agisce più
lentamente rispetto ad un intervento chirurgico. Sembra probabile che questa
complicanze siano più comune nelle pazienti che hanno tumori di piccole
dimensioni.
In
queste situazioni l'iperventilazione induce un nistagmo che batte verso la
lesione (a differenza del nistagmo provocato dalle vibrazioni che batte in
direzione opposta alla lesione). Spesso è un nistagmo molto intenso . Nei
pazienti con questo segno, ci si può aspettare che scompaia (questa scomparsa
del nistagmo indotto da iperventilazione potrebbe richiedere diversi anni), si
può provare qualche farmaco che riduca l'irritabilità del nervo, in caso
contrario si riconsiderare il trattamento chirurgico.
Radioterapia
stereotassica. Radiazione diversi dai
raggi gamma possono essere utilizzati anche per il trattamento di neuroma
acustico. Essi comprendono l’acceleratore lineare (LINAC) e Cyberknife. Le
altre modalità sono simili a Gamma Knife nelle caratteristiche generali. La conservazione dell'udito a lungo termine è
molto raro in persone con radioterapia stereotassica (6,7% secondo Lin et al, 2005). In altre parole, anche se
l '"obiettivo" è quello di preservare l'udito, praticamente questo
non è realistico. Non vediamo alcun motivo particolare per utilizzare la
radioterapia stereotassica, piuttosto che Gamma Knife. La probabilità di
recidiva del tumore utilizzando regimi di dosaggio attuale è di circa il 5-10%.
La crescita del tumore è rara in pazienti che rimangono stabili dopo 6-7 anni
di terapia .
I Problemi
della radioterapia sono le recidive (5-10%), perdita dell’ udito (alla fine il
93%), il rischio di irradiare tumori di grandi dimensioni (> 2 cm) dovute al
rigonfiamento del tumore nel primo anno, il rischio di malignità (Tanbouzi et
al, 2011 , Markou et al, 2011), idrocefalo (raro), aneurisma rotto IAC (raro),
e accelerata aterosclerosi vertebro-basilare (es. Jackler, 2007).
Gestione di perdita di udito in NF2 Impianti
uditivi del tronco encefalico
Perché la perdita dell'udito in quelli
con NF2 si verifica quasi sempre dopo l'acquisizione di competenze linguistiche
verbali, i pazienti non si integrano sempre bene nella cultura dei sordi e sono più propensi a ricorrere a uditivo tecnologie assistive . Il più sofisticato di questi
dispositivi è l' impianto cocleare , che a volte può ripristinare un alto livello di funzione
uditiva anche quando udito naturale è totalmente persa Schwartz
MS,e 2008. . Tuttavia,
la quantità di distruzione al nervo cocleare causato dalla tipica schwannoma
NF2 spesso preclude l'utilizzo di tale impianto. In questi casi, un impianto uditivi del tronco encefalico (ABI) in grado
di ripristinare un livello primitivo di udito, che, quando è integrato da lettura labiale , in grado di ripristinare una conoscenza funzionale della
lingua parlata.
|

|
Fig.-9
Neuroma acustico molto grande (proiezione coronale, il tumore è la grande
macchia bianca). Fonte: Mayo Clinic
Neuroscience Update.
|
Trattamento
chirurgico: Lo
scopo primario della chirurgia del neurinoma dell'acustico è l'exeresi totale
del tumore conservando, ove possibile, l'integrità anatomica e funzionale dei
nervi cranici, con le minori sequele circa
la metà di tutti i neuromi acustici sono attualmente trattati con la chirurgia.
Questa opzione probabilmente diminuirà nei prossimi decenni, per l'uso
crescente del trattamento con gamma knife . La figura sopra mostra un neuroma
acustico ,di grandi dimensioni ,in questi casi è da preferire il trattamento
chirurgico. Nella maggior parte dei casi la rimozione chirurgica del tumore è
l'opzione preferita perché previene complicanze potenzialmente fatali di
crescita del tumore (anche se questa evenienza è piuttosto
insolita).L’intervento chirurgico potrebbe in teoria permettere di "conservare"
la funzionalità uditiva, anche se è molto raro che l'udito sia effettivamente
utile dopo l'intervento chirurgico. Di solito l'intervento viene effettuato
presso un centro universitario da un team di chirurghi compreso un neurotologo
(un otorinolaringoiatra specializzato) e un neurochirurgo. Ci sono diversi approci operativi.
|

|
Fig.-10 a
Comuni approcci chirurgici per il
Neuroma Acustico
testa.
Translabirintica (attraverso
l'orecchio interno).
La perdita dell'udito è previsto e
inevitabile.
Non adatto per i tumori di grandi
dimensioni.
Retrosigmoidea o suboccipitale
(attraverso il craniodietro l'orecchio).
Retrazione del cervelletto (parte
del cervello) è necessaria.
Mal di testa
sono comuni dopo tale
approccio.
(Immagine
da Jackler R, Atlas of Neurotology e
Skull Base Surgery (Mosby 1996, prima
edizione).
|
Ciascuno di questi approcci chirurgici ha vantaggi e
svantaggi che devono essere considerati nella scelta di un approccio ottimale.
Il trattamento chirurgico in cui il cervello è esposto è quasi sempre eseguita
da un team di chirurghi, di solito sono presenti un neurootologo ed un
neurochirurgo. La maggior parte dei pazienti vengono ricoverati in ospedale il
giorno prima dell'operazione. Dopo l'intervento chirurgico, è bene trascorrere
la 1a notte in una unità intensiva. La maggior parte dei pazienti sono
dimessi dall'ospedale entro 4-6 giorni dal'intervento chirurgico, ed entro 6
settimane di solito è possibile riprendere l'attività lavorativa .La RM di
solito viene effettuata dopo 1 e 5 anni per rilevare eventuali residui o
recidive tumorali. Si consiglia la rimozione del tumore totale o quasi totale
(95%) (Sanna et al, 2002). Si consiglia un attento follow-up con ricorrenti RM
.La presenza di noduli od un allargamento progressivo del condotto uditivo
interno può rappresentare una ricrescita del tumore (Brors et al, 2003).
I tumori che si estendono nel labirinto stesso (vale
a dire "gli schwannomi intracocleare") non possono essere rimossi
con l'approccio retrolabintico " e vi possono essere recidive ai tumori, e
possono ripresentarsi. Ci possono essere molte complicazioni importanti, che
possono derivare da un intervento chirurgico , queste complicazioni debbono
essere prese in considerazione (vedi sotto).
riguardo alle chirurgia conservativa dell'udito ,
conservazione sempre auspicabile, purtroppo, la possibilità che l'udito sia
preservato dopo un intervento chirurgico di neuroma acustico è minimo.
Nedzelski e colleghi hanno recentemente riferito che solo il 16% circa dei
pazienti ha avuto un udito utilizzabile nei follow-up dopo l'intervallo di
"chirurgia conservativa dell'udito". (Lin et al, 2005). Mentre la
funzionalità uditiva può essere "conservava" immediatamente dopo
l'intervento chirurgico, di solito si deteriora in pochi anni.
Prognosi
La prognosi di
neurofibromatosi tipo 2 (NF2) dipende da una serie di fattori, tra cui l'età di
insorgenza dei sintomi, il grado di sentire deficit, e il numero e la posizione
dei vari tumori. Anche se l'età di insorgenza è relativamente simile
all'interno delle famiglie, la fascia d'età può variare 2-70 anni. Mentre
i tumori stessi sono relativamente indolente e non subiscono la trasformazione
maligna, studi effettuati alla fine del 1980 e all'inizio del 1990 hanno
mostrato chiaramente che i tassi significativi di mortalità e morbilità sono
associati con la diagnosi di NF2.
Uno di questi studi ha
suggerito che la sopravvivenza dal momento della diagnosi medie effettive a 15
anni; tuttavia, questo potrebbe cambiare in meglio con diagnosi migliore,
tecniche chirurgiche, la sorveglianza, lo screening e il riconoscimento di
malattia lieve (dovuto in parte alla maggiore consapevolezza del medico e la
disponibilità di opzioni di diagnostica molecolare).
Schwannoma vestibolare
sono la caratteristica più comune e ben riconosciuto di NF2 che porta a una
significativa morbidità. I sintomi di tinnito, perdita dell'udito
progressiva, e anche la disfunzione vestibolare sono spesso i primi segnali di
NF2.Anche se la perdita uditiva unilaterale è il numero 1 che presenta sintomi,
sordità bilaterale sarebbe previsto per eventualmente verificarsi in individui
più colpiti.Schwannoma vestibolare non trattati possono estendere a livello
locale e possono causare compressione del tronco cerebrale, idrocefalo, e,
occasionalmente, paralisi del nervo facciale.
Schwannomas midollo
spinale a forma di manubrio sono abbastanza comuni in NF2 e determinano una
significativa morbilità; essi presentano una grande sfida
terapeutica. Ependimoma midollo spinale, astrocitomi e meningiomi si
verificano anche, ma meno frequentemente. Meningiomi intracranici, d'altra
parte, è frequente; essi possono essere asintomatici, o possono causare
una varietà di sintomi e deficit del SNC 10. Aboukais
R,e 2010.
Schwannomas Nonvestibular
si verificano in più della metà dei pazienti e sono spesso diagnosticati in
pazienti con una precedente età alla diagnosi di NF2.Nervi cranici III e V sono
più comunemente coinvolti, ma la rara presenza di schwannomas forame giugulare
potenzialmente impattare il glossofaringeo, vago, e / o nervi spinali
accessorio può portare a disfagia, disturbi della motilità esofagea, raucedine,
o aspirazione.
D'altra parte, schwannoma
nonvestibular in pazienti con NF2 tendono ad essere più indolente e crescere
lentamente nel tempo. Questo può complicare il trattamento del processo
decisionale, dal momento che le opzioni includono la chirurgia, la radioterapia
e vigile attesa Fisher LM,e 2008.
Subcapsulare posteriore,
o giovanile, la cataratta può precedere CNS sintomatologia. Le cataratte
possono progredire nel corso del tempo, portando a riduzione dell'acuità
visiva. Una buona percentuale di individui affetti si trovano ad avere
amartomi retinici o membrane epiretiniche che possono o non possono essere
visivamente notevole.
Polineuropatia sensoriale
motore è visto in alcuni individui con NF2 che possono o non possono avere
tumori identificabili lungo la lunghezza del nervo periferico (s) di interesse.
Educazione
del paziente
I pazienti ed i membri a
rischio della famiglia dovrebbero essere resi consapevoli dei sintomi
specifici, come tinnito, deficit dell'udito, debolezza focale, cambiamenti
sensoriali, o problemi di equilibrio, che potrebbe suggerire la crescita del
tumore e deve richiedere l'attenzione medica immediata.
I pazienti con schwannoma
vestibolare devono essere avvertiti circa le immersioni e attività subacquee, a
causa di un aumentato rischio di disorientamento e il potenziale di
annegamento.
I pazienti e le loro
famiglie possono essere attribuiti alla neurofibromatosi (NF)-specifici gruppi
regionali e nazionali di sostegno per continui aggiornamenti sui progressi nel
trattamento, nonché per il sostegno emotivo. Neurofibromatosi, Inc., per
esempio, può essere raggiunto al numero verde 1-800-942-6825.
La NF2 Review, che si
trova a Los Angeles, CA, può essere raggiunto a 1-213-483-4431 e non solo ha un
bollettino specifico NF2, ma ha anche un particolare interesse di ricerca in
NF2, con un team di specialisti che lavorano su uditiva Tronco cerebrale
impianti (Abis) e le più recenti approcci chirurgici per schwannoma
vestibolare.
Risorse online includono
il sito
Web NIH e
di un gruppo di sostegno NF2 da persona a persona conosciuta come l' equipaggio NF2 .
Approccio
dell Dr. Hain's.
Si suggerisce ai potenziali candidati per un
intervento chirurgico in primo luogo considerare la sicurezza e la probabilità
di complicazioni quando si deve prendere in considerazione la chirurgia o
gamma knife. Se uno ha un udito utilizzabile , e
non c'è altro pericolo di aspettare (come ad esempio se necessitano di una
operazione più importante ), si potrebbe ragionevolmente semplicemente
aspettare fino a che la funzionalità uditiva diventi inutilizzabile, prima di
procedere con la chirurgia o radioterapia. In questi casi la procedura
dovrebbe essere : controlli periodici della funzionalità
uditiva e meno frequentemente RM . La frequenza delle prove è
determinato principalmente dal tasso di variazione nelle misure, ma circa ogni
6 mesi per l'esame audiometrico e circa una volta / anno per l'esame MRI e di
solito una frequenza appropriata
Sia un intervento chirurgico che e gamma-knife sembrano
dei metodi ragionevoli per la gestione dei tumori acustica , la scelta
dipende da fattori individuali. La gestione chirurgica ha il vantaggio che si
"ottengono dei risultati con rapidità ". La gamma knife è meno
stressante all'inizio , ma può ritardare la risoluzione delle vertigini.
Riabilitazione
Vestibolare
Nella maggior parte dei
casi, i risultati della chirurgia del neuroma acustico comportano una perdita
completa della funzione vestibolare sul lato operato. La Gamma knife inoltre è
associato ad una diminuzione sostanziale della funzione vestibolare (Wackym,
2004). A seconda della quantità della funzione vestibolare presente prima di
un intervento chirurgico, i pazienti possono avere vertigini o disturbi
dell'equilibrio dopo l'intervento (Levo et al, 2004). La riabilitazione vestibolare può accelerare il
recupero di questo deficit. A meno che non vi sia già una completa perdita
della funzione vestibolare prima dell'intervento chirurgico o delle radiazioni
(come documentato con la ENG), pensiamo che sia meglio che il paziente che
intende sottoporsi ad un'operazione chirurgica per neuroma dell’ acustico
visiti di un fisioterapista vestibolare per assicurarsi che sia in "
buona forma ", e che imparare le procedure di base, e per iniziare un
programma singolo settimanale di PT per 1-2 mesi dopo la dimissione. È
importante che il chirurgo otologo che esegue l'operazione sia coinvolto con la
terapia, in qualche modo (ad esempio nei pazienti con perdita di CSF), in
questi casi la terapia deve essere ritardata.
Popolazioni
speciali e trattamento
Piazza e altri di
recente hanno suggerito che negli anziani, dovrebbe essere seguito il presente
algoritmo: Se il neurinoma acustico protrude meno di un 1 cm i nell'angolo
ponto-cerebellare, una risonanza magnetica dovrebbe essere ripetuta entro in un
anno. Se il tasso di crescita è <2 mm / anno, il paziente deve essere
osservato. Se la velocità è superiore superiore
, bisognerebbe proporre la chirurgia .
Secondo Piazza, per i
tumori che> sporgono 1 centimetro nel’ angolo PC (ponto-cerebellare), ai
pazienti in buona salute generale, dovrebbe essere proposto un intervento
chirurgico. Nei pazienti in cattive condizioni di salute generale, dovrebbe
essere proposta la radiochirurgia (Piazza et al, 2003)
Complicanze
della Chirurgia
Il
trattamento chirurgico, di per sé, ha un rischio notevole. Nel complesso, il rischio di
morte dovuto ad un intervento chirurgico di neuroma
acustico è di circa 0,5 al 2 per cento. Complicanze post-operatorio Impreviste
si verifica in circa il 20 per cento , ancora più complicazioni si verificano
nei soggetti anziani e infermi e quelli con tumori di grandi dimensioni (Kaylie
et al, 2001). Complicazioni, ordinato da rare a frequenti, sono elencati.
• Stroke (raro)
• Lesioni
al cervelletto, ponte o del lobo temporale (rare)
• morte (all in circa 0,5
per cento al 2%, a seconda del centro)
• perdita di CSF (5-15 per
cento di tutti i pazienti)
• Meningite (2-10 per
cento)
• Debolezza facciale
(incidenza dal 4 al 15 per cento di paralisi totale). Le dimensioni del tumore
è un grande fattore di rischio per questa complicanza.
• rischio di perdita
dell'udito (immediatamente dopo l'intervento chirurgico)
•Translabirintica - 100%
•retrosigmoidea - 60%
• Fossa cranica Media --40%. L'udito occasionalmente
migliora con l'approccio attraverso la fossa media (Stidham e Roberson, 2001).
• Mal di
testa (persistenti nel 10-34 per cento, Ruckenstein et al 1996; Soumekh et al,
1996)
• Squilibrio e vertigini (quasi in tutti i
pazienti che hanno una funzione vestibolare prima dell'intervento, avranno un
peggioramento dell'equilibrio dopo l'intervento chirurgico).
APPROFONDIMENTO DEI RISCHI
E COMPLICAZIONI DELLA CHIRURGIA DEI TUMORI DEL NERVO ACUSTICO
Non
è possibile elencare in modo dettagliato tutte le complicanze che possono
intervenire prima, durante e dopo l’atto chirurgico.
Il
seguente elenco è stato realizzato allo scopo di indicare alcuni dei
principali e più importanti rischi possibili della chirurgia dei
tumori del nervo acustico.
1
- PERDITA DELL’UDITO
Nei
piccoli tumori è talora possibile salvare l’udito rimuovendo il tumore ( vedi
paragrafo sui problemi relativi alla conservazione dell’udito ).
La
maggioranza delle neoplasie sono comunque grandi e l’udito dell’orecchio
interessato viene perso in seguito alla rimozione chirurgica. Il paziente potrà
continuare una vita del tutto normale con un solo orecchio udente.
2
– RUMORE (acufeni)
Nella
maggior parte dei casi il rumore rimane inalterato, come prima dell’intervento.
Nel 10% dei casi dopo l’intervento può essere più intenso, in alcuni casi (
20-30 % circa ) il rumore può anche scomparire.
3
- DISTURBI DEL GUSTO E SECCHEZZA DELLA BOCCA
I
disturbi del gusto e la secchezza della bocca sono comuni, per alcune
settimane, dopo l’intervento. Nel 5% dei pazienti questi disturbi possono
durare più a lungo.
4
- VERTIGINE E DISTURBI DELL’EQUILIBRIO
Nella
chirurgia dei tumori del nervo acustico è necessario anche rimuovere una parte
o tutto il nervo dell’equilibrio. Nella maggior parte dei casi è, inoltre,
necessario rimuovere il labirinto.
Poiché
il nervo dell’equilibrio è spesso danneggiato dal tumore, la sua rimozione
quasi sempre comporta un miglioramento dell’instabilità preoperatoria.
Tuttavia
la vertigine è comune nel post operatorio e può essere anche grave per alcuni
giorni o per qualche settimana. Disequilibrio, o instabilità con il movimento
della testa, possono essere presenti per lungo tempo ( nel 30% dei pazienti ),
fino a che non avviene il compenso da parte degli altri centri dell’equilibrio.
5
- PARALISI DEL NERVO FACCIALE
I
tumori del nervo acustico sono in intimo contatto con il nervo facciale ( nervo
che determina il movimento sia dei muscoli deputati alla chiusura dell’occhio,
sia quelli che controllano l’espressione del viso ). In seguito
all’asportazione di un tumore del nervo acustico può verificarsi una paralisi
temporanea dell’emiviso interessato, ciò comporta un’asimmetria del volto con
impossibilità a chiudere l’occhio.
La
paralisi del nervo facciale può essere la conseguenza di un edema, di una
lesione diretta del nervo o di una compromissione della vascolarizzazione .
Solo
tramite un’attenta chirurgia con l’ausilio del microscopio e del
monitoraggio intraoperatorio del nervo facciale è possibile conservare
l’integrità e la funzionalità del nervo. Nonostante ciò, una paralisi
transitoria del facciale può insorgere ugualmente.
Generalmente
il recupero avviene spontaneamente.
Il
recupero della funzionalità facciale, è molto variabile da soggetto a
soggetto; può avvenire nel giro di alcune settimane o di alcuni mesi (fino a
10-12 mesi) e può non essere completa al 100%. Oltre questo termine le
probabilità di recupero sono molto ridotte ed il chirurgo può proporre al
paziente l’esecuzione di un secondo intervento che ha lo scopo di collegare il
nervo facciale all’undicesimo nervo cranico ( anastomosi ipoglosso-facciale )
onde evitare l’atrofia dei muscoli della faccia e permettere la chiusura
dell’occhio.
Nel
5 % dei casi il nervo facciale è completamente avvolto o inglobato dalla massa
tumorale. In casi molto rari il tumore può anche originare direttamente dal
nervo facciale ( neurinoma del nervo facciale). In entrambe queste condizioni,
è necessario interrompere il nervo facciale per poter eseguire l’asportazione
del tumore. In tal caso può essere possibile ricostruire immediatamente
il nervo mediante un trapianto. Se ciò non è possibile, si può effettuare in un
secondo tempo un intervento per collegare il nervo facciale ad un nervo
del collo ( anastomosi ipoglosso-facciale). Debolezza facciale di vario grado , ma la debolezza grave con
i punteggi di House- Brackman V-VI A ad 1 anno si sono verificati nel 6%
(Mass et al, 1998). Wiet e altri hanno recentemente riportato risultati su
500 casi (Wiet et al, 2001).
6
- COMPLICAZIONI OCULARI
La
paralisi del nervo facciale spesso rende l’occhio asciutto e privo di difese.
La consulenza di un oculista può essere indicata. Talora si rende necessario
applicare delle lacrime artificiali, utilizzare un occhialino protettivo e/o un
pesino palpebrale esterno o parziale chiusura chirurgica delle palpebre
per ridurre il rischio di una cheratite o di un’ulcera corneale. Questi
accorgimenti mantengono l’occhio umido evitando così le complicazioni oculari.
7
- DIMINUZIONE DELLA FUNZIONALITÀ DI ALTRI NERVI NEI GRANDI TUMORI
Il tumore del nervo acustico può prendere contatto con i nervi che
controllano i muscoli oculari, della faccia, della bocca e della gola. Questi nervi
possono essere lesi e provocare una visione doppia, intorpidimento della gola,
della faccia e della lingua, debolezza della motilità della spalla, disfonia e
difficoltà alla deglutizione.
Questi
problemi possono rimanere permanentemente. Tale eventualità è però molto rara.
8
- COMPLICAZIONI CEREBRALI E MORTE
I
tumori del nervo acustico sono localizzati vicino ai centri cerebrali vitali
che controllano la respirazione, la pressione sanguigna e la funzionalità
cardiaca. Poiché il tumore ha una crescita progressiva, può venire a contatto
con questi centri cerebrali e può inglobare vasi sanguigni che irrorano queste
aree del cervello. Un’ attenta e scrupolosa dissezione del tumore permette,
generalmente, di evitare tali complicanze. Se l’irrorazione sanguigna di questi
centri cerebrali è compromessa, possono instaurarsi serie complicanze: perdita
del controllo muscolare, paralisi ed anche la morte. Vi è una incidenza complessiva dello 0,5 per cento di
morte a causa di un intervento chirurgico neuroma acustico .Nella
esperienza del gruppo si SANNA, la mortalità peri-operatoria è inferiore all’
1% nei piccoli tumori e medi; tale percentuale aumenta nei tumori grandi o
giganti ( 2-3 % ).
9
- PERDITA POSTOPERATORIA DI LIQUIDO CEREBROSPINALE MENINGITE
La
chirurgia dei tumori del nervo acustico comporta una perdita temporanea di
liquido cerebrospinale ( il liquido che avvolge il cervello ). Per evitare tale
complicanza dopo la rimozione del tumore, la cavità viene riempita con grasso
prelevato dall’addome. Occasionalmente la fuoriuscita di liquido può
presentarsi dopo l’intervento e per farla cessare può essere
necessario reintervenire oppure inserire un drenaggio lombare.
Il
controllo e la risoluzione immediata della fuoriuscita di liquor è determinante
per evitare l’insorgenza di una meningite, che è una temibile infezione del
liquido e del tessuto attorno al cervello. Quando si ha questa complicanza, è
necessaria un’ospedalizzazione prolungata.
E’
spesso indicato inoltre un trattamento con elevati dosaggi di antibiotici. Una recente revisione delle complicazioni dell’
intervento chirurgico ha riscontrato che le complicanze più comuni sono
perdite di CSF (9,4%) e la meningite (1,5%) (Slattery et al, 2001).
10
- EMORRAGIA POSTOPERATORIA ED EDEMA CEREBRALE
Emorragia
ed edema cerebrale possono svilupparsi dopo la chirurgia per tumore del nervo
acustico (1%) . Se accade, può essere necessario un ulteriore intervento,
d’urgenza, per aprire la ferita, bloccare il sanguinamento e permettere al
cervello di riespandersi.
L’emorragia
è una complicazione molto seria, e rappresenta un’urgenza chirurgica per cui il
paziente viene sottoposto a continui monitoraggi in terapia intensiva.
12
- REAZIONI DA TRASFUSIONE DI SANGUE
Raramente
è necessario praticare delle trasfusioni di sangue durante un intervento per
tumore del nervo acustico. Reazioni immediate sono rare. Una complicanza
tardiva della trasfusione è un’ infezione virale del fegato ( epatite); evento
molto raro in quanto la legge obbliga i donatori ad esami specifici prima della
donazione.
il
successo complessivo di conservare l una funzionalità uditiva
era del
27%, i risultati nettamente migliori si sono ottenuti durante
quando il paziente veniva operato attraverso la fossa media .
Anche se non proprio una
complicazione, l'udito all'orecchio operato spesso si deteriora nel tempo
in misura maggiore di quanto l'orecchio non operato, anche in assenza di
recidiva neoplastica (Chee et al. 2003). La percentuale di persone con
"udito utilizzabile" può deteriorarsi del 25% nel tardo
post-operatorio. Questo peggioramento uditivo è stata variamente attribuita:
alla cicatrizzazione, fibrosi, o microemorragie durante l'intervento . Nel
lungo periodo, pochissimi pazienti conservano una funzionalità uditiva utile
(Lin et al, 2005). Alcuni autori hanno suggerito che, dato la modesta
funzionalità uditiva che viene recuperato in pochi pazienti che sono candidati
ad un intervento chirurgico per preservare l'udito risparmiatori di, che la
conservazione dell'udito non si ritiene utile una chirurgia del neuroma
acustico che abbia come ’obiettivo per la conservazione dell'udito (Tos et al,
1988). La nostra opinione è che di tanto in tanto vale la pena tentare, ma le
aspettative devono essere realistiche.
L'equilibrio peggiora dopo l'intervento del neuroma acustico a
causa dei danni chirurgia o per la rimozione del nervo vestibolare (Levo et
al, 2004). A lungo termine (cioè 2 anni), l la funzionalità vestibolare torna
in generale a quasi normale, ma i pazienti che hanno deficit sensoriali i,
come ad esempio disturbi visivi (cataratta ), perdita di sensibilità
(neuropatia ), danni al cervello (ad danni cerebellari o al tronco cerebrale
causati dal tumore o dal’intervento chirurgico), o scarso adattamento (ad
esempio a causa dell'età avanzata) non può mai ottenere la restituzione completa
dell’ equilibrio.
In una recente riunione presso l'ANA (Associazione del neuroma acustico) si è partecipato ad una sessione di 2 ore e intervistato 8
pazienti che avevano vertigini persistenti. Come regola generale, i pazienti
che avevano vertigini 2 anni dopo l'intervento, avevano avuto
contemporaneamente una lesione del cervelletto ed una totale perdita
vestibolare, associata ad un difficile intervento chirurgico (di solito per un
tumore > 4 centimetri). La risonanza magnetica di uno di questi pazienti è
i sotto riportata
|

|
|
Fig.-22
RM di paziente che aveva un neuroma acustico rimosso per mezzo
di approccio retro labirintico e con vertigini refrattarie i. Sul lato destro
della foto (a sinistra della testa), si trova una zona nera dove c'era un
danneggiamento del cervelletto, presumibilmente connessi con la chirurgia.
|
Nella pratica clinica dell'autore a Chicago Illinois , si suggerisce che i potenziali
candidati alla chirurgia operativi considerano prioritaria la sicurezza e la
probabilità di complicazioni quando si considera la chirurgia o Gamma Knife. Se
uno ha un udito utile, e non c'è altro pericolo di attesa (ad esempio,
necessitano di un funzionamento più grande), ci si potrebbe ragionevolmente
attendere fino a quando l’udito diventa inservibile prima di procedere con la
chirurgia o la radioterapia. Ecco la procedura sarebbe: periodici test
dell'udito e le scansioni RM meno frequenti. La frequenza delle prove è
determinata principalmente dal tasso di variazione nelle misure, ma circa ogni
6 mesi test audiometrici e circa una volta l’anno scansione RM sono in genere
appropriati.
Entrambi i metodi di chirurgia e di gamma-knife di gestione tumori acustici
sembrano ragionevoli a questa scrittura, con la scelta dipende da fattori
individuali. Il trattamento chirurgico ha il vantaggio che essa "viene
finita in fretta". Gamma Knife è meno stressante acuto, ma può ritardare
la risoluzione di vertigini.
Riabilitazione vestibolare
Nella
maggior parte dei casi, come risultato della chirurgia del neurinoma dell’acustico
si ha una perdita completa della funzione vestibolare sul lato operato. Anche il
trattamento con Gamma Knife è associato ad un un sostanziale declino della funzione
vestibolare (Wackym, 2004). I pazienti spesso sperimentano vertigini e disequilibrio
post-chirurgico (Levo et al, 2004; Tufarelli et al, 2007). La riabilitazione
vestibolare può accelerare il recupero da questo deficit. A meno che non ci sia
già una perdita completa della funzione vestibolare prima dell’ intervento
chirurgico o della radioterapia (come documentato in ENG ), pensiamo che sia
meglio che il paziente che sta progettando di essere sottoposto ad un
intervento chirurgico di neurinoma dell’acustico consulti un fisioterapista
vestibolare per fare in modo che ci sia una " buon adattamento "e
impari le procedure di base, e per l'individuo di iniziare un programma
settimanale di riabilitazione per 1-2 mesi dopo la dimissione. È importante
che l’otochirurgo che comunque esegue parte della terapia come in alcune
situazioni (ad esempio pazienti con perdita del CSF ), in questi casi la
terapia riabilitativa deve essere ritardata.
Gestione di popolazioni speciali
Piazza e altri recentemente suggeriscono che negli anziani, il seguente
algoritmo dovrebbe essere seguito: Se il neurinoma dell’acustico sporge meno di
1 cm in ponto-cerebellare, una risonanza magnetica deve essere ripetuto in un
anno. Se il tasso di crescita è <2 mm / anno, occorre osservare il paziente.
Se valori maggiori di quelli soprariportati , offerto chirurgia.
Secondo
Piazza, per i tumori che sporgono> 1 cm nel angolo CP, pazienti in buona
salute generale dovrebbero essere offerti chirurgia. Ai pazienti in cattive
condizioni di salute generale, dovrebbero essere offerta la radiochirurgia
(Piazza et al, 2003).
Le complicazioni e le conseguenze di un intervento chirurgico per neurinoma
acustico:
Il trattamento chirurgico, di per sé, ha un rischio sostanziale.
Complessivamente, il rischio di morte dalla chirurgia neuroma acustico è di
circa 0,5 a 2 per cento . Inaspettate complicanze post-operatorie si verificano
in circa il 20 per cento con più complicazioni che si verificano in individui
anziani e infermi e quelli con tumori di grandi dimensioni (Kaylie et al,
2001).
Le complicazioni, ordinate da rare a frequenti, sono sottoelencati.
Corsa (raro)
Lesioni al cervelletto, ponte o lobo temporale (raro oggi (2013), ma più comune
in passato)
Decessi (circa 1/2 per cento al 2%, a seconda del centro)
Perdita di CSF (5-15 per cento di tutti i pazienti)
Meningite (2-10 per cento)
Paralisi del facciale (4 al 15 per cento l'incidenza di paralisi totale). La dimensione
del tumore è un grande fattore di questa complicanza.
Sentendo il rischio di perdita (subito dopo l'intervento chirurgico)
Translabirintica - 100%
Retrosigmoidea - 60%
Fossa media - 40%. La funzionalità uditiva occasionalmente migliora per l'approccio
della fossa media (Stidham e Roberson, 2001).
Mal di testa (persistente nel 10-34 per cento, Ruckenstein et al 1996; Soumekh
et al, 1996)
Disequilibrio e vertigini (quasi tutti i pazienti
che hanno una funzione vestibolare prima dell'intervento, si ha un
peggioramento dell’equilibrio dopo l'intervento chirurgico). Questa non
è una complicazione, ma una conseguenza.
Una
recente revisione delle complicazioni di un intervento chirurgico suggerisce che
le perdite del QCS (9,4%) e la meningite (1,5%) sono le complicanze più comuni
(Slattery et al, 2001).
Lesione cerebellare:
|

|

|
|
Risonanza
magnetica da persona che ha avuto neuroma acustico rimosso tramite approccio
retrolab, e con vertigini refrattario. Sul lato destro della figura (lato
sinistro della testa), c'è una zona nera dove erano presenti danni al
cervelletto, presumibilmente associati alla chirurgia
|
Un'altra
scansione che mostra i danni cerebellare dopo chirurgia neuroma acustico.
Questo tipo di lesione sarà probabilmente accompagnata da squilibrio
permanant grazie alla combinazione di una lesione cerebellare e perdita di
funzione dell'orecchio interno sulla sinistra.
|
|

|

|
|
Tumore
operato nel 1961. Vi è un chiaro danno cerebellare sul lato sinistro del
cervelletto (lato destro della figura).
|
Neuroma
acustico residuo nonché danni cerebellare, in questo paziente che ha avuto un
intervento chirurgico nel remoto passato.
|
In una revisione dei
risultati di 258 pazienti operati con approccio translabirintica, ictus o
lesioni del cervelletto cerebellar injury si sono verificato nel
1,1%. Lesione cerebellare può verificarsi a causa di trazione, nonché a causa
di lesioni alla arteria cerebellare inferiore anteriore (Hegarty et al, 2002).
Immagini di lesione cerebellare da trazione sono sopra riportate . Questi
pazienti hanno generalmente segni oculomotori molto importanti (ad esempio,
nistagmo) e disequilibrio persistente (ad esempio per tutta la vita).
Decessi
Vi
è nel complesso una incidenza dello 0,5 per cento di morte a causa di un
intervento chirurgico per neurinoma dell’acustico. Vi è anche le possibilità di
assistenza per la riabilitazione a lungo termine (1,2%)ed a breve termine
(4,4%) (Barker et al, 2003). Pertanto, vi è più o meno una possibilità dell 1,7%
di morte o di assistenza o cura necessaria a lungo termine dopo l'intervento
chirurgico di neuroma dell’acustico. Le probabilità sono migliori se si sceglie
un ospedale e chirurgo con"alto volume" di interventi.
Altre
complicazioni includono perdita del CSF nel
7,8%, la meningite a 1,6%.
Paralisi
facciale
Paralisi
facciale di vario grado apparso in più, ma una grave paralisi
del facciale, di grado V-VI con la classificazione di House-Brackman ad 1 anno
si è verificato nel 6% (Messa et al, 1998). Wiet e altri hanno recentemente
riportato risultati in 500 casi (Wiet et al, 2001). Successo complessivo a
mantenere una funzionalità uditiva utile è stata del 27%, con risultati
decisamente migliori ottenuti tramite l'approccio della fossa media.
la
conservazione dell’udito con l'intervento chirurgico è di solito solo un pio
desiderio.
l’udito
all'orecchio operato spesso si deteriora nel tempo in misura maggiore dell'orecchio
non operato, anche senza un tumore recidivante
(Chee et al. 2003). La percentuale di persone con "udito funzionale"
potrebbe deteriorarsi del 25% nel periodo post-operatorio . Questo è stato
variamente attribuito a cicatrici, fibrosi, o micro emorragie durante l’operazione.
Nel
lungo termine, pochissimi pazienti conservano un udito utilizzabile
(Lin et al, 2005). Alcuni autori hanno suggerito che, dato la modesta funzione
uditiva che è recuperata in pochissimi pazienti che sono candidati per sentire
con la chirurgia conservativa, la conservazione dell'udito come obiettivo
della chirurgia neuroma acustico non è utile (Tos et al, 1988). La nostra
opinione è che di tanto in tanto la pena di tentare, ma le aspettative di uno
devono essere realistico.
L'equilibrio
generalmente peggiora dopo l'intervento chirurgico neuroma acustico
L'equilibrio
si deteriora dopo l'intervento del neurinoma acustico perché la chirurgia danneggia
o rimuove la rimantenente funzione del nervo vestibolare (Levo et al, 2004;
Tufarelli et al, 2007). Tufarelli e associati hanno riferito che il 10% dei 459
pazienti ha giudicato il loro squilibrio come invalidante, e il 73% ritiene di
avere una oscillopsia moderata (difficoltà a vedere con la testa in movimento)
E
'stata la nostra esperienza che nel lungo periodo (cioè 2 anni), bilancia
ritorna in generale a quasi normale, ma le persone che hanno altri deficit,
come disturbi visivi (ad esempio, cataratta), perdita sensoriale (ad esempio
neuropatia), danni cerebrali (ad es cerebellare o danno cerebrale a causa del
tumore o intervento chirurgico), o scarso adattamento (ad esempio a causa
dell'età avanzata) non possono mai ottenere completo ritorno di equilibrio.
In
una recente riunione presso la ANA (neuroma acustico associazione), l'autore di
questa pagina ha partecipato ad una sessione di 2 ore al giorno e ha
intervistato otto pazienti che hanno avuto vertigini persistente. Come regola
generale, i pazienti che avevano vertigini due anni dopo l'intervento, avevano
avuto una miscela di una lesione cerebellare e perdita totale vestibolare,
associato ad un difficile intervento (di solito per un tumore + 4 centimetri).
La risonanza magnetica di due pazienti sono qui sopra riportati. Come regola
generale, i pazienti che hanno perso sia la funzione dell'orecchio interno (dal
acustico), e la sostanziale funzione cerebellare (da un intervento chirurgico dell’
acustico), avranno una perdita durevole di equilibrio
Immediatamente dopo l'intervento chirurgico, la maggior parte dei
pazienti hanno vertigini. Una discussione
dettagliata di capogiri, vertigini e squilibrio, prima e dopo l'intervento
chirurgico può essere trovato
Mal di testa post-operatorio
Mal di testa significativi
possono verificarsi in seguito ad interventi chirurgici per neurinomi
dell'acustico (revisione Driscoll e Beatty, 1997). L'incidenza varia molto
tra un chirurgo e l'altro e dipende anche dalla scelta dell’approccio
chirurgico, ma effettuando una panoramica della letteratura si è riscontrata
una incidenza di circa il 20-35%. Di fronte di un'incidenza di circa l'8% dopo
radiochirurgia.
Schessel et al (1996) hanno
osservato e documentato i l'aderenza dei muscoli del collo, sulla dura , dopo
craniotomia e segnalato una diminuzione drastica del mal di testa nei pazienti
che avevano craniotomia con la sostituzione del lembo osseo. Allo stesso modo,
Harner anche notato una riduzione del di mal di testa nei pazienti nei quali
avevano avuto una craniotomia in cui era stato utilizzato metacrilato di
metile al posto della sola craniotomia (Harner et al, 1995). Si pensa che Il
meccanismo sia dovuto, alla trazione sulla dura da parte dei movimenti dei
muscoli del collo. Molti pazienti affetti da questa sindrome avevano montato un
aggravamento con la tosse o lo sforzo.
Schessel et al (1996)
affermano che, nei pazienti che avevano avuto un intervento chirurgico per
via retrosigmoidea , la frequenza di mal di testa era significativamente più
elevata rispetto a quelli che avevano avuto un approccio translabirintico.
Molti altri gruppi di ricercatori hanno trovato dei dati simili . Schaller e
Bauman (2003) hanno riscontrato forti mal di testa che richiedono farmaci
giornalmente, accompagnati da una sensazione di incapacità nel 34% dei
pazienti dopo 3 mesi dall'intervento per via retrosigmoidea. Essi hanno
scoperto che questi mal di testa sono stati associati con meningite asettica e,
inoltre, che sono associati all'utilizzo di colla di fibrina e di perforazione
in faccia posteriore del condotto uditivo interno. Hanno suggerito che la
prevenzione del mal di testa post-operatoria può essere realizzata mediante la
sostituzione del lembo osseo, alla fine di un intervento chirurgico, l'uso di
duraplastic invece di diretta chiusura durale, ed evitare l'uso di colla di
fibrina o di perforazione estesa della faccia posteriore del condotto uditivo
interno.
Hanno suggerito che la
prevenzione del mal di testa post-operatorio può essere realizzata mediante la
sostituzione del lembo osseo, alla fine di un intervento chirurgico,
utilizzando duraplastica invece della chiusura diretta con la dura ed
evitando l'uso di colla di fibrina o di una perforazione estesa della faccia
posteriore del condotto uditivo interno
Attualmente ci sono poche informazioni circa l'incidenza di mal
di testa utilizzando il metodo della fossa, ma i pochi dati disponibili
indicano una incidenza piuttosto bassa (Driscoll et al, 1997).
Nella gestione della cefalea post operatoria si utilizzano analgesici,
miorilassanti, antidepressivi e anticonvulsivanti, in modo simile alla gestione dell'emicrania . I farmaci per l'emicrania e comunque, e I farmaci specifici
profilattici per l'emicrania non sono raccomandati nella maggior parte dei
casi. Tuttavia, un recente rapporto ha rilevato che sumatriptan (un farmaco per
l’ emicrania), migliora il mal di testa in 9 / 10 pazienti che avevano una
cefalea post-chirurgica. Ciò riflette probabilmente il fatto che , l'emicrania
è una condizione molto comune per la salute, che peggiora con qualsiasi tipo di
mal di testa.
Un dolore persistente , da incisione, si può verificare per
L’intrappolamento del nervo occipitale o dalla formazione di un neuroma
occipitale. I massaggi, il calore locale, e gli analgesici possono aiutare.
Blocchi del nervo occipitale (come avviene nella clinica del dolore) possono
anche essere utile.
Un altro meccanismo che è stato suggerito è che, la polvere ossea,
intrappolata all'interno della cavità intracranica possa causare una risposta
infiammatoria protratta con conseguente mal di testa cronici (Driscoll, 1997).
Le immagini di RM talvolta mostrano un accrescimento della dura (la membrana
che ricopre il cervello "sale sopra") e le immagini TC possono
mostrare calcificazioni lungo il tronco cerebrale (Schaller e Bauman, 2003).
Questo tipo di mal di testa non dovrebbe rispondere al blocco dei nervi del
cuoio capelluto (come avviene nella clinica del dolore), e tale procedura può
essere di qualche utilità diagnostica. In questi pazienti, logicamente, il
trattamento potrebbe includere gli agenti anti-infiammatori ed eventualmente
corticosteroidi. Analgesici narcotici sono talvolta indicati..
RM
Post-operatoria
Non esistono norme in materia di follow-up del paziente
dopo resezione completa del neuroma acustico. In media, però, 3-6 scansioni
sono comuni è comune nel corso di un follow-up di circa 5 anni. (Lee e Isaacson,
2005).
Impianti Cocleari
Molto raramente, una persona con un neuroma
acustico potrebbe desiderare un impianto cocleare. Ciò potrebbe verificarsi se
un tumore acustico è presente nel solo orecchio funzionante o dopo una
chirurgia che abbia rimosso un neurinoma acustico bilateralmente. Belal (2001)
ha riferito che l'impianto cocleare è possibile solo se vi è un nervo cocleare
intatto (come mostrato da una risposta positiva alla stimolazione promontorio),
e se l'impianto è fatto al momento della rimozione del tumore acustico, prima
della ossificazione della coclea. .
Links:
·
Acoustic Neuroma
Association
·
Support
Groups (Acoustic Neuroma Association)
·
Presentation by Dr.
Hain at ANA association meeting 2009 on balance issues pre and post surgery
·Acoustic
Neuroma. NIH Consensus Statement Online 1991 Dec 11-13 ;9(4):1-24
· Anderson, T. D., L.
A. Loevner, et al. (2000). "Prevalence of unsuspected acoustic neuroma
found by magnetic resonance imaging." Otolaryngol Head Neck Surg 122(5):
643-646.
· Asthagiri AR, Vasquez
RA, Butman JA, Wu T, Morgan K, Brewer CC, King K, Zalewski C, Kim HJ, Lonser
RR.PLoS One. Mechanisms of hearing loss in neurofibromatosis type 2.
2012;7(9):e46132. doi: 10.1371/journal.pone.0046132. Epub 2012 Sep 26.
· Baker R, Stevens-King
A, Bhat N and Leong P (2003). "Should patients with asymmetrical
noise-induced hearing loss be screened for vestibular schwannomas?" Clin
Otolaryngol 28(4): 346-51.
· Barker FG, 2nd,
Carter BS, Ojemann RG, Jyung RW, Poe DS and McKenna MJ (2003). "Surgical
excision of acoustic neuroma: patient outcome and provider caseload."
Laryngoscope 113(8): 1332-43.
· Belal A. Is cochlear
implantation possible after acoustic tumor removal ? Otol Neurotol 22:497-500,
2001.
· Brors D, Schafers M,
Bodmer D, Draf W, Kahle G, Schick B. Postoperative magnetic resonance imaging
findings after transtemporal and translabyrinthine vestibular schwannoma
resection. Laryngoscope 2003 Mar;113(3):420-6
· Chee GH, Nedzelski JM
and Rowed D (2003). "Acoustic Neuroma Surgery: The Results of Long-term
Hearing Preservation." Otol Neurotol 24(4): 672-6.
· Driscoll CLW, Beatty
CW. Pain after acoustic neuroma surgery. Otolaryngologic clinics of North
America, vol 30, #5, 1997, 893-903
· Daniels and others.
Causes of unilateral sensorineural hearing loss screened by high-resolution
fast spin echo magnetic resonance imaging: review of 1070 consecutive cases.
Am. J. otol 21:173-180, 2000
· Evans, D. G., A.
Moran, et al. (2005). "Incidence of vestibular schwannoma and
neurofibromatosis 2 in the North West of England over a 10-year period: higher
incidence than previously thought." Otol Neurotol26(1): 93-7.
· Falcioni M, Taibah A,
Di Trapani G, Khrais T, Sanna M. Inner ear extension of vestibular schwannomas.
Laryngoscope. 2003 Sep;113(9):1605-8.
· Haggard M, Gatehouse
S, Davis A. The high prevalence of hearing disorders and its implications for
services in the UK. Brit J. Audiol 1981;15:241-51
· Harner SG, Beatty CW,
Ebersold MJ. Headache after acoustic neuroma excision. Am J. Otolaryngol
14:552, 1993
· Hegarty JL. Distal
anterior inferior cerebellar artery syndrome after acoustic neuroma surgery.
Otol Neurotol 23:560-571, 2002
· Hoistad DL and
others. Update on conservative management of acoustic neuroma. Otol Neurotol
22:682-685, 2001
· House JW, Bassim MK,
Schwartz M. false-positive magnetic resonance imaging in the diagnosis of
vestibular schwannoma. Otology and Neurotology 29:1176-1178, 2008
· Hulshof JH, Hilders
CGJM, Barrsma EA. Vestibular investigations in acoustic neuroma. Acta
Otolaryngol (stockh) 198, 108; 38-44
· Tanbouzi Husseini S,
Piccirillo E, Taibah A, Paties CT, Rizzoli R, Sanna M Malignancy in vestibular
schwannoma after stereotactic radiotherapy: A case report and review of the
literature. .Laryngoscope. 2011 May;121(5):923-8. doi: 10.1002/lary.21448.
· Jackler RF. Acoustic
Neuroma (chapter 21) in Neurotology (Eds Jackler and Brackman, Mosby, 1994).
· Jackler RF.
Diagnosing Acoustic Neuromas. Audio-Digest Otolaryngology 33, 04, Feb 21, 2000
· Jackler RF. Acoustic
neuromas: selective management Audio Digest Otolaryngology, April 7, 2007.
· Kaplan DM, Hehar SS,
Tator C, Guha A, Laperriere N, Bance M, Rutka JA. Hearing loss in acoustic
neuromas following stereotactic radiotherapy..J Otolaryngol. 2003
Feb;32(1):23-32.
· Kaylie and others.
Acoustic neuroma surgery outcomes. Otol Neurotol 22:686-689, 2001
· Kennedy RJ and
others. Intralabyrinthine schwannomas" diagnosis, management, and a new
classification system. Otol Neurotol 25:166-167, 2004.
· Komatsuzaki A,
Tsunoda A. Nerve origin of the acoustic neuroma. J Laryngol Otol 2001
May;115(5):376-9
· Khrais T, Romano G,
Sanna MJ . Nerve origin of vestibular schwannoma: a prospective study..Laryngol
Otol. 2007 Nov 27;
· Lee, W. J. and J. E.
Isaacson (2005). "Postoperative imaging and follow-up of vestibular
schwannomas." Otol Neurotol26(1): 102-4.
· Levo H, Blomstedt G,
Hirvonen T, Pyykko I I. Causes of persistent postoperative headache after
surgery for vestibular schwannoma. Clin Otolaryngol 2001; 26: 401-406.
· Levo H, Blomstedt G,
Pyykko I. Postural stability after vestibular schwannoma surgery. Ann Otol
Rhinol Laryngol 2004;113:994-9.
· LIMB CJ, Long DM,
Niparko JK. Acoustic Neuromas after Failed Radiation Therapy: Challenges of
Surgical Salvage. Laryngoscope 2005;115:93-98.
· Lin VY, Stewart C,
Grebenyuk J, Tsao M, Rowed D, Chen J, Nedzelski J. Laryngoscope. Unilateral
Acoustic Neuromas: Long-Term Hearing Results in Patients Managed with
Fractionated Stereotactic Radiotherapy, Hearing Preservation Surgery, and
Expectantly.2005 Feb;115(2):292-296.
· Lin, D., J. L.
Hegarty, et al. (2005). "The prevalence of "incidental" acoustic
neuroma." Arch Otolaryngol Head Neck Surg 131(3): 241-244.
· Markou K, Eimer S,
Perret C, Huchet A, Goudakos J, Liguoro D, Franco-Vidal V, Maire JP, Darrouzet
VUnique case of malignant transformation of a vestibular schwannoma after
fractionated radiotherapy. .Am J Otolaryngol. 2011 Jun 20.
· Mass S, Wiet RJ,
Dinces E. Complications of the translabyrinthine approach for removal of
acoustic neuromas. Arch Otolaryngol HNS 1999:125:801-804
· Massuda A and others.
Hearing changes after diagnosis in neurofibromatosis type 2. Otol Neurotol
25:150-154, 2004
· Mayo clinical update.
Volume 14, #2, 1998.
· Morrison GA, Sterkers
JM. Unusual presentations of acoustic tumors. Clin Otolaryngol 1996, 21(1)
80-3.
· Muscat JE and others.
Handheld cellular phones and risk of acoustic neuroma. Neurology
2002:58:1304-06
· Nageris BI, Popovtzer
A. Acoustic neuroma in patients with completely resolved sudden hearing loss.
Ann Otol Rhinol Laryngol 2003 May;112(5):395-7
· Neff B, Willcox T,
Sataloff R. Intralabyrinthine schwannomas. Otol Neurotol 24: 299-307, 2003
· Nikolopoulos TP,
O'Donoghue Gm. Acoustic neuroma management: an evidence-based medicine
approach. Otol Neurotol 23:534-41, 2002
· Noren G and others.
Gamma knife surgery in acoustic neuroma. Acta Neurochirg Suppl 1993:58:104-7
· Perry BP, Gantz BJ,
Rubinstein JT. Acoustic neuromas in the elderly. Otol Neurotol 22: 389-391,
2001
· Piazza F and others.
Management of acoustic neuromas in the elderly: Retrospective study. ENT
journal, May 2003, 374-378
· Pollock BE, Lunsford
LD, et al. Outcome analysis of acoustic neuroma management: a comparison of
microsurgery and stereotactic radiosurgery. Neurosurgery 1995:36:215-229.
· Pothula VB, Lesser T,
Mallucci C, May P, Foy P. Vestibular schwannomas in children. Otol Neurotol
22:903-907, 2001
· Ruckenstein MJ, and
others. Pain subsequent to resection of acoustic neuromas via suboccipital and
translabyrinthine approaches. Am J. Otology 17:620-624, 1996
· Sanna M and others.
Treatment of residual vestibular schwannoma. Otol Neurotol 23:980-987, 2002
· Schaller B, Baumann A
Headache after removal of vestibular schwannoma via the retrosigmoid approach:
A long-term follow-up-study. Otolaryngol Head Neck Surg 2003 Mar;128(3):387-95
· Schessel DA,
Nedzelski JM, Rowed D, et al. Pain subsequent to resection of acoustic neuromas
via suboccipital and translabyrinthine approaches. Am J Otol 17:620, 1996
· Shin YJ et al.
Effectiveness of conservative management of acoustic neuromas. AM J. Otol
21:857-862, 2000
· Slattery WH, Francis
S, House KC. Perioperative mortality of acoustic neuroma surgery. Otol Neurotol
22:895-902, 2001
· Soumekh B, Levine S,
Haines SJ, Wulf J. Retrospective study of postcraniotomy headaches in
suboccipital approach: diagnosis and management. Am J. Otology 1996:17:617-619
· Stewart, T. J., J.
Liland, et al. (1975). "Occult schwannomas of the vestibular nerve."
Arch Otolaryngol 101(2): 91-95.
· Stidham KR, Robserson
JB. Hearing improvement after middle fossa resection of vestibular schwannoma.
Otol Neurotol 22:917-921, 2001
· Tos M, Thomsen J,
Harmsen A. Is preservation of hearing in acoustic neuroma worthwhile ? Acta
Otolarygol (Stockh) 1988: 452: 57-68
· Tufarelli D, Meli A, Labini FS,
Badaracco C, De Angelis E, Alesii A, Falcioni M, Sanna M. Balance impairment
after acoustic neuroma surgery. Otol Neurotol. 2007
Sep;28(6):814-21.
· UNGER F, Dominikus K,
Haselsberger K. [Stereotactic radiosurgery and fractionated stereotactic
radiotherapy of acoustic neuromas.] HNO. 2010.
· Wackym PA and others.
Gamma knife radiosurgery for acoustic neuromas performed by a neurotologist:
early experiences and outcomes. Otol Neurotol 25:752-761, 2004
· Warrick P, Bance M,
Rutka J. The risk of hearing loss in nongrowing, conservatively managed
acoustic neuromas. Am J Otol 20:758-762,
·
Wiet RJ, Mamikoglu B, Odom L, Hoistad DL. Long-term results of the first 500
cases of acoustic neuroma surgery. Otolaryngol Head Neck Surg 2001; 124:
645-51. (Comment: Note that Dr. Wiet sees patients in the same location
as Dr. Hain, the author of this review)
BIBLIOGRAFIA
NEURINOMI: Gruppo Otologico Sanna
1)
Diagnosi radiologica del neurinoma dell'acustico intracanalare: la
cisternografia opaca è ancora giustificata? (in coll. con P. Bassi, C. Zini, G.
Jemmi) Atti 69° Congr. Soc. Ital. O.R.L., Roma 19-23 Maggio 1982.
2)
Hearing preservation in acoustic neuroma surgery: middle fossa versus sub
occipital approach. (in coll. con C. Zini, A. Mazzoni, A. Gandolfi, R.
Pareschi, E. Pasanisi, R. Gamoletti) Am. J. Otol. 8, 500-506, 1987.
3)
Hearing preservation in acoustic neuroma surgery: middle fossa vs. sub
occipital approach. (in coll. con C. Zini, A. Mazzoni, A.
Gandolfi, R. Pareschi, R. Pasanisi, R. Gamoletti) Clinical Audiology 87.
4)
Management of facial nerve in acoustic tumors surgery. (in
coll. con A. Gandolfi, A. Mazzoni, C. Zini, E. Pasanisi) Atti International
Conference on: Controversies in Otology and Otoneurosurgery, 31 agosto 6
settembre 1986, Alghero
5)
Facial nerve and acoustic neuroma. (in coll. con C. Zini, A.
Mazzoni, A. Gandolfi, E. Pasanisi, R. Pareschi) In: Neurinomes de L'Acoustique
- Acquisitions et Controverses, 71-80, 1988. Ed
Medicales Pierre Fabre.
6) The clinical diagnosis of acoustic neuromas. (in coll. con A. Gandolfi, C.
Zini, F. Piazza) Neurological Surgery of the ear and skull base. Kugler
and Ghedini Pubb. Amsterdam, l55-159, 1989133) Atypical presentation of
acoustic neuroma. (In coll. con L. Vassalli, M. Landolfi. A.K. Taibah, A.
Russo, E.Pasanisi, M. Shaan) Acoustic Neuroma, 1992 Proceedings of the First
International Conference - Copenhagen, Denmark, August 25-29, 1991 Kugler and
Ghedini Pub., Amsterdam, 23-30, 1992.
7)
Hearing preservation: a criticai review of the literature. (in coll. con C.
Zini, R. Gamoletti, M. Landolfi, M. Shaan, F. Piazza) Acoustic Neuroma,
1992
Proceedings of the First International Conference Copenhagen, Denmark, August
25-29, 1991 Kugler and Ghedini Pub., Amsterdam, 631-638, 1992
8)
Growth rate of acousdc neuromas. (in coll. con A.K. Taibah, M.Landolfi, L.
Vassalli, A. Russo, E. Pasanisi, M. Shaan)Acoustic Neuroma, 1992 Proceedings of
the First International Conference Copenhagen, Denmark, August 25-29, 1991
Kugler and Ghedini Pub., Amsterdam, 183-186, 1992.
9)
Preservation of the facial nerve in acoustic neuroma Surgery via the
translabyrinthine approach. (in coll. con A.K. Taibah, M. Landolfi, L.
Vassalli, A. Russo, E. Pasanisi, M. Shaan) Acoustic Neuroma, 1992 Proceedings
of the First International Conference Copenhagen, Denmark, August 25-29, 1991
Kugger and Ghedini Pub., Amsterdam, 389-390, 1992.
10)
Translabyrinthine removal of an acoustic neuroma in a contracted
mastoid. Acoustic Neuroma, 1992 Proceedings of the First International
Conference Copenhagen, Denmark, August 25-29,1991 Kugler and Ghedini Pub.,
Amsterdam, 391-392,1992.
11)
Translabyrinthine removal of a very large acoustic neuroma. (in
coll. con A. Russo, A.K. Taibah, M. Landolfi, L. Vassalli, E. Pasanisi, G.
Chelmis)
Acoustic
Neuroma,1992 Proceedings of the First Internadonal Conference Copenhagen,
Denmark, August 25-29,1991 Kugler and Ghedini, Amsterdam, 393-395, 1992.
12)
Acoustic neuroma removal through enlarged middle fossa.
(in coll. con A.K Taibah, M. Landolfi, L. Vassalli, E. Pasanisi, M.
Shaan)
Acoustic Neuroma, 1992 Proceedings of the First International
Conference Copenhagen, Denmark, August 25-29, 1991 Kugler and Ghedini
Pub., Amsterdam, 495-496, 1992
13)
The pors and cons of the translabyrinthine, middle cranial fossa and
retrosigmoid approaches in the of acoustic neuromas. (in coll. con C. Zini, A.
Gandolfi, F. Piazza) Acoustic Neuroma, 1992 Proceedings of the First
International Conference Copenhagen, Denmark, August 25-29, 1991 Kugler
and Ghedini Pub., Amsterdam, 499-500, 1992
14)
The problem of facial nerve anatomical and functional preservation in relation
to different approaches(in coll. con F. Piazza, C. Zini, C.
Iagher) Acoustic Neuroma, 1992 Proceedings of the First International
Conference Copenhagen, Denmark, August 25-29, 1991 Kugler and Ghedini
Pub., Amsterdam, 767-770, 1992
15)
Rerouting and end-to-end anastomosis of the facial nerve in translabyrinthine
removal of acoustic neuromas. (in coll. con L. Vassalli, A.K. Taibah, M.
Landolfi, A. Russo, E. Pasanisi, G. Chelmis) Acoustic Neuroma, 1992 Proceedings
of the First International Conference Copenhagen, Denmark, August
25-29, 1991 Kugler and Ghedini Pub., Amsterdam, 775-776, 1992
16)
Removal of a meningioma of the cerebellopontine angle via the extended
translabyrinthine approach. (in coll. con M. Landolfi, L. Vassalli, A.K.
Taibah, A. Russo, E. Pasanisi, G. Chelmis) Acoustic Neuroma, 1992 Proceedings
of the First International Conference Copenhagen, Denmark, August 25-29,1991
Kugler and Ghedini Pub., Amsterdam, 965-968,1992
17)
Synopsis on: Hearing preservation following acoustic neuroma surgery. (in
coll. con R. Gamoletti, M. Tos, J. Thomsen) Acoustic Neuroma, 1992 Proceedings
of the First International Conference Copenhagen, Denmark, August 25-29,
1991 Kugler and Ghedini Pub., Amsterdam, 965-968, 1992
18)
Atypical preservation of acoustic neuroma(in coll. con M. Shaan, L. Vassalli,
M. Landolfi, A. Taibah, A. Russo) Otolaryngol. Head Neck Surg., 109,
865-870, 1993.159) Decision making in acoustic neuroma management: the only
hearing ear. (in coll. con M. Naguib, E. Saleh, M. Aristegui,
A. Mazzoni) Skull Base Surgery 4, 1, 43-47, 1994.
19)
Management of the high jugular bulb in the translabyrinthine approach.(in coll.
con E. Saleh, M. Aristegui, A. Taibah, A. Mazzoni) Otolaryng. Head Neck Surg.
110, 397-399, 1994.
20)
The enlarged translabyrinthine approach for removal of large vestibular
schwannomas. (in coll. con M. Naguib, E. Saleh, Y. Cokkeser, M.
Aristegui, M. Landolfi, A. Taibah, A. Mazzoni) Journ. Laryng. Otol. 108,
545-550,1994.
21)
Via della fossa cranica media allargata: una analisi morfometrica. (in coll.
con M. Landolfi, M. Aristegui, A. Taibah, A. Russo, E. Saleh) Acta
Otorhinol. Ital. 14, 127-134,1994
22)
Management of the high jugular bulb in the translabyrinthine approach. (in
coll. con E. Saleh, M. Aristegui, A. Taibah, A. Mazzoni) Otolaryngol.
Head Neck Surg. 110, 397- 399, 1994.
195)
Incidenza della normacusia nel neurinoma dell'acustico. (in coll. con G. De
Donato, A. Russo, E. Saleh) Acta Otorhinol. Ital.
15, 1995.
23)
Measurement of endocochlear DC potentials in ears with acoustic neuromas: a
preliminary report. (In coll. con T. Kobayashi, A. Aslan, T. Chiba, T.
Takasaka)Acta Otolaryngol. (Stockh) 116, 791-795,1996.
24)
Vestibular schwannoma and the only hearing ear. (In coll. con S. Bhatia, S.
Karmarkar, A. Taibah, A. Russo) The Journal of Laryng. and Otol. 110,
366-369,1996.
25)
Hearing preservation following the enlarged middle fossa approach for
vestibular schwannoma removal. (In coll. con A. Russo, S. Karmarkar, E. Saleh,
A. Taibah, F. Mancini) Acoustic Neuroma and Skull Base Surgery, pp.
241-249 Proceedings of the 2nd International Conference on Acousdc Neuroma
Surgery and 2nd European Skull Base Society Congress, Paris, France, April
22-26, 1995. Edited by J. M. Sterkers, R. Charachon and 0. Sterkers1996
Kugler Publications, Amsterdam/New York
26)
Management of acoustic neuroma through the enlarged translabyrinthine approach.
How can we improve the results ? (In coll. con F. Mancini, M. Falcioni, M.
Landolfi, A. Taibah, A. Russo, A. Mazzoni) Acoustic Neuroma and Skull Base
Surgery, pp. 185-193Proceedings of the 2nd International Conference on Acoustic
Neuroma Surgery and 2nd European Skull Base Society Congress, Paris, France,
April 22-26,1995. Edited by J. M. Sterkers, R. Charachon and O. Sterkers
1996 Kugler Publications, AmsterdanvNew
27)
Normal hearing in acoustic neuroma. (In coll. con M. Falcioni, G. De
Donato, E. Saleh, A. Taibah, A. Russo) Acoustic Neuroma and Skull Base
Surgery, pp. 83-86.Proceedings of the 2nd International Conference on Acoustic
Neuroma Surgery and 2nd European Skull Base Society Congress, Paris, France,
April 22-26, 1995.
Edited by J. M. Sterkers, R. Charachon and O. Sterkers
1996 Kugler Publications, Amsterdam/New York
28)
Normal hearing in acoustic neuroma patients: a critical evaluation. (In coll.
con E. Saleh, M. Aristegui, M. Naguib, Y. Cokesser, M. Landolfi)
The American Journal of Otology 17, 127-132,1996.
29)
La liquorrea come complicanza della via translabirintica nel trattamento del
neurinoma dell'acustico. (In coll. con Falcioni M., Taibah A., De Donato G.,
Sanna M.) Acta Otorhinolaryngol. Ital. 18, 63-69,1998
30)
Coesistenza di un neurinoma dell'acustico e di un tumore glomico timpanico.
(in coll. con Falcioni M,Caruso A,) Acta Otorhinol. Ital. 18; 398-401,
1998
31)
Identificazione del nervo facciale nella via translabirintica: un metodo
alternativo. (in coll. con Falcioni M, De Donato G, Piccirillo E, Taibah A,
Russo A, Mancini F, Caruso A, Piccirillo E.) Acta Otorhinol. Ital. 19; 1-5,
1999
32)
Transpetrous removal of residual vestibular schwannoma.
(in coll. con Falcioni M, Taibah A, De Donato G, Russo A, Mancini F, Piccirillo
E, Amico Giuseppe.) Third International Conference on
Acoustic Neurinoma and Other C.P.A. Tumors. Rome, 12 to 17 June 1999, CIC
international editions.
33)
Translabyrinthine vs retrosigmoid approach for small tumors.(in coll. con
Bacciu A, Bruzzo M, Falcioni M, Chays A, Magnan J.)
Third International Conference on Acoustic Neurinoma and Other C.P.A. Tumors.
Rome, 12 to 17 June 1999, CIC international editions.
34)
Technical refinements in translabyrinthine approach for acoustic tumor removal.
(in
coll con Aristegui M, Falcioni M, De Donato G, Taibah A, Russo A, Mancini F.) Third
International Conference on Acoustic Neurinoma and Other C.P.A. Tumors. Rome,
12 to 17 June 1999, CIC international editions.
35)
Facial nerve in translabyrinthine approach: an alternative technique.
(in
coll. con Russo A, Taibah A, Mancini F, Falcioni M, De Donato G, Piccirillo E.)
Third Intemational Conference on Acoustic Neurinoma and
Other C.P.A.
Tumors.
Rome, 12 to 17 June 1999, CIC edizioni internazionali.
36) Is the modified translabyrinthine approach suitable for large and giant
acoustic tumors?(in coll. con Mancini F, Taibah A, Russo A, Falcioni M,
De Donato G, Piccirillo E, Piccioni L.) Third Intemational Conference on
Acoustic Neurinoma and Other C.P.A. Tumors. Rome, 12 to 17 June 1999, CIC
intemational editions.
37)
Complications in translabyrinthine approach. (in coll. con De
Donato G, Taibah A, Russo A, Mancini F, Falcioni M, Piccirillo E.)
Third Intemational Conference on Acoustic Neurinoma and
Other C.P.A. Tumors. Rome, 12 to 17 June 1999, CIC intemational editions.
38)
Hospital stay in CPA surgery. (in coll. con Piccioni L, Taibah A,
Mancini F, Falcioni M, De Donato G, Piccirillo E.) Third
Intemational Conference on Acoustic Neurinoma and Other C.P.A. Tumors. Rome, 12
to 17 June 1999, CIC intemational editions.
39)
Decision making in acoustic neuroma of only hearing ear.
(in
coll. con Caruso A, Taibah A, Russo A, Mancini F, Falcioni M, De Donato G,
Piccirillo E.) Third International Conference on
Acoustic Neurinoma and Other C.P.A. Tumors. Rome, 12 to 17 June 1999, CIC
international editions.
40)
Normal hearing and sudden hearing loss in acoustic neurinoma.
(in coll. con Piccioni L, Taibah A, Russo A, Mancini F, Falcioni M, De Donato
G, Amico G.)Third International Conference on Acoustic Neurinoma and Other
C.P.A. Tumors. Rome, 12 to 17 June 1999, CIC international editions.
41)
Intraoperative facial nerve monitoring: personal experience and considerations.
(in
coll. con Piccirillo E, Nakao Y, Burdo A, Taibah A, Falcioni M, Mancini F.) Third
International Conference on Acoustic Neurinoma and Other C.P.A. Tumors. Rome,
12 to 17 June 1999, CIC international editions.
42)
Il trattamento dei neurinomi dell'acustico residui. (in coll. con Falcioni M,
Piccioni L, Taibah A, De Donato G, Russo A, Piccirillo E.) Acta
Otorhinol. Ital. 20; 151-8; 2000.
43)
Hearing preservation in vestibular schwannoma surgery: fact or fantasy.Grading
Systems for pre-and post-operative hearing session III Nov. 7, Wed. 15:35. The
kejo Journal of medicine – Volume 50 supplement 4 – October 2001
44)
Fast growing vestibular schwannoma. (in coll. con Falcioni M,
Taibah A, De Donato G, Piccirillo E, Russo A.) Skull
Base Surgery 10; 95-99, 2000.
45)
Arachnoid cysts of the petrous apex in a patient with vestibular schwannoma.(in
coll. con Falcioni M, Caruso A, Taibah A, De Donato G, Piccirillo E, Russo A.) Otolaryngol.
Head Neck Surg. 123, 657-60, 2000.
46)
Electromyographic evaluation of facial nerve damage in acoustic neuroma
surgery. (in coll. con Nakao Y, Piccirillo E, Falcioni M, Taibah
A, Kobayashi T.) Otol. & Neurotol. 22, 554-557, 2001.
47)
La via translabirintica allargata nei neurinomi dell'acustico di grandi
dimensioni. (in coll. con Falcioni M, Russo A, Mancini F, Taibah A, Piccioni L,
De Donato G, Caruso A.) Acta Otorhinol. Ital. 21,
226-236, 2001.
48)
Identification of the facial nerve in the translabyrinthine approach: an
alternative technique. (in coll con Saleh E, Russo A, Falcioni M.)
Otolaryngol. Head Neck Surg. 124, 105-6, 2001.
49)
Electromyographic evaluation of facial nerve damage in acoustic neuroma surgery.
(in
coll. con Nakao Y, Piccirillo E, Falcioni M, Taibah A, Kobayashi T.) Otol.
& Neurotol. 22, 554-557, 2001.
50)
Treatment of residual vestibular schwannoma. (in coll. con
Falcioni M., Taibah A.K., De Donato G., Russo A. Piccirillo E.) Otology
and Neurotology 2002.
51)
Prediction of facial nerve outcome using electromyographic responses in
acoustic neuroma surgery. (in coll. con Nakao Y, Piccirillo E,
Falcioni M, Taibah A, Russo A, Kobayashi T.) Otol. & Neurotol. 23, 93-95,
2002.
52)
Residual vestibular schwannomas treatment. (in coll. con Falcioni M, Taibah A,
De Donato G, Russo A, Piccirillo E.) Otol. & Neurotol. 23: 980-987;
2002
53)
Neurinoma dell'acustico ipervascolarizzato. (in coll. con Di Trapani G,
Falcioni M, Taibah A, Russo A.) ORL up-to-date. 89° Congresso Nazionale
della Società Italiana di Otorinolaringologia e Chirurgia
Cervico-Facciale, San Benedetto del Tronto, 22-25 Maggio 2002. Passali.
-Bellussi L. edts, 369-371.
54) A retrospective correlation of ABR and magnetic resonance imaging for
acoustic neuromas/vestibular schwannomas. (in coll. con Skinner LJ,
Piccirillo E, Agarwal M, Falcioni M.) IVth international
conference on vestibular shwannoma and other CPA lesions. Cambridge
UK, 13th-17th July 2003. Baguley D, Ramsden R and Moffat D eds. Immediate
proceedings LDT, 84-85.
55)
Hearing preservation surgery in vestibular schwannomas. (in coll. con
Piccirillo E, Russo A, Khrais T, Rohit, Falcioni M.) IVth international conference on
vestibular shwannoma and other CPA lesions. Cambridge UK, 13th-17th July 2003.
Baguley D, Ramsden R and Moffat D eds. Immediate proceedings LDT,167-8.
56)
Facial nerve function after vestibular schwannoma removal. (in
coll. con Falcioni M, Luppino L, Agarwal M, Romano G.) IVth
international conference on vestibular shwannoma and other CPA lesions.
Cambridge UK, 13th-17th July 2003. Baguley D, Ramsden R and Moffat D eds.
Immediate proceedings LDT, 169-170.
57)
CSF Teak after vestibular schwannoma surgery. (in coll. con Mancini F, Khrais
T, Falcioni M, Di Trapani G.) IVth international conference on vestibular
shwannoma and other CPA lesions. Cambridge UK, 13th-17 th July 2003. Baguley D,
Ramsden R and Moffat D eds. Immediate proceedings LDT, 2001.
58)
Enlarged translabyrinthine approach for the management of large and giant
acustic neuromas (vestibular schwannomas). A report of 175 consecutive cases. (in
coll. con Russo A, Taibah A, Falcioni M, Agarwal M.) Ann. Otol. Rhinol.
Laryngol
59)
Perioperative complications in acoustic neuroma ( vestibular schwannoma) surgery.
(in coll. con Taibah A., Russo A., Falcioni M., Agarwal M.) Otology
and Neurotology 25.000-000; 2004.
60)
Facial nerve grafting in the cerebellopontine angle. (
in coll con Yogesh J., Falcioni M., Mancini F., Romano G.) The
Laryngoscope 114: April 2004
61) Trasapical extension in difficult cerebellopontine angle tumors. ( in coll
con Agarwal M., Mancini F., Taibah a.) Annals of Otology, Rhinology
and Laryngology, Volume 113, number 8, August 2004.
62)
Hearing preservation surgery in vestibular schwannoma: the hidden truth. (in
coll con: Khrais T., Russo A., Piccirillo E., Augurio A.) Annals
of Otology, Rhinology and Laryngology, Volume 113, number 2, February
2004.
63) Management of acoustic neuroma in the only hearing ear. Eur Arch
Otorhinolaryngol. 2005 Feb;262(2). (in coll con Naguib MB, Cokkessr Y)
64)
[Clinical experience in 36 cases of using of the extended translabyrinthine
technique for the treatment of large acoustic neuromas]
Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2005 Sep;40(9):705-7.
(in coll con Tong MC, Lam JM, Hu BH).
65)
Preoperative predictive factors for hearing preservation in vestibular
schwannoma surgery. Ann Otol Rhinol Laryngol. 2006 Jan;115(1):41-6. (in
coll con Rohit, Piccirillo E, Jain Y, Augurio A).
66)
Hearing preservation surgery in vestibular schwannoma.
J Laryngol Otol. 2006 May;120(5):366-70. Epub 2006 Mar 24.
67)
Quality of life after acoustic neuroma surgery. Otol Neurotol. 2006
Apr;27(3):403-9. (in coll con Tufarelli D, Meli A, Alesii A, De Angelis E,
Badaracco C, Falcioni M)
68)
Intracanalicular meningioma: clinical features, radiologic findings, and
surgical management. Otol Neurotol. 2007 Apr;28(3):391-9. (in
coll con Bacciu A, Piazza P, Di Lella F).
69)
Management of intralabyrinthine schwannomas. Auris Nasus Larynx. 2007
Dec;34(4):459-63. Epub 2007 Apr 27. (in coll con Di Lella F, Dispenza F,
De Stefano A, Falcioni M)
70)
Intraoperative cochlear nerve monitoring in vestibular schwannoma surgery--does
it really affect hearing outcome? Audiol Neurootol. 2008;13(1):58-64. Epub 2007
Sep 20. in coll con Piccirillo E, Hiraumi H, Hamada M, Russo A, De
Stefano323) Cerebrospinal Fluid Leak After Retrosigmoid Excision of Vestibular
Schwannomas. Otol Neurotol. 2007 Dec 28; (in coll con Maurizio
Falcioni, Romano G, Nitin Aggarwal) 71) Nerve origin of vestibular schwannoma:
a prospective study. J Laryngol Otol. 2007 Nov
27;:1-4(in coll con Khrais T, Romano G) 327) Decision making for solitary
vestibular schwannoma and contralateral Meniere's disease.
Dispenza
F, De Stefano A, Flanagan S, Romano G, Sanna M.
Audiol Neurootol. 2008;13(1):53-7. Epub 2007 Sep 11.PMID: 17848792 [PubMed -
indexed for MEDLINE]
72)
Intraoperative cochlear nerve monitoring in vestibular schwannoma urgery--does
it really affect hearing outcome? Piccirillo E, Hiraumi H,
Hamada M, Russo A, De Stefano A, Sanna M. Audiol Neurootol. 2008;13(1):58-64.
Epub 2007 Sep 20.