TRAUMI PADIGLIONE AURICOLARE
Ferite del padiglione.pag.1
Otoematomi e contusioni del padiglione.pag.2
Amputazioni del padiglione.pag.2
Orecchio lacerato.pag.3
Tecnica.pag.3
Complicazioni.pag.7
bibliografia.pag.8
Panoramica
Lacerazioni del padiglione e delle orecchie sono comunemente riscontrati nei traumi, spesso legato ad infortuni sportivi o morsi di animali. [1, 2, 3] .
I traumi del padiglione espongono a diversi rischi: il rischio di sequela estetica e il rischio infettivo. Ogni trauma che porta a un'esposizione della cartilagine richiede un'attenzione particolare volta a individuare il minimo segno evolutivo verso una condrite. [28]
Il padiglione auricolare o dell'orecchio esterno, si sviluppa a partire da 6 tubercoli che fondono per formare il trago, elice crus, elica, antelice, antitrago, e lobulo. La muscolatura intrinseca ed estrinseca dell'orecchio è di nessuna importanza significativa, anche se si ha un trauma. Vedere l'immagine qui sotto.
 Anatomia dell'orecchio esterno.
Anatomia dell'orecchio esterno.
L'orecchio è composto da pelle eccezionalmente vascolarizzata strettamente applicata ad una struttura cartilaginea avascolare. Lacerazioni all'orecchio possono coinvolgere la pelle, i tessuti fibrocartilaginee o grassi del padiglione auricolare, o una loro combinazione. L'arteria temporale superficiale e posteriore dell'arteria auricolare garantiscono l'apporto di sangue all'orecchio. Quando riparato adeguatamente, lacerazioni all'orecchio generalmente guariscono bene a causa di questa generosa offerta dual sangue. Un unico peduncolo vascolare, contenente il ramo superiore auricolare dell'arteria temporale superficiale, in grado di fornire alimentazione sufficiente sangue per l'intero orecchio. [4] Per ulteriori informazioni sulla anatomia pertinente, vedere Ear Anatomy .
Ferite del padiglione
Esse richiedono un trattamento sotto anestesia locale, o eventualmente generale, in caso di ferita estesa e contusa. Il principio è semplice: dopo detersione e disinfezione della ferita, viene effettuata una sutura cutanea, che permette un affrontamento serrato dei margini cutanei. Non è necessario suturare la cartilagine sezionata, ma la sua copertura deve essere perfetta, pena il rischio di condrite al padiglione. In caso di necessità, è auspicabile una resezione economica della cartilagine per ottenere la sua buona copertura con i piani tegumentari. Come nel caso delle condriti, deve essere posta in sede una medicazione spessa che garantisca una buona conformazione dei rilievi, con l'obiettivo di limitare i traumi sull'orecchio infiammato. È consigliabile un antibiotico profilassi, soprattutto se la ferita è slabbrata o suturata in modo differito (per esempio con Augmentin®, 3 g al di per os).
Otoematomi e contusioni del padiglione
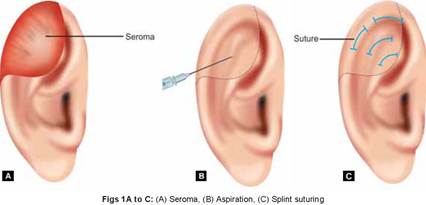
Come per le ferite, gli otoematomi e le contusioni che non si limitano a semplici ecchimosi cutanee superficiali possono essere all'origine di condriti secondarie (Figura 17 ). La presenza di un ematoma impone la sua evacuazione, che è realizzata il più delle volte sotto anestesia generale data l'entità del dolore. Per prevenire le recidive di ematoma del padiglione è possibile ricorrere a una tecnica affidabile che consiste nel posizionare uno o due punti trapassanti a U, annodati su una batuffolo da una parte e dall'altra del padiglione. Alcuni autori hanno proposto una medicazione gessata. Le medicazioni devono essere lasciate in sede diversi giorni e anche in questo caso deve essere prescritta una profilassi antibiotica.
Amputazioni del padiglione
L'amputazione traumatica del padiglione è un incidente raro. Può trattarsi di amputazione legata a un incidente stradale, ma anche in via non eccezionale della conseguenza di un morso. In questo caso, se il morso è dovuto a un cane, bisogna prendere le precauzioni comuni nei confronti dei rischi infettivi specifici per esso: disinfezione prolungata, profilassi mirata contro le Pasteurelle (di tipo tetracicline). Non bisogna dimenticare di richiedere un esame veterinario dell'animale, che deve essere rinnovato 7 giorni e 15 giorni dopo l'esame iniziale allo scopo di ricercare la presenza di anomalie nell'animale che possano far temere un rischio di esposizione al virus rabico. Nell'ambito di questa ipotesi può essere decisa una vaccinazione terapeutica.
Se il paziente non ha portato con sé il frammento di padiglione, la ferita è recentata e la cute suturata in modo da prevenire ogni esposizione della cartilagine. È possibile, in funzione della richiesta del paziente, proporgli secondariamente una correzione estetica per otopoiesi parziale o per epitesi.
Se il frammento del padiglione è portato dal paziente in un periodo di tempo ragionevole (meno di 6 ore), può essere proposto un reimpianto. Il principio è quello di includere il frammento di cartilagine sotto la cute periauricolare, disepidermizzando una delle sue facce, quindi eseguire una lateralizzazione secondaria con posizionamento di un piccolo innesto di cute secondo il principio del secondo tempo delle otopoiesi. [29] Il paziente deve tuttavia essere bene informato dei rischi di necrosi cartilaginea, che rendono aleatorio il tentativo di trapianto del padiglione. I tentativi di reimpianto con microanastomosi sembrano fornire dei risultati molto incostanti, legati all'impossibilità di eseguire un'anastomosi venosa di buona qualità. [30]
Gli obiettivi primari di gestione delle ferite a lacerazioni orecchie sono la copertura espediente di cartilagine esposta e la minimizzazione di ematoma della ferita. [5] In questo argomento vengono lacerazioni auricolari parziali; tuttavia, si verificano anche avulsioni totale dell'orecchio. [6] Reimpianto del totale avulsioni orecchio è stata accolta con un certo successo, ma deve essere eseguita solo da un professionista esperto. (Vedere Orecchio, la ricostruzione e salvataggio ). [7, 8]
Indicazioni
Le indicazioni sono ferite e lacerazioni al padiglione auricolare (vedere l'immagine qui sotto).
 Orecchio lacerato.
Orecchio lacerato.
Controindicazioni
Le lesioni specifici dell'orecchio richiedono un rinvio urgente un chirurgo plastico o uno specialista otologo od otorino. Tali lesioni sono i seguenti:
· Grande avulsione sovrastante la cute (circa 5 mm o superiore)
· Gravi lesioni da schiacciamento
· Avulsioni complete o quasi complete [6] o amputazioni [8, 9]
· Auricolare ematoma
· Grande difetti della cartilagine (circa 5 mm o superiore)
· Ferite che richiedono la rimozione di più di circa 5 mm di tessuto
· Significativo coinvolgimento del canale uditivo
· Devitalizzazione Attrezzatura
Dispositivi di protezione individuale è la seguente:
· Guanti
· Visiera
· Toga
Apparecchiature anestesia è il seguente:
· Lidocaina
· Siringa, 10 mL
· Ago, calibro 27
· Ago, 18 gauge
Attrezzatura per l'irrigazione è il seguente:
· Saline o acqua
· Siringa o irrigazione dispositivo
· Scudo Splash
· Bacino
Materiale di sutura è il seguente [14] :
· Suture assorbibili (ad esempio, Dexon, Vicryl), 5-0 o 6-0
· Suture assorbibili (ad esempio, nylon, Ethilon), 5-0 o 6-0
· Vassoio di sutura
· Kit sutura standard
· Forbici Belle
· Morsetto
· Pinze dei tessuti
· Autista Needle
· Bisturi, No. 15 blade
Garze è il seguente:
· Garza, Xeroform
· Garza, 4 x 4 in
· Garza, fluffed
· Kling garza, 3 in
· Avvolgere Bende elastiche (ad esempio, Ace), 3 in
Posizionamento
Il decubito laterale è preferito, con l'orecchio feriti rivolto verso l'alto. La posizione supina può anche essere usato.
Tecnica
Tutti i tessuti devitalizzati o contaminata deve essere sbrigliata. Questo passaggio è particolarmente importante in ferite da morso. Tuttavia, essere sicuri non sbrigliare il meno tessuto necessario. Come risultato di generosa vascolarizzazione, devitalizzazione è relativamente poco frequenti.
Pulire la ferita con abbondante irrigazione. Recenti studi hanno dimostrato che i tassi di infezione della ferita non differivano in quelli irrigati con acqua di rubinetto o soluzione salina sterile. [15] garza possono essere immessi nel canale uditivo esterno per il comfort prima di irrigazione.
Mantenere la sterilità durante la preparazione e drappeggio la ferita.
La cartilagine avascolare deriva il suo apporto di sangue dalla pelle sovrastante.Pertanto, la cartilagine esposto deve essere né sbrigliata o coperto da pelle per sopravvivere. Pelle auricolare spesso si estende per consentire la copertura della maggior parte dei difetti. Se la pelle restante non può coprire la cartilagine, la cartilagine deve essere tagliato fuori dal margine della ferita per consentire la chiusura della pelle sovrastante.
Nel caso di una lacerazione lineare pinna in cui la pelle non approssimativa, può essere utilizzata una tecnica di escissione a cuneo. Vedere l'immagine qui sotto.
 Ferita che richiede una escissione cuneiforme.
Ferita che richiede una escissione cuneiforme.
Per eseguire una escissione a cuneo, viene utilizzato un bisturi No. 15 per tagliare un triangolo dalla antelice a tutto spessore. Vedere l'immagine qui sotto.
 La cartilagine è asportato, lasciando una sporgenza di 1 mm di pelle.
La cartilagine è asportato, lasciando una sporgenza di 1 mm di pelle.
Una sporgenza di 1 mm della pelle al di là della cartilagine, si raccomanda che l'eversione della pelle in fase di chiusura. Vedere l'immagine qui sotto.
 Dopo l'asportazione, la pelle rimanente è chiuso con eversione.
Dopo l'asportazione, la pelle rimanente è chiuso con eversione.
Fino a 5 mm di cartilagine possono essere rimossi senza significative deformità.
Se una parte del padiglione auricolare è asportata, è generalmente sconsigliabile riattaccare la parte amputata, specialmente nei casi di ferite da morso. I margini del difetto dovrebbero essere tagliati, e la pelle anteriore e posteriore devono essere ravvicinate per una guarigione primaria.
In caso di estese ferite, la cartilagine può essere approssimata separatamente dalla pelle in una tecnica a 2 strati. Questo metodo viene utilizzato solo in grandi lesioni al fine di ridurre la tensione dai bordi della ferita. Utilizzando 5-0 o 6-0 suture riassorbibili, inizierà alla profondità della ferita e continuare verso l'esterno. La cartilagine è fragile; per evitare strappi, includere solo il pericondrio con ogni punto. Solo delicata approssimazione della cartilagine è necessaria. Per preservare monumenti normali, i primi punti di sutura posti dovrebbero essere in pieghe e creste.
Ferite più piccole possono essere approssimate con un singolo strato di suture attraverso la pelle e pericondrio come descritto in di seguito.
Nella maggior parte dei casi, la pelle viene chiusa con semplici punti staccati.Vedere l'immagine qui sotto.
 La pelle dell'orecchio viene suturata in una semplice tecnica interrotto.
La pelle dell'orecchio viene suturata in una semplice tecnica interrotto.
Approssimazione sciolto viene utilizzato nei casi di ferite contaminate.
Se necessario, sbrigliare tutta la pelle devitalizzata,.
A partire dalla profondità della ferita verso l'esterno, chiudere prima la pelle posteriormente e successivamente la la pelle anteriore e laterale superficiale dell'elice.
Per questo, possono essere usati 5-0 o 6-0 suture assorbibili.
Se possibile, rovesciare la pelle sul bordo libero per evitare una successiva dentellatura e ridurre al minimo i difetti estetici.
Per eversione ottimale e cosmesi (ad esempio, per evitare rimo dentellatura), possono essere richiesti suture a materasso verticali per lacerazioni che coinvolgono il bordo dell'orecchio.
Le suture devono essere collocate attraverso la pelle ed il pericondrio, non attraverso la cartilagine stessa.
La pelle dell'orecchio e la cartilagine sottostante aderiscono l'uno all'altro così bene che di solito è necessaria la chiusura separata della cartilagine.
Dopo la riparazione, imballare strisce Xeroform nelle fessure per le orecchie.
Posizionare un pezzo di garza (4 x 4 pollici) dietro l'orecchio e posizionare garza fluffed sopra l'orecchio.
Quindi, applicare una medicazione pressione per evitare la formazione di ematomi. Vedere l'immagine qui sotto.
 Una medicazione a compressione è collocata per prevenire la formazione di ematomi.
Una medicazione a compressione è collocata per prevenire la formazione di ematomi.
Avvolgere la testa e l'orecchio ferito con 3-in Kling seguito da un involucro 3-in fasciatura elastica (ad esempio, Ace). Vedere l'immagine qui sotto.
 La medicazione a compressione finale viene coperta con un impacco a bendaggio elastico.
La medicazione a compressione finale viene coperta con un impacco a bendaggio elastico.
Lasciare l'orecchio inalterato libera di vestire.
Elevare la testa per diversi giorni.
Rivalutare la ferita in 24 ore per la formazione di eventuali ematomi e possibili drenaggi.
Le suture vengono rimossi in 4-5 giorni.
Casi clinici dimostrano i benefici della terapia aggiuntiva con farmaci per la rivascolarizzazione assistita di grandi ferite dell'orecchio. [16] La terapia Leech è indicata dove si osservano edema, macchie scure-viola, o drenaggio venoso insufficiente. [17]
Perle
Nel caso di traumi, ispezionare la membrana timpanica per hemotympanum o rottura ed esaminare il canale uditivo esterno per lacerazioni o prova di una perdita CNS.
Eseguire sempre un esame approfondito del nervo facciale. [18]
Può essere necessario l’asportazione di ematomi prima della chiusura.
L’emostasi deve essere eseguita per prevenire la conseguente formazione di un ematoma.
La vaccinazione antitetanica dovrebbe essere richiamata, e la profilassi della rabbia dovrebbe essere affrontato quando necessario.
Gli antibiotici possono essere prescritti per lesioni ad alto rischio, tra cui i seguenti:
· Ferite contaminate
· Bite lesioni
· Ferite che mostrano segni di infiammazione
Complicazioni
Le complicazioni possono comprendere i seguenti:
· Condrite erosiva: La cartilagine dell'orecchio è avascolare; con interruzione o la rimozione della pelle sovrastante, il rischio di condrite erosiva esiste. L'uso di suture cartilagine aumenta il rischio di condrite, e deve essere utilizzato solo quando necessario. Condrite ritardate possono verificarsi dopo ustioni e altre lesioni e possono rispondere alla terapia antibiotica.
· Ematomi auricolari : ematomi Auriculari si verificano quando un infortunio da taglio separa la cartilagine auricolare dal pericondrio, creando uno spazio che raccoglie il sangue. Gli ematomi auricolari possono provocare cambiamenti fibrotici e il progressivo sviluppo di una deformità cronica nota come orecchio a cavolfiore. [19] Per evitare questo sfregio, l'ematoma deve essere asportato e l'orecchio compresso per una settimana.
· Altre complicazioni: Queste possono includere la formazione di cheloidi ed infezioni.
Cura peri procedurale
Educazione del paziente e consenso
Il consenso deve essere ottenuto dal paziente o membro della famiglia per la riparazione. [10] Il motivo è la procedura di (sospetta diagnosi); i rischi, i benefici e le alternative della procedura; i rischi ei benefici di qualsiasi procedura alternativa; e i rischi ei benefici di non subire la procedura dovrebbero essere discusse. Il fornitore deve permettere al paziente la possibilità di fare tutte le domande e risolvere eventuali problemi che potrebbero incontrare e devono assicurarsi che il paziente ha una comprensione circa la riparazione in modo che possano prendere una decisione informata.
Il paziente va informato sui rischi di condrite erosiva, infezioni, danni a un vaso sanguigno, asportazione di tessuto, formazione di cheloidi, e la formazione di ematomi auricolari.
Il paziente deve essere informato che la procedura può non avere successo e possono essere necessari ulteriori procedure
Il chirurgo deve anche discutere di come questi rischi possono essere evitati o prevenuti.
Per le piccole ferite all'orecchio senza coinvolgimento cartilagineo, l’infiltrazione locale può essere utilizzata (per maggiori informazioni vedi anestetici locali, somministrazione per infiltrazione e Anestesia dell’orecchio . Tuttavia, è generalmente meglio evitare l'anestesia locale perché l’infiltrazione nello spazio dell'orecchio relativamente compatto provoca dolore e può modificare i punti di riferimento che sono cruciali per la cosmesi. Blocchi nervosi regionali o blocchi di campo sono il metodo preferito di anestesia nelle lacerazioni significative dell'orecchio. [11]
Il dolore associato alle iniezioni nell’anestesia locale può essere diminuito utilizzando un ago di calibro più piccolo e somministrando lentamente l'anestetico. [12] Cfr l'immagine qui sotto. Infiltrazione di anestesia locale (Nota: L'immagine visualizzata per la dimostrazione di tecnica, l'anestesia locale non è raccomandata in queste grandi lacerazioni).
Infiltrazione di anestesia locale (Nota: L'immagine visualizzata per la dimostrazione di tecnica, l'anestesia locale non è raccomandata in queste grandi lacerazioni).
Alcuni esperti suggeriscono di evitare l'uso di adrenalina quando anestetizzare l'orecchio per timore di necrosi ischemica in questo settore delle estremità. Tuttavia ci sono pochi dati che mostra un danno nel suo utilizzo, e una certa letteratura in realtà supporta l'uso di adrenalina quando si anestetizza l'orecchio. Uno studio ha dimostrato che l’epinefrina, insieme con un anestetico locale, è stato utilizzato in oltre 10.000 procedure chirurgiche sull'orecchio senza complicazioni. [13]L'uso di adrenalina può essere utile per la riparazione di lacerazione, in quanto diminuisce la quantità di sangue sul campo operatorio, prolunga l'anestesia, e riduce il tempo della procedura chirurgica.
References
1. Martin-Smith JD, Chan JC, Power KT, Crowley PJ, Clover AJ. Do helmets worn for hurling fail to protect the ear? Identification of an emerging injury pattern. Br J Sports Med. Dec 2012;46(16):1134-6. [Medline].
2. Hwang K. Torn earlobe caused by an earring trapped in the net of goalposts. J Craniofac Surg. May 2012;23(3):946. [Medline].
3. Kuvat SV, Bozkurt M, Kapi E, Karakol P, Yaçsar Z, Güven E. Our treatment approaches in head-neck injuries caused by animal bites. J Craniofac Surg. Jul 2011;22(4):1507-10. [Medline].
4. Erdmann D, Bruno AD, Follmar KE, Stokes TH, Gonyon DL, Marcus JR. The helical arcade: anatomic basis for survival in near-total ear avulsion. J Craniofac Surg. Jan 2009;20(1):245-8. [Medline].
5. Brown DJ, Jaffe JE, Henson JK. Advanced laceration management. Emerg Med Clin North Am. Feb 2007;25(1):83-99. [Medline].
6. Saad Ibrahim SM, Zidan A, Madani S. Totally avulsed ear: new technique of immediate ear reconstruction.J Plast Reconstr Aesthet Surg. 2008;61 Suppl 1:S29-36. [Medline].
7. Steffen A, Katzbach R, Klaiber S. A comparison of ear reattachment methods: a review of 25 years since Pennington. Plast Reconstr Surg. Nov 2006;118(6):1358-64. [Medline].
8. Komorowska-Timek E, Hardesty RA. Successful reattachment of a nearly amputated ear without microsurgery. Plast Reconstr Surg. Apr 2008;121(4):165e-9e. [Medline].
9. Ihrai T, Balaguer T, Monteil MC, et al. [Surgical management of traumatic ear amputations: literature review]. Ann Chir Plast Esthet. Apr 2009;54(2):146-51. [Medline].
10. Roberts JR, Hedges JR, eds. Clinical procedures in emergency medicine. 5th ed. Philadelphia, Pa: WB Saunders; 2009.
11. Zide BM, Swift R. How to block and tackle the face. Plast Reconstr Surg. Mar 1998;101(3):840-51.[Medline].
12. Forsch RT. Essentials of skin laceration repair. Am Fam Physician. Oct 15 2008;78(8):945-51. [Medline].
13. Hafner HM, Rocken M, Breuninger H. Epinephrine-supplemented local anesthetics for ear and nose surgery: clinical use without complications in more than 10,000 surgical procedures. J Dtsch Dermatol Ges. Mar 2005;3(3):195-9. [Medline].
14. Osterberg B, Blomstedt B. Effect of suture materials on bacterial survival in infected wounds. An experimental study. Acta Chir Scand. 1979;145(7):431-4. [Medline].
15. Edmonds M. Irrigation of simple lacerations with tap water or sterile saline in the emergency department did not differ for wound infections. Evid Based Med. Dec 2007;12(6):181. [Medline].
16. Hullett JS, Spinnato GG, Ziccardi V. Treatment of an ear laceration with adjunctive leech therapy: a case report. Journal of Oral and Maxillofacial Surgery. October 2007;65:2112-2114. [Medline].
17. Cho BH, Anh HB. Microsurgical replantation of partial ear, with leech therapy. Annals of Plastic Surgery. 1999;43:427.
18. Hogg NJ, Horswell BB. Soft tissue pediatric facial trauma: a review. J Can Dent Assoc. Jul-Aug 2006;72(6):549-52. [Medline].
19. Belleza WG, Kalman S. Otolaryngologic emergencies in the outpatient setting. Med Clin North Am. Mar 2006;90(2):329-53. [Medline].
20. Daver BM, Antia NH, Furnas DW. Handbook of Plastic Surgery for the General Surgeon. 2nd ed. New York, NY: Oxford University; 2000:145-8 Chap 9.
21. Section Six: Emergency Wound Management. In: Tintinalli JE, Klen GD, Stapczynki JS, eds. Emergency Medicine: A Comprehensive Study Guide. 6th ed. New York, NY: McGraw-Hill; 2004:303 Chap 43.
22. Greer WE, Benhaim P, Lorenz HP, et al. Soft tissue Injuries to the Face, Non-congenital Ear Reconstruction. In: Handbook of Plastic Surgery. New York, NY: Marcel Deuker; 2004:135-41 Chap 27, 171-4 Chap 35.
23. Lawrence PF, Reath DB, Chun JT. Diseases of the skin and soft tissue, face and hand. In: Bell RM, Dayton MT, eds. Essentials of Surgical Specialties. 2nd ed. Philadelphia, Pa: Lippincott, Williams and Wilkins; 2000:4.
24. Marks MW, Marks C. Reconstructive Procedures of the Face. In: Fundamentals of Plastic Surgery. Philadelphia, Pa: WB Saunders; 1997:240-2, 244-6 Chap 13.
25. Reichman FF, Simon RR. Management of Soft Tissue Injuries. In: Emergency Medicine Procedures. New York, NY: McGraw-Hill; 2004:748-62 Chap 80.
26. Sweitzer BJ, Pilla M. Local anesthetics. In: Hurford WE, ed. Clinical anesthesia procedures of the Massachusetts General Hospital. 5th ed. Philadelphia, Pa: Lippincott-Raven; 1998:233-41.
27. Weatherley-White RC, Lesavoy MA. The integument. In: Hill GJ, ed. Outpatient Surgery. 2nd ed. Philadelphia, Pa: WB Saunders; 1980:334.
28. Templer J., Renner G.J. Injuries of the external ear Otolaryngol Clin North Am 1990 ; 23 : 1003-1018.
29. Roeser R.J., Ballachanda B.B. Physiology, pathophysiology, and anthropology/epidemiology of human ear canal secretions J Am Acad Audiol 1997 ; 8 : 391-400.
30. Elsahy N.I. Ear replantation Clin Plast Surg 2002 ; 29 : 221-223 [cross-ref]
30.
Ricostruzione del padiglione auricolare
Ricostruzione del padiglione auricolare. pag.10
Storia della Procedura. pag.10
Problemi. pag.10
Epidemiologia. pag.11
Abrasioni, Aplasia. pag.11
Avulsione e amputazione lesioni .pag.12
Ustioni .pag.13
Difetti compositi, Congelamento. pag.13
Lacerazioni (semplici vs complesse) .pag.13
Anatomia Rilevante.pag.14
Terapia chirurgica. pag. 15
Anestesia chirurgica e principi generali di trattamento .pag.16
Le tecniche chirurgiche: innesti, flaps, e reimpianto .pag.19
Tecniche specifiche. pag. 21
Complicazioni .pag.22
Futuro e controversie. pag. 23
bibliografia .pag.23
Storia della Procedura
La Ricostruzione dell'orecchio ha una storia lunga e varia. Un testo indiano 8 ° secolo, il Susrata, contiene una delle descrizioni registrata della prima di ricostruzione dell'orecchio (l'uso di un lembo guancia per riparare un difetto lobo dell'orecchio.) Un rapporto 1551 contiene la prima descrizione di un reimpianto orecchio totale. [ 1]. Nel 1920, Gillies usava cartilagine autologa per una ricostruzione totale di dell'orecchio. Questa evoluzione derivava dalla necessità di far fronte con i risultati di deformità congenite dell'orecchio. Nel 1959, Tanzer ha inaugurato l'era moderna in ricostruzione dell'orecchio con il successo nell'uso di autologhi innesti cartilagine costale. [2, 3] Brent avanzate sono le norme della ricostruzione dell'orecchio con materiali autogeno e fu il primo a segnalare il successo nell'uso di espansione del tessuto in ricostruzione dell'orecchio. [4] Molte delle tecniche innovative utilizzate per la ricostruzione totale di difetti congeniti dell'orecchio può essere applicato a difetti acquisiti.
Problemi
Le Deformità acquisite dell'orecchio sono in genere il risultato di un trauma, escissioni lesioni della pelle, e ematomi o infezioni. Le criticità di ricostruzione per ciascuno di questi 3 eziologie sono diversi.
Il successo di ricostruzione dell'orecchio dopo trauma dipende da due fattori principali. Il primo di questi è la pervietà vascolare. La sopravvivenza di un padiglione auricolare ricostruito, dipende da un flusso arterioso sufficiente a nutrire l'innesto di guarigione. Inoltre, la congestione venosa causata dopo l’amputazione parziale o totale può portare a perdita della cartilagine. Il secondo fattore riguarda la disponibilità della copertura dei tessuti molli oltre alla cartilagine reimpiantata o raccolta. La mancanza di copertura dei tessuti molli a seguito di una lesione traumatica può limitare le opzioni disponibili per la riparazione o può richiedere una copertura del lembo più complessa.
Ottenere un equilibrio tra le dimensioni e la forma è il fattore più importante per ricostruzioni dopo l’escissione della pelle per la lesione. Per rendere un orecchio che sembri normale, il chirurgo spesso deve sacrificare la dimensione della cartilagine sottostante per conservare una forma normale ed evitare distorsioni. Poiché entrambe le orecchie non sono in genere viste contemporaneamente , la è più importante mantenere la simmetria delle dimensioni. conservando i punti di riferimento anatomici.
La ricostruzione dell’orecchio dopo infezioni o ematomi dipende dalla quantità residua della cartilagine di sostegno Più ampio è il coinvolgimento della cartilagine nelle infezioni o ematomi più richiede demolizione . Una perdita estesa della cartilagine può comportare una ricostruzione dell'orecchio totale simile a quella necessaria per un orecchio con deformità congenita .
Questa discussione presenta principi di chirurgia plastica di base e la loro applicazione a deformità acquisite dell'orecchio. Il soggetto con lesioni traumatiche all'orecchio è seguito da tecniche di riparazione seguenti all’estirpazione controllate di lesioni cutanee. Molte delle tecniche descritte per la ricostruzione di lesione cutanea escisse può essere utilizzato in ricostruzioni di lesioni traumatiche e viceversa.
Epidemiologia
Circa 800.000 persone sviluppano il cancro della pelle negli Stati Uniti ogni anno. Di questi, il 90% sono dovuti a lesioni nella regione della testa e del collo, il 12% dei quali coinvolgono lesioni sull'orecchio e zona periauricolare. Dal cinquanta al sessanta per cento di tutte le lesioni cutanee dell'orecchio esterno sono carcinomi a cellule squamose , il 30-40% sono carcinomi a cellule basali , e solo il 2-6% sono i melanomi . Il padiglione auricolare è coinvolto nel 45-55% di queste lesioni. Circa un terzo dei carcinomi cutanei dell'orecchio estendono direttamente nella cartilagine sottostante e richiedono passante e passante escissione.
Il padiglione auricolare esterno ha un alto potenziale di lesioni a causa della sua posizione esposta e non protetta lungo la testa. Uno studio retrospettivo di Bardsley e Mercer guardando i registri ospedalieri nei casi di lesioni auricolari ha rivelato che i morsi umani costituiscono la causa più comune di lesioni (42%). [5] Questa percentuale è seguita dalle cadute (20%), incidenti automobilistici (16%) , e morsi di cane (14%). L'infortunio più comune osservata era l’amputazione incompleta dell'orecchio, perdita di tessuto del bordo solitamente elicoidale. Le lesioni auricolari aperti non trattate invariabilmente provocano infezioni, deformità che ne derivano, ed ulteriore perdita di tessuto. Per ulteriori informazioni sul trattamento di tutti i tipi di trauma, visitare il sito di Medscape Trauma Resource Center .
Eziologia
Difetti e deformità del padiglione auricolare acquisiti hanno varie cause. Eziologie comuni sono elencati di seguito. [6]
Le zone abrase devono essere pulite e lavate i accuratamente. I detriti devono essere rimossi completamente e in modo aggressivo, spesso con curettage. L'area coinvolta dovrebbe essere coperto con garza impregnata di antibiotico topico per 24 ore. Successivamente, queste lesioni devono essere trattati come le ferite aperte, avendo cura di mantenere la zona umida con pomata antibiotica. Perossido di idrogeno diluito al 3% può essere usato per rimuovere le croste di sangue essiccato e le altre secrezioni. L’epitlelizzazione secondaria deve essere completa in 7-10 giorni. La copertura antibiotica per le ferite contaminate dovrebbe includere la copertura per lo pseudomonas.
Deformità congenite del padiglione auricolare richiedono la ricostruzione auricolare . La ricostruzione auricolare totale è oltre la portata di questo articolo.
Avulsione e amputazione lesioni
Le avulsioni o amputazioni dell’orecchio possono presentare con il completo segmento interessato o di una parte esso a disposizione per la ricostruzione. L’amputazione isolata traumatica dell’orecchio è un evento raro e spesso si verifica in concomitanza con i principali traumi della testa e del collo. [7]
Le lesioni al padiglione auricolare da colpi alla testa comunemente provocano ematomi e la formazione di siero sulla superficie anteriore dell'orecchio tra la cartilagine e il pericondrio. Se non corretta, può provocare forme fibrose cartilaginee in questo settore e una deformità permanente dell'orecchio noto come "orecchio cavolfiore," illustrato di seguito. Il trattamento acuto comporta il drenaggio del versamento tramite ago aspirato o incisione seguita da applicazione di una medicazione a pressione.
 Orecchio a Cavolfiore.
Orecchio a Cavolfiore.
Se il versamento si ripresenta o se il danno è non eliminato inizialmente o da diversi giorni, e può essere necessario l’incisione lo sbrigliamento del pericondrio coinvolto e la fibroneocartilage di recente formazione. Una medicazione rafforzata, garze impregnate di antibiotico topico su entrambi i lati del padiglione auricolare fissato con passante e attraverso suture, può essere utilizzato per mantenere la pressione sulla zona interessata.
 Drenaggio di effusione tra cartilagine e pericondrio.
Drenaggio di effusione tra cartilagine e pericondrio.
In primo luogo, ustioni di secondo e terzo grado possono portare ad una serie di lesioni che vanno da un semplice denudamento della pelle ad una perdita totale dell'orecchio. Queste lesioni comportano il rischio di infezione a causa della contaminazione da stafilococco o pseudomonas. E’ essenziale una pulizia accurata per prevenire o limitare queste infezioni. Agenti patogeni responsabili sono di flora mista, Pseudomonas aeruginosa è presente nel 95% degli incidenti. Con l'uso profilattico di crema di acetato di mafenide (Sulfamylon) l'incidenza della condrite è diminuita nei casi di ustioni auricolari dal 29% al 19% . Una volta diagnosticata, la condrite suppurativa può essere trattata con l'instillazione locale di gentamicina, neomicina e polimixina antibiotici 2-5 volte al giorno.
Difetti compositi sono lesioni che coinvolgono la pelle e cartilagine e in cui una parte del padiglione auricolare è mancante.
Temperature di -19 ° C o inferiore di solito causano lesioni. La Flebite di solito è superficiale e si traduce in eritema ed edema della pelle senza (primo grado) o con bolle (secondo grado). Ferite profonde del terzo e quarto grado risultato congelamento con necrosi della pelle senza perdita del padiglione auricolare e portano a necrosi completa, cancrena, e perdita di tessuto.
Lacerazioni (semplici vs complesse)
Semplici lacerazioni sono difetti lineari nella pelle del padiglione auricolare senza tessuto mancante. Di solito coinvolgono la pelle con o senza tessuto sottocutaneo. La cartilagine non è coinvolto; tuttavia, si può trovare esposizione della cartilagine . Questo tipo di lesione può essere chiuso in un unico strato con o senza una medicazione rafforzata .
Lacerazioni complesse sono anche difetti lineari che coinvolgono la cartilagine. Queste lesioni non hanno mancanza di pelle o difetto nella cartilagine. In generale, sono richiesti chiusure a più strati che comprendono il pericondrio sono tenuti con una medicazione rafforzata . Le medicazioni Bolster sono importanti per evitare la formazione di ematomi. Per una descrizione dettagliata di riparazione, consultare eMedicine Procedure cliniche articolo Lacerazione complesse, dell’orecchio .
 Lacerazione dell’orecchio.
Lacerazione dell’orecchio.
Difetti superficiali (pericondrio presente vs pericondrio assente)
Difetti superficiali sono lesioni in cui una zona di pelle è avulsa e mancanti dalla cartilagine sottostante. Queste lesioni possono avere presenza di pericondrio o assenza della cartilagine. La presenza di pericondrio deve essere determinata, in quanto è altamente vascolarizzata ed è essenziale per la sopravvivenza della cartilagine. Questo permette la determinazioni del tipo di ricostruzione ammissibile. Difetti non strutturali della ciotola della conca o quelli tra l'elice ed antelice non necessitano della ricostruzione di cartilagine, a differenza del bordo dell’elice.
Anatomia Rilevante
Il padiglione auricolare è tipicamente orientato ad un angolo di rotazione anteroposteriore di 15-20 °. La distanza dalla parte superiore della crus elicoidale canto laterale dell'occhio è circa 6 cm. L'altezza media del padiglione dalla parte superiore dell'elica al fondo del lobulo è circa 6 cm. La sporgenza normale fuori del cranio è di 30 °.
Punti di riferimento del padiglione auricolare sono identificati da pieghe e curve nel cartilagine e la pelle (vedi immagine sotto). Il limite anteriore del padiglione auricolare è trago, una protuberanza a forma di cupola cartilagineo orientata in un posto laterale verticale del condotto uditivo esterno. L'elica è la più importante svolta superiore del padiglione auricolare e termina anteriormente appena superiore al trago al cru elicoidale. Appena sotto l'elica è la antihelix, una piega che divide anteriormente e superiormente a formare la triangularis fossa. Inferiormente, il anithelix finisce come una prominenza formare la antitragus. Mediale al antihelix e trago è la conca cavum, che è in continuità con la porzione cartilaginea del canale uditivo esterno. Appeso al padiglione auricolare cartilaginea è pelle flaccida chiamato il lobulo.
 Anatomia del posteriore (mediale) la superficie dell'orecchio.
Anatomia del posteriore (mediale) la superficie dell'orecchio.
L'orecchio esterno contiene un unico pezzo di cartilagine elastica con pericondrio strettamente aderente. I due terzi superiori del padiglione auricolare contengono cartilagine; il terzo inferiore (lobulo) è privo di cartilagine. La cartilagine ha fornitura diretta di sangue, come nutrienti sono forniti e assorbiti direttamente dal suo pericondrio sovrastante. La pelle del padiglione auricolare aderisce strettamente alla cartilagine sottostante e contiene poco tessuto sottocutaneo. L'orecchio posteriore / mediale ha più tessuto sottocutaneo, ha un ricco apporto di sangue, ed è più vagamente legato al quadro.
Tre muscoli estrinseci collegano il padiglione auricolare al cuoio capelluto: muscoli auricolari anteriore, superiore, e posteriore. Il legamento anteriore si estende dal trago alla radice del processo zigomatica dell'osso temporale. Il legamento posteriore passa dalla superficie posteriore della conca alla superficie laterale del processo mastoide. Il padiglione auricolare è attaccato all'osso temporale per il suo tessuto fibrocartilagineo.
Il ricco apporto di sangue auricolare è composto da interconnessioni tra l'arteria auricolare posteriore (PAA) e l'arteria temporale superficiale (STA) (vedi immagine sopra). Questi forniscono una vascolarizzazione, straordinaria permettendo al padiglione auricolare di subire un trauma significativo, sia chirurgicamente o accidentalmente, senza perdere la sua vitalità. Il PAA fornisce la maggior parte del sangue all'orecchio anteriore. Essa deriva dalla STA appena sotto il livello del lobulo. Il PAA passa cefalica nel solco retroauricolare, dando rami alla superficie mediale dell'orecchio. Termina unendo un ramo posteriore della STA, completando un anello vascolare attorno alla base dell'orecchio. La STA emana un ramo auricolare solo anteriore al trago. Di per sé, fornisce un contributo minore al padiglione auricolare.
La profondità di questo anello vascolare può variare da pochi millimetri sotto la pelle ad una profondità di 1 cm. Fornisce una superficie di 6 cm per 11 centimetri che si estende dal trago a 5 cm posteriormente al canale uditivo esterno 6 cm inferiori alla mastoide. Fornitura alla zona conchal è derivato da perforatrici costantemente trovati penetranti pavimento conchal e provenienti dal PAA. Inoltre, esiste una fitta rete anastomotica tra il PAA e l'arteria occipitale.
Il padiglione auricolare ha anche una innervazione ricca, che è costituito da più nervi cranici nonché rami del plesso cervicale. Le maggiori forniture nervose auricolari maggior parte del padiglione auricolare, dalla parte posteriore / mediale per anteriore / laterale lobulo, elica, e antelice. Si estende superiormente, dove condivide innervazione con il nervo auricolotemporale. Il nervo auricolotemporale è un ramo della divisione mandibolare del nervo trigemino (CN V3), che fornisce il trago, crus elicoidali, e la pelle superiore al padiglione auricolare. Il minore forniture nervo occipitale pelle posteriore al padiglione auricolare. Nervi cranici (CN) VII e X fornitura maggior parte della innervazione alla cavum conchae e posteriore canale uditivo esterno derivante dall'orecchio medio. Questi sono importanti per l'indirizzo quando si cerca di ottenere un blocco del nervo completo quando la riparazione del padiglione auricolare.
 Anterior Anatomia (laterale) superficie dell'orecchio.
Anterior Anatomia (laterale) superficie dell'orecchio.
Per ulteriori informazioni sulla anatomia, v Ear Anatomy .
Terapia chirurgica
Al fine di consentire al chirurgo di meglio pianificare ricostruzione del padiglione auricolare può essere suddivisa in zone o subunità. Queste subunità anatomiche richiedono diversi metodi di riparazione. Il primo di questi è il cerchio e lobulo elicoidale, che crea l'aspetto complessivo dell'orecchio rispetto al lato opposto.Difetti lievi o deformità sottili in questa subunità possono creare il più grande asimmetria cosmetici. Pertanto, si ha cura in questa subunità di mantenere la continuità, ridurre deformità step-off, mantenere l'altezza, e prevenire profilo o di linea regolare anomalie.
La prossima è la subunità antihelix e antitragus. Queste pieghe cartilaginee complessi conferiscono struttura per l'orecchio e il supporto. Perdere cartilagine in questa zona può produrre deformità lop-orecchie, cavolfiore orecchio, e cambiamenti nella protrusione del cerchio elicoidale.
Probabilmente la zona meno importante è la ciotola conchal o conchae cavum perché contribuisce poco al generale forma, supporto, o la dimensione dell'orecchio. Cartilagine in questa subunità può essere utilizzato come innesti ricostruzione di difetti ipsilaterale o controlaterale senza conseguenze negative.
Anestesia chirurgica e principi generali di trattamento
L’anestesia locale o i blocchi regionali sono il fondamento per il trattamento chirurgico del padiglione auricolare. L'anestesia generale , naturalmente, viene offerto come necessario per il comfort del paziente (ad esempio, i bambini), lunghezza estesa di procedura, e ricostruzioni complesse. Tuttavia, il chirurgo può ottenere un blocco completo dell'orecchio se l'innervazione sopra descritto si comprende.
Completa anestesia regionale richiede infiltrazione di anestetico locale (comunemente, 2% lidocaina con 1: 100.000 epinefrina) circonferenzialmente attorno al padiglione auricolare nel piano sottocutaneo. In particolare, il grande nervo auricolare può essere situato nel solco retroauricolare e l'infiltrazione anestetizza efficacemente l'aspetto mediale del padiglione auricolare, nonché contributi al lobulo, elica, e antelice. Un'ampia anterior infiltrazioni trago anestetizza la distribuzione del nervo auricolotemporale: trago, crus elicoidali, e la porzione superiore-laterale del padiglione auricolare. Se la ciotola conchal deve essere affrontato, agenti supplementari devono essere infiltrati ampiamente intorno alla parte posteriore del condotto uditivo esterno, anestetizzante quindi rami sensoriali del CN VII e X.
I principi generali di trattamento sono raccomandati come segue:
· Pulire accuratamente l'orecchio con soluzioni contenenti iodio.
· Sbrigliare e rimuovere qualsiasi corpo estraneo (FB).
· Sbrigliare bordi frastagliati della pelle o macerate.
· Irrigare con grandi quantità di soluzione fisiologica sterile.
· Suturare la pericondrio con piccoli punti di sutura riassorbibili (5-0, 6-0 monofilamento).
· Chiudere la pelle con sutura riassorbibile (5-0, 6-0 in nylon).
· Utilizzare suture materasso verticali sul bordo elicoidale per prevenire dentellatura.
· Pulire quotidianamente con acqua ossigenata e applicare Telfa vestirsi con pomata antibiotica.
· Utilizzare una medicazione mastoide e rafforzare vestirsi come richiesto per evitare ematomi o sieroma.
· Utilizzare un antibiotico ad ampio spettro per 1 settimana.
· Rimuovere suture in 5-7 giorni.
Opzioni per la ricostruzione in base alla posizione
Antero-superiore difetti rim elicoidali, terzo superiore
· Difetti del cerchio elicoidale sono particolarmente evidenti dal punto di vista estetico e può essere difficile ricostruire. Difetti superficiali della pelle possono essere riparati con l'uso di lembi cutanei vascolarizzati basati sulla pelle retroauricolare. Questo funziona bene in presenza o assenza del pericondrio. Particolare attenzione è rivolta a fornire un lembo di pelle non-capelli-cuscinetto. Innesti cutanei a tutto spessore, non sono generalmente consigliati per il cerchio elicoidale. Scarsi risultati di innesti cutanei sono dovuti a difetti biscotto bite-contrattura produzione. Piccoli difetti orlo elicoidali potrebbero essere suscettibili di lembi avanzamento chondrocutaneous, soprattutto se il difetto è inferiore a 2 cm. Tuttavia, questo probabilmente comporta una diminuzione dell'altezza del padiglione auricolare.
· Per i difetti che sono più grandi di 2 cm, un lembo tubo in scena dalla pelle retroauricolare può essere una scelta eccellente. Due incisioni parallele sono realizzati in pelle postauricolare adiacente al difetto bordo elicoidale. La pelle è minata tra incisioni e il lembo bipedicled è tubed nel centro. La fase successiva prevede asportare uno dei peduncoli e recepimento della falda sulla adiacente vizio bordo elicoidale. Dopo 2 settimane, il secondo peduncolo viene asportato e il lembo tubed è inserto nel difetto rimanente del cerchio elicoidale. Il difetto retroauricolare viene poi chiuso in primo luogo.
· Per maggiori difetti del terzo superiore del padiglione auricolare, possono essere utilizzati lembi temporoparietale. Basato sul dell'arteria temporale superficiale, questi lembi possono fornire buona vascolarizzazione alla cartilagine raccolto. Lembi del cuoio capelluto non sono adatti a causa dello spessore delle proprietà della pelle e capelli portante. Flaps temporoparietale sono estremamente sottili e possono essere ruotati inferiormente per coprire una vasta area. Dopo la cartilagine è raccolto e tagliato per adattarsi il difetto, il lembo temporoparietale viene ruotato e tunnel sotto il solco temporoparietale per coprire l'innesto. Un innesto a tutto spessore della pelle viene quindi posto sopra il lembo e si applica una medicazione rafforzare.Questa tecnica è utile per difetti e risultati in cosmesi accettabile grandi.
Fossa scafoide e fossa triangolare dell’ antelice
· Il difetto più comune acquisito da escissioni a tutto spessore di lesioni auricolari è probabile dello scafoide e fossa triangolare del antihelix. Difetti di questa regione generalmente sono combinati con un difetto del cerchio elicoidale. Essi possono essere superficiali, con pericondrio assente o presente. Essi possono anche comportare difetti a tutto spessore, tra cui la cartilagine e la pelle retroauricolare.
· Difetti superficiali con pericondrio presenti sono suscettibili di innesti cutanei a tutto spessore o di guarigione per seconda intenzione. Innesti cutanei a tutto spessore devono essere aggressivo diradati e tinta di fornire un buon risultato estetico. Pelle retroauricolare fornisce un sito donatore adeguato per questi difetti. Se il pericondrio è assente, deve essere utilizzato un innesto cutaneo vascolarizzato.
· Per difetti compositi del cerchio elicoidale ed antelice, esistono vari metodi di ricostruzione. Per i difetti più piccoli di 2 cm, la chiusura primaria può essere opportuno. Bordi della pelle dovrebbero rinfrescare e chiusure pelle e cartilagine devono essere sfalsati, se possibile. La cartilagine è riapprossimato con lunga durata suture assorbibili in modo interrotto. La pelle è chiusa con suture permanenti monofilamento, che vengono rimossi in 5-7 giorni.
· Per i difetti più grandi di 2 cm, un innesto composito può essere presa da un orecchio controlaterale. Questo innesto è generalmente la dimensione del difetto, che fornisce la simmetria con l'orecchio donatore. Anche in questo caso, i reapproximations pelle e cartilagine devono essere sfalsati con sovrapposizione vascolarizzato pelle. Una seconda tecnica sarebbe una escissione forma stellate della lesione coinvolge l'intero spessore del padiglione auricolare. Questo facilita la chiusura distribuendo tensione in tutto il padiglione auricolare. Un inconveniente di questa tecnica è la notevole riduzione delle dimensioni del padiglione auricolare. Si può richiedere una riduzione padiglione auricolare controlaterale per fornire la simmetria.
Rim elica posteriore-inferiore; difetti antelice, terzo medio
· Simile a RIM e antelice difetti elicoidali superiori, la regione del terzo medio del padiglione auricolare richiede il supporto e la simmetria. Vari lembi sono disponibili per la ricostruzione di questa regione. Il più semplice di questi è il lembo di avanzamento elicoidale, che può essere utilizzato per i difetti compositi fino a 25 mm di lunghezza. La regione del difetto è rinfrescato e sbrigliata, se necessario. L'avversario cartilagine, pericondrio, e la pelle sono riapprossimato principalmente. Il principale svantaggio di questo lembo è la riduzione complessiva delle dimensioni del padiglione auricolare. Tuttavia, questo lembo è semplice da usare e ha complicazioni minime.
· Lembi di trasposizione sono disponibili dalla regione retroauricolare anche.Essi sono tipicamente utilizzati per i difetti solo la pelle in cui la cartilagine è intatto. Una procedura in più fasi è necessario per preservare la vascolarizzazione del lembo e sostenere la cartilagine, se necessario. Il lembo può essere diviso dal peduncolo e sostituita nel sito donatore posteriori dopo circa 3-4 settimane. Se la pelle anteriore e posteriore è avulsed dalla cartilagine del padiglione auricolare, può essere utilizzata una modifica di tale lembo. Invece di sostituire il lembo sezionato nel sito donatore, può facilmente essere capovolto per coprire posteriormente al difetto mediale e cerchione elicoidale. Il sito donatore può essere coperto con un innesto cutaneo a spessore parziale.
· Flaps avanzamento Chondrocutaneous sono disponibili per difetti orlo elicoidali sia del cerchio elicoidale superiore ed inferiore anche. Una porzione di cerchio elicoidale adiacente al difetto è sezionato e liberato dai suoi allegati mediale. Questo permette al lembo chondrocutaneous di ruotare attorno al padiglione auricolare centrifuga di mantenere la continuità di difetti grandi come 25 mm. Sebbene una leggera variazione della curvatura del padiglione auricolare può comportare, la diminuzione complessiva delle dimensioni dell'orecchio sarà minimo.
Trago e Crus dell’ Elice
· I difetti della sola pelle possono essere riparati in una varietà di modi. Innanzitutto, la pelle tragale può essere sostituito facendo ruotare un lembo lobulo superiormente. Inoltre, la pelle preauricolare può essere avanzata posteriormente con attenzione per la pelle dei capelli-I difetti del trago e quelle dei croce dell’ elicei possono provocare anomalie significative se è coinvolta la cartilagine. Innesti di cartilagine possono essere collocati in modo appropriato in tessuto ben vascolarizzato, se necessario.
· I difetti della Croce dell’elice possono essere riparati utilizzando tecniche di cui sopra. I Flaps temporoparietale possono permettere una buona ricostruzione dei difetti più grandi in questa regione.
cavo della Conca
· Il cavo della conca contribuisce poco alla forma generale, dimensioni, e sostegno del padiglione auricolare. Difetti in questa regione possono essere riparati con solo lembi cutanei locali od innesto cutaneo, o possono essere lasciati guarire per seconda intenzione. Per i difetti, che coinvolgono la superficie laterale senza interessamento della cartilagine, il miglior risultato estetico si ha se si permettendo alla lesione di di guarire per seconda intenzione crea.
· Per i difetti compositi, possono bastare lembi di avanzamento locali con innesto cutaneo posteriore / mediale. Difetti più grandi possono richiedere lembi di recepimento della regione retroauricolare con innesto cutaneo posteriormente / mediale. Non è richiesto innesto di cartilagine per la ricostruzione di questa regione. Infatti, la ciotola conchal può essere una fonte donatore ideale di cartilagine per la ricostruzione in altre regioni del padiglione auricolare.
Le tecniche chirurgiche: innesti, flaps, e reimpianto
Trapianti di pelle
· Trapianti di pelle possono essere utilizzati per coprire le aree con pericondrio impressionati ma non assumono cartilagine senza copertura pericondrale. Un lembo locale del tessuto sottocutaneo può essere utilizzata per coprire la cartilagine, e quindi un innesto di pelle può essere posizionato sopra il sito donatore. Pelle retroauricolare fornisce un'eccellente partita di colore. Prima e dopo le foto sono riportati di seguito.Difetto pronto per la copertura innesto cutaneo. Riparare con tutto spessore innesto cutaneo.

Lembi cutanei
· Thin tubed flap: Questo lembo viene utilizzato per ricostruire difetti cerchio elicoidali, come quelli che in genere risultano dopo ustioni. Una striscia di pelle retroauricolare è sollevata a fianco il difetto elicoidale che è abbastanza lungo da coprire. Vedere l'immagine qui sotto. Il lembo viene lasciata attaccata ad entrambe le estremità in una fase di ritardo, poi staccati ad una estremità e suturati al bordo elicoidale corrispondente. Dopo un ritardo, il bordo opposto viene sollevata e fissata al bordo corrispondente. Svantaggi associati a questa ricostruzione sono molteplici messe in scena.Sottile tubed lembo.
· Banner flap: Questo lembo, indicato di seguito, costituito da pelle di sovra-auricolari basato sul solco auriculocephalic che viene utilizzato per ricostruire difetti del terzo superiore del padiglione auricolare. La pelle viene sollevata ripiegato il difetto. Questo lembo primo è stato descritto da Crikelair e può essere utilizzato con una piccola cartilagine trapianto per garantire la stabilità strutturale. [8] Banner lembo.
Banner lembo.
· Procedura Tunnel: Questa tecnica, mostrato sotto, è stato proposto da Converse nel 1958 per correggere difetti elicoidali superiori e medie. [9] In primo luogo, un innesto di cartilagine forma alla dimensione del difetto elicoidale è incanalato sotto la pelle della zona mastoide e unito le corrispondenti estremità del difetto. In una seconda fase, il padiglione auricolare è separata dalla zona mastoide con l'innesto allegata. Innesti retroauricolare controlaterale tutto spessore possono essere utilizzati per coprire mastoide risultante e difetti retroauricolari.Procedura Tunnel.
· Lembo mastoide: definito Anche la tecnica di attacco postauricolare, questa tecnica è utilizzata per correggere difetti di massima coinvolgono il margine auricolare centrale. Nella prima fase, la pelle postauricolare è parallelo incisa all'asse del difetto in cui il bordo del difetto incontra la pelle postauricolare. La pelle auricular anterior viene poi suturata alla pelle postauricolare sul bordo posteriore della incisione e la pelle auricolare posteriore viene suturato al bordo anteriore della incisione. Nella seconda fase, la pelle auricolare posteriore necessario per riempire il difetto viene asportato. Un innesto di pelle è di solito necessario per coprire il mastoide risultante e difetti zona retroauricolare.
Flaps Condrocutaneo
· Antia-Buch chondrocutaneous avanzamento lembo: Questo lembo viene utilizzato per la ricostruzione di difetti elicoidali da 3 cm di diametro o meno.In questa tecnica, una escissione cuneo è combinato con un lembo elicoidale chondrocutaneous basato su posteriore pelle auricolare e rami perforanti dal PAA. Il lembo viene ruotato lungo il conchal cartilagine intatta e margini cuneo vengono suturati con meno sforzo e deformazione di quella vista con chiusure primarie di grandi escissioni cuneo. Vedere le immagini qui sotto.ricostruzione Antia-Buch (1).Antia-Buch ricostruzione (2).Antia-Buch ricostruzione (3).Antia-Buch ricostruzione (4).



o Il successo di questa tecnica dipende liberare l'intero lembo elicoidale dal scapha e minare la pelle auricolare posteriore superficiale al pericondrio. Un avanzamento VY della radice elicoidale può fornire la lunghezza supplementare. Se il difetto si estende oltre l'elica e nella scapha, un'estensione cutanea delle alette elicoidali chondrocutaneous può fornire copertura per questo difetto.
o Come descritto da Argamoso e Lewin, il lembo Antia-Buch può essere modificato per l'utilizzo in ricostruzioni elicoidali mezza terzo utilizzando una combinazione di lembi condrocutanei superiormente ed inferiormente basati basate ruotato insieme al sito di escissione cuneo o difetto. [10] Questo ricostruzione è limitata ai difetti di diametro di 3 cm o meno . Ulteriori modifiche di questa tecnica includono il suo uso nella ricostruzione difetti lobo dell'orecchio e la sua combinazione con lembi cutanei locali ricostruire difetti più grandi ulteriormente dal bordo elicoidale.
· flap Condrocutane della conca:. Prima proposta da Davis nel 1974, viene utilizzato per ricostruire gravi perdite del terzo superiore del padiglione auricolare [11] Il lembo è costituito dalla superficie di concal chondrocutaneous sollevata su un peduncolo pelle dalla radice dei cru elicoidali e trasposta difetto marginale (vedi sotto). Il difetto dei donatori è coperto sul lato preauricolare con un retroauricolare sottocutaneo peduncolo lembo e sulla superficie retroauricolare con un lembo cutaneo di recepimento.Un innesto di pelle viene quindi utilizzato per coprire il sito peduncolo lembo donatore sottocutaneo retroauricolare.conchal Lembo Condrocutaneo.
· Isola chondrocutaneous lembo retroauricolare: definito anche rotazione del lembo posteriore auricolare, falda flip-flop, girevole ribalta, e retroauricolare miocutaneo isola falda, questo primo è stato descritto da Masson nel 1972.[12] E 'in genere utilizzato per ricostruire Conchal lesioni ciotola risultanti da escissioni tumorali. Il lembo si basa sul solco retroauricolare con margini corrispondenti al difetto asportato. Una volta che il lembo viene sollevato, viene ruotato sul suo asse lungo di 180 ° in modo che la pelle postauricolare copre il difetto anterolaterale della ciotola conchal. Il difetto della pelle posteriore è poi chiuso in primo luogo.
Il principio tasca
· Descritto da Mladick nel 1971, il principio tasca ha dimostrato di essere una buona procedura di salvataggio per la cartilagine auricolare nella cornice di avulsione o amputazione lesioni. In primo luogo, il segmento amputato o avulso del padiglione auricolare viene pulita e denudata della sua pelle.Pericondrio deve essere lasciato al suo posto, se disponibile. La cartilagine amputata viene ricollegato al padiglione auricolare nella sua appropriata posizione anatomica. La parte denudato viene poi sepolto in una tasca retroauricolare e lasciato in sede per 2 settimane. Ciò permette di mantenere la cartilagine suo apporto di sangue essenziale. La tasca è resecato e il segmento amputato permesso di reepithelialize spontaneamente nell'arco di diverse settimane.
· Variazioni di questa tecnica hanno prodotto risultati migliori. Le piccole perforazioni possono essere messi in cartilagine dissodata e lasciati sul posto per tutto il tempo 3 mesi. La porzione laterale del lembo cutaneo può essere lasciato attaccato alla cartilagine, e la parte posteriore / mediale può essere innestato pelle. Un'altra variante prevede la cartilagine sandwich tra un lembo retroauricolare anteriormente e posteriormente un lembo fasciale.
Reimpianto microvascolare
· Nel 1980, Pennington ha eseguito con successo il primo reimpianto microvascolare di un orecchio amputato. [13] Da allora, sono stati riportati in letteratura circa 25 ulteriori casi di successo di reimpianto microvascolare di un orecchio amputato o avulso. [7]
· Prima di iniziare reimpianto, l'anatomia vascolare della parte amputata deve essere attentamente valutato e sezionato. Irrigazione Gentle del lume vascolare con soluzione salina eparinizzata permette la visualizzazione dell'intima e può aiutare a determinare la presenza di danni. Una volta che la dissezione microvascolare è completa, l'orecchio amputato viene suturato in posizione. Riparazione arteriosa microvascolare primaria viene eseguita utilizzando una arteria adatto trovato vicino al bordo della ferita. Solitamente, l'anastomosi arteriosa è seguita dalla riparazione venosa. Una volta che le riparazioni microvascolari sono complete, la pelle è chiuso liberamente. [7]
· Se l'arteria è di lunghezza sufficiente, un innesto venoso può essere utilizzato. Inoltre, quando l'unica imbarcazione identificabile è una vena, può essere presa in considerazione la riparazione arterovenosa. Inoltre, sono stati segnalati diversi reimpianti auricolari eseguiti con successo senza una riparazione venosa. Ciò dimostra la capacità dell'orecchio nel formare nuovi mezzi di deflusso durante un periodo di congestione venosa, e la fattibilità di metodi non invasivi per decomprimere adeguatamente un orecchio senza vene intatte. [7]
Complicazioni
Infezioni presenti come dolore, infiammazione, gonfiore, o la tenerezza più di 3 giorni dopo l'intervento. Il trattamento antibiotico deve essere iniziato tempestivamente per evitare lo sviluppo di condrite suppurativa. La condrite appare come un edema persistente, arrossamento, e la tenerezza sopra il padiglione auricolare. Ospedalizzazione, il drenaggio, la cultura della ferita, e terapia antibiotica per via endovenosa adeguato per 1 settimana a 10 giorni devono risolvere i sintomi.
Gli ematomi sono preannunciati da dolore eccessivo o la tenerezza dell'orecchio il primo o il secondo giorno postoperatorio. Occorre esposizione Prompt dell'orecchio. Questa complicazione può essere evitato con un aspiratore postauricolare scarico provetta e una medicazione di pressione postoperatoria costituito da rafforzare medicazioni o rotoli dentali montati i contorni del padiglione auricolare e tenuto da through-e-attraverso suture.
Formazione di cheloidi può essere trattata con una terapia a pressione o iniezioni intralesionali steroidee di triamcinolone acetonide. Lo steroide deve essere iniettato solo per via intradermica, poiché l’iniezione sottocutanea può provocare la necrosi del grasso. Gli steroidi iniezioni devono essere somministrate ogni 2-4 settimane fino risultati clinici, che includono rammollimento e appiattimento della lesione, sono evidenti. Se il cheloide persiste, escissione chirurgica in combinazione con radiazioni e iniezioni di steroidi intralesionali può eliminarli. Iniezioni di steroidi possono essere somministrati prima dell'intervento, durante l'intervento, e dopo l'intervento. L'applicazione di pressione dopo l'intervento può essere realizzato con gli orecchini di clip-on con grandi piastre base. E’ importante discutere con il paziente delle possibili complicanze di uso di steroidi, tra cui atrofia cutanea, ipopigmentazione e teleangectasie,.
Lesione del nervo facciale
Il nervo facciale è a un maggiore rischio di lesioni nel neonato e bambino appena esce e corsi più superficialmente a causa del processo mastoideo non sviluppato. Più tardi nella vita, quando il bambino ha raggiunto circa 6 mesi, può sollevare la testa da una posizione supina, e il nervo facciale sposta inferiormente e profondo con la crescita del processo mastoide. Anomalie del nervo facciale sono associati a maggiori rischi di resezione a causa di posizioni anomale.
Suture, suture assorbibili soprattutto monofilamenti, possono erodere attraverso la pelle. Ciò si verifica di solito mesi o anni dopo l'intervento. La rimozione delle suture è garantito se non sono essenziali. Suture polifilamento hanno meno di una tendenza per l'erosione, ma portano un più alto tasso di infezione.
Dolore persistente di recente insorgenza può derivare da lesioni ai nervi Rami del nervo grande auricolare. Iniezioni seriali di bupivacaina sono utili per alleviare i sintomi. Una complicazione significativa è lo sviluppo di distrofia simpatica riflessa dell'orecchio successiva ricostruzione. La terapia di massaggio può essere utile per alleviare il dolore associato a questa complicanza.
Perdita di pelle parziale
Necrosi cutanea e la perdita può derivare da indebolimento molto superficiale dei lembi cutanei utilizzati nella ricostruzione, che porta a insufficienza circolatoria, desquamazione, e atrofia. Questo viene corretto minando ad un livello più profondo, conservando il plesso vascolare sottocutaneo e un sottile strato di tessuto sottocutaneo. Questa complicanza è trattato con crema antibiotica e pressione ridotta sulla pelle coinvolti.
La necrosi da pressione è la complicanza più disastrosa. Tutte le suture devono essere posizionati con cura per evitare necrosi da pressione. Medicazione orecchio Stretto dovrebbe essere evitato per prevenire questa complicanza.
Scarsar corrispondenza di colore
Poor corrispondenza di colore si verifica quando si utilizza innesti cutanei da aree non contigue con cartilagini auricolari. Questa complicanza può essere evitato utilizzando mastoide o pelle sopraclavicolare.
Congestione venosa dei lembi
Posizionamento ottimale testa, rimozione delle fonti ostruttive, terapia con ossigeno iperbarico, e sanguisughe possono aiutare ad evitare questa complicazione.
Outcome e prognosi
Come detto inizialmente, ricostruzione postlesion escissione è un equilibrio di dimensioni rispetto dela forma, e la ricostruzione trauma è un equilibrio tra afflusso vascolare contro deflusso. Tutte le tecniche descritte nel presente documento in grado di fornire risultati eccellenti sotto il coordinamento di chirurghi esperti. Esistono tecniche per il recupero della maggior parte delle deformità auricolari acquisito, e risultati soddisfacenti sono possibili a condizione che le molte complicazioni possibili siano previste e sorvegliate .
Futuro e controversie
I progressi nelle tecniche microchirurgiche e la disponibilità di chirurghi addestrati in queste tecniche sia attraverso il miglioramento dei sistemi di trasporto di emergenza o telemedicina farà del reimpianto un'opzione di prima linea nel trattamento della maggior parte delle lesioni da amputazione importanti. [14] In un prossimo futuro, i progressi nel trapianto immunologia e chirurgia aggiungerà il trapianto di orecchiette cadavere al armamentario di nuove procedure emersione in questo campo. Inoltre, lo sviluppo di cartilagine sintetico biocompatibile tramite ingegneria tissutale può comportare la riparazione del tessuto personalizzato auricular traumatizzato con completa conservazione della normale anatomia.
References
- Grabb WC, Dingman RO. The fate of amputated tissues of the head and neck following replacement. Plast Reconstr Surg. Jan 1972;49(1):28-32. [Medline].
- Tanzer RC. Total reconstruction of the external ear. Plast Reconstr Surg. 1959;23:1.
- Park SE, Park BY. Salvage of expanded skin flap perforation and infection after total ear reconstruction with autogenous costal cartilage. J Craniofac Surg. May 2011;22(3):805-8. [Medline].
- Brent B. The acquired auricular deformity. A systematic approach to its analysis and reconstruction. Plast Reconstr Surg. Apr 1977;59(4):475-85. [Medline].
- Bardsley AF, Mercer DM. The injured ear: a review of 50 cases. Br J Plast Surg. Oct 1983;36(4):466-9.[Medline].
- Luo X, Yang J, Yang Q, Wang X. Classification and reconstruction of posttraumatic ear deformity. J Craniofac Surg. May 2012;23(3):654-7. [Medline].
- Kind GM. Microvascular ear replantation. Clin Plast Surg. Apr 2002;29(2):233-48, vii. [Medline].
- Crikelair GF. A Method of Partial Ear Reconstruction for Avulsion of the Upper Portion of the Ear. Plastic and Reconstructive Surgery. 1956;17:438.
- Converse JM. Reconstruction of the auricle. Plast Reconstr Surg. 1958;22:230.
- Argamaso RV, Lewin ML. Repair of partial ear loss with local composite flap. Plast Reconstr Surg. Nov 1968;42(5):437-41. [Medline].
- Davis J. Reconstruction of the upper third of the ear with a chondrocutaneous composite flap based on the crus helix. Symposium on Reconstruction of the Auricle. 1974;247.
- Masson JK. A simple island flap for reconstruction of concha-helix defects. Br J Plast Surg. Oct 1972;25(4):399-403. [Medline].
- Pennington DG, Lai MF, Pelly AD. Successful replantation of a completely avulsed ear by microvascular anastomosis. Plast Reconstr Surg. Jun 1980;65(6):820-3. [Medline].
- Lin PY, Chiang YC, Hsieh CH, Jeng SF. Microsurgical replantation and salvage procedures in traumatic ear amputation. J Trauma. Oct 2010;69(4):E15-9. [Medline].
- Aguilar EF 3rd. Auricular reconstruction of congenital microtia (grade III). Laryngoscope. Dec 1996;106(12 Pt 2 Su 82):1-26. [Medline].
- Alanis SZ. A new method for earlobe reconstruction. Plast Reconstr Surg. Mar 1970;45(3):254-7. [Medline].
- Alconchel MD, Rodrigo J, Cimorra GA. A combined flap technique for earlobe reconstruction in one stage.Br J Plast Surg. Jun 1996;49(4):242-4. [Medline].
- Anous MM, Hallock GG. Immediate reconstruction of the auricle using the amputated cartilage and the temporoparietal fascia. Ann Plast Surg. Oct 1988;21(4):378-81. [Medline].
- Antia NH, Buch VI. Chondrocutaneous advancement flap for the marginal defect of the ear. Plast Reconstr Surg. May 1967;39(5):472-7. [Medline].
- Apfelberg DB, Waisbren BA, Masters FW, Robinson DW. Treatment of chondritis in the burned ear by the local instillation of antibiotics. Plast Reconstr Surg. Feb 1974;53(2):179-83. [Medline].
- Bardsley AF. Primary reconstruction of a severed ear fragment using a flap of temporo-parietal fascia. Br J Plast Surg. Oct 1986;39(4):524-5. [Medline].
- Bauer BS, Fortes B. Ear reconstruction. In: Plastic Surgery Secrets. 1999.
- Berghaus A, Toplak F. Surgical concepts for reconstruction of the auricle. History and current state of the art. Arch Otolaryngol Head Neck Surg. Apr 1986;112(4):388-97. [Medline].
- Bhandari PS. Use of triamcinolone acetonide injection in ear reconstruction. Ann Plast Surg. Oct 2000;45(4):458-61. [Medline].
- Bialostocki A, Tan ST. Modified Antia-Buch repair for full-thickness upper pole auricular defects. Plast Reconstr Surg. Apr 1999;103(5):1476-9. [Medline].
- Brent BD. Ear reconstruction. In: Grabb and Smith's Plastic Surgery. 5th ed. 1997.
- Chana JS, Grobbelaar AO, Gault DT. Tissue expansion as an adjunct to reconstruction of congenital and acquired auricular deformities. Br J Plast Surg. Sep 1997;50(6):456-62. [Medline].
- Cho BH, Ahn HB. Microsurgical replantation of a partial ear, with leech therapy. Ann Plast Surg. Oct 1999;43(4):427-9. [Medline].
- Chun JK, Sterry TP, Margoles SL, Silver L. Salvage of ear replantation using the temporoparietal fascia flap. Ann Plast Surg. Apr 2000;44(4):435-9. [Medline].
- Concannon MJ, Puckett CL. Microsurgical replantation of an ear in a child without venous repair. Plast Reconstr Surg. Nov 1998;102(6):2088-93; discussion 2094-6. [Medline].
- Dabb RW, Malone JM, Leverett LC. The use of medicinal leeches in the salvage of flaps with venous congestion. Ann Plast Surg. Sep 1992;29(3):250-6. [Medline].
- David SK, Cheney ML. An anatomic study of the temporoparietal fascial flap. Arch Otolaryngol Head Neck Surg. Oct 1995;121(10):1153-6. [Medline].
- David SK, Cheney ML. An anatomic study of the temporoparietal fascial flap. Arch Otolaryngol Head Neck Surg. Oct 1995;121(10):1153-6. [Medline].
- de Chalain T, Jones G. Replantation of the avulsed pinna: 100 percent survival with a single arterial anastomosis and substitution of leeches for a venous anastomosis. Plast Reconstr Surg. Jun 1995;95(7):1275-9. [Medline].
- Destro MW, Speranzini MB. Total reconstruction of the auricle after traumatic amputation. Plast Reconstr Surg. Nov 1994;94(6):859-64. [Medline].
- Donelan MB. Conchal transposition flap for postburn ear deformities. Plast Reconstr Surg. Apr 1989;83(4):641-54. [Medline].
- Dowling JA, Foley FD, Moncrief JA. Chondritis in the burned ear. Plast Reconstr Surg. Aug 1968;42(2):115-22. [Medline].
- Dujon DG, Bowditch M. The thin tube pedicle: a valuable technique in auricular reconstruction after trauma.Br J Plast Surg. Jan 1995;48(1):35-8. [Medline].
- Earley MJ, Bardsley AF. Human bites: a review. Br J Plast Surg. Oct 1984;37(4):458-62. [Medline].
- Elsahy NI. Reconstruction of the cleft earlobe with preservation of the perforation for an earring. Plast Reconstr Surg. Feb 1986;77(2):322-4. [Medline].
- English GM. Common injuries to the ear. Prim Care. Sep 1976;3(3):507-20. [Medline].
- Eriksson E, Vogt PM. Ear reconstruction. Clin Plast Surg. Jul 1992;19(3):637-43. [Medline].
- Furnas DW. Complications of surgery of the external ear. Clin Plast Surg. Apr 1990;17(2):305-18. [Medline].
- Giffin CS. Wrestler's ear: pathophysiology and treatment. Ann Plast Surg. Feb 1992;28(2):131-9. [Medline].
- Hackney FL, Snively SL. Plastic surgery of the ear. In: Selected Readings in Plastic Surgery. Vol 8(16). 1997:1-26.
- Harris PA, Ladhani K, Das-Gupta R, Gault DT. Reconstruction of acquired sub-total ear defects with autologous costal cartilage. Br J Plast Surg. Jun 1999;52(4):268-75. [Medline].
- Henrich DE, Logan TC, Lewis RS, Shockley WW. Composite graft survival. An auricular amputation model.Arch Otolaryngol Head Neck Surg. Oct 1995;121(10):1137-42. [Medline].
- Jenkins AM, Finucan T. Primary nonmicrosurgical reconstruction following ear avulsion using the temporoparietal fascial island flap. Plast Reconstr Surg. Jan 1989;83(1):148-52. [Medline].
- Juri J, Irigaray A, Juri C, et al. Ear replantation. Plast Reconstr Surg. Sep 1987;80(3):431-5. [Medline].
- Kind GM, Buncke GM, Placik OJ, et al. Total ear replantation. Plast Reconstr Surg. Jun 1997;99(7):1858-67. [Medline].
- Leferink VJ, Nicolai JP. Malignant tumors of the external ear. Ann Plast Surg. Dec 1988;21(6):550-4.[Medline].
- Lehmuskallio E, Lindholm H, Koskenvuo K. Frostbite of the face and ears: epidemiological study of risk factors in Finnish conscripts. BMJ. Dec 23-30 1995;311(7021):1661-3. [Medline].
- Low DW. Modified chondrocutaneous advancement flap for ear reconstruction. Plast Reconstr Surg. Jul 1998;102(1):174-7. [Medline].
- Martinez JM, Alconchel MD, Olivares C, Cimorra GA. Reconstruction of the tragus after tumour excision. Br J Plast Surg. Oct 1997;50(7):552-4. [Medline].
- Mellette JR Jr. Ear reconstruction with local flaps. J Dermatol Surg Oncol. Feb 1991;17(2):176-82.[Medline].
- Menick FJ. Reconstruction of the ear after tumor excision. Clin Plast Surg. Apr 1990;17(2):405-15.[Medline].
- Millard DR Jr. Reconstruction of one-third plus of the auricular circumference. Plast Reconstr Surg. Sep 1992;90(3):475-8. [Medline].
- Mladick RA. Salvage of the ear in acute trauma. Clin Plast Surg. Jul 1978;5(3):427-35. [Medline].
- Mohan M, Appukuttan PK, Srinivasan A. Earlobe reconstruction with a preauricular flap. Plast Reconstr Surg. Aug 1978;62(2):267-70. [Medline].
- Nath RK, Kraemer BA, Azizzadeh A. Complete ear replantation without venous anastomosis. Microsurgery. 1998;18(4):282-5. [Medline].
- Ohsumi N, Iida N. Ear reconstruction with chondrocutaneous postauricular island flap. Plast Reconstr Surg. Sep 1995;96(3):718-20. [Medline].
- Okada E, Maruyama Y. A simple method for earlobe reconstruction. Plast Reconstr Surg. Jan 1998;101(1):162-6. [Medline].
- Orticochea M. Reconstruction of partial loss of the auricle. Plast Reconstr Surg. Oct 1970;46(4):403-5.[Medline].
- Pardue AM. Repair of torn earlobe with preservation of the perforation for an earring. Plast Reconstr Surg. Apr 1973;51(4):472-3. [Medline].
- Park C, Chung S. A single-stage two-flap method for reconstruction of partial auricular defect. Plast Reconstr Surg. Sep 1998;102(4):1175-81. [Medline].
- Park C, Lineaweaver WC, Rumly TO, Buncke HJ. Arterial supply of the anterior ear. Plast Reconstr Surg. Jul 1992;90(1):38-44. [Medline].
- Presutti RJ. Bite wounds. Early treatment and prophylaxis against infectious complications. Postgrad Med. Apr 1997;101(4):243-4, 246-52, 254. [Medline].
- Pribaz JJ, Crespo LD, Orgill DP, et al. Ear replantation without microsurgery. Plast Reconstr Surg. Jun 1997;99(7):1868-72. [Medline].
- Ramirez OM, Heckler FR. Reconstruction of nonmarginal defects of the ear with chondrocutaneous advancement flaps. Plast Reconstr Surg. Jul 1989;84(1):32-40. [Medline].
- Scott MJ, Klaassen MF. Immediate reconstruction of the helical rim after bite injury using the posterior auricular flap. Injury. 1992;23(5):333-5. [Medline].
- Talmi YP, Horowitz Z, Bedrin L, Kronenberg J. Auricular reconstruction with a postauricular myocutaneous island flap: flip-flop flap. Plast Reconstr Surg. Dec 1996;98(7):1191-9. [Medline].
- Talmi YP, Liokumovitch P, Wolf M, et al. Anatomy of the postauricular island "revolving door" flap ("flip-flop" flap). Ann Plast Surg. Dec 1997;39(6):603-7. [Medline].
- Tanaka Y, Tajima S, Tsujiguchi K, et al. Microvascular reconstruction of nose and ear defects using composite auricular free flaps. Ann Plast Surg. Oct 1993;31(4):298-302. [Medline].
- Templer J, Renner GJ. Injuries of the external ear. Otolaryngol Clin North Am. Oct 1990;23(5):1003-18.[Medline].
- Thomas SS, Matthews RN. Squamous cell carcinoma of the pinna: a 6-year study. Br J Plast Surg. Mar 1994;47(2):81-5. [Medline].
- Turpin IM, Altman DI, Cruz HG, Achauer BM. Salvage of the severely injured ear. Ann Plast Surg. Aug 1988;21(2):170-9. [Medline].
- van der Lei B, Spronk CA. Reconstruction of non-marginal ear defect by a postauricular wedge transposition flap. Br J Plast Surg. Jan 1998;51(1):14-6. [Medline].
- Wilkes GH, Wolfaardt JF. Osseointegrated alloplastic versus autogenous ear reconstruction: criteria for treatment selection. Plast Reconstr Surg. Apr 1994;93(5):967-79. [Medline].
- Yotsuyanagi T, Nihei Y, Sawada Y. Reconstruction of defects involving the upper one-third of the auricle.Plast Reconstr Surg. Sep 1998;102(4):988-92. [Medline].
- Yotsuyanagi T, Urushidate S, Sawada Y. Helical crus reconstruction using a postauricular chondrocutaneous flap. Ann Plast Surg. Jan 1999;42(1):61-6. [Medline].
- Yousif NJ, Denny AD, Forte R, et al. The effect of frostbite on the reconstructed ear. Ann Plast Surg. Feb 1994;32(2):132-4. [Medline].
Tumori dell’orecchio esterno
Forme Neoplastiche
L’orecchio esterno può essere sede di neoplasie benigne: quelle di più comune osservazione sono gli angiomi, i fibromi e i condromi ed il nodulo doloroso dell’elice. Le neoplasie maligne più frequenti sono gli epiteliomi sia lo spinocellulare sia il basocellulare
Tumori benigni:
• Ateromi, cheloidi (lobulo e regione auricolare),(Fig 1-2-3 )da Bechara Y. Ghorayeb
• Corno cutaneo (Fig. 4) verruche o cheratosi seborroiche (bordo dell’elice) (Fig. 5).
• Tofi gottosi (bordo dell’elice) (Fig. 6)
• Acantosi senile (bordo dell’elice).
• Cisti dermoidi (retroauricolari, imbocco del condotto uditivo esterno, preauricolari). (Fig. 6)
|

|

|

|
|
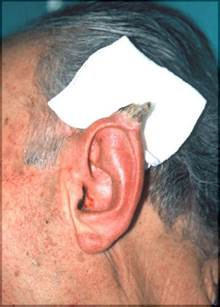
Fig.1 Cheloidi delpadiglione auricolare
|
Fig.2 La formazione di cheloidi nel lobo del padiglione auricolare è una rara complicanza dovuta all’utilizzo di orecchini.
|
Fig.3 Essa si verifica più comunemente nei afro-americani rispetto ai caucasici
|
|
|

|
|
|
Fig. 4a Corno cutaneo
|
Fig. 4b Corno cutaneo
|
|
|

|

|
|
|
Fig.5a Verruche o cheratosi seborroiche
|
Fig.5b Acantosi senile (bordo dell’elice).
|
|
| |
|
|
|
|
|

|

|
|
Fig. 6 Questa immagine mostra, il nodulo duro tipico della gotta avanzata.
|
Fig. 7 Questa immagine mostra una grande cisti epidermoide, noto anche come cisti sebacee (un termine improprio), infetta, che si sta prosciugando dal pus.
|
Angioma -Emangioma (Fig.8)
L’angioma può localizzarsi a livello del padiglione o del CUE. e può essere congenito o acquisito. L’orecchio esterno può essere la localizzazione primitiva dell’angioma o può divenire sede di esso per estensione della neoplasia da strutture adiacenti Si presentano sotto forma di una massa rossa o violacea, di morfologia assolutamente tipica, che interessa spesso il fondo del condotto uditivo esterno e può prolungarsi nella cassa.
Di più frequente riscontro è l’angioma cavernoso, che si presenta come una tumefazione di colorito rossastro, a superficie spesso irregolare. La sintomatologia soggettiva è scarsa, il dolore, se compare. è in rapporto alla rapidità ed all’entità dell’accrescimento della lesione. L’ipoacusia è presente solo nei casi in cui la localizzazione a livello del CUE ne determini una stenosi. La TC è indispensabile per valutare l'estensione di questo tumore nella mastoide e per guidare la resezione chirurgica, che deve essere sufficientemente ampia da prevenire la recidiva.
La terapia è essenzialmente chirurgica e consiste nell’exeresi della neoplasia. eventualmente preceduta. soprattutto nelle forme localmente estese da un’embolizzazione vascolare selettiva.
|

|
Fig. 8 Emangioma del condotto uditivo esterno: Il paziente è un uomo di 71 anni che aveva una perdita uditiva progressiva lenta. All'esame otoscopico del canale uditivo è stata vista una massa bluastra che bloccava il timpano. La biopsia ha rivelato una crescita vascolare benigna chiamata emangioma.
|
Fibroma. Il fibroma è un tumore connettivale benigno che trova a livello del lobulo. solitamente, la sua più frequente localizzazione, I fibromi si presentano solitamente come tumefazioni di piccole dimensioni. sessili o peduncolate. di consistenza duro elastica, non dolenti, a lento accrescimento.
La terapia è chirurgica. Per i fibromi peduncolati può essere sufficiente recidere alla base la neoformazione e cauterizzare la sede d’impianto. L’exeresi dei fibromi sessili può essere invece pur nella sua semplicità un po’ più laboriosa.
Condroma (fig.9) da Bechara Y. Ghorayeb.La localizzazione auricolare dei condromi è rara. Tali neoplasie si osservano più spesso in corrispondenza del CUE. Si presentano solitamente come neoformazioni della grandezza di un alcuni mm. di forma tondeggiante e di consistenza duro-elastica.
Il condroma non da luogo a sintomatologia dolorosa ne ad altri sintomi di rilievo a meno che non si determini una stenosi del CUE con conseguente ipoacusia trasmissiva. L’exeresi chirurgica è l’unica terapia razionale (Fig. 2).
|

|
Fig.9:Condroma del padiglione auricolare, tumore solido che distorce il padiglione auricolare e distrugge l'architettura normale, Assomiglia un orecchio cavolfiore, ma è molto più difficile a trattare e non può essere compresso schiacciando con le dita.
|
Nodo doloroso d’elice (Fig.10) il nodulo doloroso dell’elice (di Darrier) ha sede elettiva nell’elice, Si presenta solitamente come una piccola formazione nodulare ricoperta da croste, la cui asportazione rileva una unica ulcerazione che si approfondìsce fino alla cartilagine. Clinicamente si caratterizza per la vivace sensazione dolorosa evocata dalla sua pressione. tanto da impedire al soggetto di dormire appoggiando quel lato della testa sul cuscino.
|

|
|
Fig.10 Nodulo doloroso dell’elice (di Darrier) Nodulo doloroso dell’elice (di Darrier)
|
Tumori maligni dell'orecchio esterno
I tumori maligni dell’orecchio esterno rappresentano da soli il 70% circa di tutta la patologia neoplastica dell’osso temporale, tuttavia costituiscono una rara entità clinica, con un’incidenza approssimativa di 6-7 casi per milione di abitanti per anno. La gran parte delle neoplasie dell’orecchio esterno è di origine epiteliale, con il carcinoma basocellulare che prevale nettamente a livello del padiglione auricolare (70% di tutti i tumori), ed il carcinoma squamoso che prevale a livello del CUE, ove rappresenta l’ 80% circa di tutti i tumori maligni. Circa l'80% di questi tumori è localizzato al padiglione. Gli altri tumori sono divisi a metà tra il condotto uditivo esterno e l'orecchio medio (o la mastoide).
Tumori maligni (non esiste stadiazione TNM): Il 6% di tutti i tumori cutanei insorge in corrispondenza del padiglione auricolare:
• Forme:
- Carcinoma a cellule basali , Epitelioma (Fig. 11-12-13)da Bechara Y. Ghorayeb
- Carcinoma spinocellulare (Fig. 14) Epitelioma: da moderatamente a ben differenziato (85% di tutti i carcinomi della regione auricolare), Fig. 4.6.
- Melanoma maligno (7% di tutti i melanomi maligni del distretto capocollo), (Fig.15).
• Fattori predisponenti: esposizione solare cronica, infezioni croniche della pelle, psoriasi, ustioni chimiche.
• Localizzazioni prevalenti:
- Basalioma: dorso del padiglione auricolare, bordo del padiglione aurico1 are, regione pretragica, regione anteriore dell’ elice.
- Carcinoma spinocellulare: fossetta triangolare, bordo dell’elice, imbocco del condotto uditivo.
- Melanoma maligno: (Fig.15) da Bechara Y. Ghorayeb assenza di localizzazioni preferenziali (controllare sempre la piega retroauricolare!).
|

|
|
Fig.15: Questo paziente aveva due tumori adiacenti. La lesione piatta nera sotto l’ antitrago è un melanoma maligno. La lesione bianca elevata cheratosica è un carcinoma a cellule squamose.
|
• Metastasi regionali (nel carcinoma spinocellulare): nell’8-12% dei casi: linfonodi parotidei, giugo-digastrici, lungo il bordo posteriore del rn. sternocleidomastoideo (nucali), lungo il n. grande auricolare.
|

|
Fig. 11:In questo paziente anziano si è riscontrato un carcinoma basocellulare della conca, appena dietro il trago.
|
|

|
Fig.12:Il tumore è stato rimosso e il difetto chiuso con un innesto di pelle a tutto spessore (FTSG) prelevato dal collo.
|
|

|
Fig.13:Il tumore è stato rimosso e il difetto eliminato con un innesto di pelle a tutto spessore (FTSG) ) prelevato dal collo.
|
Epidemiologia
I carcinomi cutanei della testa e del collo insorgono quasi esclusivamente in soggetti di razza bianca e pelle chiara[i], di età media intorno ai 70 anni[ii]. adulti in età avanzata (soprattutto lavoratori agricoli, contadini, pescatori: esposizione protratta alla luce solare [ultravioletti]), prevalentemente maschi (80%). Nei soggetti di razza nera la pigmentazione scura rappresenta una protezione naturale nei confronti degli effetti dannosi delle radiazioni solari.
I due principali istotipi sono costituiti dal carcinoma squamo cellulare (SCC) che rappresenta tra l’80 e l’85% delle neoplasie del CUE e dal carcinoma basocellulare (BCC), il più comune tumore cutaneo. L’incidenza di queste due neoplasie è andata aumentando negli ultimi venti anni. Altri tumori più rari localizzati prevalentemente al CUE sono rappresentati dagli adenocarcinomi, dai carcinomi adenoido-cistici (cilindromi) e dagli adenomi ceruminosi
Fattori di rischio
L’esposizione prolungata i raggi solari e quindi ai raggi ultravioletti è sicuramente il primo fattore di rischio per la genesi dei tumori cutanei.
Lo xeroderma pigmentoso, malattia autosomica recessiva, è caratterizzato da una incapacità di riparare i danni del DNA, specie quelli prodotti dai raggi UV. I soggetti affetti da questa particolare patologia tendono a sviluppare molto precocemente tumori cutanei multipli, sincroni e metacroni, addirittura nella prima decade di vita, specialmente SCC e BCC. Tali pazienti sono ad alto rischio di sviluppare neoplasie del padiglione auricolare.
I trattamenti radioterapici per i tumori epiteliali del distretto cervico-facciale, in particolare del carcinoma del rinofaringe, comportano l’assorbimento di alte dosi di radiazioni, fino a 72 Gy totali. I soggetti sottoposti a tali trattamenti hanno un rischio molto più elevato di sviluppare un tumore cutaneo a livello dell’orecchio esterno e, in misura minore, dell’orecchio medio. Le neoplasie possono insorgere in un arco temporale compreso tra 3 e 27 anni dal trattamento radioterapico con una media di 17 anni[iv].
Le cicatrici da ustione rappresentano un altro importante fattore di rischio. Cosi come l’esposizione ai raggi, tali lesioni sono più frequentemente coinvolte nello sviluppo di SCC che può essere più aggressivo e con alta propensione a sviluppare metastasi.
Il Carcinoma squamocellulare(SCC) è il tumore maligno più comune a livello della cute del condotto uditivo osseo, arrivando a rappresentarne il 69-90% dei casi riportati in letteratura. Esistono sei diverse varianti istologiche di carcinoma squamoso: ben differenziato, moderatamente differenziato, scarsamente differenziato, a cellule chiare, a cellule fusate, verrucoso. Questi dati indicano che la sua insorgenza in tale sede non è correlata con l’esposizione ai raggi solari. Nelle aree dell’orecchio più esposte alle radiazioni solari l’elice è la sottosede più frequentemente colpita, con una percentuale che oscilla tra il 53 ed il 55% delle lesioni, seguita dall’antielice e dalla fossa triangolare (19%), la superficie posteriore del padiglione (14%), ed il complesso lobulo, conca, trago (12%).
A livello del padiglione auricolare, il carcinoma squamoso si presenta come una lesione a placca o nodulare, solitamente localizzata all’elice o all’antielice, più raramente alla superficie posteriore del padiglione auricolare. La lesione è facilmente sanguinante e resta indolente fino a quando non raggiunge la cartilagine sottostante.
A livello del condotto uditivo esterno, il tumore si presenta come una lesione polipoide facilmente sanguinante o come zona lievemente rilevata ed ulcerata. Può simulare un’ otite esterna cronica sia per l’aspetto che per i segni clinici; in questa localizzazione sono di costante riscontro l’otorrea persistente e l’otalgia profonda.
Il carcinoma squamoso localizzato all’orecchio esterno è contraddistinto da una particolare aggressività del comportamento biologico, mostrando una percentuale di metastatizzazione molto più elevata (fino al 18%) rispetto a quella registrata in altre sedi anatomiche (dal 2 al 3%). La prognosi è quindi determinata dalla notevole invasività locale della neoplasia, che tende ad invadere l’osso timpanico con un pattern tipicamente infiltrativo, raggiungendo spesso la base cranica e la superficie durale esterna
E’ un tumore tipico dell’età avanzata, a comparsa quasi esclusiva tra la sesta e la settima decade di vita, con una netta predominanza nel sesso maschile, con un rapporto M/F 2:1.
Il carcinoma basocellulare(BCC) è il tumore maligno più comune a livello della cute del padiglione auricolare e del condotto uditivo esterno, dove rappresenta circa il 90% delle lesioni neoplastiche cutanee. Il carcinoma basocellulare è una neoplasia a basso grado di malignità che si origina dallo strato basale dell’epidermide. Colpisce frequentemente la cosiddetta “zona H”, la regione del volto nella quale si concentra la quasi totalità della neoplasie cutanee. Esistono diverse varianti istologiche del carcinoma basocellulare, ognuna con un peculiare comportamento biologico: nodulare, ulcerativo, superficiale, pigmentato, sclerosante, differenziato, basaloide/squamoso. Qualunque sia la struttura della neoplasia, gli elementi cellulari costituenti il tumore sono di piccola taglia, con nucleo ovoidale, scarso citoplasma e mitosi. Colpisce prevalentemente la superficie posteriore del padiglione e la regione pre e retro-auricolare per l’alta concentrazione di unità pilo sebacee in questi distretti. All’interno del condotto si localizza per lo più al terzo laterale, rappresentando il secondo istotipo, dopo lo squamo cellulare, con una incidenza compresa tra il 15 ed il 20%. Il carcinoma basocellulare è una neoplasia con un basso indice di metastatizzazione, tra lo 0,003 e lo 0,01%,5,6; la disseminazione, quando presente, si verifica per via linfatica, interessando i linfonodi cervicali nel 70% dei casi. La prognosi del carcinoma basocellulare dipende in massima parte dall’istotipo, risultando migliore per il tipo nodulare e differenziato e peggiore per l’ulcerato e per il basaloide/squamoso.
Si presenta quasi esclusivamente a partire dalla sesta decade, mostrando una preponderanza per il sesso maschile con un rapporto M/F 2:1.
Il BCC origina primitivamente dalla superficie posteriore del padiglione auricolare, specie nella sua metà superiore, e nella regione retro e pre-auricolare.
Sintomatologia e segni clinici
La sintomatologia delle neoplasie del padiglione auricolare è particolarmente povera; i basaliomi si presentano come delle lesioni a lento accrescimento e diagnosi tardiva. dolore scarso o assente, secrezione fetida acquosa o emorragica, sanguinamento.
Nella variante nodulare, la più comune, la lesione si presenta come una papula madreperlacea o translucida, con teleangectasie nella regione cutanea circostante. La mancanza della cheratina rende la superficie nodulare più vulnerabile; spesso la zona centrale del nodulo si rompe dando luogo ad una lesione ulcerata nota come “ulcus rodens”. Il sanguinamento dell’ulcera è sovente il principale sintomo. L’invasione dello scheletro cartilagineo si verifica esclusivamente nelle lesioni trascurate, determinando la comparsa o l’esacerbazione del dolore.
Nella variante superficiale la lesione si presenta coma un’area di aspetto eczematoso
Stadiazione
Non esiste un sistema di stadiazione specifico per i tumori maligni dell’orecchio esterno; l’American Joint Committee on Cancer (AJCC) li inserisce nel gruppo dei tumori non-melanocitici della cute(tab. 2). Il sistema ha molte limitazioni quando viene applicato all’orecchio infatti, la cute sottile di tale distretto favorisce una più rapida infiltrazione del sottocutaneo profondo rispetto a quanto si verifica in altre sedi. Questo fa si che in molti casi il tumore si trova in uno stadio T4 con prognosi e trattamento chirurgico differente dai T4 localizzati in altre sedi. Inoltre l’unicità anatomica dell’orecchio rende poco pratica una stadiazione basata sulle dimensioni della lesione. Perfino piccoli tumori localizzati in determinate aree (regione pre-auricolare, conca e trago) possono richiedere interventi chirurgici più estesi, sia per il difetto creato sia per la vicinanza con altre strutture come la ghiandola parotide. Infine, la stadiazione dell’AJCC non tiene conto del tipo istologico. Il carcinoma squamocellulare e quello basocellulare possono avere un comportamento molto diverso l’uno dall’altro, ed i sottotipi istologici ne possono influenzare notevolmente l’aggressività.
Diagnostica
Indispensabile:
• Ispezione: con lente d’ingrandimento o microscopio.
• Palpazione: dimensione, consistenza e mobilità del tumore. Palpazione delle vie linfatiche di drenaggio.
• Valutazione ORL.
• Otomicroscopia.
• Ecografia: linfonodi regionali.
• Biopsia: nel sospetto di tumore, biopsia cuneiforme (quando possibile biopsia escissionale). Nel sospetto di melanoma maligno, escissione completa ampia e profonda, macroscopicamente di almeno i cm in tessuto sano (biopsia escissionale). Successiva resezione in caso di riscontro istologico positivo.
Utile in casi particolari:
• RM tessuti molli del collo, esclusione di metastasi a distanza.
• Consulto interdisciplinare: dermatologo, internista (stadiazione del tumore).
|

|
Fig. 14
Immagine di un Carcinoma a cellule squamose (o spinocellulare) dell'orecchio esterno.
Questa lesione cheratosica esofitica del padiglione auricolare sinistro è un carcinoma a cellule squamose ben differenziato.
|
Diagnosi differenziale di tumore maligno
Acantosi senile.
Eczema cronico.
Corno cutaneo.
Verruca seborroica.
Terapia
Terapia medica: nessuna.
Indicazioni all’intervento chirurgico: tutti i tumori del padiglione auricolare.
Principi dell’intervento:
• Ateromi: enucleazione completa della sede di origine inclusa una losanga cutanea (luogo d’origine), da effettuare in assenza di flogosi.
• Cheloidi: rimozione della cute interessata.
• Carcinoma a cellule basali (basalioma): ampia escissione in tessuto sano con controllo istologico estemporaneo dei margini di resezione.
• Carcinoma spinocellulare: nel caso di tumori con diametro inferiore ad i cm, escissione ampia in tessuto sano. Nel caso di tumori di dimensioni maggiori (con interessamento della cartilagine), asportazione parziale o totale del padiglione auricolare con controllo delle vie linfatiche di drenaggio e radioterapia complementare. Ricostruzione rinviata a più tardi.
• Melanoma maligno: a seconda delle dimensioni del tumore, della sua localizzazione e del suo stadio, ampia escissione in tessuto sano! Solitamente sacrificio completo del padiglione auricolare. Discussione interdisciplinare per svuotamento radicale delle vie linfatiche di drenaggio con parotidectomia e chemio o radioterapia adiuvante.
Terapia Chirurgica
I tumori dell’orecchio tendono a crescere lungo i piani di fusione embriologica. La derivazione e l’accrescimento degli abbozzi embrionali dell’orecchio esterno hanno un ruolo significativo sull’invasione tumorale E’ opinione comune che i piani di fusione tra gli abbozzi embrionali rappresentino un ostacolo alla marcia tumorale ma nel contempo una via lungo la quale microscopiche diffusioni del tumore possono essere favorite.
Poiché la cute di questo distretto è molto sottile, invadono i tessuti sottostanti molto più velocemente di quanto ci si aspetta, ed hanno una rapida crescita orizzontale. Per tali motivi è importante valutare accuratamente i margini di resezione. Alcuni autori raccomandano 8 mm di margine intorno ad un carcinoma basocellulare se il tumore misura meno di 3 cm ed 1,5 cm di margine se di dimensioni maggiori. Il carcinoma squamo-cellulare merita margini di resezione più ampi, da 1 a 2 cm14.
Tumori dell’Elice, antielice, lobulo
L’asportazione a tutto spessore di piccoli carcinomi dell’elice e dell’antelice può essere effettuata mediante incisione a cuneo a tutto spessore, per cui viene rimossa un’area triangolare di padiglione auricolare comprendente un segmento di elice e di antelice con l’apice che si estende all’area della conca. L’angolo di apertura dell’apice non dovrebbe superare i 30° (Fig. 16-17).

Fig. 16-17
Per lesioni che richiedono un’asportazione del padiglione superiore al 25% si può eseguire una exeresi a stella per distribuire le linee di tensione nella fase ricostruttiva.
Per la ricostruzione di perdite di sostanza, ad esempio dell’orletto auricolare e dell’elice, possono essere eseguiti lembi piani di vicinanza (Spina, Nelaton-Ombredanne, Lewin) (Fig. 18-19-20), lembi peduncolati tubulati e lembi di rotazione.

Fig. 18-19-20 Carcinoma basocellulare, exeresi e ricostruzione con lembo di rotazione
Trattamento linfonodale
Il trattamento dei linfonodi latero-cervicali è indicato quando le dimensioni del tumore superano i 2 cm ed in particolare per i tumori della regione pre-auricolare; quando l’infiltrazione profonda è maggiore di 4 mm ed è presente invasione perineurale; quando l’istotipo è scarsamente differenziato ed il paziente è immunocompromesso.
Si esegue uno svuotamento laterocervicale radicale modificato sempre associato alla parotidectomia.
La radioterapia post-operatoria è indicata in caso di coinvolgimento linfonodale multiplo o di invasione extra-capsulare.
Fase ricostruttiva
Per quanto riguarda i tumori di piccole dimensioni del padiglione auricolare, i difetti inferiori ai 2 cm si riparano mediante sutura diretta dei margini. Il padiglione residuo è più piccolo, ma ancora esteticamente accettabile.
In caso di exeresi subtotale o totale dell’orecchio esterno, associata a parotidectomia e/o petrosectomia, la ricostruzione prevede l’uso di lembi miocutanei peduncolati (muscolo grande pettorale) o liberi (muscolo retto addominale). Il lembo di muscolo grande pettorale pur avendo una grande massa, non sempre raggiunge il limite superiore del difetto (Fig. 9, 10, 11, 12). Il lembo di muscolo retto dell’addome è, fra i lembi liberi, quello che meglio si addice alla ricostruzione di questi distretti (Fig. 21, 22, 23, 24).

Fig. 21, 22, 23, 24 Recidive multiple di carcinoma basocellulare del padiglione auricolare sn. Exeresi del tumore, parotidectomia, svuotamento latero-cervicale, petrosectomia laterale e ricostruzione con lembo mio-cutaneo peduncolato di muscolo grande pettorale.
Ambulatoriale/con ricovero:
• Biopsie, biopsie escissionali ed asportazione completa del padiglione auricolare:
possibili ambulatoriamente.
• Resezione tumorale con ricostruzione e / o controllo delle vie di drenaggio linfatico mediante svuotamento latero-cervicale: ricovero.
Prognosi
Buona in caso di basaliomi dopo rimozione completa controllata istologica- mente (quasi 100% di guarigioni). In caso di recidiva o persistenza dopo intervento insufficiente o radioterapia nuova rimozione con controllo istologico con congelatore. Dopo radioterapia (non raccomandabile!) o trattamento obsoleto con pomate citostatiche la prognosi peggiora.
In caso di carcinomi spinocellulari la probabilità di sopravvivenza a 5 anni è di circa l’80% (tutti gli stadi) se il trattamento è stato condotto secondo regola.
In caso di melanomi la probabilità di sopravvivenza è di circa il 30%, in relazione alle dimensioni ed allo stadio del tumore
Anatomia patologica
Tumori sviluppati a partenza dalla cute
Si tratta il più delle volte di carcinomi epidermoidi (Figura 14 ). I carcinomi basocellulari sono più rari; essi evolvono a partire della regione della conca e del meato uditivo.
Epitelioma I tumori epiteliali maligni più frequenti ,baso e spinocellulari, a localizzazione nell’orecchio esterno sono gli epiteliomi. Nell’ambito del padiglione le sedi più frequenti sono in ordine di frequenza; l’elice. la faccia interna del padiglione. l’antelice. la conca. il lobulo. il trago.
Molto meno frequente è la localizzazione in corrispondenza del condotto uditivo. Tali neoplasie sono più frequenti nel sesso maschile (M:F = 2:1) e nella fascia d’età compresa tra 60 e 80 anni.
Numerosi fattori sono stati imputati di responsabilità più o meno diretta nell’ insorgenza degli epiteliomi: la preesistenza di talune dermopatie. quali l’eczema o la psoriasi: le cicatrici da vecchie ustioni: fattori traumatici locali ripetuti (es. quelli provocati dalle stanghette degli occhiali): pregressa terapia radiante.
Macroscopicamente l’epitelioma può manifestarsi con aspetto ulcerativo. infiltrante e vegetante (Fig. 3). Le forme istologiche più frequenti sono: l’epitelioma spinocellulare ed il baso cellulare, Di maggior incidenza il primo, che ha anche un’evoluzione più rapida. essendo dotato di maggiore invasività. locale e sistemica (maggiore possibilità di metastasi).
Solitamente all’inizio la neoplasia si manifesta sotto forma di un piccolo nodulo. ricoperto da cute liscia e sottile: tende presto ad ulcerarsi. trasformandosi quindi nella tipica lesione ne ulcerativa a fondo sanioso. a margini rilevati ed irregolari, non dolente o scarsamente dolente, ma facilmente sanguinante al toccamento.
Dal distretto di insorgenza il tumore per continuità tende ad infiltrare tutto il padiglione. Le presenza di adenopatie satelliti, quasi mai constatabili negli epiteliomi baso-cellulari è invece quanto mai frequente negli spino cellulari. I gruppi linfoghiandolari più frequentemente interessati sono quelli mastoidei. quelli superiori della catena della giugulare interna, meno spesso quelli pre-tragici. Le linfoadenopatie si presentano in genere come tumefazioni di dimensioni variabili, dure, indolenti. Nella fase conclamata dell’affezione la diagnosi non prospetta difficoltà; per le forme iniziali, attraverso l’esame bioptico, sarà possibile giungere ad una precisa definizione istopatologica. La terapia degli epiteliomi del padiglione auricolare è essenzialmente chirurgica. Nel caso di tumori circoscritti e di recente insorgenza si potrà far ricorso ad interventi parziali, con resezioni cuneiformi, che, oltre a consentire la completa exeresi del tumore, eviteranno peraltro gravi perdite di sostanza e/o deformazioni. Le neoplasie localmente molto estese andranno invece trattate mediante l’exeresi totale del padiglione: la necessità di effettuare anche uno svuotamento laterocervicale si impone in caso di presenza di linfoadenopatie metastatiche.
Altri tumori maligni
I tumori maligni mesenchimali primitivi sono rari: fibro-, condro-, osteosarcoma, sarcoma di Ewing, sono stati descritti ripetutamente. I rabdomiosarcomi sono molto particolari nel bambino.
I melanomi maligni colpiscono il più delle volte il padiglione auricolare, ma possono estendersi al condotto uditivo esterno.
Ceruminoma maligno degenerato,
Le emopatie possono presentare delle localizzazioni auricolari che interessano il condotto uditivo esterno ed evolvono spesso anche nell'orecchio medio.
Le localizzazioni auricolari dell'istiocitosi sono classiche, ma molto rare.
Le localizzazioni metastatiche all'orecchio medio e alla rocca di un cancro osteofilo sono più spesso dei tumori della rocca che si estendono al condotto uditivo esterno.
Clinica
Segni rivelatori
Non sono specifici e si rivelano spesso ingannevoli. Il segno rivelatore più frequente è un'otorrea monolaterale purulenta che evolve da alcuni mesi e resistente alle terapie locali. Essa si trova rapidamente associata a otalgia sempre meno alleviata dagli antalgici classici.
Più raramente, la malattia è rivelata da una paralisi faciale o anche dalla lesione di altri nervi cranici o da adenopatie cervicali.
Esame clinico
Esso si basa su un'otoscopia effettuata sotto microscopio dopo aspirazione. In caso di stenosi, si può ricorrere al posizionamento di un tampone di Merocel® con delle instillazioni di gocce antisettiche. La sua asportazione dopo 48 ore permette di esaminare il condotto nelle migliori condizioni e di guidare una biopsia, effettuata al minimo dubbio, che deve essere rinnovata in caso di risposta negativa se il dubbio rimane.
Trattamento
Il trattamento dei carcinomi è principalmente chirurgico. Esso comporta una resezione ampia, che passa a distanza dai margini del tumore ed estesa se necessario alla mastoide, all'orecchio medio con conservazione o meno del sistema timpano-ossiculare e del nervo faciale. Questo intervento chirurgico di petrectomia è di solito completato da una radioterapia esterna postoperatoria.
Nelle forme inoperabili può essere proposta un'associazione di radioterapia e di chemioterapia concomitanti.
BIBLIOGRAFIA
Afzelius LE, Gunnarsson M, Nordgren H. Guidelines for prophylactic radical lymph node dissection in cases of carcinoma of the external ear. Head Neck Surg 1980; 2: 361-365.
Arriaga M, Curtin HD, Takahashi H. Staging proposal for external auditory meatus carcinoma based on preoperative clinical examination and computed tomography findings. Ann Otol Rhinol Laryngol 1990; 99: 714-21.
Arriaga M, Curtin HD, Takahashi H. The role of preoperative CT scan in staging external auditory meatus carcinoma: radiologic-pathologic correlation study. Otolaryngol Head Neck Surg 1991; 104: 58-66.
Balough BJ, O’Leary MJ, Martin PJ. Basal and squamous cell Carcinoma of the auricle. In: Jackler RK, Driscoll CLW editors.Tumors of the ear and temporal bone.Philadelphia: Lippincott Williams and Wilkins; 2000. p. 29-55.
Bumstead RM, Ceilley RI, ed altri Auricolar malignant neoplasm: when is chemotherapy (mohs’ technique) necessary? Arch Otolaryngol 1981; 107: 721-4.
Byers R, Kesler K, Redmon B. Squamous carcinoma of the external ear. Am J Surg 1983; 146: 447-50).
Clark LJ, Narula AQ, Morgan DA. Squamous cell carcinoma of the temporal bone: a revised staging. J Laryngol Otol 1991; 105: 346-8.
Freedlander E, Chung FF. Squamous cell carcinoma of the pinna. Br J Plast Surg 1983; 36(2): 171-175.
Hayden RC III. Cutaneous squamous carcinoma and related lesion. Otolaryngol Clin North Am 1993; 26: 57-71
Goodwin WJ, Jesse RH. Malignant neoplasm of the external auditory canal and temporal bone. Arch Otolaryngol 1980;106: 675-9.
Graham MD, Sataloff RT, Kemink JL. Total en bloc resection of the temporal bone and carotid artery for malignant tumor of the ear and temporal bone. Laryngoscope 1984; 94: 528-533.
Lo WC, Ting LL, Ko JY, Laryngoscope 2008; 118 (12): 2151-2155.
Moffat DA, Grey P, Ballagh RH Extended temporal bone resection for squamous cell carcinoma. Otolaryngol Head Neck 1997; 116:617-23
Pensak ML, Gleich LL, GluckmanJL. Temporal bone carcinoma: contemporary prospectives in the skull base surgical era. Laryngoscope 1996; 106: 1234-1237.
Sataloff RT, Myers LD. Total temporal bone resection for squamous cell carcinoma. Otolaryngol Head Neck Surg 1987; 96: 4-14.
Stell PM, Mc Cormick MS. Carcinoma of the external auditory meatus and middle ear: prognostic factors an a suggested staging system. J Laryngol Otol 1985; 99: 847-50.
Swartz JD, Harnsberger. Imaging of the temporal bone. New York: Thieme. Third edition. 1998